18 березня, 2024
Оптимізація лікування гострих респіраторних вірусних інфекцій: етіотропна, патогенетична та симптоматична терапія
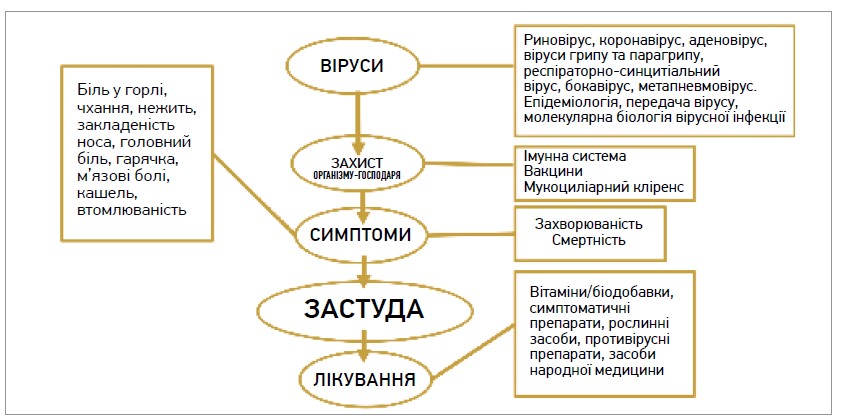
Гостра застуда – самообмежувальне захворювання верхніх дихальних шляхів. Застуда зазвичай має помірну тяжкість і виникає під дією низки вірусів різних родин (найчастіше – риновірусів). Основними симптомами застуди є біль у горлі, гострий кашель, чхання, закладеність та виділення з носа (рис. 1). Інкубаційний період застуди триває зазвичай 24-72 год, а сама хвороба – в межах 1 тиж. Застуда асоціюється зі значним економічним тягарем для суспільства через потребу у візитах до лікаря, витрати на фармакопрепарати і біодобавки та тимчасову непрацездатність (Al-Haddad M.S. et al., 2016).
Рис. 1. Концепція застуди (за Eccles R., 2023)
Результати досліджень свідчать, що пацієнти нерідко лікують застуду самостійно за допомогою безрецептурних або рецептурних препаратів. Недостатні знання хворих про етіологію цього патологічного процесу зумовлюють застосування невідповідних медикаментів або тиск на лікаря з метою отримання бажаних призначень, наприклад антибіотиків, які є неефективними при гострих респіраторних вірусних інфекціях (ГРВІ). Антибіотикотерапія застуди не лише спричиняє зайві витрати, а й сприяє розвитку антибіотикорезистентності основних патогенів (Al-Haddad M.S. et al., 2016).
У медичній літературі широко застосовується термін «застуда» (common cold), однак застуда є скоріше культурним поняттям, ніж клінічним діагнозом, оскільки зазвичай пацієнт сам установлює собі цей діагноз і лікується теж самостійно (Eccles R., 2013). Термін «застуда» використовується вже протягом декількох століть; його виникнення пов’язано з гіпотезою, що симптоми цього стану зумовлені впливом холоду. Однак популярні хибні переконання про те, що застуда виникає після виходу на вулицю з мокрим волоссям, потрапляння під дощ або промочування ніг, розвіяли експериментальні дослідження, які не виявили впливу холоду на схильність до інфекцій. Але можлива така ситуація, коли субклінічна інфекція перетворюється на клінічно виражену під дією охолодження поверхні тіла. Цю ідею вперше висунули S. Mudd і S. Grant, які продемонстрували, що охолодження поверхні тіла спричиняє ішемію й охолодження глотки та мигдаликів, а це провокує рефлекторну вазоконстрикцію в ділянці епітелію дихальних шляхів із подальшим зниженням опору до інфекцій (Eccles R., 2023).
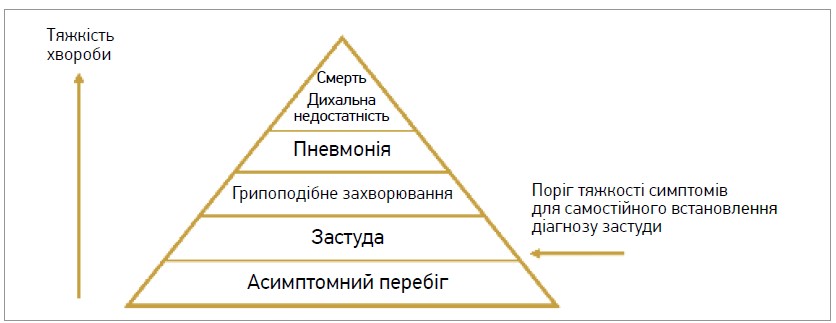
Наукове пояснення етіології застуди стало можливим лише в 1950-х рр., коли були відкриті риновіруси. Складний симптомокомплекс, відомий як застуда, можуть спричиняти всі відомі респіраторні віруси, а також віруси кору, ентеровіруси і навіть деякі бактерії (Eccles R., 2023). Цей симптомокомплекс є лише частиною т. зв. айсберга вірусних інфекцій (рис. 2).
Рис. 2. Айсберг клінічних проявів ГРВІ (Eccles R., 2023)
Більшість ГРВІ – субклінічні або безсимптомні процеси, малопомітні для організму-господаря, імунна система якого долає вірус упродовж декількох днів. Зазвичай симптоми застуди локалізовані лише у верхніх дихальних шляхах; натомість грипоподібне захворювання передбачає наявність системних симптомів на кшталт гарячки, м’язових болів і загальної слабкості. За наявності несприятливих фонових факторів (літнього віку, незадовільного стану імунної системи, неправильного харчування) може виникати тяжке респіраторне захворювання – бронхіоліт чи пневмонія, здатні навіть зумовити смерть (Eccles R., 2023).
Фактори ризику розвитку ГРВІ – перебування в місцях підвищеного скупчення людей (у навчальних закладах, громадських місцях – кінотеатрах, театрах, супермаркетах, ресторанах тощо, а також транспорті), висока соціальна активність, стрес, шкідливі звички (зловживання алкоголем, куріння), незадовільна якість сну, вітамінодефіцити. Певний вплив мають також стать і вік. Загалом чоловіки є схильнішими до тяжкого перебігу ГРВІ в дитячому / підлітковому та літньому віці; натомість у жінок фертильного віку (від пубертату до менопаузи) ризик тяжкої застуди є вищим, ніж у чоловіків (Eccles R., 2023).
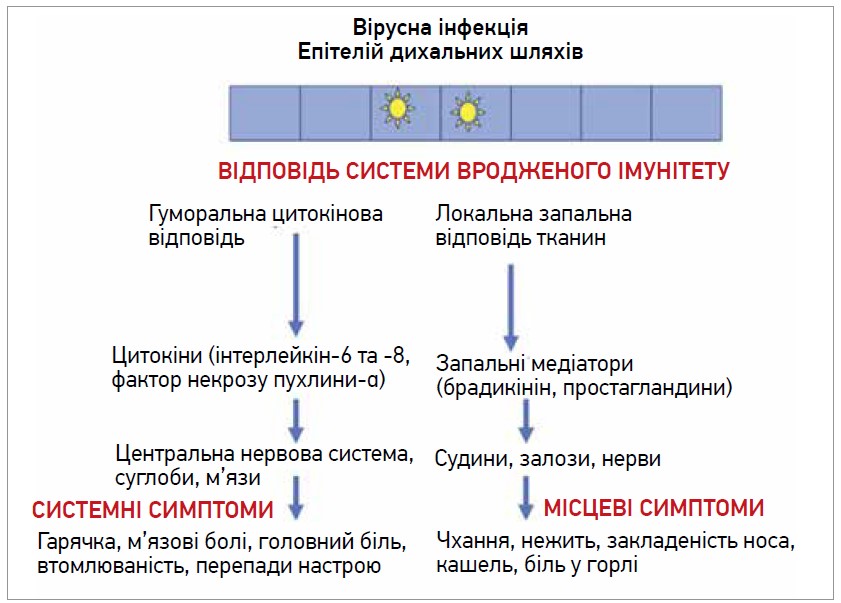
Системні та локальні симптоми ГРВІ мають різне патогенетичне походження (рис. 3), хоча глобально обидві ці групи симптомів спричиняє не сам вірус, а імунна відповідь організму-господаря. Системні симптоми застуди опосередковані прозапальними цитокінами (інтерлейкіном-6 та -8, фактором некрозу пухлини), а локальні – брадикініном і простагландинами (Eccles R., 2023).
Рис. 3. Механізм виникнення симптомів ГРВІ (Eccles R., 2023)
Лікування застуди передбачає комплексний багатогранний підхід із використанням етіотропної, патогенетичної та симптоматичної терапії. Водночас недоцільно перевантажувати пацієнта декількома різними медикаментами та біодобавками, які можуть мати лікарські взаємодії, а також за рахунок складного режиму прийому несприятливо впливати на прихильність до лікування. Отже, варто вирішувати якнайбільшу кількість клінічних задач за допомогою якнайменшої кількості засобів.
Ергоферон (ТОВ «Матеріа Медика-Україна») – противірусний препарат, який ефективно діє на всі респіраторні віруси. Ергоферон створений на основі антитіл до інтерферону-γ (ІФН-γ), гістаміну та рецептора CD4. Його противірусна й імуномодулювальна дія реалізується за рахунок впливу на систему інтерферонів у поєднанні з активацією процесів розпізнавання вірусів системою CD4-клітин, що забезпечує зупинку розмноження вірусів, їхнє знешкодження та видалення (табл.).
|
Таблиця. Функції антитіл, які входять до складу Ергоферон |
|
|
Антитіла |
Функції |
|
До ІФН-γ |
Регулювати функціональну активність і продукцію ендогенних інтерферонів завдяки конформаційним змінам молекули ІФН-γ, а також підвищенню її афінності (спорідненості) до рецептора ІФН-γ |
|
До рецептора CD4 |
Регулювати функціональну активність СD4-рецептора, сприяючи підвищенню функціональної активності СD4-лімфоцитів, а також нормалізації імунорегуляторного індексу (СD4/СD8) та субпопуляційного складу імунокомпетентних клітин (СD3, СD4, СD8, СD16, СD20) |
|
До гістаміну |
Модифікувати гістамінозалежну активацію периферичних і центральних H1-рецепторів, сприяючи зменшенню проникності судин і зниженню агрегації тромбоцитів під час контакту з алергеном, пригніченню вивільнення гістаміну з опасистих клітин і базофілів, оптимізації продукції лейкотрієнів |
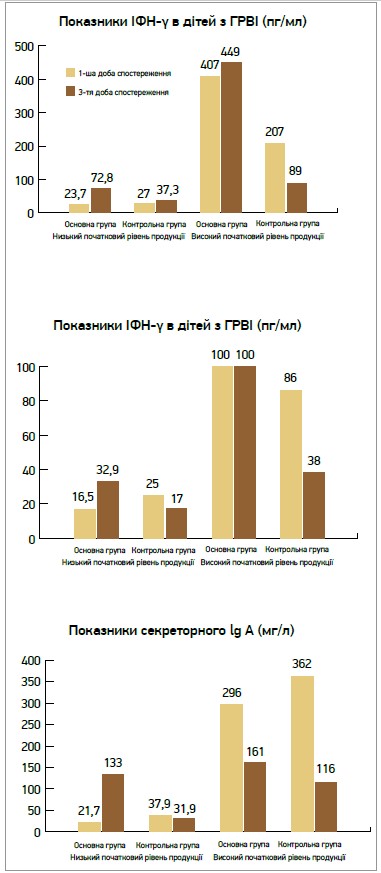
Цікаво, що відповідно до результатів вітчизняного дослідження С.О. Крамарьова та Л.В. Закордонець (2014), Ергоферон чинить імунокоректувальну дію без виснаження імунної системи, тобто за прийому Ергоферону продукція ІФН-α збільшувалася в усіх пацієнтів, але переважала в дітей із низьким початковим рівнем. Ергоферон стимулював синтез ІФН-α винятково в дітей зі зниженою імунною відповіддю на вірусну інфекцію. Аналогічно збільшення секреції імуноглобулінів класу A спостерігалося лише при застосуванні Ергоферону в дітей з низьким початковим рівнем цих антитіл (рис. 4).
Рис. 4. Коригувальна дія Ергоферону залежно від вихідного рівня продукції інтерферонів
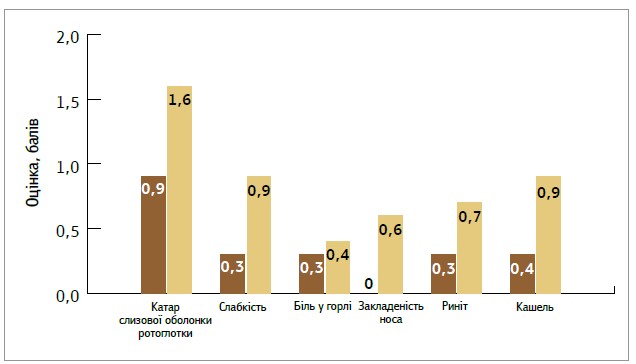
В аспекті багатогранного лікування ГРВІ важливо, що Ергоферон чинить не лише противірусну дію, а й має протизапальний та антигістамінний ефекти, що забезпечує водночас патогенетичну, а також симптоматичну терапію. Ці ефекти реалізуються за рахунок дії антитіл до гістаміну, які впливають на алергічний компонент вірусних інфекцій, знижуючи тонус гладкої мускулатури бронхів і зменшуючи проникність капілярів, а це зумовлює скорочення тривалості й інтенсивності ринореї, зменшення набряку слизової оболонки носа, кашлю, чхання, а також зниження вираженості алергічних реакцій, що нерідко супроводжують інфекційні процеси. У вищезазначеному дослідженні С.О. Крамарьова та Л.В. Закордонець (2014) Ергоферон удвічі швидше зменшував вираженість основних симптомів ГРВІ: кашлю, риніту та закладеності носа (рис. 5).
Рис. 5. Вираженість основних симптомів ГРВІ через 2 дні лікування
Клінічна ефективність та безпека Ергоферону доведені за допомогою проведення численних рандомізованих досліджень, результати яких демонструють, що на тлі застосування Ергоферону скорочується тривалість основних проявів ГРВІ, грипу, частота бактеріальних ускладнень, а також полегшується тяжкість перебігу захворювання. Так, дані нещодавнього метааналізу (2021) свідчать, що Ергоферон є у 1,5 раза ефективнішим у зменшенні тривалості гарячки, ніж плацебо (відношення ризиків 1,499; р=0,0002). Крім того, Ергоферон достовірно зменшував тяжкість хвороби (зa показником площі під кривою: до 32,83±18,12 проти 36,94±19,08 одиниць у групі плацебо; p=0,0083) і знижував частоту бактерійних ускладнень у 7 разів. Безпеку терапії Ергофероном підтверджувала менша кількість осіб, у яких виникали побічні ефекти (в 0,6 проти 10,8% у групі плацебо; р=0,0006) та відсутність лікарських взаємодій (Gorelov A.V. et al., 2021).
Під час оцінки динаміки температури та проявів інтоксикації в амбулаторних пацієнтів із сезонним грипом виявлено, що результати застосування Ергоферону є зіставними з такими прийому озельтамівіру (Rafalsky V. et al., 2016).
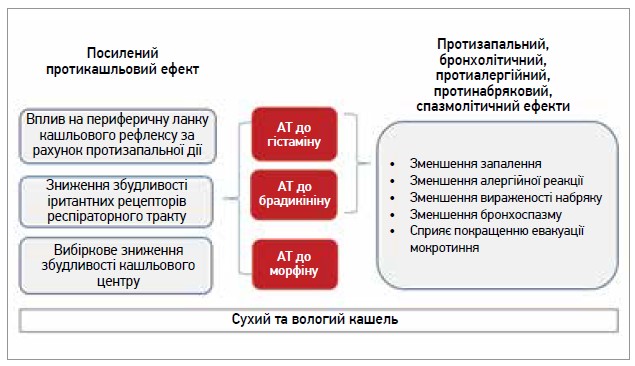
Частим симптомом ГРВІ є кашель, який виникає внаслідок запалення верхніх дихальних шляхів. За наявності в пацієнта з ГРВІ цього симптому протикашльове лікування є обов’язковим компонентом призначуваної комплексної терапії. Ефективним в усуненні сухого і вологого кашлю є Ренгалін (ТОВ «Матеріа Медика-Україна»). До його складу входять антитіла до гістаміну та брадикініну, які чинять протизапальну, бронхолітичну, протинабрякову й антиалергічну дії, в результаті чого зменшуються потужність запалення, вираженість набряку, бронхоспазм, проникність судин, інтенсивність продукції слизу. Антитіла до морфіну, що також містяться в Ренгаліні, протидіють центральному компоненту кашлю, знижуючи збудливість кашльового центру (рис. 6).
Рис. 6. Механізми дії Ренгаліну
Ренгалін з успіхом застосовується для лікування кашлю в дорослих. Відповідно до інструкції для медичного застосування препарату та низки проведених досліджень, Ренгалін зменшує тяжкість кашлю в пацієнтів із гострими респіраторними захворюваннями вже з 1-ї доби терапії, а на 3-й день лікування спостерігається значущий клінічний результат за всіма параметрами ефективності препарату. Ренгалін застосовується для лікування як продуктивного, так і непродуктивного кашлю; знижує потребу в додатковій муколітичній терапії, добре поєднується з іншими препаратами для лікування ГРВІ та не спричиняє побічних реакцій, характерних для протикашльових препаратів центральної дії (седативного та снодійного ефектів, пригнічення дихання, порушення моторики шлунково-кишкового тракту, звикання, формування залежності).
За даними літератури, 80% пацієнтів із постінфекційним кашлем, які приймали Ренгалін протягом 7 днів, не потребували подальшого лікування. Порівняно з відомим протикашльовим препаратом (бутамірату цитрат у поєднанні з гвайфенезином) Ренгалін продемонстрував достовірно кращу оцінку за індексом кашльового синдрому: через 7 днів лікування оцінка в 0 балів спостерігалася в 47% осіб групи Ренгаліну та в 27% осіб контрольної групи (Матюха Л.Ф., 2020). Для Ренгаліну також виявлено вищу клінічну ефективність щодо усунення денного кашлю порівняно із фенспіридом: через 7 діб терапії кашель зник у 96% пацієнтів, які отримували Ренгалін, і лише в 39% осіб, котрі приймали фенспірид, тобто ефективність Ренгаліну була в >2,5 раза вищою (Кочуєва М.М., 2020; Чуловська У.Б., 2021).
Висновки
ГРВІ були і залишаються однією з основних груп захворювань у сімейній медицині та терапії, а проблема застосування необґрунтованої фармакотерапії (насамперед антибактеріальних препаратів) значно ускладнює ведення таких хворих. Пацієнти з гострими респіраторними захворюваннями потребують засобів, які виконують водночас функції етіотропної, патогенетичної, симптоматичної терапії. Прикладом таких засобів можуть бути Ергоферон і Ренгалін, яким притаманні багатогранні механізми дії. Високу ефективність та відмінний профіль безпеки Ергоферону і Ренгаліну було продемонстровано в низці клінічних досліджень.
Підготувала Лариса Стрільчук