24 січня, 2021
Нове в можливостях терапії в період вірусних інфекцій
 Передбачається, що цьогорічний епідемічний сезон буде особливо напруженим. Потужна друга хвиля коронавірусної хвороби (COVID‑19) не збирається вщухати й водночас до неї приєднуються вже звичні гострі респіраторні вірусні інфекції (ГРВІ) та грип. Чи можливо знизити ризик інфікування та зменшити тяжкість перебігу зазначених захворювань? Ці питання сьогодні неабияк хвилюють свідоме населення нашої планети. Відповіді на них можна було почути в спеціальному випуску для сімейних лікарів, який відбувся 15 грудня у форматі прямого ефіру. Із доповіддю «Нове в можливостях терапії в період вірусних інфекцій» виступила заступник керівника Центру алергічних захворювань верхніх дихальних шляхів ДУ «Інститут отоларингології ім. О. С. Коломійченка НАМН України» (м. Київ), доктор медичних наук Інна Володимирівна Гогунська.
Передбачається, що цьогорічний епідемічний сезон буде особливо напруженим. Потужна друга хвиля коронавірусної хвороби (COVID‑19) не збирається вщухати й водночас до неї приєднуються вже звичні гострі респіраторні вірусні інфекції (ГРВІ) та грип. Чи можливо знизити ризик інфікування та зменшити тяжкість перебігу зазначених захворювань? Ці питання сьогодні неабияк хвилюють свідоме населення нашої планети. Відповіді на них можна було почути в спеціальному випуску для сімейних лікарів, який відбувся 15 грудня у форматі прямого ефіру. Із доповіддю «Нове в можливостях терапії в період вірусних інфекцій» виступила заступник керівника Центру алергічних захворювань верхніх дихальних шляхів ДУ «Інститут отоларингології ім. О. С. Коломійченка НАМН України» (м. Київ), доктор медичних наук Інна Володимирівна Гогунська.
На початку свого виступу спікер звернула увагу, що захворюваність на ГРВІ з початком зими значно зросла. За даними Центру громадського здоров’я МОЗ України, захворюваність на ГРВІ нині становить 509 випадків на 100 тис. населення, що вже на 5,4% перевищує епідемічний поріг.
Також починають фіксувати окремі спорадичні випадки грипу. Тож існують реальні ризики, що й без того напружена ситуація з COVID‑19 погіршиться епідемією чи навіть пандемією грипу. Ці побоювання підтверджують слова генерального директора Всесвітньої організації охорони здоров’я (ВООЗ) Т. А. Гебреєсуса, котрий, презентуючи нову Глобальну стратегію з грипу на 2019-2030 роки, сказав: «Загроза пандемії грипу присутня постійно. Завжди існує реальний ризик передачі нового вірусу грипу від тварин людині й, можливо, виникнення пандемії. Питання не в тому, чи станеться ще одна пандемія, а в тому, коли вона відбудеться».
Інна Володимирівна зазначила, що охоплення вакцинацією від грипу в Україні є дуже низьким: від початку епідемічного сезону профілактичні щеплення від грипу зробили лише 135 тис. осіб. Отже, найдієвіший засіб профілактики грипу майже не використаний, тому існує загроза різкого спалаху захворюваності на грип.
Профілактичні заходи щодо COVID‑19 та інших ГРВІ мають недостатньо високу ефективність. Як результат, стрімко зростає захворюваність на ГРВІ.
Саме тому сьогодні велика увага приділяється сучасним можливостям лікування вірусних інфекцій, включаючи COVID‑19. Наразі як терапевтичні стратегії при вірусних захворюваннях широко використовують засоби з противірусною, протизапальною, імуномодулювальною дією (вітамін С, кверцетин, цинк, мелатонін, вітамін D3).
Особливий інтерес становить саме кверцетин, який продемонстрував противірусні, антиоксидантні й імуномодулювальні властивості в численних дослідженнях. У медичній базі PubMed згадок про кверцетин понад 17 тис.! Понад 200 клінічних досліджень виконані in vivo (Kelly G. S., 2011). Сьогодні виявлено досить багато позитивних клінічних ефектів кверцетину.
Спектр дії та сфери терапевтичного застосування кверцетину (D’Andrea G., 2015):
- стани, котрі супроводжуються запаленням;
- алергія;
- астма;
- функціонування імунної системи й інфекції;
- розлади настрою;
- артрит;
- протипухлинна дія;
- цукровий діабет;
- гастропротекція;
- anti-age стратегії та ін.
Утім, найбільш вивченими є саме противірусні властивості кверцетину.
Відомо, що кверцетин блокує проникнення вірусу всередину клітини шляхом інгібування РІ‑3’-кінази, транскрипцію вірусного геному через інгібування РНК-полімерази, пригнічує трансляцію вірусних білків. Це специфічний шлях впливу кверцетину на реплікацію вірусу. Крім того, кверцетин пришвидшує виведення вірусу з клітини за рахунок посилення мітохондріальної противірусної відповіді.
Кверцетин має універсальну противірусну активність, тому оцінюється як перспективний засіб у лікуванні ГРВІ різної етіології. Це підтверджують і результати низки клінічних досліджень.
Кверцетин: результати досліджень in vitro
Доведено, що кверцетин активно діє проти вірусів грипу, парагрипу, риносинцитіального вірусу, адено- та риновірусів.
E. Ohnishi та H. Bannai в публікації в журналі Antiviral Research наголосили, що кверцетин посилює противірусну активність, індуковану фактором некрозу пухлини (TNF). TNF зумовлює дозозалежне інгібування вірусу везикулярного стоматиту (VSV), вірусу енцефаломіокардиту (EMCV) та простого герпесу 1 типу в умовах in vitro. Противірусна активність TNF проти VSV та EMCV значно посилюється при його застосуванні в комбінації з кверцетином.
Також в умовах in vitro кверцетин виявляв активність проти вірусу грипу. Група дослідників (Wu W. et al., 2015) встановила, що кверцетин:
блокує злиття вірусної мембрани з клітиною людини в разі грипу;
- порушує проникнення та реплікацію вірусу, пригнічуючи ферментативну активність зворотної транскриптази;
- має імуномодулювальний вплив, сприяючи ранній продукції інтерферонів;
- модулює інтерлейкіни;
- прискорює дозрівання Т-клітин і фагоцитарну активність.
Встановлено, що кверцетин є потужним інгібітором 3CL-протеази SARS-CoV‑2 (Abian O. et al., 2020).
Кверцетин: результати досліджень in vivo
У рандомізованому подвійному сліпому плацебо-контрольованому дослідженні (Heinz S. A. et al., 2010) 1002 пацієнти застосовували кверцетин (500/1000 мг/добу) чи плацебо протягом 12 тиж. Серед хворих віком понад 40 років терапія кверцетином 1000 мг/добу супроводжувалася зниженням загальної кількості днів із ГРВІ та вираженості симптомів.
W. Wu, R. Li та співавт. (2015) продемонстрували, що кверцетин здатний зменшувати рівень смертності, зумовленої тяжкими ускладненнями вірусу грипу А/H1N1.
Наразі кверцетин розглядають як потенційний противірусний агент щодо COVID‑19; також вивчається ефективність комбінації цинку та кверцетину: вона вже пройшла випробування на тваринах для використання проти вірусу Ебола та SARS-CoV‑1 і схвалена Управлінням із контролю якості продуктів харчування та лікарських засобів США (FDA) для клінічних випробувань за участю людей (D’Adamo P., 2020).
Результати виконаних робіт є обнадійливими в аспекті дієвості кверцетину стосовно SARS-CoV‑2.
Біодоступність кверцетину – «камінь спотикання» на шляху до мети
Більшість засобів кверцетину характеризуються дуже низькою біодоступністю – на рівні 2% (її навіть описують так: зникає так само швидко, як і сніжинка, що падає на гарячу сковорідку).
Відомі випадки, коли тривале застосування кверцетину дозою 2000 мг не давало змоги досягти очікуваних позитивних змін (D’Andrea G., 2015). Саме його низька розчинність у воді ускладнює створення ефективних пероральних форм препарату. Водночас дозозалежний ефект кверцетину потребує його належного всмоктування в шлунково-кишковому тракті. Інна Володимирівна зазначила, що для забезпечення високої біодоступності кверцетину необхідно застосовувати спеціальні технології доставки.
Інноваційною розробкою італійської компанії INDENA стала нова рецептура кверцетину, що базується на системі доставки за технологією мікрокапсулювання, QFit (Cesarone M. et al., 2019). Вона застосовується для збільшення розчинності активних природних інгредієнтів із низькою біодоступністю. Це підвищує здатність кверцетину проникати крізь біологічні бар’єри, покращує його біодоступність і посилює біологічну активність.
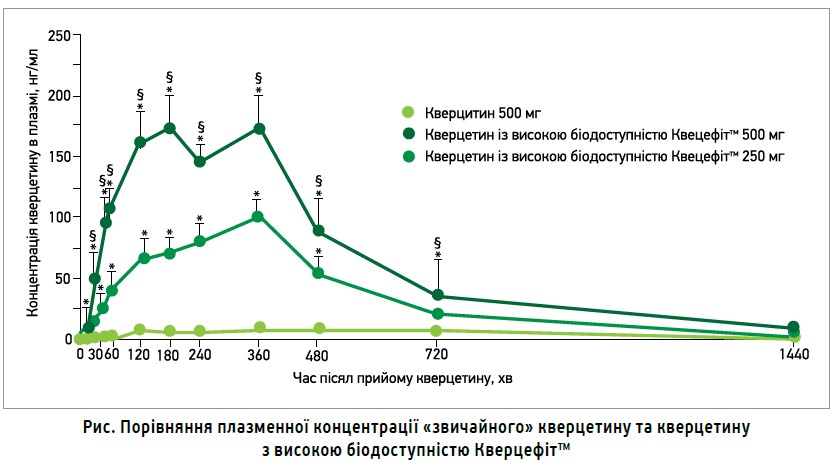
У спостереженні A. Riva та співавт. (2018) за участю 12 здорових добровольців віком 18-50 років порівнювали біодоступність «звичайного» кверцетину (500 мг/добу; група А) та кверцетину з високою біодоступністю Кверцефіт™ (250 і 500 мг/добу; група В та С відповідно). Протягом доби в них 12 разів виконували лабораторні тести, необхідні для вивчення фармакокінетики.
! Вчені встановили, що показник Сmax (максимальна концентрація в плазмі) для кверцетину з високою біодоступністю Кверцефіт™ 500 мг до 20 (!) разів, а AUC (концентрація діючої речовини в плазмі крові протягом усього часу спостереження) у 18 разів перевищує такі для «звичайного» кверцетину в аналогічній дозі (рис.).
Аналіз фармакокінетичного профілю «звичайного» кверцетину та кверцетину з високою біодоступністю Кверцефіт™ дав змогу зробити висновок про значно кращу пероральну абсорбцію останнього як у зіставних дозах (500 мг/добу), так і в разі використання 250 мг кверцетину з високою біодоступністю Кверцефіт™ порівняно з 500 мг «звичайного» кверцетину.
«Цинкова куля» для вірусів
У рейтингу засобів для запобігання ГРВІ, що наразі користуються шаленою популярністю серед пацієнтів, є й цинк. За даними ВООЗ, в Україні частота цинкодефіцитних станів становить близько 23%.
Іонний цинк давно вивчають як противірусний агент. Він має здатність блокувати два життєво важливі вірусні білки, необхідні для реплікації (в т. ч. SARS-CoV), – Plp2 та 3CL-протеазу. Вважається, що двовалентний цинк знижує сприйнятливість до вірусних інфекцій нижніх дихальних шляхів (а також у разі застосування >3 міс на рік полегшує їхній перебіг у дітей), оскільки забезпечує модулювальну дію на імунну систему та цілісність респіраторного епітелію при запаленні/ушкодженні легень.
Надходженню цинку в клітину сприяють хлорохін, кверцетин, епігалокатехін-3-галат (D’Andrea G., 2015).
Кверікс™: коли форма та вміст однаково важливі
Комплекс Кверікс® (Universe Pharm) поєднує два активні компоненти – кверцетин із високою біодоступністю Кверцефіт™ 250 мг (еквівалентно 85 мг чистого кверцетину у фітосомі) та цинку бісгліцинат 25 мг (еквівалентно 7 мг чистого цинку).
Це evidence-based, науково обґрунтована формула компонентів, у якій перспективні та відомі діючі речовини використовуються в інноваційній формі.
! Використання потужної комбінації кверцетину з високою біодоступністю Кверцефіт™ і цинку бісгліцинату забезпечує синергічну противірусну дію, імуномодулювальний ефект і позитивно впливає на респіраторну систему.
Комплекс Кверікс® дозволений для застосування дітям віком із 6 років. Рекомендується як засіб, який має імуномодулювальну дію та підвищує захисні сили організму. У рамках відповідей на запитання Інна Володимирівна повідомила, що рекомендована доза комплексу Кверікс® становить по 1 капсулі 1 р/день (діти віком від 6 років) і по 1 капсулі 2 р/день (дорослі).
Підготувала Олександра Марченко
Медична газета «Здоров’я України 21 сторіччя» № 24 (493), 2020 р.