30 листопада, 2023
Гіперурикемія за хронічної хвороби нирок: механізми та клінічні наслідки
Хронічна хвороба нирок (ХХН) є глобальною проблемою охорони здоров’я. Поступове зниження екскреторної функції нирок спричиняє затримку розчинених у воді мінералів і метаболітів. Одним із таких метаболітів є сечова кислота (СК) – продукт розпаду пуринових нуклеотидів. У міру зниження кліренсу СК при ХХН G3-5 стадії виникає гіперурикемія. Крім того, гіперурикемії сприяють інші чинники: генетичні варіанти транспортерів уратів, дієта та певні ліки, в т. ч. діуретики й імунодепресанти, які погіршують нирковий кліренс СК. Цікавий огляд H.-J. Anders, Q. Li та S. Steiger, опублікований в одному з останніх номерів Clinical Kidney Journal, продовжує дискусію щодо біологічної ролі СК, і надає відповідь на важливе терапевтичне запитання: коли та як лікувати пацієнтів із гіперурикемією на тлі ХХН.
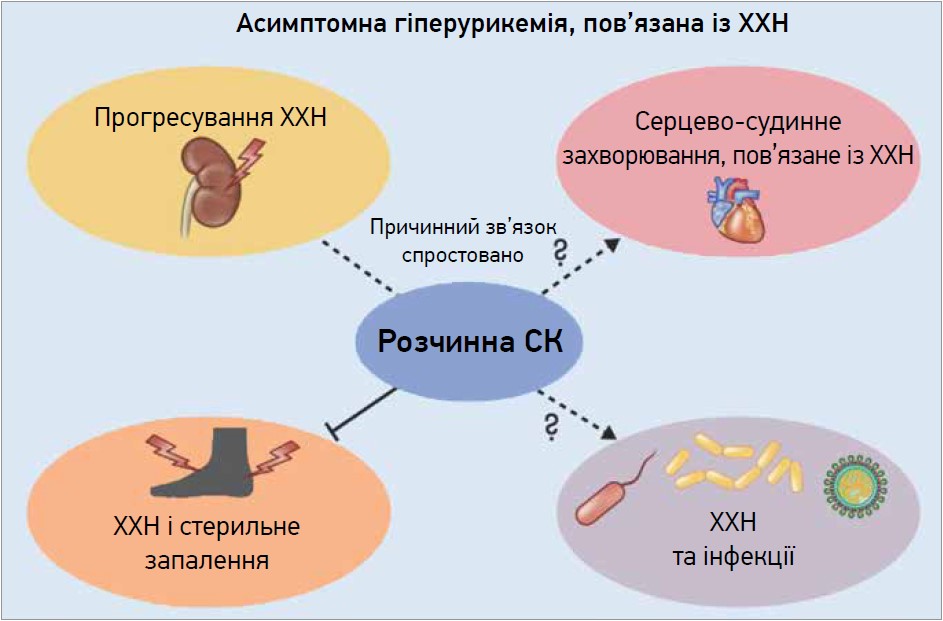
Гіперурикемія, що визначається як рівень СК >6,5 мг/дл у сироватці крові, має задокументовану причинну роль у розвитку подагричного артриту, гострої уратної нефропатії, сечокам’яної хвороби, тому пацієнтам із цими захворюваннями рекомендують уратознижувальну терапію (УЗТ). Автори звертають увагу на те, що в патогенезі всіх вищезазначених захворювань ключову роль відіграє саме кристалічна форма СК – кристали моноурату натрію. Натомість розчинна СК вивчається як потенційний фактор ризику для багатьох інших розладів, включаючи метаболічний синдром, серцево-судинні захворювання і гіпертензію, інфекції (здебільшого на основі епідеміологічних даних), які повідомляють про стійкий зв’язок цих станів із гіперурикемією (рис.).
Рис. Зв’язки розчинної СК та асимптомної гіперурикемії з різними захворюваннями
Асимптомна та симптомна гіперурикемія при прогресуванні ХХН
Гіперурикемія є поширеним станом серед пацієнтів із ХХН, що прогресує зі зниженням екскреторної функції нирок. Чи сприяє асимптомна гіперурикемія прогресуванню ХХН? Результати двох досліджень з менделівською рандомізацією не виявили причинно-наслідкового впливу гіперурикемії на швидкість клубочкової фільтрації (ШКФ) або ризик ХХН. Експериментальні дані з використанням нової моделі гіперурикемії на трансгенних тваринах також показали, що навіть виразна та стійка асимптомна гіперурикемія (рівень СК у сироватці >12 мг/дл) сама собою не спричиняє ураження нирок і не прискорює прогресування ХХН. Метааналіз потужних багатоцентрових рандомізованих досліджень, включаючи CKD-FIX і PERL, не підтвердив, що УЗТ затримує прогресування ХХН.
Зовсім інша ситуація виникає, коли СК випадає в осад у нирці. Кристалізація відбувається за рН сечі ≤5,5. Закисленню сечі сприяють різні фактори: стан дегідратації, літній вік, ожиріння, кислотне навантаження раціону (вживання продуктів із високим умістом фруктози, білка, пурину, наприклад червоного м’яса, морепродуктів, зернових), а також певні ліки, як-от пробенецид, сульфінпіразон, лозартан, бензбромарон і саліцилова кислота. Відкладення кристалів СК спричиняють тубулярну обструкцію, запалення, інфільтрацію та активацію макрофагів, інтерстиціальний фіброз, що в сукупності позначають терміном «хронічна уратна нефропатія». В цій ситуації гіперурикемія стає симптомною і загрожує ниркам. Сучасні наукові дані свідчать про те, що прогресуванню ХХН сприяє лише гіперурикемія із кристалурією СК. Отже, виявлення кристалів СК у сечі може слугувати додатковим діагностичним сигналом щодо того, чи потрібно пацієнтам із ХХН і гіперурикемією (але без олігоанурії) розпочинати УЗТ.
Коли та як лікувати гіперурикемію в пацієнтів із ХХН?
Наразі бракує якісних доказів, які б скеровували лікування подагри в пацієнтів із гіперурикемією та ХХН, оскільки з випробувань ліків від подагри зазвичай виключали пацієнтів із виразною нирковою дисфункцією. Мережа вивчення подагри, гіперурикемії та захворювань, пов’язаних із кристалами, в консенсусній заяві (2021) узагальнила деякі докази щодо того, як лікувати напади подагри, а також призначати УЗТ у пацієнтів із ХХН. Опубліковані дані про нестероїдні протизапальні препарати свідчать про потенційні побічні ефекти з боку нирок у людей із ХХН. Через порушення кліренсу колхіцину рекомендації щодо його застосування в разі ХХН залишаються переважно емпіричними. З іншого боку, кортикостероїди загалом вважаються безпечними для більшості людей із загостреннями подагри та супутньою ХХН. Інгібітори IЛ‑1 анакінра та канакінумаб не досліджувалися в пацієнтів із подагрою і ХХН. Але серії випадків і звіти про застосування виглядають обнадійливо. Дані показують, що кліренс анакінри безпосередньо пов’язаний із функцією нирок у людей без подагричного артриту та що препарат не виводиться за допомогою діалізу. Пацієнтам із ШКФ <30 мл/хв/1,73 м2 анакінру слід вводити через день. Канакінумаб є людським імуноглобуліном G із великим розміром молекули, тому очікується незначне його виведення нирками.
Зазвичай УЗТ для профілактики подагричного артриту слід обережно розглядати в пацієнтів із ХХН, оскільки її ефективність при ХХН знижується, а ризик побічних ефектів зростає. Стосовно інгібіторів ксантиноксидази відомо, наприклад, про підвищений ризик розвитку синдрому гіперчутливості до алопуринолу в пацієнтів із ШКФ <30 мл/хв/1,73 м2. Фебуксостат є прийнятнішим у пацієнтів із ХХН, оскільки він метаболізується здебільшого в печінці, а його екскреція здійснюється печінкою та нирками в співвідношенні практично 50/50.
У пацієнтів із термінальною ХХН діаліз певною мірою знижує рівень СК у сироватці крові, тому специфічна УЗТ більше не потрібна. Однак це не є загальним правилом, оскільки сироваткові концентрації СК можуть не досягати цільового рівня. Дані щодо застосування алопуринолу та фебуксостату в пацієнтів на діалізі обмежені звітами про окремі випадки та серії випадків. Алопуринол та його активні метаболіти ефективно діалізуються, тому алопуринол доцільно застосовувати після процедури. В будь-якому разі слід уважно підбирати дози інгібіторів ксантиноксидази під час лікування подагри в пацієнтів із ХХН і нирковою недостатністю через ризик виникнення реакцій гіперчутливості та раптових загострень подагри внаслідок швидкого зниження рівня СК у сироватці крові.
Як зазначалося вище, дослідження спростували причинно-наслідковий зв’язок між асимптомною гіперурикемією та прогресуванням ХХН. Утім, можна очікувати, що пацієнти із хронічною уратною нефропатією отримають користь від УЗТ.
Було проведено декілька клінічних випробувань для оцінки впливу УЗТ на серцево-судинні наслідки, серед яких вивчалися і ниркові кінцеві точки. Порівняльне дослідження фебуксостату проти алопуринолу FAST оцінювало вплив УЗТ на серцево-судинний ризик у пацієнтів із подагрою та не виявило доказів підвищення смертності при застосуванні фебуксостату порівняно з алопуринолом протягом середнього періоду спостереження 48 міс. Смертність від усіх причин в абсолютному вираженні була навіть нижчою в групі фебуксостату: 3,5 проти 5,7% у групі алопуринолу (відносний ризик 0,75; 95% довірчий інтервал від 0,59 до 0,95). У дослідженні CARES ризик серцево-судинних подій не відрізнявся в пацієнтів із нормальним, легким або помірним порушенням функції нирок, які отримували фебуксостат або алопуринол. Окрім того, в дослідженні FREED повідомлялося про зниження частоти церебральних, серцево-судинних і ниркових подій у групі лікування фебуксостатом (23,3%) порівняно із групою без нього (28,7%) протягом середнього періоду спостереження 35 міс (p=0,02); цей результат зумовлювався здебільшого зменшенням випадків погіршення протеїнурії.
Висновки
Експериментальні та клінічні дані свідчать про те, що асимптомна гіперурикемія є наслідком прогресування ХХН.
Симптомна гіперурикемія через кристалізацію СК спричиняє хронічну уратну нефропатію, яка згодом прогресує до термінальної ХХН.
У пацієнтів із ХХН фебуксостат має переваги завдяки фармакокінетичним властивостям, здатності знижувати кардіоваскулярний ризик і загальну смертність.
Підготував Ігор Петренко