25 червня, 2021
Оптимізація лікування болю: фокус на спондилоартрит
.jpg) Першим проявом спондилоартриту (СпА) є звичайний біль у спині, з яким багато хто живе роками, не приділяючи проблемі належної уваги. Через це хворобу часто виявляють на пізній стадії, коли в організмі вже сталися незворотні зміни. Тому дуже важливо вчасно поставити правильний діагноз і допомогти пацієнтам зберегти звичну якість життя, зокрема за рахунок використання похідних колагену, які можуть бути доречною стратегією у веденні пацієнтів зі СпА. Свої міркування з цього приводу висловила під час школи-семінару «Клініко-практичні аспекти в сучасній неврології» (3 березня 2021 року) професорка кафедри неврології № 1 Національного університету охорони здоров’я імені П.Л. Шупика (м. Київ), д. мед. н. Тетяна Миколаївна Слободін.
Першим проявом спондилоартриту (СпА) є звичайний біль у спині, з яким багато хто живе роками, не приділяючи проблемі належної уваги. Через це хворобу часто виявляють на пізній стадії, коли в організмі вже сталися незворотні зміни. Тому дуже важливо вчасно поставити правильний діагноз і допомогти пацієнтам зберегти звичну якість життя, зокрема за рахунок використання похідних колагену, які можуть бути доречною стратегією у веденні пацієнтів зі СпА. Свої міркування з цього приводу висловила під час школи-семінару «Клініко-практичні аспекти в сучасній неврології» (3 березня 2021 року) професорка кафедри неврології № 1 Національного університету охорони здоров’я імені П.Л. Шупика (м. Київ), д. мед. н. Тетяна Миколаївна Слободін.
«Порочне коло» патогенетичних механізмів
Ураження фасеткових суглобів може спостерігатися у поєднанні з іншими проявами, зокрема дискогенними і м’язово-тонічним синдромами, а також маніфестувати болем у спині.
Спікерка виділила такі причини неспецифічного болю у спині, як (Balague et al., 2012):
- Залучення мязів: м’язово-тонічний синдром, міофасціальний синдром.
- Спондилоартропатія (фасетковий синдром): проявляється у вигляді рефлекторних больових синдромів та функціонального блокування фасеткових суглобів.
- Патологія міжхребцевого диска з/без корінцевого ураження: рефлекторні та компресійні синдроми.
У більшості випадків до больових синдромів залучаються усі структури хребтово-рухового сегмента. Виникає «порочне коло» патогенетичних механізмів (рис. 1).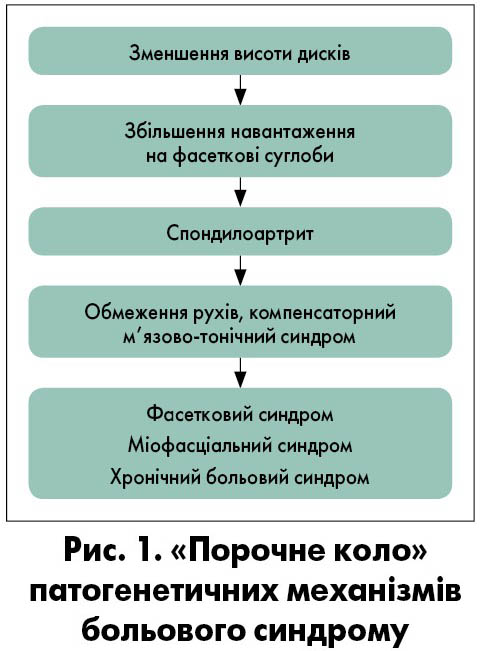
Критеріями фасеткового синдрому є:
- згладженість поперекового та шийного лордозу;
- ротація або викривлення хребта при рентгенографічних дослідженнях;
- початок болю, пов’язаний із ротацією та розгинанням хребта;
- біль має латералізований або дифузний характер, іррадіація болю йде не нижче коліна;
- характерні ранкова скутість і біль після відпочинку;
- біль посилюється у статичних положеннях, розминка хребта його зменшує;
- наявний симптом «пружинення»;
- терапія ex juvantibus: блокада з анестетиками.
Ураження фасеткових суглобів може бути першопричиною больового синдрому. Зокрема, фасеткові суглоби шийного відділу несуть 17% навантаження на спину, в шиї вони відіграють роль похилих площин, що уможливлюють рухи шиї вперед та назад. Фасеткові суглоби поперекового відділу є масивнішими, орієнтовані під кутом, при цьому верхня частина ніби «вкладена як у гніздо» в нижню. Вони стабільніші проти ротації та чинять опір вертикальній компресії. Меніски нагадують меніски коліна, тому всі лікарські засоби, що використовують для великих суглобів, підходять і для фасеткових.
Патогенетичною основою для формування фасеткового синдрому є:
- дегенерація диску (дегідратація, зниження висоти);
- зношення суглоба, запалення, розростання кісткових крайових тканин, звуження суглобової щілини;
- наявність дегенеративних змін може не призводити до больового синдрому, поки не з’являться додаткові чинники.
Коли відсутня впевненість у тому, що саме викликає больовий синдром, здійснюють діагностично-лікувальну блокаду фасеткового суглоба (виключно під відеонаглядом). При цьому 50‑65% хворих відчувають зменшення больового синдрому, а період поліпшення може тривати 2‑3 місяці. Якщо біль не зменшується, повторну блокаду робити не варто.
Якщо ситуація не поліпшується, проводять блокаду та радіочастотну абляцію медіальної гілки чутливого нерва. Існують суперечливі думки щодо зазначених процедур, але інколи їхнє застосування є вимушеним. При цьому відбувається зменшення больового синдрому. Однак дані методи не впливають на стан фасеткових суглобів та прогресування артриту, не сприяють зменшенню тиску на міжсуглобову щілину, а отже й відновленню рухів.
Ведення пацієнтів із болем у спині
Відповідно до сучасних настанов щодо ведення пацієнтів із болем у нижній частині спини, необхідно стратифікувати рівень ризику і прогноз. Це можна зробити, наприклад, за допомогою шкали STarT Back для виявлення груп пацієнтів із меншою ймовірністю швидкого відновлення для призначення інтенсивнішої терапії (Lenahan et al., 2018).
Як зауважила Т.М. Слободін, довготривале лікування передбачає виконання спеціальних фізичних вправ, спрямованих на покращення стану пацієнтів, протягом 15 хв на день упродовж місяців. Передусім це вправи на згинання, що поліпшують кровообіг та трофіку, а також зменшують навантаження на суглоби. Крім того, необхідною є підтримка загальної фізичної активності (кардіонавантаження по 30 хв чотири рази на тиждень), а також протизапальна терапія.
Основними компонентами неінвазивного лікування для всіх пацієнтів із болем у спині та ішіасом мають бути вправи на розтягнення, аеробіка, йога тощо. Мануальна терапія та психологічні підходи рекомендовані тільки разом із фізичними заняттями, тоді як голковколювання чи електротерапія не рекомендовані.
Доцільним може виявитися короткий курс нестероїдних протизапальних препаратів (НПЗП) або слабких опіоїдів (якщо НПЗП неефективні або погано переносяться). За наявності невропатичного болю необхідно розглянути можливість призначення габапентиноїдів та епідуральні блокади зі стероїдами при ішіасі.
Не рекомендовано використовувати парацетамол у монотерапії при болю в нижній частині спині, а опіати – при хронічному болю у спині.
Інноваційний препарат неденатурованого колагену ІІ типу
Хондропротектори привернули до себе увагу в першу чергу при лікуванні уражень великих суглобів. Проте ефект цих препаратів можна екстраполювати на ушкодження будь-яких інших суглобів. У короткостроковій перспективі (≤3 місяців) більшість хондропротекторів продемонстрували переконливі терапевтичні результати. За тривалості терапії 3‑6 місяців більшість клінічних наслідків не були кращими за плацебо. Натомість при застосуванні неденатурованого колагену ІІ типу (UC‑II) мало місце суттєве поліпшення стану хворих із плином часу.
UC‑II (в Україні має назву Меркана) – інноваційний хондропротектор, який був розроблений та запатентований у США. Застосування UC-II дозволяє покращити стан пацієнтів з ураженням суглобів, як на початку терапії, так і протягом всьго часу використання. На відміну від денатурованого (гідролізат), неденатурований колаген є нативним: він ініціює каскад імунних реакцій, усуваючи запальний процес у суглобі та активуючи процес відновлення хрящової тканини.
У шлунково-кишковому тракті неденатурований колаген II типу (UC-II) захоплюється пеєровими бляшками та контактує з неспеціалізованими Т‑лімфоцитами, перетворюючи їх на спеціалізовані регуляторні Т‑лімфоцити (T-регулятори), які, зі свого боку, починають синтезувати протизапальні фактори – інтерлейкін‑10 (ІЛ‑10), трансформуючий фактор росту β (ТФР-β) тощо, які своєю чергою впливають на уражений хрящ. Зокрема, Т-регулятори з системного кровотоку потрапляють у капіляри синовіальної мембрани, а синтезовані ними цитокіни (ІЛ‑10, ТФР-β) опиняються у синовіальній рідині, де і починають діяти. Під впливом ІЛ-10 як потужного протизапального цитокіну відбувається пригнічення синтезу ІЛ-1 та фактора некрозу пухлин (ФНП), які змушують хондроцити виділяти агресивні ферменти – матриксні металопротеїнази (колагеназу та ін.) й оксид азоту, що беруть участь в руйнації хрящової тканини суглоба. ТФР-β як потужний хондропротекторний цитокін стимулює синтез хондроцитами компонентів матриксу хряща: колагену, хондроїтину сульфату (який входить до складу агрекану – основного елемента міжклітинного матриксу хряща) та гіалуронової кислоти.
У багатоцентровому рандомізованому подвійному сліпому плацебо-контрольованому дослідженні вивчали ефективність та переносимість UC‑II у пацієнтів із болем при остеоартриті (ОА) колінного суглоба і пов’язаними з ним симптомами порівняно із комбінацією глюкозаміну гідрохлориду / хондроїтину сульфату (Г+Х) та плацебо (Lugo et al., 2016). Пацієнти (n=191) були рандомізовані на три групи для отримання UC‑II (40 мг/добу), Г+Х (1500 та 1200 мг/добу глюкозаміну й хондроїтину відповідно) або плацебо протягом 180 днів. Первинною кінцевою точкою була зміна індексу виразності ОА за WOMAC від вихідного рівня до 180-го дня для групи UC‑II порівняно із Г+Х та плацебо. Вторинні кінцеві точки включали показники функціонального індексу Лекена (LFI), візуальної аналогової шкали (ВАШ) для оцінки болю і субшкал WOMAC.
На 180-й день у групі UC‑II було продемонстроване значне зменшення загального бала за WOMAC порівняно із плацебо (p=0,002) та Г+Х (p=0,04). Вживання UC‑II також сприяло значущим змінам за всіма трьома підшкалами WOMAC (як-то біль, скутість, фізична функція). Також на тлі застосування UC‑II було досягнуте зниження потреби у знеболювальних препаратах на 61%. Ефективність комбінації Г+Х через шість місяців лікування не відрізнялася від плацебо, тоді як UC‑II достовірно сприяв знеболюванню та поліпшував функції (на 41% та 36% дієвіше, ніж Г+Х відповідно). Водночас результати щодо безпеки були зіставними між групами.
Таким чином, дослідники дійшли висновку, що вживання UC‑II (в Україні має назву Меркана) сприяло зменшенню проявів ОА колінного суглоба. UC‑II добре переносився і був достовірно ефективнішим, ніж Г+Х, за показниками шкали WOMAC.
Окрім того, пероральне застосування UC‑II зменшувало погіршення стану суглобового хряща в експериментальній моделі ОА колінного суглоба у лабораторних тварин (рис. 2). Вживання UC‑II запобігало дегенеративним змінам у хрящовій тканині суглоба та утворенню остеофітів (Bagi et al., 2017).
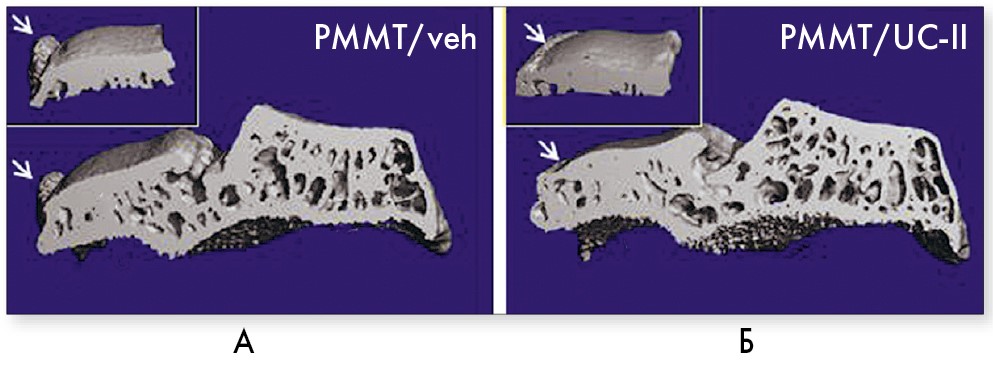 Рис. 2. Комп’ютерне 3D-зображення епіфізу великогомілкової кістки: А – без лікування, Б – ефект UC‑II (хондропротектора Меркана)
Рис. 2. Комп’ютерне 3D-зображення епіфізу великогомілкової кістки: А – без лікування, Б – ефект UC‑II (хондропротектора Меркана)
Примітки: Стрілки вказують на ступінь остеофітів; у верхніх лівих кутах – вид зверху на медіальне плато.
Адаптовано за С.М. Bagi et al., 2017
Висновки
Загалом натепер не існує хворобомодифікуючих засобів для лікування ОА, а застосування традиційних препаратів пов’язане із проблемами щодо безпеки (Honvo et al., 2020). Тому триває пошук альтернативних підходів, до яких належить застосування похідних колагену. Важливим аспектом є те, що вживання похідних колагену є безпечним для пацієнтів з ОА, що підтверджено лабораторними дослідженнями з перевірки токсичності. На думку професорки, отримані результати дозволяють припустити, що використання похідних колагену може бути переконливою стратегією у веденні пацієнтів з ОА та СпА.
Одна капсула хондропротектора Меркана містить 40 мг хрящового неденатурованого (натурального) колагену (UC‑II), вживання якого сприяє нормалізації функціонального стану суглобів, зокрема при фізичному навантаженні, зменшенню скутості суглобів, поліпшенню їхньої рухливості та гнучкості.
Меркана характеризується зручною схемою прийому (1 капсула на добу ввечері принаймні через дві години після їжі) та здатна чинити протизапальний ефект без додаткового призначення НПЗП.
При станах, що пов’язані з дегенеративним ураженням суглобів (ОА, СпА тощо), щоденне вживання капсул Меркани протягом тривалого часу сприяє усуненню запалення, знеболенню, відновленню хрящової тканини та поліпшенню функції суглобів.
Підготувала Олександра Демецька
Тематичний номер «Неврологія, Психіатрія, Психотерапія» № 2 (57) 2021 р.



