7 травня, 2023
Герпесвірусні інфекції: можливості системної терапії
Герпетичні вірусні інфекції (ГВІ) – група вірусних захворювань, що вражають не лише шкіру та слизові оболонки людини, але також центральну нервову систему й внутрішні органи, викликаючи латентну, гостру та хронічну форми інфекції, що потребує системного лікування. Нині відомо про більш ніж 100 герпесвірусів, серед яких для людини патогенними є вісім вірусів.
Віруси герпесу належать до ДНК-вмісних. За даними глобального огляду результатів досліджень, захворюваність на ці інфекції збільшуються з віком, а найвищою частота вперше інфікованих є серед підлітків (Kimberlin, 2005). Незалежно від того, яким шляхом вірус потрапляє до організму людини, початкове його розмноження відбувається у так званих вхідних воротах, якими найчастіше є слизові оболонки; далі він проникає до регіонарних лімфовузлів, потім у кров, із якою розноситься по внутрішніх органах (Danaher, 2006). Захворювання нервової системи може поєднуватися з ураженням інших органів і систем або мати ізольований перебіг. Джерело збудника інфекції – хвора людина або вірусоносій. Чинниками активації інфекції є травми слизових оболонок, шкіри, тривале перебування на сонці, переохолодження, перегрівання організму, зловживання алкоголем, наркотиками, емоційне виснаження, перенесені інші інфекції (Андрєєва та ін., 2020). Після первинного інфікування ГВІ пожиттєво персистують в організмі, а на тлі імунної недостатності можлива їх реактивація (Steiner et al., 2007).
Первинне зараження зазвичай супроводжується латентністю вірусу, а вірусні реактивації мають більш виразну симптоматику, ніж первинні інфекції, і частіше потребують медичної консультації. У повсякденній практиці здебільшого фіксують інфекції, зумовлені вірусом простого герпесу (Herpes simplex, ВПГ) і вірусом вітряної віспи (Varicella zoster virus, ВЗВ). Якщо первинні інфекції ВПГ клінічно маніфестують у вигляді характерних системних симптомів, то реактивації інфекції ВПГ зазвичай є нетяжкими, самообмежувальними та мають вигляд згрупованих герпетиформних везикул на еритематозній основі. Тоді як первинна інфекція ВЗВ призводить до клінічної картини вітряної віспи, а реактивація виявляється як оперізувальний лишай (оперізувальний герпес, ОГ) і може супроводжуватися сильним гострим невралгіформним болем. В осіб із імуносупресією можливі ускладнені прояви (зокрема, некротичні, виразкові, геморагічні, генералізовані) (Wilms et al., 2022).
Вірус простого герпесу людини
Віруси простого герпесу поділяють на два підтипи: простого герпесу типу 1 (ВПГ‑1); простого герпесу типу 2 (ВПГ‑2). Як правило, ВПГ‑1 вражає шкіру та слизові оболонки порожнини рота, ВПГ‑2 – слизові оболонки статевих органів. Проте ВПГ‑1 виявляють також і за генітального герпесу (Knox et al., 2011). За даними дослідження Всесвітньої організації охорони здоров’я, 2016 року поширеність ВПГ‑1 у світі становила 66,6% населення віком до 49 років; ВПГ‑2 –13,2% осіб віком 15‑49 років (James et al., 2020).
Генітальний герпес є інфекцією, що передається статевим шляхом; його можуть викликати і ВПГ‑1, і ВПГ‑2. Клінічній картині генітального герпесу притаманне виникнення болючих пухирців на еритематозному тлі місця інфікування. Ці ураження можуть виразкуватися з подальшим прогресуванням. Первинна інфекція здебільшого супроводжується гострими загальними симптомами (лихоманка, сильний біль, лімфаденіт). Також можуть виникати атипові ураження, які легко сплутати з іншими генітальними дерматозами, тому для діагностування беруть мазок з ураженої ділянки слизової оболонки (Wilms et al., 2020).
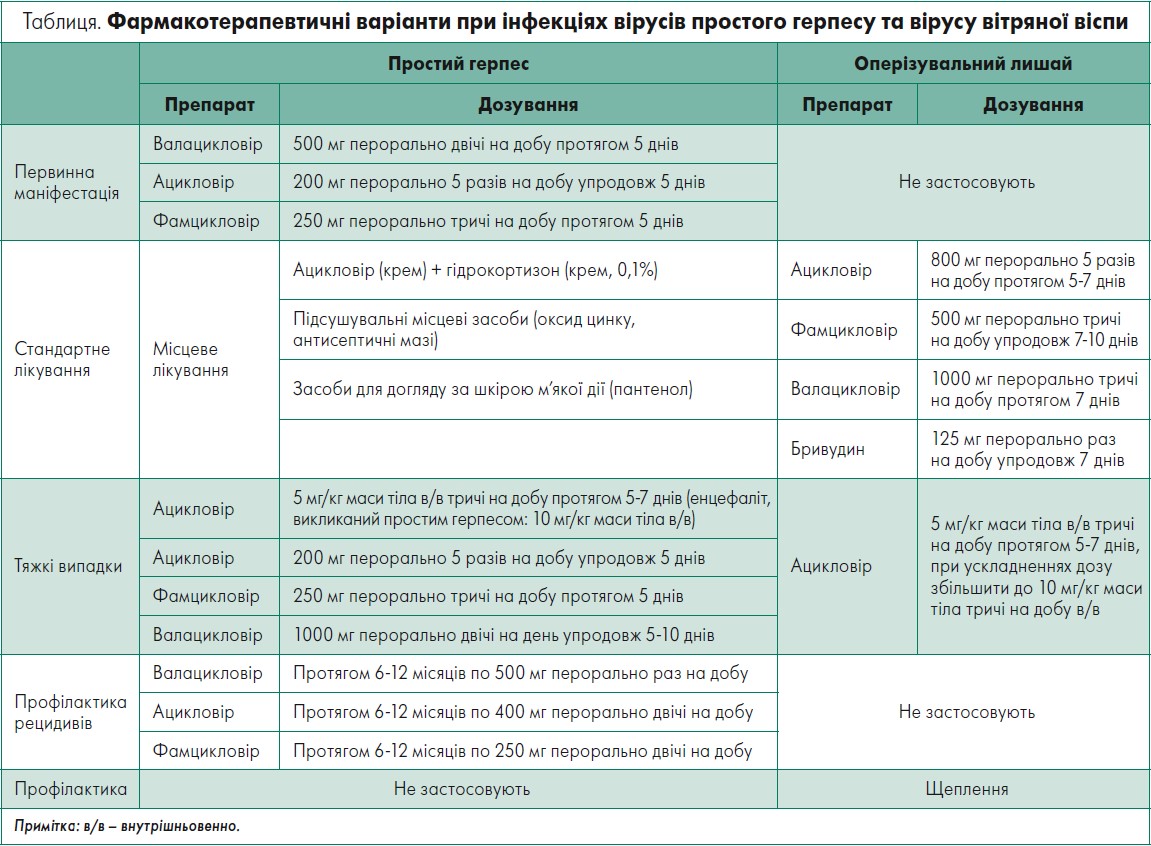
Неускладнену первинну інфекцію простого герпесу лікують місцево вірусостатичними або антисептичними засобами (Gupta et al., 2014). Системне лікування пероральними вірусостатиками є однаковим для інфекції ВПГ‑1 та ВПГ‑2, однак воно потребує корекції залежно від індивідуальних ускладнень. За системного лікування ВПГ-інфекцій застосовують противірусні препарати, як-от ацикловір, валацикловір або фамцикловір (табл.).
Ацикловір – вірусостатичний засіб із групи нуклеозидних аналогів, що поглинається клітиною як проліки та перетворюється на ацикловіру трифосфат, убудовується в ДНК вірусу під час її синтезу і згодом призводить до розриву ланцюга під час реплікації (Wilms et al., 2020). Валацикловір є попередником ацикловіру, який швидко і майже повністю перетворюється на ацикловір і L-валін у кишечнику та печінці; це підвищує біодоступність до 54%, тому валацикловір потрібно вводити рідше. Фамцикловір також є проліками, які метаболічно перетворюються на пенцикловір. Справжнім вірусостатичним агентом є пенцикловіру фосфат, для якого продемонстровано такий самий механізм дії, що й для цикловіру, у клітинах, інфікованих вірусом герпесу (Shiraki, 2018).
Фамцикловір має довший період напіввиведення, ніж цикловір, тому лікування цим препаратом потребує менше дозувань на добу (табл.). У разі застосування трьох згаданих препаратів слід враховувати функцію нирок пацієнта, оскільки всі вони виводяться нирками в незмінному вигляді (Hara et al., 2008).
Вірус герпесу людини 3 типу, або вірус вітряної віспи
Зазвичай первинне зараження ВЗВ відбувається в дитинстві через краплинну інфекцію або прямий контакт. У латентний період вірус зберігається в спинномозкових гангліях заднього рогу. Після інфікування вірус розмножується в епітеліальних клітинах дихальних шляхів, що призводить до вірусемії з розвитком типової екзантеми та енантеми. Такі пацієнти можуть заражати інших за кілька днів до появи типових пухирців. Як тільки везикули висихають і утворюються кірочки, ймовірність зараження стає набагато меншою (Plewig et al., 2018).
Вітряна віспа, як правило, є самообмежувальною хворобою, яка переноситься спонтанно. Для підсушування пухирців та запобігання бактеріальній суперінфекції можна застосовувати місцеві засоби (оксид цинку, антисептики). Системне противірусне лікування рекомендоване за тяжкого перебігу, імуносупресії, новонародженим і вагітним (Plewig et al., 2018; Salavastru et al., 2022). ОГ є результатом реактивації вірусу вітряної віспи, що призводить до нейро- та епідермотропного поширення на поверхні шкіри із залученням однієї або кількох дерматом (ділянок шкіри, іннервованих волокнами від певної пари спинномозкових нервів). Захворюваність на ОГ зростає з віком, але загалом можуть хворіти пацієнти всіх вікових груп (Koshy et al., 2018). Відповідно до систематичного огляду, опублікованого 2014 року, захворюваність на ОГ становить 3‑5 випадків на 1 тис. пацієнто-років (Kawai et al., 2014). Локалізований біль в ураженій дерматомі іноді супроводжується неспецифічним загальним нездужанням (Gross et al., 2020). Після продромальної стадії з’являються групи пухирців на еритематозному тлі, найчастіше на грудній клітці або в ділянці трійчастого нерва (залежно від ураженої гілки нерва, можуть бути також уражені органи чуття, розташовані у відповідній дерматомі). Рідко виникають енцефаліт або менінгіт, пов’язані з ОГ. Однак відповідні клінічні ознаки з менінгізмом і сплутаністю свідомості мають викликати підозру на оперізувальний енцефаліт (Herlin et al., 2021).
Терапія ОГ охоплює три основні компоненти: 1) противірусні заходи; 2) полегшення болю; 3) лікування можливих ускладнень. Для противірусного лікування ОГ як засоби першої лінії схвалено ацикловір, валацикловір, фамцикловір, бривудин. Противірусні заходи слід починати негайно, в ідеалі протягом 72 год після появи перших симптомів.
Фамцикловір – ефективний противірусний засіб
Як зазначалося, фамцикловір є проліками противірусного засобу. Він модифікується естеразою та оксидазою, які перетворюють його на активний противірусний агент пенцикловір. Окрім лікування гострого ОГ, губного герпесу, первинних і рецидивних епізодів генітального герпесу в імунокомпетентних та ВІЛ-інфікованих пацієнтів, він є засобом для супресивної терапії генітального герпесу. Доведено, що фамцикловір може знижувати рівень ДНК вірусу гепатиту В у пацієнтів за довгострокового лікування. Застосування цього препарату сприяє підвищенню комплаєнсу пацієнтів і полегшенню лікування ОГ, оскільки фамцикловір потрібно приймати лише тричі на добу, на відміну від інших ліків, які використовували раніше. За оральних герпетичних інфекцій фамцикловір необхідний лише як однодозова терапія, що також полегшує лікування і сприяє кращому комплаєнсу (Gopal et al., 2013; Semaan et al., 2023).
Ефективність терапії фамцикловіром підтверджено у низці досліджень. Так, порівняльне рандомізоване контрольоване дослідження оцінювання ефективності валацикловіру та фамцикловіру в лікуванні ОГ засвідчило, що у групі терапії фамцикловіром частки пацієнтів, які повідомляли про легкий, помірний або сильний біль, становили 0, 63,9 і 30,6% на 7-й день відповідно. У групі лікування валацикловіром мали такі показники: 1, 69 і 12,33% пацієнтів відповідно. Обидва втручання були ефективними й безпечними. Фамцикловір порівняно з валацикловіром продемонстрував значну перевагу щодо повного припинення болю, пов’язаного з ОГ (Mustafa et al., 2022).
Метааналіз даних щодо ефективності та безпеки противірусних препаратів у різних дозуваннях при ОГ підтвердив, що ацикловір (800 мг 5 разів на добу), валацикловір (900‑1000 мг тричі на добу) та фамцикловір (250 мг тричі на добу) є кращими схемами противірусного лікування. Серед переваг лікування фамцикловіром – нижче дозування та менша кількість приймань на добу, що сприяє кращому комплаєнсу (Deng et al., 2022).
Біль є основним симптомом ОГ, а постгерпетична невралгія (ПГН) – тривалий нестерпний біль – чинить серйозний вплив на якість життя пацієнтів, а також є складною проблемою для клініцистів. Раннє противірусне лікування вважається ключовим заходом для зменшення гострого болю та ПГН. У більшості пацієнтів біль не припиняється після 7 днів противірусного лікування, а в деяких розвивається ПГН. J. Kong et al. (2022) мали на меті визначити, чи може більша тривалість противірусної терапії сприяти зменшенню гострого болю при ОГ і виникненню ПГН. Порівняно з традиційною 7-денною противірусною терапією 14-денний курс лікування фамцикловіром сприяв зменшенню гострого болю й частоти розвитку ПГН у літніх пацієнтів із ОГ, особливо в осіб із помірним або сильним початковим болем. Подовження курсу лікування не призвело до посилення побічних ефектів. Найпоширеніші побічні ефекти фамцикловіру – головний біль, нудота й діарея. Серйозніші побічні реакції після лікування фамцикловіром, як-от гепатотоксичність і синдром Стівенса–Джонсона, виникають рідко. Зокрема, не виявлено суттєвих ознак того, що збільшення дози фамцикловіру спричиняє більше побічних ефектів (NIDDK, 2018).
Сьогодні на вітчизняному фармацевтичному ринку доступний препарат фамцикловіру Віростат® виробництва АТ «Київський вітамінний завод» (біоеквівалентність засобу доведено; він виробляється із субстанції, синтезованої в Європі, відповідно до стандартів належної виробничої практики [GMP]). Препарат випускається у формі таблеток, що містять по 250 і 500 мг фамцикловіру. Показаннями до його застосування є інфекції, спричинені вірусами Herpes simplex і Varicella zoster, насамперед генітальний герпес і оперізувальний лишай.
Висновки
Герпесвірусні інфекції є одними з найпоширеніших, вражаючи всі органи й системи організму людини. Для системного лікування цих інфекцій нині успішно застосовують противірусні препарати, одним із яких є фамцикловір. Препарат ефективний при інфекціях, збудниками яких є віруси простого герпесу (зокрема, генітального герпесу), а також вірус вітряної віспи (зокрема, оперізувальний лишай). Терапія фамцикловіром є безпечною, сприяє зменшенню болю та поліпшенню комплаєнсу.
Підготувала Наталія Купко