13 січня, 2024
Неврологічні захворювання та вітамінодефіцитні стани: чи все нам відомо?
За матеріалами Міжнародної неврологічної конференції «ХV Нейросимпозіум»
(12‑15 вересня 2023 р., Львів, Україна)
У вересні поточного року Львів приймав учасників Міжнародної неврологічної конференції «ХV Нейросимпозіум», яка розпочала осінній освітній неврологічний сезон. У межах заходу, що проходив у змішаному форматі (офлайн і онлайн), відбувся сателітний симпозіум, під час якого учасники обговорювали актуальну проблему – зв’язок неврологічних порушень і вітамінодефіцитних станів.
Сьогодні добре відомо про важливу біологічну роль вітамінів для функціонування організму людини, зокрема через їхню залученість до процесів, що відбуваються на клітинному рівні. Нині описано 13 різних типів вітамінів, класифікованих за біологічною та хімічною активністю, які поділяють на дві великі групи: водо- та жиророзчинні вітаміни. Водорозчинні, як-от вітаміни групи В (В1, В2, В3, В5, В6, В8, В9, В12) і вітамін С, на відміну від жиророзчинних, не зберігаються в організмі, тому є потреба в щоденному їх споживанні. Вітамінний статус організму людини залежить від багатьох чинників. Різний доступ до адекватного харчування і медичної допомоги зумовлює значні відмінності щодо її дефіцитного статусу в країнах із низьким / високим рівнем доходу.
 Погляд невролога на взаємозв’язок клінічних ознак і дефіциту вітамінів групи В, особливі стани, спричинені вітамінодефіцитами та практичні шляхи діагностичного пошуку представила у своїй доповіді д.мед.н., професорка кафедри неврології № 1 Національного університету охорони здоров’я України імені П. Л. Шупика (м. Київ) Тетяна Миколаївна Слободін.
Погляд невролога на взаємозв’язок клінічних ознак і дефіциту вітамінів групи В, особливі стани, спричинені вітамінодефіцитами та практичні шляхи діагностичного пошуку представила у своїй доповіді д.мед.н., професорка кафедри неврології № 1 Національного університету охорони здоров’я України імені П. Л. Шупика (м. Київ) Тетяна Миколаївна Слободін.
– Як зазначила пані Слободін, лікар будь-якої спеціальності у своїй практиці стикається з явищем полінейропатії. Для цього стану характерне симетричне ураження периферичної нервової системи, що зазвичай спричинює сенсорний, моторний та/або вегетативний дефіцит. Через неоднорідність причин етіологічна діагностика полінейропатії є доволі складним процесом (Ducci, 2022).
Чинниками, що призводять до полінейропатії, можуть бути цукровий діабет (ЦД), зловживання алкоголем, генетичні захворювання, дефіцит харчування, токсичність ліків, аутоімунні причини, інфекції та злоякісні новоутворення (Pasnoor, 2013; Felix, 2010).
За даними різних країн світу, найбільшу частку (30‑66%) серед причин периферичної полінейропатії становить ЦД (England, 2004). Тоді як від 20 до 46% випадків причин полінейропатії лишаються неуточненими (ідіопатичні нейропатії). Серед них значна кількість, ймовірно, пов’язана з дефіцитом вітамінів групи В. Діабетична периферична полінейропатія є найпоширенішим захворюванням периферичних нервових волокон, однак не всі пацієнти із ЦД та полінейропатією можуть мати діабетичну полінейропатію (Freeman et al., 2009).
Так, за різним даними, у 10‑50% пацієнтів із діабетом є додаткові причини, що можуть призводити до розвитку полінейропатії, наприклад нейротоксична дія медикаментів, метаболічний синдром, ниркова недостатність, хронічна демієлінізуюча полінейропатія, зловживання алкоголем та дефіцит вітаміну В12. Дефіцит В12 може бути спричинений шлунково-кишковими захворюваннями, як-от гастрит, синдром мальабсорбції, целіакія, хвороба Крона, панкреатит, застосуванням препаратів для лікування захворювань ШКТ, що блокують абсорбцію В12 (приймання антагоністів Н2-рецепторів або інгібіторів протонної помпи >12 міс.), нераціональною харчовою дієтою, алкоголізмом, спадковим дефіцитом транскобаламіну, резекцією шлунка (Langan, 2011).
Згідно з настановами Американського товариства метаболічної та баріатричної хірургії (ASMBS, 2017) пацієнтам, які перенесли баріатричне хірургічне втручання, рекомендовано приймати перорально 1 мг вітаміну В12 пожиттєво (Parrott et al., 2017).
Особливої уваги потребують пацієнти, які отримують метформін за терапії ЦД. Гіповітаміноз B12 нині вважається поширеною побічною реакцією у пацієнтів, які приймають метформін, особливо у тих, хто лікується вищими його дозами або така терапія триває >4 місяці.
Вважається, що механізм цього явища є мультифакторним: зміна моторики кишківника, підвищення інтестинальної концентрації глюкози (що призводить до надмірного бактеріального росту та мальабсорбції), а також інгібування всмоктування комплексу вітаміну В12 та внутрішнього фактора Касла (спричиняють дефіцит цього вітаміну) (Bauman et al., 2000).
Американська діабетична асоціація (ADA, 2022) наголошує, що через зв’язок біохімічного дефіциту вітаміну В12 із тривалим застосуванням метформіну слід регулярно виконувати моніторинг у цій когорті пацієнтів. Нині немає ідеального тесту для визначення вітамінодефіциту, тому клінічний стан пацієнта та його анамнез мають найважливіше значення під час встановлення діагнозу.
У разі ізольованих неврологічних симптомів, причину яких неможливо встановити, слід розглядати діагноз дефіциту вітамінів групи В, оскільки неврологічні порушення можуть прогресувати і стати незворотними. Пацієнти з такими станами отримають користь лікування, навіть якщо неможливо встановити чіткий діагноз дефіциту або виявлено лише субоптимальний рівень вітамінів («граничний дефіцит») (Pfeiffer, 2009; David Smith, 2012). Це також підтверджують дані дослідження M. Hakim et al. (2018), у якому пацієнти з периферичною полінейропатією різної етіології отримували вітаміни групи В (зокрема, В1, В6 і В12) у високих дозах протягом 90 днів без попереднього визначення їхніх рівнів. Завдяки лікуванню пацієнти відчули прогресуюче полегшення стану, зменшення таких симптомів, як біль, печіння, парестезії та оніміння.
Різноманітність нейропсихіатричних змін спостерігають також і через дефіцит фолієвої кислоти. Крім ознак полінейропатії, у таких пацієнтів можуть виникати депресивні розлади, дратівливість, безсоння, когнітивне уповільнення, забудькуватість, деменція, психотичні розлади, екстрапірамідні порушення (Langan, 2011).
Доцільно перевіряти рівень дефіциту вітаміну В12 у пацієнтів із недостатністю фолієвої кислоти, оскільки це може мати очевидну позитивну реакцію на приймання добавок фолієвої кислоти з нормалізацією гематологічних показників. Однак застосування фолієвої кислоти не може чинити впливу на неврологічні порушення, спричинені дефіцитом вітаміну В12, що, своєю чергою, зумовлюватиме їх незворотне прогресування в разі корекції виключно нестачі фолієвої кислоти без додаткового призначення вітаміну В12.
Дефіцит вітаміну В12 зазвичай розвивається протягом багатьох років, оскільки загальних запасів в організмі в багатьох випадках достатньо для забезпечення адекватного рівня вітаміну впродовж 5‑10 років. У разі легкого та помірного дефіциту В12 розвивається макроцитарна та мегалобластна анемія, що може супроводжуватись слабкістю, задишкою, відчуттям прискореного серцебиття. Проте, якщо В12-дефіцитна анемія є зворотним явищем, симптоми полінейропатії, яка виникає внаслідок тяжкого дефіциту цього вітаміну, навпаки, можуть призводити до незворотних процесів в організмі людини.
Початкова двобічна периферична нейропатія може прогресувати до дегенерації аксонів, і якщо не призначати лікування вітамінодефіциту – спричиняти загибель нейронів. На початку захворювання може виникнути порушення пропріоцепції, вібраційного відчуття та арефлексії. Такі пацієнти скаржаться на незграбність, погану координацію і труднощі під час ходи. Без належного лікування у них розвиваються слабкість і скутість (на кшталт спастичної атаксії).
У разі виконання нейровізуалізації методом магнітно-резонансної томографії (МРТ) у пацієнта з дефіцитом В12 можна виявити класичні зміни підгострої комбінованої дегенерації дорсального (заднього) і бічного стовпів спинного мозку внаслідок демієлінізації, описані як «перевернута V-подібна картина» в шийному і грудному відділах спинного мозку (Stabler, 2013).
Призначення пацієнтам із діагностованою периферичною нейропатією комплексу вітамінів В1, В6 і В12 сприяє редукції симптомів протягом усього курсу лікування. За даними дослідження NENOIN, у пацієнтів, які отримували лікування препаратом комбінації вітамінів В1, В6 і В12, вдалося усунути щонайменше один легкий симптом периферичної нейропатії будь-якого ґенезу або один «помірний» симптом класифікувати як змінений за тяжкістю на «легкий» (Hakim et al., 2018).
Сьогодні зареєстрований в Україні препарат Нейробіон, що містить 100 мг вітаміну В1, 100 мг вітаміну В6 і 1 мг вітаміну В12, для ефективного лікування станів, що пов’язані з дефіцитом вітамінів групи В, забезпечуючи добову потребу у вітамінах групи В і сприяючи усуненню їх дефіциту.
Проте не лише полінейропатія може бути ознакою вітамінодефіциту. Як відомо, наслідком дефіциту вітаміну B1 є енцефалопатія Верніке і амнестичний синдром Корсакова.
Енцефалопатія Верніке часто асоціюється з алкоголізмом, проте також може бути спричинена внаслідок тяжкого токсикозу у вагітних, баріатричних оперативних втручань, онкологічних захворювань та хіміотерапії, гемодіалізу, синдрому набутого імунодефіциту (СНІД), спадкової схильності. Діагностика енцефалопатії Верніке має охоплювати щонайменше два з таких чотирьох критеріїв Кейна: дієтичний дефіцит, окуломоторні порушення, мозочкові симптоми, зміна психічного стану або легке порушення пам’яті (Galvin et al., 2010).
У разі встановлення зазначених порушень необхідно виконати лабораторну діагностику, що передбачає вимірювання активності тіамінтранскетолази еритроцитів до і після додавання тіамінпірофосфату. Рівень сироваткового тіаміну можна визначити за допомогою високоефективної рідинної хроматографії. Втім, якщо встановлено діагноз енцефалопатії Верніке, негайне призначення тіаміну має пріоритет над лабораторною діагностикою.
Організм людини не синтезує самостійно вітаміни групи В, тому вони мають надходити у достатній кількості з раціоном. Вітаміни В1 та В6 містяться у рослинних продуктах, як-от цільнозерновий хліб, дикий рис, зелені овочі, бобові, картопля, горіхи, а також у продуктах тваринного походження. Тоді як вітамін B12 людина може отримати лише з продуктами тваринного походження: м’ясом, печінкою, рибою, яйцями, молочними продуктами. Ефект поліпшення харчового статусу менш виразний порівняно з медикаментозним лікуванням, проте він може сприяти первинній профілактиці вітамінодефіциту. Пацієнти віком >50 років можуть не мати змоги адекватно засвоювати вітамін В12 з їжею, тому рекомендована дієтична норма вітаміну В12 становить 2,4 мкг на добу для дорослих чоловіків і невагітних жінок, і 2,6 мкг на добу – для вагітних жінок.
У разі підтвердженого дефіциту вітаміну В12 лікування можна призначити у вигляді внутрішньом’язових ін’єкцій кобаламіну або пероральної терапії. У пацієнтів із необоротною причиною нестачі цього вітаміну слід продовжувати лікування необмежений час, тоді як в осіб з оборотною причиною терапія триває до усунення дефіциту і зникнення симптомів. Передбачене покращення неврологічних симптомів можна спостерігати від шести тижнів до трьох місяців. Британське товариство гематології (BSH) не рекомендує повторно перевіряти рівень вітаміну В12 після початку лікування (Devalia et al., 2014).
 Продовжила тему вітамінодефіциту у своєму виступі клінічна фармакологиня, к.мед.н., доцентка кафедри клінічної фармакології Вінницького національного медичного університету імені М. І. Пирогова Олександра Олексіївна Клекот.
Продовжила тему вітамінодефіциту у своєму виступі клінічна фармакологиня, к.мед.н., доцентка кафедри клінічної фармакології Вінницького національного медичного університету імені М. І. Пирогова Олександра Олексіївна Клекот.
– Як зазначила пані Клекот, вітаміни групи В є водорозчинними, тому вони не можуть депонуватись в організмі людини і потребують щоденного надходження. За результатами популяційного дослідження NHANES (National Health and Nutrition Examination Survey), кожен 10-й мешканець США має дефіцит вітаміну В6 – його поширеність була вищою навіть за дефіцит заліза, вітамінів D та В12.
Вітаміни групи В не лише залучені до важливих фізіологічних функцій в організмі людини, а й чинять нейроспецифічні ефекти. Особливо суттєвий вплив на роботу нервової системи мають вітаміни B1 (тіамін), B6 (піридоксин) і B12 (кобаламін) (Zempleni, 2013; Sechi, 2016).
Тіамін є коферментом циклу Кребса, тому він діє на регуляцію синтезу аденозинтрифосфату (АТФ) у нейронах; забезпечує енергетичний компонент, необхідний для синтезу нуклеїнових кислот, нейромедіаторів і мієлінової оболонки; регулює метаболізм ацетилхоліну (Martin, 2001, 2003; Nolan, 1991).
Піридоксин є коферментом понад 140 ензимів біосинтезу амінокислот, нейромедіаторів, дезоксирибонуклеїнової кислоти (ДНК) / рибонуклеїнової кислоти (РНК); він бере участь у регуляції імунної відповіді та процесів запалення в нейронах; зв’язує вільні радикали (Spinneker, 2006; MacKenzie, 2006; Ohtahara, 2011).
Кобаламін чинить вплив на метаболізм жирних кислот, стимулює нейрорегенерацію та ремієлінізацію, підтримує процеси метилювання ДНК / РНК (Kumar, 2014; Stabler, 2013). Взаємодія піридоксину і кобаламіну в циклі метіоніну, а також їхня участь у циклі лимонної кислоти (разом з іншими вітамінами групи В, зокрема тіаміном) свідчать, що ці три елементи пов’язані з біохімічного погляду (Kennedy, 2016; Mikkelsen, 2016).
На думку C. A. Calderуn-Ospina and M. O. Nava-Mesa (2020), синергетична функція нейротропних вітамінів групи В може бути обґрунтована впливом вітамінів на цикл фолієвої кислоти та функціями кожного вітаміну окремо: вітаміну B1 – як нейропротектора, що поліпшує функціонування нейронів; вітаміну B6 як антиоксиданта, що також сприяє підвищенню провідності у нейронах; вітаміну B12 як компонента регенерації нервових клітин.
Результати дослідження на тваринних моделях переконливо продемонстрували, що жоден із вітамінів групи B окремо (B1, B6 і B12) не був настільки ефективним для полегшення нейропатичного болю та відновлення нервової функції, як комбінація цих трьох вітамінів (Jolivalt, 2009).
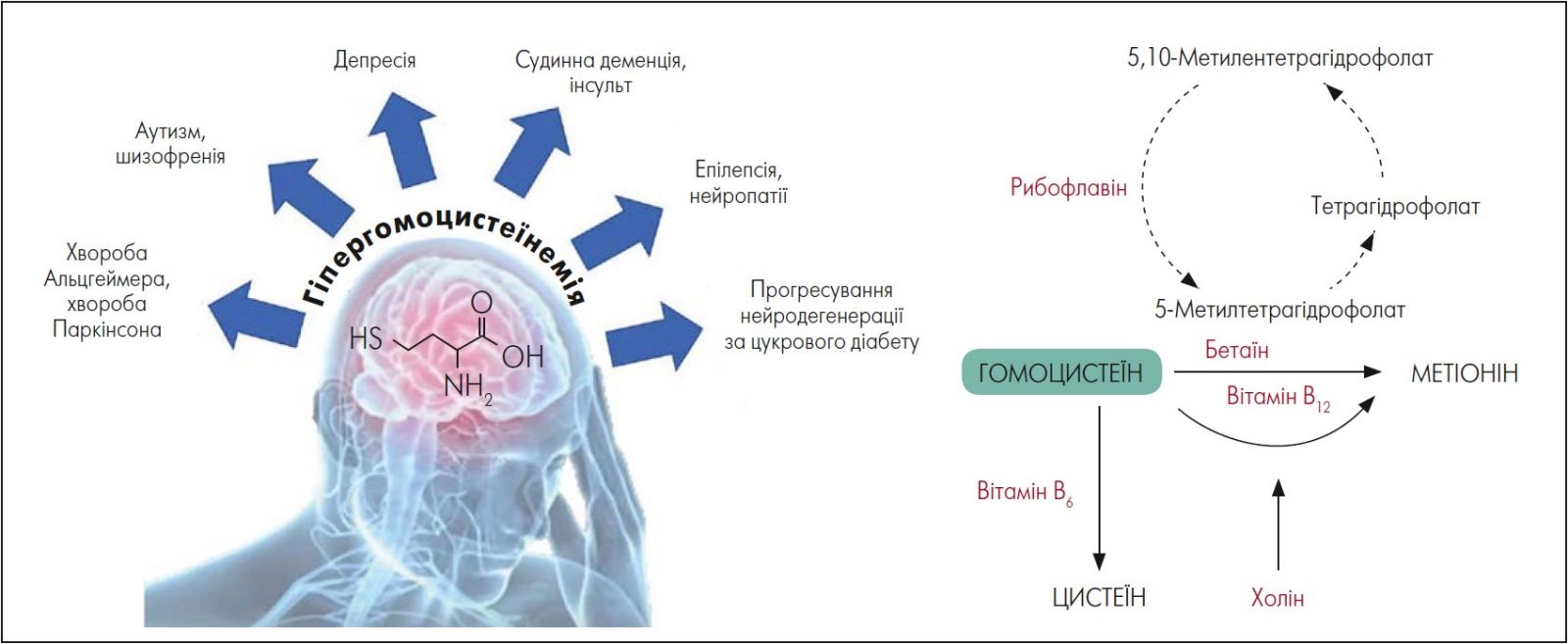
За даними метааналізу 46 обсерваційних та семи інтервенційних досліджень, полінейропатії асоціюються з низькими рівнями в плазмі B12 та підвищеним рівнем метилгомоцистеїну, який, імовірно, має нейротоксичний ефект (рисунок).
Рис. Роль гіпергомоцистеїнемії в розвитку неврологічних хвороб
Адаптовано за Corado M. et al., 2021.
Підвищення вмісту метилгомоцистеїну призводить до окиснювального стресу та нейродегенерації, що формує патологічне коло внаслідок нейрогенного запалення, мітохондріальної дисфункції, підвищення глутаматної ексайтотоксичності і, своєю чергою, посилюють оксидативний стрес (Marashy et al., 2017).
Це може бути чинником ризику деменції, зниження когнітивних функцій, розвитку хвороби Альцгеймера та енцефалопатії Верніке (Kennedy, 2016; Mikkelsen, 2016; Smith, 2018).
Часто вітамінні добавки призначають як тактику підтримки для профілактики захворювання, натомість, слід розглядати призначення вітамінів групи В як терапію, що здатна змінити прогноз захворювання.
У межах дослідження NENOIN було представлено, що приймання комбінації вітамінів В1, В6 і В12 у складі препарату Нейробіон сприяло редукції симптомів периферичної нейропатії різної етіології на 62,9% після закінчення лікування. При цьому суттєве зменшення ознак нейропатії пацієнти відчули вже після 14 днів застосування цього препарату, із подальшим покращенням клінічного стану.
Нейробіон доступний у двох лікарських формах – ампулах для парентерального застосування і таблетках. Незалежно від форми препарат рекомендовано приймати раз на добу. Доза тіаміну дисульфіду (гідрохлориду) в обох випадках становить 100 мг, піридоксину гідрохлориду – в ін’єкційній формі вдвічі нижча, ніж у таблетованій (100 проти 200 мг), а ціанокобаламіну – в ін’єкційній перевищує таку в таблетованій формі у >4 рази (1 мг проти 240 мкг). Така різниця насамперед зумовлена різною біодоступністю активних компонентів через різні шляхи введення.
Комбіноване застосування вітамінів B1, B6 і B12 не позначається на фармакокінетиці окремих вітамінів. Раніше вважалося, що їх не можна поєднувати, проте сучасне фармакологічне рішення передбачає комбінацію однієї ліпофільної та двох гідрофільних молекул у слабко лужному розчині-носії, що забезпечує максимальну біодоступність кожного компонента препарату та перешкоджає утворенню нерозчинних комплексів.
Такий підхід дає можливість лікарю призначати індивідуалізовану ступеневу терапію, що сприятиме поліпшенню комплаєнсу, а отже, і результатам лікування.
Підготувала Ольга Загор
Тематичний номер «Неврологія. Психіатрія. Психотерапія» № 4 (67) 2023 р.