13 січня, 2021
Сучасні особливості діагностики та патогенетичного лікування місцево-поширеного та метастатичного гормоночутливого раку передміхурової залози
27 листопада в режимі онлайн відбулася науково-практична конференція «Мовембер‑2020» Рак передміхурової залози – UPDATE. Захід приурочено міжнародному проєкту боротьби з раком передміхурової залози Movember («Вусатий листопад», або «Вусопад»), що традиційно триває упродовж листопада із характерним відпусканням вусів з метою привернути увагу суспільства до питань чоловічого здоров’я, а саме – до раку простати та інших онкологічних захворювань.
 У рамках конференції про особливості лікування місцево-поширеного та метастатичного гормоночутливого раку передміхурової залози (мГЧРПЗ) розповів провідний науковий співробітник відділення пластичної та реконструктивної онкоурології Національного інституту раку (м. Київ), кандидат медичних наук Олег Анатолійович Войленко.
У рамках конференції про особливості лікування місцево-поширеного та метастатичного гормоночутливого раку передміхурової залози (мГЧРПЗ) розповів провідний науковий співробітник відділення пластичної та реконструктивної онкоурології Національного інституту раку (м. Київ), кандидат медичних наук Олег Анатолійович Войленко.
– Велика кількість пацієнтів з раком передміхурової залози (РПЗ) звертається за медичною допомогою на запущених стадіях раку, коли є метастази або місцево-поширений процес. За даними Американського онкологічного товариства (American Cancer Society, ACS) за 2020 р., у США РПЗ лідирує за поширеністю серед усіх онкологічних захворювань у чоловічого населення та посідає друге місце за смертністю від злоякісних новоутворень. Для чоловіків імовірність захворіти на РПЗ упродовж життя становить 11,6% (1 із 9 осіб). Водночас, за даними ACS 2020 р., рання діагностика та сучасні методи лікування цієї патології дозволили збільшити 5-річну виживаність пацієнтів із неметастатичним РПЗ до 99%. Прогноз та наслідки РПЗ залежать від стадії захворювання та рівня диференціації ракових клітин на момент встановлення діагнозу. Усі пацієнти із РПЗ помирають від метастатичного кастраційно-резистентного РПЗ (М. McNamara, 2018).
Відповідно до рекомендацій Європейської асоціації урології (European Association of Urology, EAU) 2020 р., лікування мГЧРПЗ базується на виявленні метастазів з допомогою комп’ютерної томографії (КТ) й остеосцинтиграфії. Сьогодні активно вивчається роль у діагностиці РПЗ позитронно-емісійної КТ (ПЕТ-КТ) із використанням простатичного специфічного антигену (ПСА) (P. Cornford et al., 2020).
Стандартом лікування при мГЧРПЗ вже впродовж 50 років є гормональна терапія (ГТ), яка застосовується пожиттєво та не припиняється навіть після розвитку кастраційної резистентності. Більшість експертів надає перевагу у лікуванні мГЧРПЗ андрогенній депривації з використанням найдоступніших на сьогодні агоністів гонадотропін-рилізинг-гормону (ГнРГ) у поєднанні із коротким курсом антиандрогену I покоління або без нього (S. Gillessen, 2017). Моніторинг ефективності такої терапії зазвичай проводять шляхом вимірювання рівня тестостерону.
Кастраційним рівнем сироваткового тестостерону впродовж багатьох років вважався показник <50 нг/дл (або 1,7 нмоль/л). Проте, за даними EAU 2020 р., кращі результати спостерігаються при рівні тестостерону <20 нг/дл (0,7 нмоль/л). Проведені дослідження демонструють вищий рівень канцер-специфічної виживаності та триваліший термін відповіді на ГТ в осіб із нижчим рівнем тестостерону впродовж першого року ГТ (рис. 1; L. Klotz, 2015). Рекомендованою є рутинна оцінка рівня тестостерону через кожні 3-6 міс, при його недостатньому зниженні слід розглянути можливість переходу на інший аналог ГнРГ (агоніст чи антагоніст) або виконання хірургічної кастрації.
Одним із найбільш вивчених ГнРГ-агоністів є трипторелін (Диферелін®, Ipsen Pharma). Прийом препарату Диферелін® дозволяє знизити рівень тестостерону до <20 нг/дл у більш як 90% пацієнтів, що було продемонстровано у клінічних дослідженнях (Shim et al., 2019; N.D. Shore et al., 2016; J. Morote et al., 2007 тощо). Перевагою цього препарату є наявність 6-місячної форми, що, враховуючи пожиттєве лікування, робить його найбільш оптимальним та зручним у використанні.
Вагоме значення для контролю ефективності лікування має визначення вмісту ПСА. Зниження рівня ПСА <4 нг/мл через 7 міс на фоні андрогендеприваційної терапії (АДТ) впливає на загальну виживаність (ЗВ) пацієнтів. У дослідженні M. Hussain та співавт. (2006) продемонстровано, що при рівні ПСА <0,2 нг/мл медіана ЗВ досягає 75 міс, 0,2-4,0 нг/мл – 44 міс, а при >4 нг/мл – лише 13 міс.
Андрогенної депривації можна також досягти шляхом застосування медикаментозної чи хірургічної кастрації з одночасним блокуванням андрогенних рецепторів простати антиандрогенами, які пригнічують вплив негонадних андрогенів на клітини передміхурової залози – так звана максимальна андрогенна блокада (МАБ). Проте дані систематичних оглядів свідчать, що МАБ не має переваг у лікуванні пацієнтів із мГЧРПЗ порівняно з монотерапією агоністами ГнРГ та зумовлює виражені побічні ефекти. Саме тому сьогодні МАБ не є стандартом лікування хворих на мГЧРПЗ. Метааналіз 27 досліджень клінічної ефективності АДТ при її комбінуванні з антиандрогенами I покоління із включенням 8 тис. пацієнтів продемонстрував відсутність впливу вказаної комбінації на виживаність пацієнтів. За даними Кокранівського систематичного огляду, монотерапія нестероїдними антиандрогенами є менш ефективною з точки зору ЗВ, клінічного прогресування та припинення терапії через виникнення побічних реакцій, ніж медикаментозна чи хірургічна кастрація (M. Kunath et al., 2014).
Згідно з рекомендаціями Національної онкологічної мережі США (2020), медикаментозна та хірургічна кастрація є оптимальними й зіставними за ефективністю методами ГТ, а використання МАБ не забезпечує додаткової користі для пацієнтів із мГЧРПЗ. Однак призначення антиандрогенів можливе у пацієнтів з мГЧРПЗ, які мають високий ризик розвитку «феномену спалаху» пухлини (підвищення секреції лютеїнізуючого, фолікулостимулюючого гормонів, тестостерону та дигідротестостерону) при монотерапії ГнРГ. У такому випадку терапія антиандрогенами має передувати або призначатись одночасно із ГнРГ та тривати щонайменше 7 днів. Монотерапія антиандрогенами є менш ефективною, ніж медикаментозна чи хірургічна кастрація, та не рекомендована.
Відомо що антагоністи ГнРГ знижують секрецію лютеїнізуючого, фолікулостимулюючого гормонів і тестостерону без розвитку феномену спалаху. Проте проведений Sciara та співавт. (2016) систематичний огляд не виявив значних відмінностей між групами агоністів та антагоністів ГнРГ і засвідчив необхідність проведення тривалішого дослідження й вивчення впливу на виживаність (A. Sciarra, 2016).
Дискусійними залишаються питання щодо застосування безперервної чи інтермітуючої та ранньої чи відстроченої ГТ.
У метааналізі 8 рандомізованих клінічних досліджень не виявлено різниці впливу на виживаність постійної чи інтермітуючої антиандрогенної ГТ, проте лише 3 із 8 досліджень були проведені із включенням пацієнтів із мГЧРПЗ (D. Brungs, 2014). На сьогодні немає чітко визначених порогових рівнів ПСА, при яких АДТ може бути припинена чи має продовжуватись, та не отримано переконливих доказів того, що цей вид терапії сприяє подовженню часу до розвитку гормонорефрактерного РПЗ. Таким чином, на даному етапі перевага надається постійній ГТ.
Дані нового Кокранівського систематичного огляду (2019) підтвердили переваги застосування ранньої АДТ у пацієнтів із мГЧРПЗ. Було показано, що невідкладна ГТ, призначена відразу після встановлення діагнозу, сприяє збільшенню тривалості життя порівняно з відтермінованою терапією (M. Kunath et al., 2019).
Серед нових підходів до лікування РПЗ виділяють комбіновану терапію. У рандомізованих клінічних дослідженнях було встановлено, що поєднання тривалої ГТ із дистанційною променевою терапією (ДПТ) підвищує ЗВ у пацієнтів із місцево-поширеним гормоночутливим РПЗ порівняно з ГТ чи ДПТ у режимі монотерапії (P. Cornford et al., 2020).
Популяція пацієнтів із мГЧРПЗ є неоднорідною. Сьогодні пропонується низка прогностичних факторів для визначення об’єму метастатичних уражень при РПЗ. Зокрема, у дослідженні CHAARTED (Chemo-hormonal Therapy versus Androgen Ablation Randomized Trial for Extensive Disease in Prostate Cancer) як потенційний прогностичний фактор використовується об’єм пухлини. При цьому критеріями великого об’єму метастатичного ураження є ≥4 метастазів у кістках із принаймні ≥1 метастатичним ураженням за межами хребта або наявність вісцеральних метастазів (C.J. Sweeney, 2015).
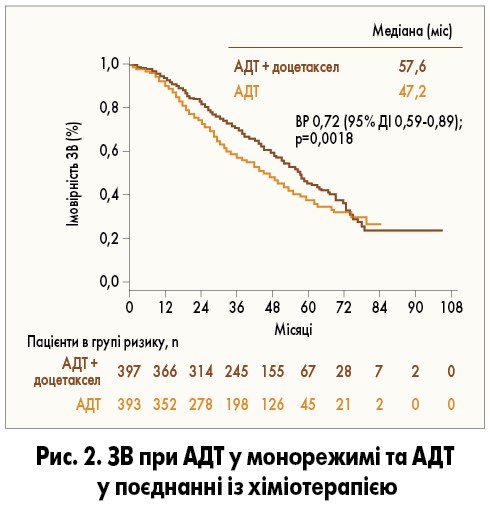 У клінічному дослідженні CHAARTED було продемонстровано, що призначення доцетакселу додатково до АДТ достовірно покращує медіану ЗВ у пацієнтів із мГЧРПЗ порівняно з монотерапією ГнРГ: 57,6 та 47,2 міс відповідно (рис. 2). Проте додавання доцетакселу підвищило ЗВ лише у пацієнтів із великим об’ємом метастазів, тоді як в осіб із малим об’ємом метастатичного ураження додавання доцетакселу не мало переваги над монотерапією ГнРГ. Аналогічні результати було отримано і в групі хворих із вперше виявленим мГЧРПЗ. Однак було встановлено, що додавання хіміотерапії до АДТ достовірно збільшує час до розвитку кастраційної рефрактерності в усіх групах хворих (C.E. Kyriakopoulos et al., 2018).
У клінічному дослідженні CHAARTED було продемонстровано, що призначення доцетакселу додатково до АДТ достовірно покращує медіану ЗВ у пацієнтів із мГЧРПЗ порівняно з монотерапією ГнРГ: 57,6 та 47,2 міс відповідно (рис. 2). Проте додавання доцетакселу підвищило ЗВ лише у пацієнтів із великим об’ємом метастазів, тоді як в осіб із малим об’ємом метастатичного ураження додавання доцетакселу не мало переваги над монотерапією ГнРГ. Аналогічні результати було отримано і в групі хворих із вперше виявленим мГЧРПЗ. Однак було встановлено, що додавання хіміотерапії до АДТ достовірно збільшує час до розвитку кастраційної рефрактерності в усіх групах хворих (C.E. Kyriakopoulos et al., 2018).
Результати клінічного дослідження ІІІ фази ARCHES показали, що додавання ензалутаміду до АДТ істотно знижує ризик метастатичного прогресування чи смерті у пацієнтів з мГЧРПЗ порівняно із застосуванням лише АДТ, включаючи хворих із малим об’ємом метастатичного ураження та/або після лікування доцетакселом (рис. 3; A.G. Armstrong et al., 2019).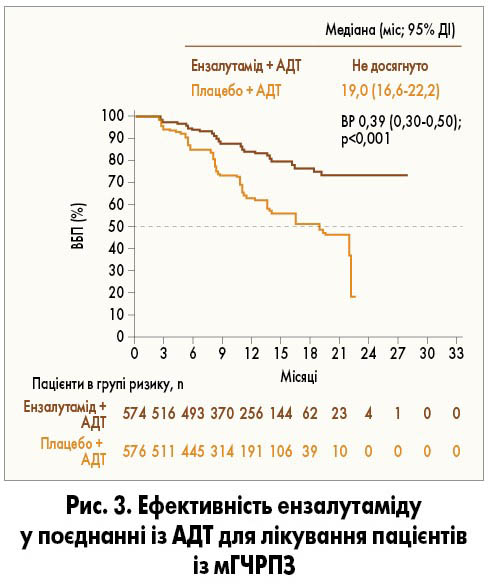
У рандомізованому дослідженні ІІІ фази TITAN порівнювали ефективність апалутаміду з АДТ та лише АДТ для лікування пацієнтів із мГЧРПЗ. У цьому дослідженні було продемонстровано значне покращення виживаності без прогресування (ВБП; медіана ВБП не була досягнута у групі апалутаміду проти 22,1 міс у групі плацебо; відносний ризик – ВР – прогресування чи смерті 0,48; 95% довірчий інтервал – ДІ – 0,39-0,60; p<0,0001) та ЗВ (медіана ЗВ не досягнута в обох групах; ВР смерті 0,67; 95% ДІ 0,51-0,89; p<0,0053). Токсичність препарату була мінімальною (K.N. Chi et al., 2019).
У дослідженні STAMPEDE було продемонстровано достовірну перевагу комбінації абіратерону та преднізолону з АДТ порівняно з призначенням лише АДТ, що проявлялось збільшенням ЗВ у групах хворих із малим і великим об’ємом метастатичного ураження (A.P. Hoyle et al., 2019). Сьогодні абіратерон і преднізолон у комбінації із АДТ також входять до стандартів лікування пацієнтів із мГЧРПЗ.
Наразі очікуються результати дослідження PEASE‑1. У ньому порівнюють групи пацієнтів, які отримують АДТ ± доцетаксел; АДТ + абіратерон з преднізолоном ± доцетаксел; АДТ + променеву терапію ± доцетаксел та АДТ + променеву терапію + абіратерон з преднізолоном ± доцетаксел. У 2022 р. очікуються результати дослідження ARASENS, у якому вивчають ефективність застосування даролутаміду у поєднанні з АДТ, а більш далекими перспективними напрямами досліджень є вивчення інгібіторів контрольних точок (ніволумаб, пембролізумаб та іпілімумаб) у цієї категорії хворих.
Таким чином, згідно з рекомендаціями EAU (2020), першою лінією терапії пацієнтів з мГЧРПЗ є негайне призначення АДТ з метою зменшення симптомів і зниження ризику потенційно серйозних наслідків метастатичного ураження, таких як компресія спинного мозку, патологічні переломи та обструкція сечоводу. Агоністи ГнРГ (Диферелін®) є стандартом ГТ при РПЗ. Прийом цих препаратів супроводжується мінімальною кількістю побічних ефектів, характеризується хорошою переносимістю та високою ефективністю, особливо у пацієнтів із загрозою компресії спинного мозку та обструкції сечового міхура.
.jpg) Із доповіддю «Роль контролю рівня тестостерону у патогенетичному лікуванні РПЗ» виступив професор кафедри хірургії № 1 Дніпропетровської медичної академії, доктор медичних наук Роберт Миколайович Молчанов.
Із доповіддю «Роль контролю рівня тестостерону у патогенетичному лікуванні РПЗ» виступив професор кафедри хірургії № 1 Дніпропетровської медичної академії, доктор медичних наук Роберт Миколайович Молчанов.
– Андрогенна депривація може бути досягнута за допомогою пригнічення секреції андрогенів яєчок або блокування дії циркулюючих андрогенів на рівні їх рецепторів. Ці два способи можна поєднати з метою досягнення повної (максимальної, загальної) андрогенної блокади – МАБ. На сучасному етапі розвитку онкоурології АДТ рекомендована як основна чи додаткова терапія у пацієнтів із III та IV стадією РПЗ за наявності метастазів або без них і пацієнтів із кастраційно-резистентним РПЗ. За необхідності ГТ впродовж 6 міс може бути використана при РПЗ I та II стадій як ад’ювантна терапія у хворих із поганим прогнозом (N. Mottet et al., 2019).
Таким чином, АДТ є основою лікування поширеного та стандартом лікування метастатичного РПЗ. Основними препаратами для ГТ РПЗ на сучасному етапі є ГнРГ.
Отже, андрогенної депривації можна досягти шляхом хірургічної кастрації, використання агоністів або антагоністів ГнРГ, естрогенів та антиандрогенів. Дія цих препаратів спрямована на основні ланки шляху передачі стимулюючого андрогенного сигналу – мішені протипухлинної терапії при РПЗ.
Сьогодні в умовах традиційного лікування метастатичного РПЗ рівень пригнічення тестостерону відіграє вагому роль у прогнозуванні відповіді на АДТ. Сучасні технології дозволяють виявляти концентрацію тестостерону, нижчу за традиційні <50 нг/дл (або 1,7 нмоль/л). Таким чином, хірургічний рівень тестостерону становить 15 нг/мл (або 0,5 нмоль/л), порогом ефективності вважається рівень 32 нг/дл (або 1,1 нмоль/л), а рівнем, рекомендованим стандартами, є <20 нг/дл (0,7 нмоль/л; N. Mottet et al., 2015; J. Morote et al., 2007; S. Dason et al., 2013; N. Mottet et al., 2016).
Середня концентрація тестостерону після білатеральної орхіектомії становить 15 нг/дл, що значно нижче за історичний показник 50 нг/дл (M.G. Oefelein et al., 2000). Проте окрім тотальної існує субкапсулярна орхіектомія, проведення якої також дозволяє досягти кастраційного рівня тестостерону, але у цьому випадку йдеться про рівень тестостерону <50 нг/дл. Зокрема, при порівнянні показників тестостерону при медикаментозній і хірургічній (субкапсулярна орхіектомія) кастрації у дослідженні P.B. Ostergren та співавт. (2016), рівень тестостерону був вищим в оперованих пацієнтів через 12 тижнів після операції, і ця різниця зберігалась значущою протягом 24 тижнів. Це підтверджує меншу ефективність пригнічення тестостерону при проведенні субкапсулярної орхіектомії порівняно з медикаментозною кастрацією (P.B. Ostergren et al., 2016).
Як зазначалося, зниження кастраційного рівня тестостерону впливає на збільшення тривалості ВБП. Опубліковані Morote та співавт. (2007) дані свідчать про прискорення прогресування РПЗ до кастраційно-резистентної стадії у разі недосягнення рівня тестостерону <20 нг/дл на тлі терапії агоністами ГнРГ. Окрім цього, дослідники відмітили також пришвидшення розвитку кастраційно-резистентної стадії при рівні тестостерону >32 нг/дл та навпаки – подовження часу до її настання на 4 роки при рівні <32 нг/дл (J. Morote et al., 2007). Подібні дані були отримані й у дослідженні P. Perachino та співавт. (2009): рівень тестостерону через 6 міс ГТ був вагомим фактором розвитку кастраційної резистентності (P. Perachino et al., 2009). Поріг 32 нг/дл також використовувався у дослідженні S. Dason та співавт. (2013) як такий, що впливає на час до розвитку кастраційно-резистентної стадії.
 У дослідженні T. Pickles та співавт. (2012) 2196 пацієнтів отримували агоніст ГнРГ під час та після променевої терапії. При цьому ризик підвищення рівня тестостерону >1,1 нмоль/л спостерігався у 6,6% пацієнтів, >1,7 нмоль/л – у 3,4%, а повторне підвищення – у 16,0% пацієнтів (рис. 4).
У дослідженні T. Pickles та співавт. (2012) 2196 пацієнтів отримували агоніст ГнРГ під час та після променевої терапії. При цьому ризик підвищення рівня тестостерону >1,1 нмоль/л спостерігався у 6,6% пацієнтів, >1,7 нмоль/л – у 3,4%, а повторне підвищення – у 16,0% пацієнтів (рис. 4).
Також варто зазначити, що молодший вік хворих (<70 років) був фактором ризику підвищення рівня тестостерону під час АДТ (T. Pickles et al., 2012).
Отже, вищенаведені результати досліджень показують, що рівень тестостерону у хворих, що отримують АДТ, є потужним прогностичним фактором розвитку мГЧРПЗ.
За даними M. Shim та співавт. (2019), отриманими при проведенні ретроспективного аналізу історій хвороб 125 пацієнтів із місцево-поширеним або метастатичним РПЗ, після 9 міс застосування агоністів ГнРГ найнижчий рівень тестостерону відзначали при лікуванні триптореліном (Диферелін®), лейпрорелін і гозерелін забезпечували нижчу ефективність (р=0,001; рис. 5).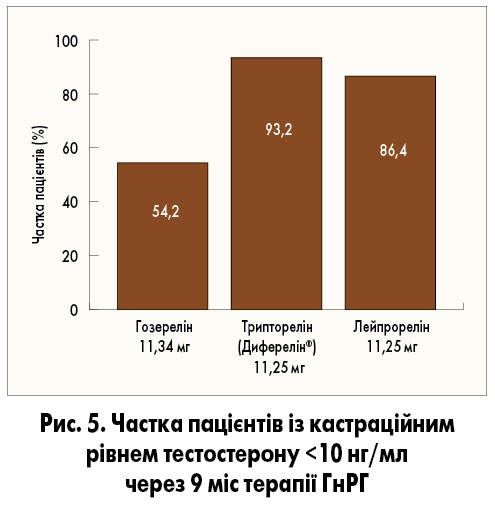
При виборі препаратів для АДТ важливо враховувати їх різні властивості. Зокрема, це температура зберігання, готовність лікарського засобу до негайного вживання, спосіб введення (підшкірно чи внутрішньом’язово).
Одним із найкраще вивчених агоністів ГнРГ є Диферелін® (трипторелін). Диферелін® показаний при місцево-поширеному та метастатичному РПЗ як монотерапія або як супутня та ад’ювантна терапія у поєднанні з променевою терапією.
Диферелін® випускається у флаконах у формі порошку для приготування суспензії для внутрішньом’язового введення. Моніторинг ефективності терапії можна проводити шляхом вимірювання рівня тестостерону в сироватці крові та ПСА.
Підготувала Ольга Нестеровська
Тематичний номер «Онкологія, Гематологія, Хіміотерапія» № 6 (67) 2020 р.



