21 квітня, 2026
Кишкова мікробіота та імунотерапія раку: нові горизонти персоналізованого лікування
Кишкова мікробіота відіграє ключову роль у формуванні імунної відповіді при онкологічних захворюваннях, впливаючи на ефективність терапії через модуляцію імуноцитів, перебудову пухлинного мікрооточення і секрецію специфічних метаболітів. Останні дослідження свідчать, що такі стратегії, як трансплантація фекальної мікробіоти (ТФМ), застосування пробіотиків і дієтотерапія, є перспективними методами підвищення чутливості до інгібіторів контрольних точок імунітету (ІКТ) та адоптивної клітинної терапії. Крім того, корекція мікробного складу дає змогу суттєво знизити частоту і тяжкість імуноопосередкованих небажаних явищ.
Клінічні дані підтверджують, що показники різноманітності мікробіому можуть слугувати надійними предикторами результатів лікування, а цілеспрямована модуляція мікробного профілю здатна долати первинну та набуту резистентність до імунопрепаратів. В огляді (за матеріалами Lei W. та співавт., 2025) систематизовано результати сучасних доклінічних і клінічних випробувань, деталізовано молекулярні механізми імуномодуляції та окреслено вектори розвитку прецизійної онкології крізь призму мікробіому.
Уявлення про людський організм як замкнену систему давно відійшло в минуле. Сьогодні ми знаємо, що всередині нас мешкає приблизно 40 трильйонів мікроорганізмів включно з бактеріями, грибами, археями і вірусами. Цікаво, що кількість їхніх генів перевищує людський геном більш ніж у сто разів. Серед усіх мікробних популяцій організму особливе місце належить кишковій мікробіоті, яка колонізує товсту кишку і становить понад 97% загальної мікробної популяції. І це не просто «пасажири» – кишечник містить до 60-70% периферичних імунних клітин, що дає підстави вважати його найбільшим периферичним імунним органом. Мікробні метаболіти, зокрема коротколанцюгові жирні кислоти та жовчні кислоти, відіграють вирішальну роль у формуванні вродженого й адаптивного імунітету.
Але який стосунок ці мікроскопічні мешканці мають до онкології? Як виявилося – безпосередній. Злоякісні пухлини залишаються другою провідною причиною смерті у світі, і хоча традиційні методи лікування суттєво покращили прогноз для багатьох пацієнтів, вони часто обмежені резистентністю до препаратів і побічними ефектами. Справжнє досягнення останніх років – імунотерапія, зокрема ІКТ та адоптивна клітинна терапія, що здійснила революцію в лікуванні раку. Однак чомусь одні пацієнти добре відповідають на лікування, а інші – ні. Це допоміг з’ясувати наш кишечник.
Кишкова мікробіота й інгібітори контрольних точок імунітету
ІКТ діють просто й елегантно: вони блокують «гальма» імунної системи – контрольні точки PD‑1, PD-L1 та CTLA‑4, даючи змогу імунним клітинам атакувати пухлину. Проте реальність виявилася складнішою за теорію. Загалом лише 20-40% пацієнтів із найбільш чутливими типами пухлин (меланома, рак легені, нирково-клітинна карцинома) відповідають на цю терапію. Що ж відрізняє респондерів від нереспондерів?
Несподівано під час клінічних досліджень з’ясували, що склад і різноманітність кишкової мікробіоти можуть прогнозувати відповідь на ІКТ. Пацієнти з недрібноклітинним раком легені та нирково-клітинною карциномою, які мали багатшу мікробну різноманітність, демонстрували кращі результати анти-PD‑1 терапії. З’ясувалося, що при метастатичній меланомі у респондерів виявляли підвищені рівні конкретних бактерій – Bifidobacterium longum, Collinsella aerofaciens та Enterococcus faecium.
Щоб перевірити, чи це кореляція, чи причинно-наслідковий зв’язок, дослідники провели експеримент: трансплантували фекальну мікробіоту від пацієнтів-респондерів безмікробним мишам. Результат приголомшив – миші почали краще відповідати на анти-PD-L1 терапію. Паралельно завдяки ретроспективним дослідженням з’ясували, що використання антибіотиків асоціювалося зі зниженою ефективністю ІКТ та гіршою виживаністю у пацієнтів із солідними пухлинами.
Варто зазначити, що універсального «корисного» мікроба не існує. Бактерії, асоційовані з ефективністю анти-PD‑1, можуть відрізнятися від тих, що впливають на відповідь на анти-CTLA‑4. При меланомі сприятливий прогноз пов’язують із Bifidobacterium, Ruminococcaceae та Lachnospiraceae, тоді як при інших пухлинах на перший план виходить Akkermansia muciniphila.
Механізми імунної модуляції
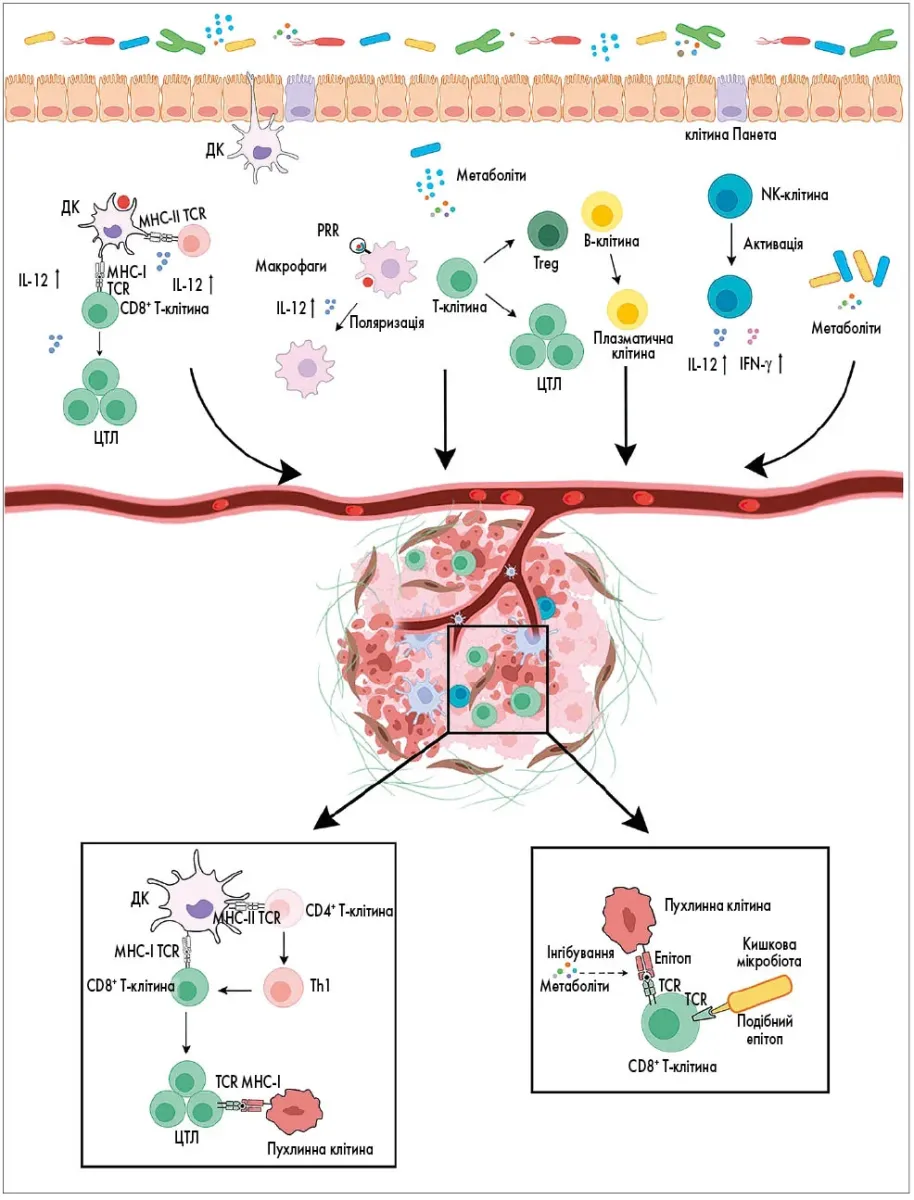
Постає слушне запитання: яким чином бактерії, що мешкають у кишечнику, впливають на пухлину, розташовану в зовсім іншому органі? Рис. 1 наочно демонструє, наскільки різноманітними та взаємопов’язаними виявилися ці механізми.
Рис. 1. Вплив кишкової мікробіоти на вроджений та адаптивний імунітет у кишечнику і пухлинному мікрооточенні
ДК – дендритна клітина; ЦТЛ – цитотоксичний Т-лімфоцит; PRR – рецептори розпізнавання патерну; Treg – регуляторна Т-клітина; TCR – Т-клітинний рецептор; NK – природний кілер; IFN-γ – інтерферон-гамма; MHC – головний комплекс гістосумісності.
Передусім мікробіота формує розвиток і функцію ключових клітин вродженого імунітету – дендритних клітин та макрофагів. Коли мікробний баланс порушується, слизовий бар’єр кишечника послаблюється, і мікробні продукти (ліпополісахариди, пептидоглікани) потрапляють у кровообіг. Ці молекули активують рецептори розпізнавання патерну, запускаючи каскад імунних реакцій: продукцію прозапальних цитокінів, дозрівання дендритних клітин, активацію природних кілерів.
Але вплив мікробіоти сягає далі вродженого імунітету. Через механізм молекулярної мімікрії та стимуляцію диференціації Т-клітин вона формує адаптивні імунні відповіді. Дослідження демонструють, що кишкові мікроби регулюють субпопуляції CD4+ Т-клітин – Th1, Th2, Th17 та регуляторні Т-клітини. Окрему роль відіграють мікробні метаболіти. Коротколанцюгові жирні кислоти – бутират та пропіонат – впливають на диференціацію Т-клітин через інгібування гістондеацетилази. Bacteroidetes, Lachnospiraceae та Roseburia продукують пропіонову кислоту, тоді як види Firmicutes генерують масляну кислоту.
Двоспрямована регуляція токсичності імунотерапії
Імунотерапія – потужна зброя, але, як і будь-яка зброя, вона може завдати шкоди не лише ворогу. Імуно-асоційовані небажані явища залишаються серйозною клінічною проблемою. І тут знову роль мікробіоти виявилася вирішальною.
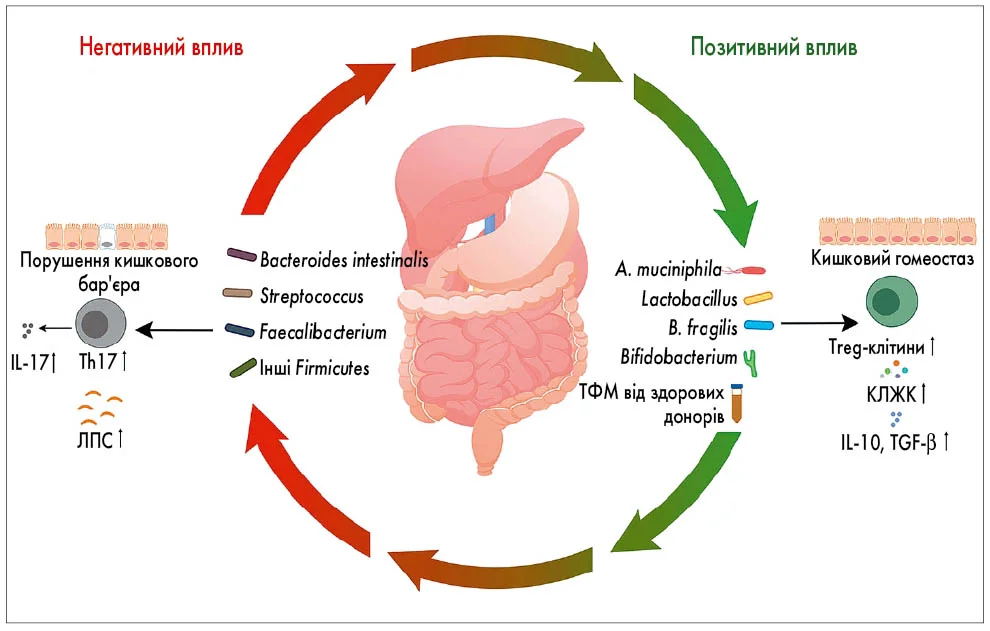
Подвійна роль мікробіоти – захист від токсичності через підтримку імунного гомеостазу або, навпаки, посилення побічних ефектів через імунну дисрегуляцію – схематично відображена на рис. 2. Характер токсичності залежить від типу терапії: анти-CTLA‑4 частіше спричиняє коліт і запалення гіпофіза, анти-PD‑1 – дисфункцію щитоподібної залози та пневмоніт, а CAR-T-терапія – синдром вивільнення цитокінів і нейротоксичність.
Рис. 2. Двоспрямована регуляція токсичності імунотерапії кишковою мікробіотою
ЛПС – ліпополісахариди; КЛЖК – коротколанцюгові жирні кислоти.
Отже, на токсичність можна впливати. Дієти, багаті на коротколанцюгові жирні кислоти, здатні значно зменшити шлунково-кишкову токсичність. Специфічні мікробні таксони – Akkermansia muciniphila та Ruminococcaceae – асоціюються і з кращою відповіддю на лікування, і з меншою частотою побічних ефектів. Ба більше, ТФМ від здорових донорів може відновити мікробне різноманіття, збільшити частку регуляторних Т-клітин і пом’якшити коліт, індукований ІКТ.
Стратегії модуляції кишкової мікробіоти
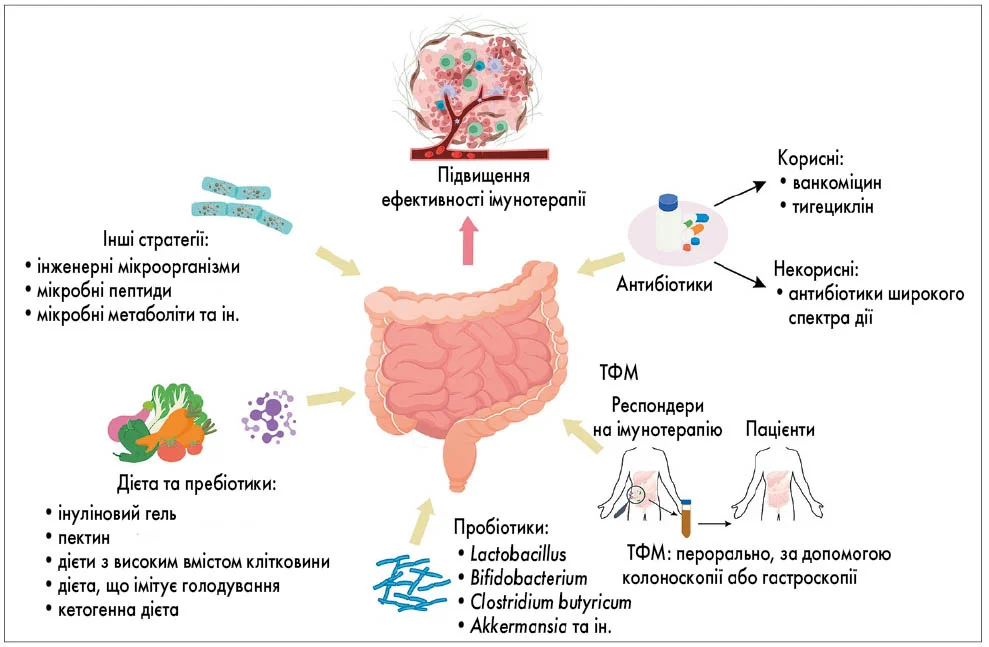
Сучасний арсенал втручань, спрямованих на мікробіоту, охоплює кілька напрямків, систематизованих на рис. 3.
Рис. 3. Терапевтичні стратегії модуляції кишкової мікробіоти для підвищення ефективності імунотерапії
Респондери – пацієнти, що відповідають на лікування.
ТФМ – мабуть, найбільш радикальний підхід. Суть методу проста: функціональну флору зі здорових фекалій пересаджують у шлунково-кишковий тракт пацієнта перорально або через колоноскопію. Два незалежних клінічних випробування продемонстрували, що ТФМ може подолати резистентність до ІКТ при метастатичній меланомі. У пацієнтів із PD‑1-рефрактерною меланомою після ТФМ і поновленої анти-PD‑1 терапії спостерігалося зменшення пухлини включно із частковими і повними відповідями.
Менш інвазивний підхід – застосування пробіотиків. Ці живі мікроорганізми під час введення в достатніх кількостях можуть посилювати протипухлинну імунотерапію. Доклінічні дослідження вказують на перспективність Lactobacillus, Bifidobacterium, Enterococcus та Akkermansia – вони активують Т-клітини і збільшують секрецію інтерферону-гамма.
Нарешті, найдоступніший інструмент – дієта. Обмеження калорій, дієти з високим вмістом клітковини та кетогенні дієти можуть підвищувати ефективність імунотерапії через модуляцію складу мікробіоти. Пребіотики – неперетравлювані волокна, такі як інулін і пектин, – вибірково стимулюють ріст корисних мікробів, покращуючи цілісність епітелію та активуючи клітини вродженого імунітету.
Виклики та перспективи
Впровадженню цих методів у клінічну практику стає на заваді низка суттєвих перешкод. Взаємодія між мікробіотою та імунною системою виявилася двоспрямованою: одні мікробні спільноти посилюють імунітет, інші – пригнічують. Варіації пухлинного мікрооточення додатково ускладнюють картину. Багато висновків отримано з моделей на тваринах, але біологічні розбіжності між ними й організмом людини обмежують можливість прямої екстраполяції отриманих результатів у клініку. Модуляція мікробіоти стикається з практичними перешкодами: невеликі розміри вибірок у дослідженнях, відсутність стандартизації протоколів, питання безпеки.
Проте перспективи надихають. Завдяки прогресу персоналізована імунотерапія раку може стати реальністю. Пацієнти з незбалансованим мікробіомом отримають користь від специфічних штамів пробіотиків, терапії інженерними бактеріями або дієтичних модифікацій. Штучний інтелект допоможе стратифікувати пацієнтів та ідентифікувати ключові механізми, опосередковані мікробіотою. Міждисциплінарна співпраця імунологів, мікробіологів та онкологів може вивести дослідження мікробіоти на центральне місце в прецизійній онкології.
Отже, корекція складу кишкової мікробіоти – це перспективний допоміжний метод підвищення ефективності онкотерапії. І хоча не на всі запитання є відповіді, очевидно, що майбутнє імунотерапії – персоналізоване, і кишкова мікробіота відіграватиме в ньому ключову роль.
За матеріалами: Lei W., Zhou K., Lei Y., Li Q., Zhu H. Gut microbiota shapes cancer immunotherapy responses. npj Biofilms and Microbiomes. 2025;11:143. doi:10.1038/s41522-025-00786-8
Підготувала Анна Сочнєва
Тематичний номер «Онкологія. Гематологія. Хімієтерапія» № 1 (101) 2026 р.