16 квітня, 2026
Сучасні стратегії терапії рецидивуючої та рефрактерної множинної мієломи: роль і переваги карфілзомібу
Множинна мієлома (ММ) залишається невиліковним гематологічним захворюванням, при якому рецидив є неминучим для більшості пацієнтів навіть на тлі сучасної терапії. Попри появу нових класів препаратів, оптимізація застосування інгібіторів протеасом є важливим складником послідовного лікування рецидивуючої та рефрактерної множинної мієломи (р/р ММ). Карфілзоміб – незворотний селективний інгібітор протеасом епоксикетонового ряду – продемонстрував перевагу над бортезомібом за виживаністю без прогресування (ВБП) і загальною виживаністю (ЗВ), а також покращення результатів лікування у складі триплетних комбінацій з імуномодуляторами. Наявність карфілзомібу (Корліса®) в Україні забезпечує доступ вітчизняних клініцистів до сучасної терапії з доведеною ефективністю.
Незважаючи на суттєвий прогрес у терапії з впровадженням імуномодуляторів, інгібіторів протеасом, моноклональних антитіл та нових класів препаратів (біспецифічних антитіл, CAR-T-клітинної терапії), у переважної більшості пацієнтів із ММ із часом настає рецидив [1, 2].
! Особливо складною є терапія хворих, які вже отримали кілька ліній лікування, оскільки розвиток резистентності зумовлений геномною нестабільністю і клональною гетерогенністю захворювання [3].
Кожна наступна лінія терапії характеризується зниженням ефективності та коротшою тривалістю відповіді. У цьому контексті оптимізація застосування добре вивчених класів препаратів, зокрема інгібіторів протеасом, залишається важливим складником послідовної терапії р/р ММ.
Карфілзоміб (carfilzomib) відрізняється від бортезомібу механізмом дії: він утворює необоротний ковалентний зв’язок із каталітичними субодиницями протеасоми, що забезпечує більш потужне та тривале пригнічення протеасомної активності [4, 5]. На відміну від бортезомібу, карфілзоміб характеризується вищою селективністю щодо протеасоми, зумовлює нижчу частоту периферичної нейропатії та можливий для ефективного застосування у пацієнтів, рефрактерних до бортезомібу.
Доказова база: огляд ключових досліджень
Дослідження ENDEAVOR: перевага над бортезомібом
Рандомізоване відкрите дослідження III фази ENDEAVOR мало вирішальне значення для встановлення переваги карфілзомібу над бортезомібом у пацієнтів із р/р ММ, які раніше отримали від однієї до трьох ліній терапії [6]. Під час дослідження порівнювали комбінацію карфілзомібу з дексаметазоном (Kd, карфілзоміб 56 мг/м2 двічі на тиждень, 30-хвилинна інфузія) із комбінацією бортезомібу і дексаметазону (Vd).
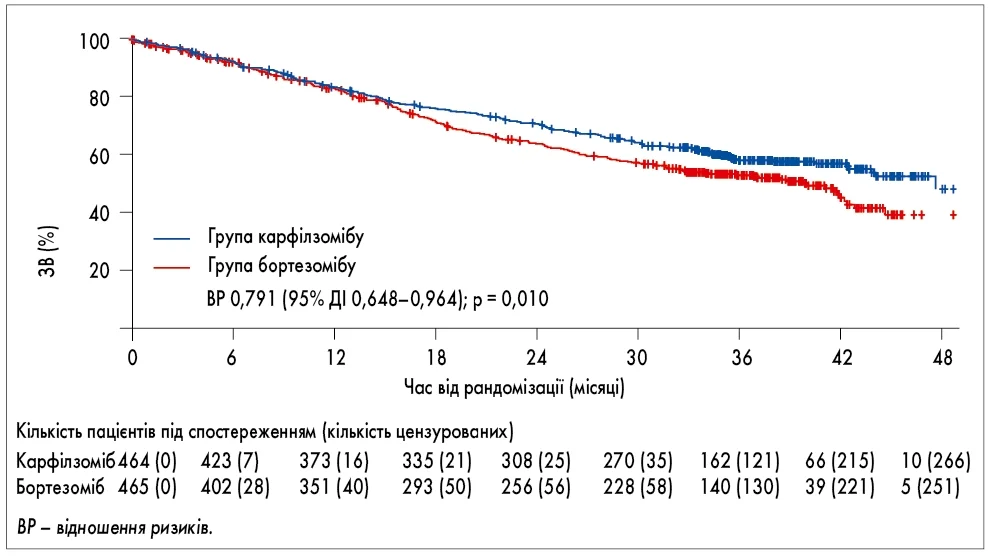
Результати дослідження продемонстрували статистично значуще покращення ВБП у групі карфілзомібу: медіана ВБП становила 18,7 місяця у групі Kd порівняно з 9,4 місяця у групі Vd (ВР 0,53; 95% ДІ 0,44-0,65; p < 0,0001). Крім того, за результатами проміжного аналізу ЗВ було виявлено значуще покращення на користь карфілзомібу (медіана ЗВ – 47,6 проти 40,0 місяця; ВР 0,79; 95% ДІ 0,65-0,96; p = 0,010; рис. 1) [7]. Скорегована за експозицією частота небажаних явищ ≥ 3 ступеня була подібною між групами, хоча у групі карфілзомібу частіше спостерігалися серцево-судинні події, зокрема артеріальна гіпертензія та анемія, тоді як у групі бортезомібу – периферична нейропатія [6, 7].
Рис.1. Загальна виживаність (дослідження ENDEAVOR) [7]
! Отже, дослідження ENDEAVOR переконливо підтвердило, що карфілзоміб у дозі 56 мг/м2 двічі на тиждень у комбінації з дексаметазоном перевершує стандартну терапію бортезомібом із дексаметазоном і за ВБП, і за ЗВ.
Дослідження ASPIRE: ефективність триплетної терапії
Дослідження ASPIRE оцінювало ефективність триплетної схеми KRd (карфілзоміб + леналідомід + дексаметазон) порівняно з Rd (леналідомід + дексаметазон) у пацієнтів із рецидивуючою ММ, які отримали від однієї до трьох попередніх ліній терапії [8].
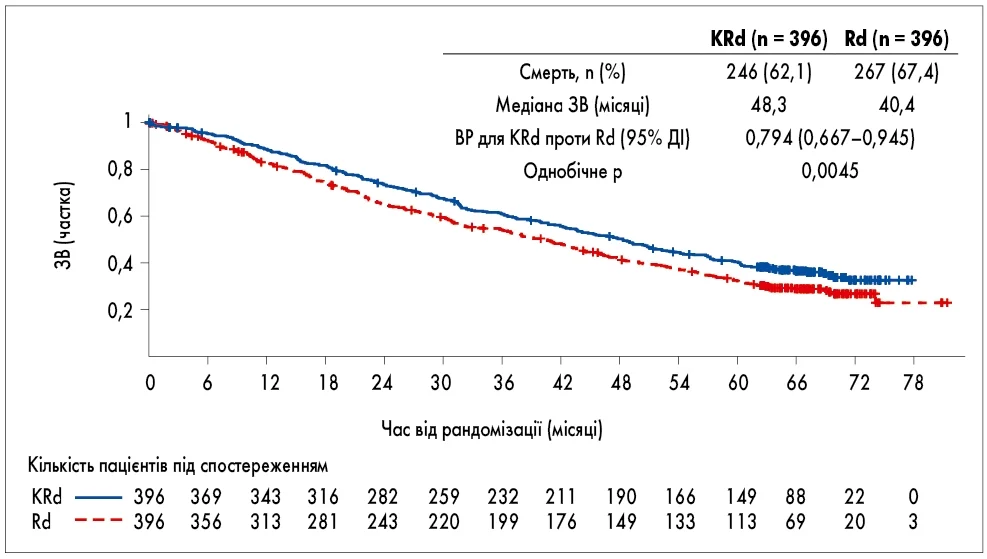
Фінальний аналіз ЗВ продемонстрував статистично значуще покращення ЗВ у групі KRd: медіана ЗВ становила 48,3 місяця у групі KRd проти 40,4 місяця у групі Rd (ВР 0,79; 95% ДІ 0,67-0,95; p = 0,0045). Медіана ВБП становила 26,3 проти 17,6 місяця на користь триплетної комбінації. Частота загальної відповіді (ЧЗВ) у групі KRd сягала 87,1% порівняно з 66,7% у групі Rd, водночас частка пацієнтів, які досягли повної відповіді або кращої, становила 31,8 і 9,3% відповідно (рис. 2) [8].
Рис. 2. Загальна виживаність (дослідження ASPIRE) [8]
! Ці результати підтвердили, що додавання карфілзомібу до леналідоміду та дексаметазону забезпечує клінічно значуще покращення ЗВ при рецидивуючій ММ, встановивши комбінацію KRd як один зі стандартів терапії для цієї категорії пацієнтів.
Реальна клінічна практика: досвід застосування K56Pd
Проспективне багатоцентрове дослідження Jiang F. та співавт. (2025), попередні результати якого були представлені у формі абстракту на 67-му конгресі Американського товариства гематологів (ASH), оцінювало ефективність і безпеку схеми K56Pd (карфілзоміб 56 мг/м2 раз на тиждень + помалідомід + дексаметазон) у пацієнтів із ММ при першому рецидиві в умовах реальної клінічної практики [10].
У дослідження було включено 31 пацієнта (медіана віку – 69 років, діапазон – 39-76). Серед включених пацієнтів 38,7% раніше перенесли аутологічну трансплантацію стовбурових клітин; 90,3% були рефрактерними до леналідоміду; 19,4% – до бортезомібу. Близько половини пацієнтів (51,6%) мала ISS стадію III, 25,8% – екстрамедулярне захворювання [10].
Результати лікування: після двох циклів терапії частка пацієнтів із ≥ ДХЧВ (дуже хрошою частковою відповіддю) становила 22,6, після чотирьох – 63,6%, після шести циклів показник ≥ ДХЧВ досяг 82,4. При медіані спостереження 8,4 місяця медіана ВБП становила 17,0 місяця [10].
Профіль безпеки: режим був керованим. Найчастішими небажаними явищами третього ступеня були анемія і лейкопенія (по 9,68%), інфекції, артеріальна гіпертензія та тромбоцитопенія (по 6,45%). Небажаних явищ четвертого ступеня зареєстровано не було; жоден пацієнт не помер через пов’язані з лікуванням ускладнення [10].
! Ці результати підтверджують ефективність і прийнятну переносимість щотижневого режиму карфілзомібу 56 мг/м2 у складі триплетної комбінації з помалідомідом та дексаметазоном при першому рецидиві ММ в умовах реальної клінічної практики.
Водночас слід враховувати обмеження цього дослідження: невеликий розмір вибірки (n = 31), відсутність контрольної групи і відносно короткий період спостереження (медіана 8,4 місяця).
Профіль безпеки і переносимість
Загальний профіль безпеки карфілзомібу добре вивчений та передбачуваний. Основними побічними ефектами, на які слід звертати увагу, є серцево-судинні події, нефротоксичність і гематологічна токсичність.
Серцево-судинні ризики
Серцева недостатність є відомим побічним ефектом інгібіторів протеасом. Однак дані дослідження A.R.R.O.W. свідчать, що частота серцевої недостатності ≥ 3 ступеня становила при стандартному режимі двічі на тиждень 4% [9]. Частота ішемічної хвороби серця і легеневої гіпертензії була низькою та порівнянною між групами. Нових серцево-судинних подій під час щотижневого режиму виявлено не було.
Нефротоксичність
Гостра ниркова недостатність була найпоширенішою причиною відміни карфілзомібу в обох групах дослідження A.R.R.O.W. (по 2% пацієнтів). Водночас сумарна частота гострої ниркової недостатності 3-4 ступенів становила 6% у групі введення двічі на тиждень, що підтверджує відсутність зростання нефротоксичності під час режиму один раз на тиждень [9].
Периферична нейропатія
На відміну від бортезомібу, карфілзоміб характеризується низькою частотою периферичної нейропатії. У дослідженні A.R.R.O.W. периферична нейропатія будь-якого ступеня спостерігалася у 6% у групі двократного введення, водночас нейропатія ≥ 3 ступеня була зареєстрована менше ніж в 1% випадків [9].
У дослідженні K56Pd профіль безпеки щотижневого карфілзомібу 56 мг/м2 у триплетній комбінації з помалідомідом та дексаметазоном також був керованим: небажаних явищ четвертого ступеня зареєстровано не було, що підтверджує сприятливий профіль безпеки щотижневого режиму в умовах реальної практики [10]. Зведені результати ключових досліджень карфілзомібу наведено в таблиці.
|
Таблиця. Результати ключових досліджень |
||||
|
Дослідження |
Порівняння |
Медіана ВБП |
ЧЗВ |
Ключова перевага |
|
ENDEAVOR |
Kd (56 мг/м2 2ґ/тижд.) vs Vd (n = 929) |
18,7 vs 9,4 міс. |
77% vs 63% |
Покращення ЗВ (47,6 vs 40,0 міс.) та ВБП |
|
ASPIRE |
KRd vs Rd (n = 792) |
26,3 vs 17,6 міс. |
87,1% vs 66,7% |
Покращення ЗВ (48,3 vs 40,4 міс.) |
|
K56Pd (Китай) |
K56Pd (56 мг/м2 1ґ/тижд.) (n = 31)* |
17,0 міс. |
90,3% |
≥ ДХЧВ 82,4% (6 циклів) |
|
K56Pd – карфілзоміб 56 мг/м2 + помалідомід + дексаметазон; vs – порівняно з. *Попередні дані, представлені у формі абстракту (ASH 2025); проспективне дослідження без контрольної групи. |
||||
Отже, сукупність наявних доказів свідчить, що карфілзоміб є ефективним засобом терапії р/р ММ, який перевершує бортезоміб за ВБП і ЗВ, демонструє високу ефективність у складі триплетних комбінацій з імуномодуляторами (леналідомідом, помалідомідом) та дексаметазоном. Гнучкість комбінаторних можливостей карфілзомібу (Kd, KRd, KPd, DKd) забезпечує клініцисту широкий вибір терапевтичної стратегії залежно від попереднього лікування та індивідуальної клінічної ситуації, а завдяки наявності препарату Корліса® в Україні ця сучасна терапія доступна для вітчизняних пацієнтів.
Література
Mina R., Radhakrishnan A., Vasudevan A. et al. (2025) Years of life lost to multiple myeloma remains high: A targeted literature review. Blood (2025) 146 (Supplement 1): 2804.https://doi.org/10.1182/blood‑2025-2804
Nijhof I.S., van de Donk N.W., Zweegman S., Henk M. Current and new therapeutic strategies for relapsed and refractory multiple myeloma: an update. Drugs 2018; 78: 19-37.
Taritsa I., Fossel E. (2026) Pathways of Resistance: Modern Multiple Myeloma Therapies and Overcoming Reliance on Genomic Integrity. Int. J. Mol. Sci., 27(3), 1439; https://doi.org/10.3390/ijms27031439
Jayaweera S.P.E., Wanigasinghe Kanakanamge S.P, Rajalingam D. et al. (2021) Carfilzomib: A Promising Proteasome Inhibitor for the Treatment of Relapsed and Refractory Multiple Myeloma. Front Oncol. Nov 10;11:740796. doi: 10.3389/fonc.2021.740796.
Mancuso F., Di Chio C., Di Matteo F. et al. (2025) Recent Advances in the Development of Immunoproteasome Inhibitors as Anti-Cancer Agents: The Past 5 Years. Molecules, 30(3), 755; https://doi.org/10.3390/molecules30030755
Dimopoulos M.A., Moreau P., Palumbo A. et al. (2016) Carfilzomib and dexamethasone versus bortezomib and dexamethasone for patients with relapsed or refractory multiple myeloma (ENDEAVOR): a randomized, phase 3, open-label, multicentre study. Lancet Oncol; 17: 27-38.
Dimopoulos M.A., Goldschmidt H., Niesvizky R. et al. (2017) Carfilzomib or bortezomib in relapsed or refractory multiple myeloma (ENDEAVOR): an interim overall survival analysis of an open-label, randomized, phase 3 trial. Lancet Oncol; 18: 1327-37.
Siegel D.S., Dimopoulos M.A., Ludwig H. et al. (2018) Improvement in overall survival with carfilzomib, lenalidomide, and dexamethasone in patients with relapsed or refractory multiple myeloma. JCO; 36: 728-34.
Moreau P., Mateos M.V., Berenson J.R. et al. (2018) Once weekly versus twice weekly carfilzomib dosing in patients with relapsed and refractory multiple myeloma (A.R.R.O.W.): interim analysis results of a randomised, phase 3 study. Lancet Oncol; 19: 953-64.
Jiang F., Wang X., He Y. et al. (2025) Once-weekly carfilzomib (56 mg/m2), pomalidomide, and dexamethasone (K56Pd) in patients with first-relapsed multiple myeloma: a Multicenter, prospective, Real-world evidence from China. Blood; 146 (Supplement 1): 7569.
Статтю підготовлено за підтримки компанії «Др. Редді’с Лабораторіз» для надання професійної інформації спеціалістам у сфері охорони здоров’я. Містить інформацію про лікарський засіб, яка наявна також у супутньому інфоблоці.
COR‑23.02.2026-ONCO‑7.1
Довідка редакції
Препарат Корліса® (карфілзоміб) – лікарський засіб, показаний для лікування дорослих пацієнтів із множинною мієломою, які отримали принаймні один попередній курс протипухлинної терапії, в комбінації з даратумумабом і дексаметазоном, леналідомідом та дексаметазоном або тільки з дексаметазоном.
Механізм дії. Карфілзоміб являє собою тетрапептидний епоксикетонний інгібітор протеасоми, який селективно і необоротно зв’язується з N-термінальним треоніном активних центрів основної протеолітичної субодиниці 20S, що входить до складу протеасоми 26S, і незначно впливає або не впливає на протеази інших класів. Карфілзоміб виявляв антипроліферативну та проапоптотичну активність у доклінічних моделях гематологічних пухлин. In vitro було виявлено, що карфілзоміб має мінімальну нейротоксичність і реактивність щодо непротеасомних протеаз.
Терапію лікарським засобом Корліса® слід проводити під наглядом лікаря, який має досвід застосування протипухлинних препаратів. Дозу розраховують відповідно до площі поверхні тіла (ППТ) пацієнта. Пацієнти з ППТ понад 2,2 м2 мають отримувати дозу, розраховану для ППТ 2,2 м2. Корегування дози не потрібне, якщо зміни маси тіла не перевищують 20% (табл. 1).
|
Таблиця 1. Режими застосування і дозування (згідно з інструкцією) |
||
|
Комбінація |
Дозування та графік |
Особливості |
|
Із дексаметазоном |
20 мг/м2 (дні 1, 2; макс. 44 мг); при переносимості – підвищення до 56 мг/м2 з 8го дня 1го циклу (макс. доза – 123 мг) |
30хвилинна в/в інфузія, дні 1, 2, 8, 9, 15, 16 |
|
Із леналідомідом та дексаметазоном |
20 мг/м2 (дні 1, 2; макс. 44 мг); з 8го дня 1го циклу – 27 мг/м2 (макс. доза – 60 мг) |
10хвилинна в/в інфузія. З 13го циклу введення у 8 та 9 дні пропускаються |
|
Із даратумумабом та дексаметазоном |
20 мг/м2 (дні 1, 2; макс. 44 мг); з 8го дня 1го циклу – 56 мг/м2 (макс. доза – 123 мг) |
30хвилинна в/в інфузія |
|
Лікування може тривати до прогресування захворювання або появи ознак неприпустимої токсичності. |
||
У разі розвитку токсичності необхідна корекція режиму дозування лікарського засобу Корліса®. Дані про зниження дози наведені у таблиці 2.
|
Таблиця 2. Зниження рівня дози лікарського засобу |
||||
|
Схема введення |
Доза |
Перший рівень зниження дози |
Другий рівень зниження дози |
Третій рівень зниження дози |
|
Корліса®, леналідомід і дексаметазон |
27 мг/м2 |
20 мг/м2 |
15 мг/м2 * |
– |
|
Корліса® і дексаметазон |
56 мг/м2 |
45 мг/м2 |
36 мг/м2 |
27 мг/м2 * |
|
Корліса®, даратумумаб і дексаметазон |
56 мг/м2 |
45 мг/м2 |
36 мг/м2 |
27 мг/м2 * |
|
У разі зниження рівня дози час інфузії лікарського засобу залишається незмінним. * Якщо симптоми зберігаються, необхідно припинити застосування лікарського засобу. |
||||
Тематичний номер «Онкологія. Гематологія. Хімієтерапія» № 1 (101) 2026 р.