31 березня, 2023
Місце інгібіторів протеасоми у сучасних стандартах лікування лімфопроліферативних захворювань: фокус на рецидивну/рефрактерну множинну мієлому
Останнє десятиріччя ознаменувалося значним прогресом у терапії множинної мієломи (ММ). Це пов’язано із застосуванням нового класу препаратів – інгібіторів протеасоми (ІП) та широким використанням аутологічної трансплантації гемопоетичних стовбурових клітин. Незважаючи на те що ММ залишається невиліковним захворюванням, медіана загальної виживаності (ЗВ) пацієнтів після впровадження нової стратегії лікування значно збільшилася. Наразі схеми на основі ІП є новим стандартом лікування рецидивної/рефрактерної (р/р) ММ.
Іксазоміб – перший і єдиний інгібітор протеасоми 20S для перорального застосування, який зв’язується з її β-субодиницею, що має хімотрипсиноподібну активність. Представляємо вашій увазі огляд сучасних даних щодо ефективності та безпеки використання іксазомібу при р/рММ.
Розширення нових ефективних методів лікування лімфопроліферативних захворювань є актуальною проблемою сучасної онкогематології. За останні десятиліття парадигма лікування лімфопроліферативних захворювань, зокрема ММ, значно змінилася. Це пов’язано із впровадженням у клінічну практику нових терапевтичних агентів, таких як імуномодулюючі препарати й ІП, наприклад, бортезоміб. Така зміна фокусу лікування ММ, ймовірно, триватиме й надалі, що пов’язано з розвитком фармацевтики та розробленням нових поколінь лікарських засобів.
Дані попередніх рандомізованих контрольованих досліджень (РКД) ІІІ фази, у яких брали участь пацієнти з уперше виявленою або р/рММ, продемонстрували, що трикомпонентні схеми лікування мають переваги порівняно з двокомпонентними, особливо при включенні до схеми ІП (наприклад, бортезомібу, карфілзомібу або іксазомібу) та кортикостероїду [1-12]. Після впровадження трикомпонентної схеми результати лікування пацієнтів з ММ значно покращилися, що відобразилося на виживаності без прогресування (ВБП), ЗВ, а також 10-річній ЗВ. Проте незважаючи на той факт, що ефективність сучасних схем терапії є значно вищою, ніж попередніх, ММ залишається невиліковним захворюванням. Тому актуальність пошуку нових ефективніших режимів терапії ММ незаперечна [16-19].
Іксазоміб (Нінларо®, Takeda) – єдиний ІП 20S для перорального прийому, що як і бортезоміб є похідним борної кислоти. У листопаді 2015 р. Управління з контролю якості харчових продуктів і лікарських препаратів США (FDA) схвалило застосування іксазомібу у комбінації з леналідомідом і дексаметазоном для лікування пацієнтів з р/рММ, які вже отримали хоча б одну лінію терапії (рис. 1).
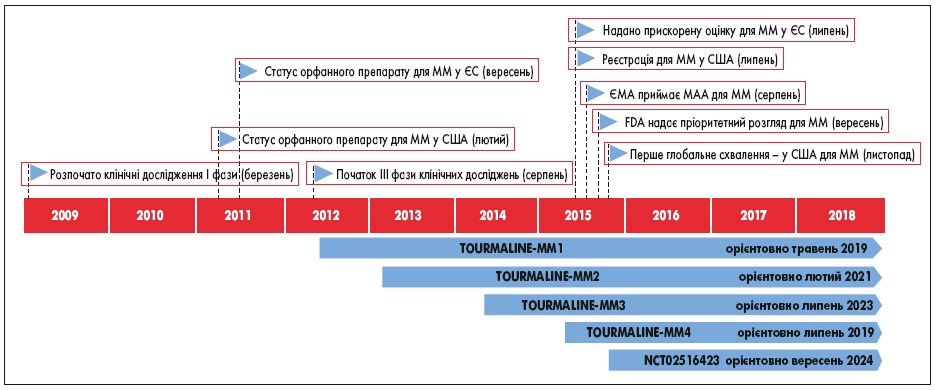 Рис. 1. Впровадження іксазомібу в клінічну практику (прапорці позначають ключові етапи затвердження препарату)
Рис. 1. Впровадження іксазомібу в клінічну практику (прапорці позначають ключові етапи затвердження препарату)
EMA – Європейське агентство з лікарських засобів; MAA – заявка на маркетингову авторизацію; ЄС – Європейський Союз.
Ефективність іксазомібу була оцінена не лише при ММ, а й при інших лімфопроліферативних захворюваннях.
Результати досліджень визначили, що іксазоміб демонструє прийнятний профіль безпеки; загальні побічні явища (ПЯ) включали діарею, закреп і тромбоцитопенію.
Клінічна фармакологія
Механізм дії
Іксазоміб – перший пероральний ІП, схвалений для лікування р/рММ [20]. Препарат є похідним борної кислоти, механізм його дії полягає в інгібуванні протеасоми 20S шляхом зв’язування переважно з її β5-субодиницею, що володіє хімотрипсиноподібною активністю. Крім того, іксазоміб здатний зв’язуватися з β1- і β2-субодиницями, проте це відбувається при концентраціях, що багаторазово перевищують терапевтичну, і тому не має практичного значення. У дослідженнях in vitro було продемонстровано, що іксазоміб запускає апоптоз мієломних клітини як по внутрішньому (каспаза-9), так і зовнішньому (каспаза-8) сигнальних шляхах через активацію проапоптотичних білкових систем p53-p21, p53-NOXA-PUMA і Rb-E2F, а також індукує стрес ендоплазматичного ретикулуму [21].
Наразі наявні результати кількох РКД І фази, проведених із метою визначення фармакологічних характеристик іксазомібу. За отриманими даними, після перорального прийому, потрапляючи у плазму крові, препарат швидко піддається гідролізу з вивільненням біологічно активної сполуки (MLN2238, іксазоміб), яка і чинить ключову фармакологічну дію. Препарат має здатність блокувати деградацію білка шляхом інгібування протеасоми 20S, що входить до складу протеасоми 26S. При нижчих концентраціях MLN2238 пригнічує β5-субодиницю протеасоми, яка має хіміотрипсиноподібну дію. У високих концентраціях MLN2238 інгібує каспазоподібну β1-субодиницю і трипсиноподібну β2-субодиницю [22] (рис. 2).
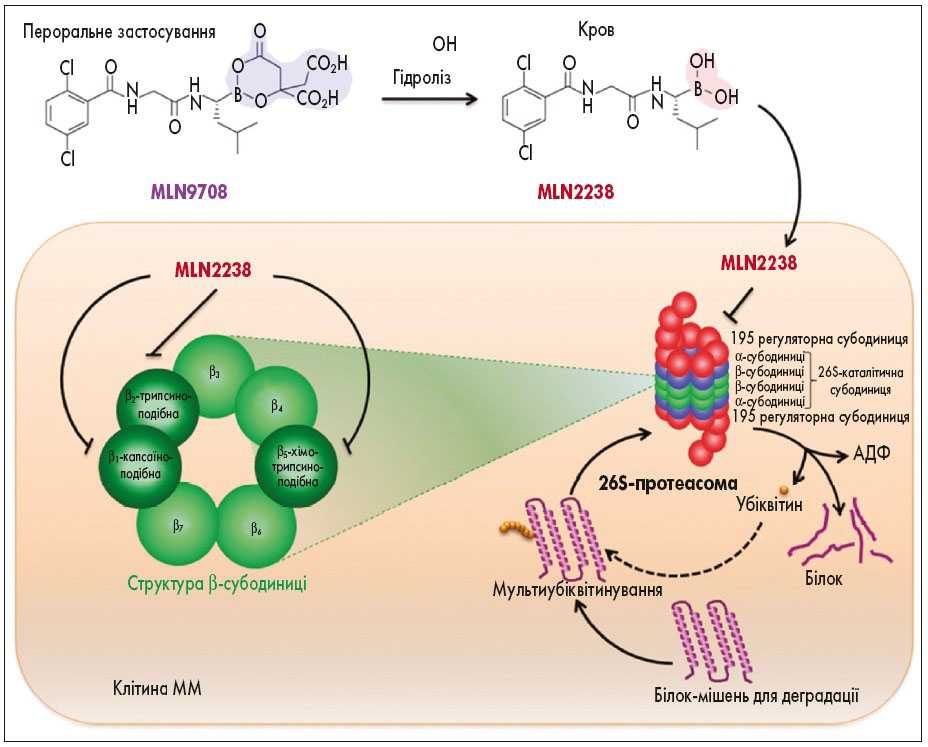 Рис. 2. Механізм дії іксазомібу (адаптовано за Muz et al., 2016)
Рис. 2. Механізм дії іксазомібу (адаптовано за Muz et al., 2016)
Фармакодинаміка
Іксазоміб індукує апоптоз мієломних клітин. Так, інгібування протеасоми за допомогою іксазомібу збільшує доступність IkB у цитоплазмі, що призводить до інгібування ядерного фактора каппа В (NF-kB) і розладу одного з антиапоптотичних механізмів виживання мієломних клітин, зменшуючи вивільнення цитокінів і порушуючи цитопротекторні ефекти на клітини ММ у кістковому мозку [23, 24].
Іксазоміб проявляє дозозалежну цитотоксичність проти клітин ММ у пацієнтів з рецидивом захворювання після кількох попередніх ліній терапії (наприклад, бортезоміб, леналідомід і дексаметазон) і синергічні цитотоксичні ефекти в клітинних лініях ММ при поєднанні з леналідомідом або дексаметазоном. Згідно з даними досліджень in vivo, препарат демонстрував протипухлинну активність на моделі ксенотрансплантата ММ миші [23].
За результатами сучасних РКД іксазоміб має сприятливий профіль безпеки. На фоні його застосування не виявлена кардіотоксичність, притаманна іншим препаратам цієї групи (зокрема, карфілзомібу): не реєструвався клінічно значущий вплив на інтервал QT або частоту серцевих скорочень [25-26].
Фармакокінетика
Після перорального прийому іксазоміб швидко всмоктується, досягаючи пікової концентрації через 1 год [28]. Значення абсолютної біодоступності після перорального застосування складає 58% за результатами популяційного аналізу фармакокінетики. Площа під фармакокінетичною кривою, що описує залежність концентрація/час (AUC), збільшується дозозалежним чином у діапазоні доз іксазомібу від 0,2 до 10,6 мг.
Метаболізм
Після перорального прийому дози препарату з радіоізотопною міткою іксазоміб становив 70% всього пов’язаного із препаратом радіоактивного матеріалу у плазмі крові. Основним механізмом виведення іксазомібу вважають метаболізм під дією множинних ферментів CYP та не-CYP білків. За рахунок того, що іксазоміб не впливає на інгібування або індукцію ферментів CYP, відсутній ризик розвитку міжлікарських взаємодій [29].
Особливі групи пацієнтів
Не спостерігалося клінічно значущого впливу віку (в діапазоні 23-91 року), статі, площі поверхні тіла або расової належності на кліренс іксазомібу [30]. Відповідно до даних РКД, пацієнтам з помірною або тяжкою печінковою недостатністю, термінальною стадією ниркової недостатності, при якій необхідний діаліз, або тяжкою нирковою недостатністю рекомендовано знизити початкову дозу іксазомібу до 3 мг [31, 32].
Клінічні дослідження
Наявна значна кількість РКД І, ІІ і ІІІ фази, в яких оцінювали ефективність і безпеку застосування іксазомібу при лімфопроліферативних захворюваннях, у тому числі при ММ. У реєстраційне подвійне сліпе порівняльне дослідження III фази TOURMALINE-MM1 було рандомізовано 722 пацієнти з рецидивуючою ММ, які додатково до стандартної схеми леналідомід (25 мг/день у 1-21-й дні) + дексаметазон (40 мг щотижня; Rd) приймали іксазоміб (IRd) у дозі 4 мг у 1-й, 8 та 15-й дні або плацебо (плацебо-Rd) в ті ж дні у 28-денних циклах [33]. За результатами дослідження, медіана ВБП була значно довшою на фоні застосування іксазомібу, ніж у групі плацебо (20,6 порівняно з 14,7 міс; відношення ризиків 0,74; р=0, 01) у загальній популяції пацієнтів. Частота об’єктивної відповіді (objective response rate – ORR) та дуже хорошої часткової відповіді (very good partial response – VGPR) були вищими в групі IRd і становили 78 та 48%, а у групі плацебо-Rd – 72 та 39% відповідно. Медіана відповіді у групах IRd та плацебо-Rd дорівнювала 1,1 та 1,9 міс відповідно. Що стосується медіани тривалості відповіді, вона складала 20,5 міс у групі IRd та 15,0 міс у групі плацебо-Rd.
Згідно з отриманими даними щодо безпеки терапії, пацієнти у групах IRd та плацебо-Rd мали подібну частоту серйозних ПЯ (47 і 49%) та відміни терапії через її токсичність (17 та 14% випадків). Тромбоцитопенію, висип і гастроінтестинальні порушення частіше реєстрували у групі IRd. Частота тромбоцитопенії становила 31% у групі IRd та 16% – плацебо-Rd. Частота периферичної нейропатії складала 27% у групі IRd та 22% у групі плацебо-Rd. Обидві групи мали зіставну якість життя.
Завдяки результатам дослідження TOURMALINE-MM1 іксазоміб був зареєстрований FDA як перший пероральний ІП, схвалений у комбінації з леналідомідом і дексаметазоном (режим IXA-LEN-DEX) для лікування пацієнтів, які попередньо отримали принаймні одну лінію терапії.
В інше дослідження J. Hou та співавт. (2017), що стало продовженням TOURMALINE-MM1, були включені пацієнти з більш запущеною стадією ММ, які отримували інтенсивніше попереднє лікування, частіше мали рефрактерну ММ [34]. Дизайн дослідження відповідав TOURMALINE-MM1, пацієнти були розподілені на дві групи: перша група отримувала IRd, друга група – плацебо-Rd. Результати дослідження продемонстрували, що на фоні застосування іксазомібу медіана ВБП і ЗВ становила 6,7 та 25,8 міс, а у групі плацебо-Rd – 4,0 та 15,8 міс. Що стосується профілю безпеки, то 67% (38/57) пацієнтів групи IRd і 74% (43/58) групи плацебо-Rd повідомили про розвиток ПЯ, таких як тромбоцитопенія, нейтропенія та анемія [34].
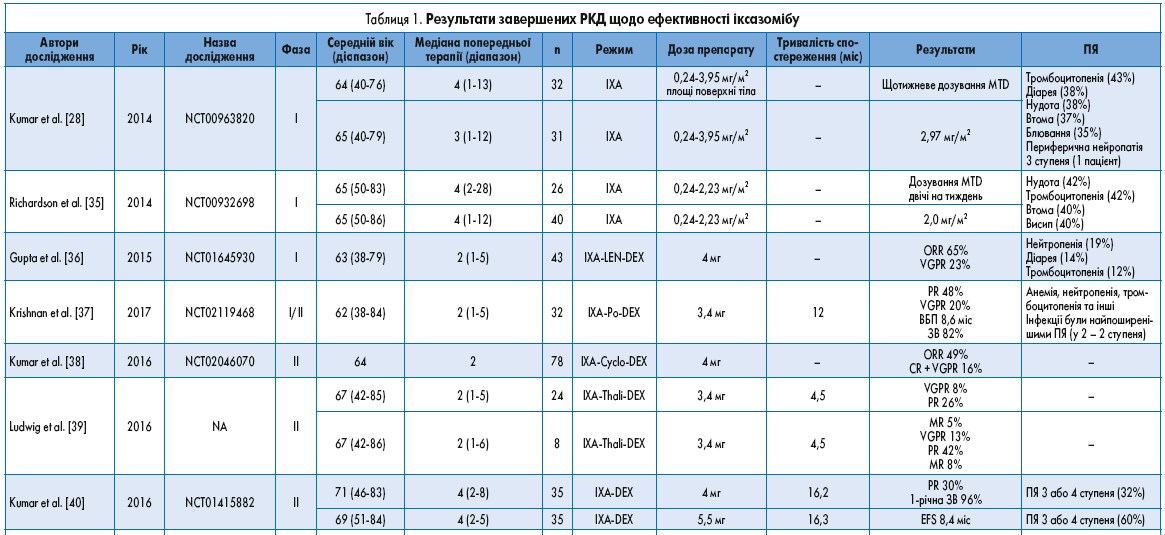
У 2017 р. були презентовані результати обсерваційного дослідження E. Terpos та співавт., ключовою метою якого було ретроспективно проаналізувати дані щодо ефективності схеми IRd у пацієнтів з р/рММ. Згідно з отриманими даними, на фоні застосування трикомпонентної терапії IRd ORR склала 68,5%, а медіана ВБП – 27,6 міс. Детальніша характеристика проведених і поточних досліджень щодо ефективності та безпеки застосування іксазомібу при р/рММ наведена в таблицях 1 і 2.
Переносимість і безпека
У згадуваному раніше дослідженні N. Gupta та співавт. (2015) [36] зазначено, що з 43 азійських пацієнтів із р/рММ, які отримували IRd, у 21 (49%) було виявлено принаймні одне ПЯ ≥3 ступеня, пов’язане з прийомом іксазомібу. Найчастішими побічними ефектами були нейтропенія (19%), діарея (14%) і тромбоцитопенія (12%). У випадках окремого використання іксазомібу у пацієнтів з ММ побічні ефекти були рідкісними. Діарея ≥2 ступеня виявлена у 24% цих пацієнтів, тромбоцитопенія ≥3 ступеня – у 28%, а втома ≥2 ступеня – у 26% [38].
У дослідженні ІІІ фази TOURMALINE-MM1 загальні ПЯ частіше спостерігалися в групі IRd, ніж у групі плацебо-Rd. В основному вони були представлені тромбоцитопенією, нудотою, блюванням, діареєю, закрепом, висипом, периферичною нейропатією, периферичним набряком і болем у спині. Ці ПЯ здебільшого були 1/2 ступеня тяжкості, за винятком тромбоцитопенії (19 проти 9% 3/4 ступеня), яка була контрольованою та зворотною, без відмінностей між групами.
Таким чином, основними проблемами безпеки, які вимагають обережного застосування іксазомібу, є тромбоцитопенія, гастроінтестинальні ураження, периферична нейропатія та набряк, шкірні реакції та гепатотоксичність [24, 26, 31, 32, 34, 37]. Імовірно, вищі дози іксазомібу будуть спричиняти ще вищу токсичність, тому пацієнтам, які отримують високодозову терапію, рекомендовано знижувати дозу іксазомібу до 4 мг. У дослідженні S.K. Kumar та співавт. (2016) було продемонстровано, що частота ПЯ 3 і 4 ступеня при введенні цього препарату в дозі 5,5 мг була значно вищою, ніж у дозі 4,0 мг (60 проти 32%) [36]. При наявності у хворого ПЯ рекомендоване поступове зниження дози аж до повної відміни препарату. Важливо також зазначити, що периферична нейропатія, яка вважається одним із ключових дозолімітуючих ПЯ бортезомібу [10, 43], була незначною при застосуванні іксазомібу. Таким чином, сучасні дані РКД свідчать, що ПЯ, які розвиваються на фоні застосування іксазомібу, є здебільшого керовані та зворотні за рахунок корекції дози препарату.
Економічна ефективність
Доведено, що іксазоміб є ефективним препаратом для лікування р/рММ. Витрати систем охорони здоров’я на лікування пацієнтів з р/рММ дуже високі в усьому світі, відповідно застосування іксазомібу асоціюється зі ще більшим фінансовим тягарем. Тому необхідний пошук балансу між вартістю лікування та клінічними результатами [44, 45].
Дані сучасних досліджень свідчать, що іксазоміб як перший ІП для перорального застосування має високий профіль ефективності та безпеки. Прийом препарату не супроводжується розвитком ПЯ, які притаманні іншим представникам цієї групи, зокрема бортезомібу і карфілзомібу. Наразі іксазоміб схвалений до застосування з метою лікування р/рММ.
Список літератури знаходиться у редакції.
За матеріалами Xie J. et al. Ixazomib – the first oral proteasome inhibitor. Leukemia & Lymphoma. 2019; 60 (3): 610-618. Doi: 10.1080/10428194.2018.1523398.
Підготувала Анна Хиць
VV-MEDMAT-81806
Тематичний номер «Онкологія. Гематологія. Хіміотерапія» № 1 (80) 2023 р.