29 жовтня, 2020
Осимертиніб у лікуванні хворих на недрібноклітинний рак легені з метастазами у головному мозку
Вибір оптимальної тактики лікування пацієнтів з недрібноклітинним раком легені (НДРЛ) – питання складне, особливо зважаючи на значну частку поширених і метастатичних форм захворювання. Вітчизняний клінічний досвід застосування таргетної терапії у пацієнтів із цією патологією був представлений такими фахівцями, як Ольга Володимирівна Пономарьова, Олег Ігорович Кобзєв та Тетяна Володимирівна Рослякова, у рамках спеціалізованих вебінарів, що відбулися 15 травня та 24 червня цього року.
Серед новітніх таргетних препаратів привертає увагу осимертиніб (osimertinib) – незворотний інгібітор тирозинкінази (TKI) рецептора епідермального фактора росту (EGFR), який чинить вплив у тому числі і на Т790М резистентну мутацію. Управління з контролю якості харчових продуктів і лікарських препаратів (FDA) США та Європейська медична асоціація (EMA) схвалили осимертиніб для першої лінії терапії місцево-поширеного або метастатичного НДРЛ з активуючими мутаціями EGFH чи позитивним статусом мутації Т790М EGFR. Наразі відомі численні TKI EGFR ІІІ покоління, проте схвалення регуляторних органів поки що отримав лише осимертиніб.
 Кандидат медичних наук, доцент кафедри онкології НМАПО ім. П.Л. Шупика, завідувачка відділення хіміотерапії № 1 КНП «Київський міський клінічний онкологічний центр» Ольга Володимирівна Пономарьова представила розбір клінічних досліджень, які були присвячені осимертинібу.
Кандидат медичних наук, доцент кафедри онкології НМАПО ім. П.Л. Шупика, завідувачка відділення хіміотерапії № 1 КНП «Київський міський клінічний онкологічний центр» Ольга Володимирівна Пономарьова представила розбір клінічних досліджень, які були присвячені осимертинібу.
– НДРЛ часто метастазує в центральну нервову систему (ЦНС). За даними M. Riihimaki та співавт. (2014), НДРЛ метастазує у ЦНС у 39-47% випадків, у кістки – у 34‑39%, у печінку – у 35%, у надниркові залози – у 8%, додаткові вогнища у легенях діагностують у 18-22% хворих. На метастазування та виживаність впливають стать хворого, гістологічний підтип, вік на момент встановлення діагнозу та локалізація первинного ураження.
Метастази у ЦНС включають метастази у головному мозку та лептоменінгеальні метастази і частіше зустрічаються при НДРЛ з мутацією EGFR. Метастази у головному мозку при первинній діагностиці частіше виявляють у пацієнтів з мутацією EGFR, ніж при його дикому типі (19-24 проти 11-13% відповідно). Під час подальшого спостереження метастази у головному мозку спостерігали щонайменше у 44% пацієнтів з НДРЛ і мутацією EGFR та 22% – з диким типом EGFR. Аналогічна тенденція відмічена і щодо лептоменінгеальних метастазів (9,4 проти 1,7% відповідно). Останні виникають внаслідок поширення пухлинних клітин у лептоменінгеальний і субарахноїдальний простір. Вони розвиваються на пізніх стадіях з більшим об’ємом пухлинної маси та при швидкому прогресуванні процесу. Лептоменінгеальні метастази пізно діагностуються та характеризуються поганим прогнозом за відсутності протипухлинного лікування.
Хворі на НДРЛ з метастатичним ураженням ЦНС донедавна мали вкрай поганий прогноз. Ситуація покращилася із впровадженням новітніх перспективних протипухлинних препаратів. Вважається, що ЦНС є недосяжною зоною для більшості традиційних хіміотерапевтичних препаратів, оскільки неушкоджений гематоенцефалічний бар’єр (ГЕБ) обмежує їх проникнення та дію. Медіана виживаності у пацієнтів з НДРЛ відрізняється залежно від часу діагностики метастатичного процесу у ЦНС. Так, якщо вторинне ураження було встановлено під час первинної діагностики, то цей показник становить 4,8 міс, якщо після встановлення діагнозу – то зростає до 9,8 міс. У пацієнтів, які отримали лікування, медіана загальної виживаності коливається в межах 6,2-12,1 міс. Лептоменінгеальні метастази за відсутності лікування призводять до летального наслідку через 4-6 тижнів. Проте у пацієнтів, які отримали протипухлинну терапію з досягненням об’єктивної відповіді, медіана виживаності становить від 4 до 9 міс.
Відповідно до публікації A.F. Eichler та співавт. (2007), метастатичне ураження може локалізуватись у різних відділах головного мозку. Близько 80% випадків припадає на вторинне ураження півкуль великого мозку. У 15% випадків метастази діагностують у мозочку, у 5% – у стовбурі мозку. Відомо, що розташування метастатичних вогнищ у головному мозку істотно впливає на якість життя пацієнтів.
Проведено дослідження (S. Peters et al., 2016) впливу олігометастатичного ураження на якість життя пацієнтів, в якому було продемонстровано найбільш виражений негативний вплив саме при ураженні ЦНС.
Метастазування НДРЛ у ЦНС відбувається шляхом гематогенного поширення клітин з первинної пухлини. Метастатичне вогнище росте завдяки пухлинному мікрооточенню, внаслідок зв’язування пухлинних клітин з ендотеліальними клітинами, екстравазацією, каскадом нейрозапальних реакцій і неоваскуляризації, що сприяє росту метастазів (H.H. Popper et al., 2016; S.A. Achal et al., 2019).
Існують особливості транспорту через ГЕБ, що впливають на ефективність протипухлинної терапії. ГЕБ – високоселективна напівпроникна мембрана, яка відділяє циркулюючу кров від мозку та позаклітинної рідини у ЦНС. ГЕБ складається з ендотеліальних клітин, перицитів, астроцитів, які формують постійні щільні з’єднання, що обмежують проникнення макромолекул у головний мозок. Проникність ГЕБ залежить від кількох факторів:
- ліпофільність речовини та щільність міжклітинних контактів, які зменшують кількість речовин, що можуть вільно проникати через ГЕБ;
- молярна маса речовини та розмір молекули. Молекули з масою понад 500 г/моль не можуть проникати через ГЕБ. Процес клітинної дифузії є динамічним і значно простішим для речовин з молярною масою 200 г/моль. Високомолекулярні сполуки (наприклад, моноклональні антитіла, рекомбінантні білки та інші) стримуються ГЕБ;
- активність транспортної ефлюкс-системи, яка здатна зменшувати концентрацію лікарських речовин у ЦНС.
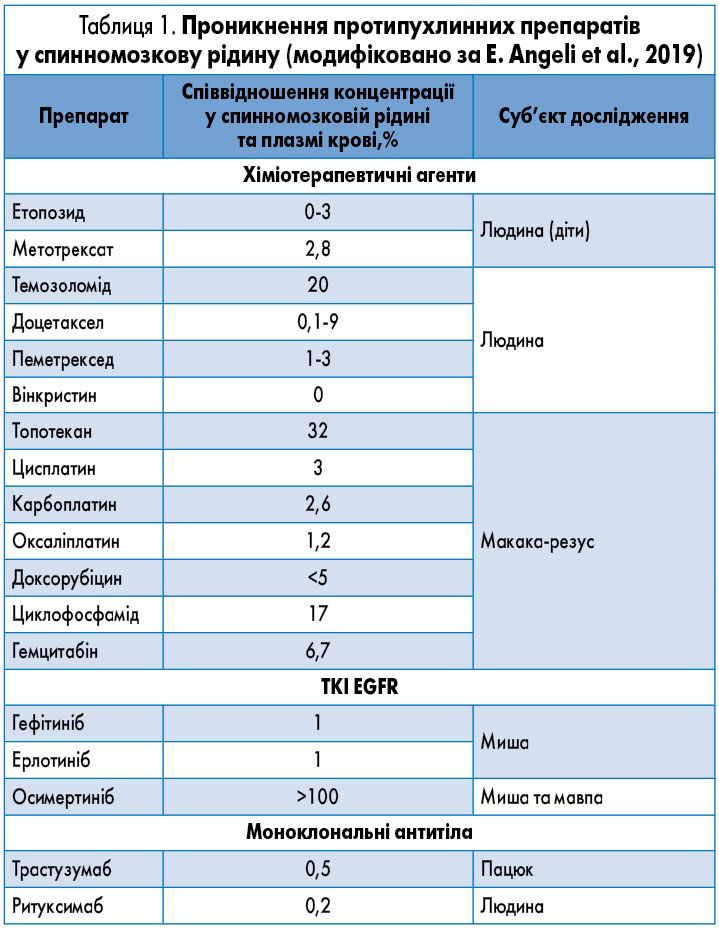 Здатність різних протипухлинних препаратів проникати у спинномозкову рідину істотно відрізняється (табл. 1). Серед традиційних цитотоксичних агентів лідерські позиції займають темозоломід і топотекан. Співвідношення концентрації осимертинібу в спинномозковій рідині до такої у плазмі крові становить понад 100%, тоді як для гефітинібу та ерлотинібу аналогічний показник дорівнює одиниці. Всі інші препарати погано проникають у спинномозкову рідину та не створюють терапевтичні концентрації у тканинах головного мозку.
Здатність різних протипухлинних препаратів проникати у спинномозкову рідину істотно відрізняється (табл. 1). Серед традиційних цитотоксичних агентів лідерські позиції займають темозоломід і топотекан. Співвідношення концентрації осимертинібу в спинномозковій рідині до такої у плазмі крові становить понад 100%, тоді як для гефітинібу та ерлотинібу аналогічний показник дорівнює одиниці. Всі інші препарати погано проникають у спинномозкову рідину та не створюють терапевтичні концентрації у тканинах головного мозку.
На сьогодні відповідно до рекомендацій Європейського товариства медичних онкологів вибір стратегії лікування при НДРЛ з метастатичним ураженням ЦНС залежить від статусу мутації (EGFR або ALK) та кількості вторинних вогнищ у головному мозку (менше чи більше трьох). Доцільність застосування тотального опромінення головного мозку останнім часом активно дискутується. При поширеному ураженні головного мозку (зважаючи на поганий прогноз у цій групі) розглядається найкраща супровідна терапія та паліативна допомога. Схематично тактика лікування наведена в таблиці 2.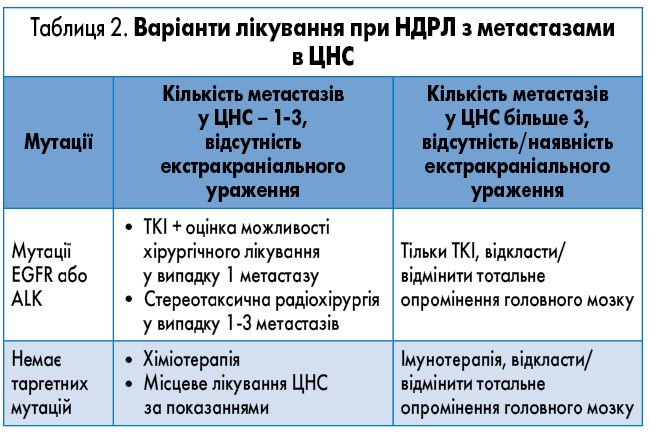
Неповне проникнення через ГЕБ TKI EGFR першого і другого поколінь робить можливим розвиток метастазів у головному мозку (в тому числі з ізольованим прогресуванням у ЦНС). Завдяки наявності ГЕБ лікарські засоби можуть потрапляти у мозок лише в субтерапевтичних дозах, що уможливлює повторний розвиток захворювання з мутацією EGFR. Нерідко субтерапевтичні дози призводять до стимуляції пухлинного росту.
Осимертиніб характеризується доброю проникністю через ГЕБ. На основі даних in vitro встановлено, що осимертиніб є інгібітором P-глікопротеїну (P-gp) та білка резистентності до раку молочної залози (BCRP), а також є субстратом як P-gp, так і BCRP.
P-gp та BCRP є транспортними системами виведення лікарських засобів, належать до сімейства білків АВС-транспортерів, великої групи трансмембранних білків, які спеціалізуються на переміщенні низькомолекулярних сполук через мембрани. АВС-транспортери розташовані в апікальній мембрані ендотеліальних клітин судин, які формують ГЕБ, де вони можуть активно виштовхувати із клітини різноманітні препарати та їх метаболіти. Підвищена активність білків-транспортерів пов’язана з розвитком резистентності до фармакотерапії у клітин пухлини. Тому пригнічення P-gp та BCRP вважається доцільним для підвищення ефективності терапії.
На клітинних лініях Сасо2, які експресують P-gp та BCRP, встановлено, що осимертиніб був єдиним препаратом без проявів ефлюксу та не зазнавав активного виведення з клітин. Це вказує на його достатню проникну здатність для подолання механізму ефлюксу у клітинних лініях. Відмічено також, що проникнення інших TKI EGFR було заблоковано внаслідок ефлюксу.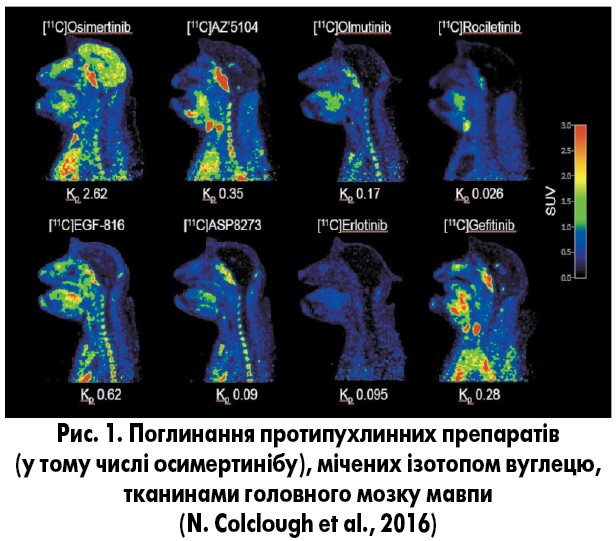
В експериментальних дослідженнях було показано найбільшу проникну здатність і тропність осимертинібу до тканини головного мозку порівняно з іншими протипухлинними препаратами, що цілком пояснює його високу клінічну активність (рис. 1). У здорових добровольців без ушкоджень ГЕБ осимертиніб також рівномірно проникав і накопичувався у всіх відділах головного мозку (рис. 2).
У дослідженні FLAURA осимертиніб порівнювали з гефітинібом та ерлотинібом. Відмічено більш прийнятний профіль токсичності осимертинібу. На рисунку 3 відображено криві виживаності, що ілюструють перевагу осимертинібу над ТКІ ранніх поколінь. Частота об’єктивної відповіді, кількість випадків повної відповіді була вища в підгрупі осимертинібу порівняно з ТКІ першого покоління. Частота об’єктивної відповіді метастатичних вогнищ у ЦНС у підгрупі з вимірюваними метастазами була також вища. Повна відповідь спостерігалась тільки в групі осимертинібу та не була характерна для ТКІ першого покоління. Медіана найкращої зміни розміру цільового вогнища в ЦНС від початкового рівня становила -64% у пацієнтів, які отримували осимертініб, тоді як для препаратів першого покоління складала -45%.

Рис. 2. Поглинання осимертинібу, міченого ізотопом вуглецю, тканинами головного мозку здорових добровольців з неушкодженим ГЕБ (A. Varrone et al., 2019)
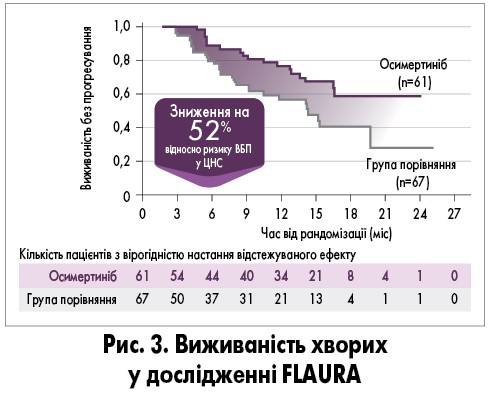 За результатами дослідження FLAURA було зроблено такі висновки. Осимертиніб продемонстрував статистично значуще й істотне з клінічної точки зору покращення виживаності без прогресування у пацієнтів з НДРЛ і мутацією EGFR, з метастатичними вогнищами в ЦНС відносно препаратів порівняння (ТКІ). Медіана виживаності без прогресування у ЦНС не була досягнута у пацієнтів, які отримували осимертиніб, у контрольній групі становила 13,9 міс (відношення ризику 0,48; 95% довірчий інтервал – ДІ – 0,26‑0,86; р=0,014). Спостерігалася менша кількість подій прогресування в ЦНС та менше нових вогнищ у ЦНС при використанні осимертинібу. Частота об’єктивної відповіді метастатичних вогнищ у ЦНС була вища в осимертинібу: у пацієнтів з вимірюваними та/або не вимірюваними метастазами в ЦНС 66 проти 43%, у підгрупі з вимірюваними метастазами в ЦНС – 91 проти 68%. Привертає увагу той факт, що відповідь на лікування осимертинібом з боку ЦНС була стійкою.
За результатами дослідження FLAURA було зроблено такі висновки. Осимертиніб продемонстрував статистично значуще й істотне з клінічної точки зору покращення виживаності без прогресування у пацієнтів з НДРЛ і мутацією EGFR, з метастатичними вогнищами в ЦНС відносно препаратів порівняння (ТКІ). Медіана виживаності без прогресування у ЦНС не була досягнута у пацієнтів, які отримували осимертиніб, у контрольній групі становила 13,9 міс (відношення ризику 0,48; 95% довірчий інтервал – ДІ – 0,26‑0,86; р=0,014). Спостерігалася менша кількість подій прогресування в ЦНС та менше нових вогнищ у ЦНС при використанні осимертинібу. Частота об’єктивної відповіді метастатичних вогнищ у ЦНС була вища в осимертинібу: у пацієнтів з вимірюваними та/або не вимірюваними метастазами в ЦНС 66 проти 43%, у підгрупі з вимірюваними метастазами в ЦНС – 91 проти 68%. Привертає увагу той факт, що відповідь на лікування осимертинібом з боку ЦНС була стійкою.
Згідно з аналізом даних по підгрупах у дослідженні AURA3, у пацієнтів з вимірюваними метастазами в ЦНС частота об’єктивної відповіді для осимертинібу становила 70% (95% ДІ 51-85) порівняно з хіміотерапією – 31% (95% ДІ 11-59); ВШ 5,13 (95% ДІ 1,44-20,64), р=0,015. Медіана тривалості відповіді складала 8,9 та 5,7 міс відповідно. Частота об’єктивної відповіді метастатичних уражень ЦНС у пацієнтів, які отримали променеву терапію протягом 6 міс після рандомізації, порівняно з попереднім опроміненням становила для осимертинібу 64 та 34% відповідно, для хіміотерапії – 22 та 16% відповідно. Медіана найкращої зміни розміру цільового вогнища в ЦНС від початкового рівня становила -43% для осимертинібу проти -16% для хіміотерапії.
Отримані дані свідчать про ефективність осимертинібу у відношенні метастатичного ураження ЦНС як терапії першої лінії у пацієнтів з НДРЛ і мутацією EGFR, а також другої лінії після прогресування на тлі TKI I покоління та наявності мутації резистентності T790M. Також ці дані вказують на зниження ризику прогресування захворювання у ЦНС при використанні осимертинібу відносно препаратів порівняння.
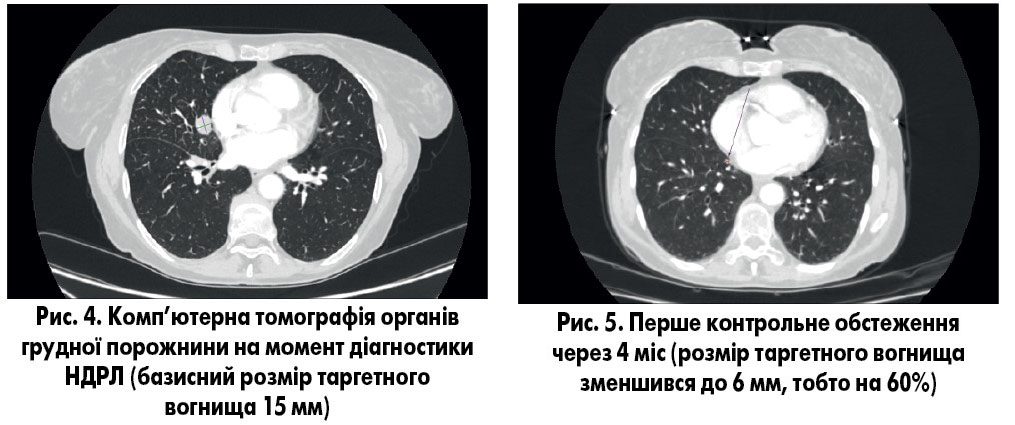
 Олег Ігорович Кобзєв (завідувач онкохірургічного відділення органів грудної порожнини КНП «Обласний центр онкології», м. Харків) під час вебінару навів клінічний випадок, який демонструє активність осимертинібу (рис. 4-6).
Олег Ігорович Кобзєв (завідувач онкохірургічного відділення органів грудної порожнини КНП «Обласний центр онкології», м. Харків) під час вебінару навів клінічний випадок, який демонструє активність осимертинібу (рис. 4-6).
Клінічний випадок 1
Пацієнтка К., 64 роки, з метастатичною формою НДРЛ (ураження легень і метастази у кістках), яка ніколи не курила, на момент встановлення діагнозу мала скарги на загальну слабкість, біль у ділянці крижово-клубового зчленування. Гістологічно встановлено, що пухлина представлена аденокарциномою, EGFR+ ALK- ROS- PDL1 5%.
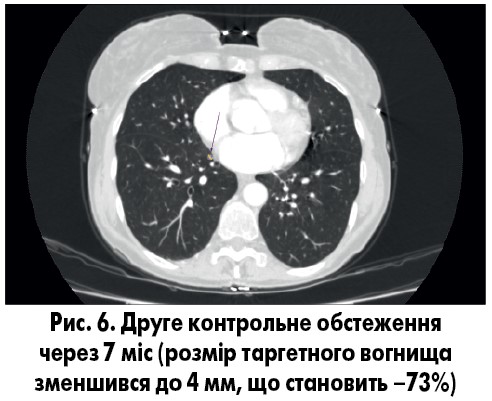 Лікування: пацієнтка отримала курс аналгезуючої дистанційної променевої терапії на ділянку крижово-клубового зчленування (сумарна вогнищева доза 30 Гр), остеомодифікуючі агенти (золедронова кислота 4 мг в/в через кожні 28 днів) та таргетну терапію осимертинібом 80 мг 1 р/д.
Лікування: пацієнтка отримала курс аналгезуючої дистанційної променевої терапії на ділянку крижово-клубового зчленування (сумарна вогнищева доза 30 Гр), остеомодифікуючі агенти (золедронова кислота 4 мг в/в через кожні 28 днів) та таргетну терапію осимертинібом 80 мг 1 р/д.
Через рік після лікування пацієнтка не має скарг, пов’язаних із основним захворюванням, відмічаються незначні побічні явища (лущення шкіри обличчя 1-2 ступеня тяжкості).
 Тетяна Володимирівна Рослякова (клінічний онколог Клініки Образцова, м. Київ) представила клінічний випадок, радіологічні дані якого яскраво ілюструють ефективність застосування осимертинібу при вторинному ураженні ЦНС у хворої на НДРЛ.
Тетяна Володимирівна Рослякова (клінічний онколог Клініки Образцова, м. Київ) представила клінічний випадок, радіологічні дані якого яскраво ілюструють ефективність застосування осимертинібу при вторинному ураженні ЦНС у хворої на НДРЛ.
Клінічний випадок 2
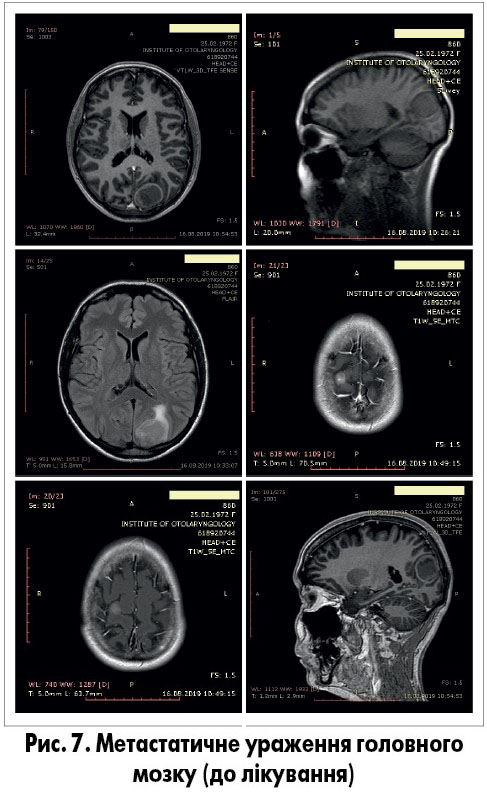 Пацієнтка М., 47 років, звернулася зі скаргами на кашель з мокротинням. За даними комп’ютерної томографії та подальшої позитронно-емісійної томографії з комп’ютерною томографією було виявлено пухлину лівої легені з метастатичним ураженням кісток. Під контролем комп’ютерної томографії виконано біопсію пухлини легені, патогістологічний висновок з імуногістохімічним дослідженням – аденокарцинома EGFR+ ALK- ROS- PDL+. Шляхом магнітно-резонансної томографії на момент встановлення діагнозу було ідентифіковано два метастатичних вогнища у головному мозку: 3,2×2,7×3,1 см у лівій тім’яно-потиличній та 1,5×1,2 см у правій лобній ділянці (рис. 7). Ураження головного мозку не супроводжувалось вогнищевою симптоматикою.
Пацієнтка М., 47 років, звернулася зі скаргами на кашель з мокротинням. За даними комп’ютерної томографії та подальшої позитронно-емісійної томографії з комп’ютерною томографією було виявлено пухлину лівої легені з метастатичним ураженням кісток. Під контролем комп’ютерної томографії виконано біопсію пухлини легені, патогістологічний висновок з імуногістохімічним дослідженням – аденокарцинома EGFR+ ALK- ROS- PDL+. Шляхом магнітно-резонансної томографії на момент встановлення діагнозу було ідентифіковано два метастатичних вогнища у головному мозку: 3,2×2,7×3,1 см у лівій тім’яно-потиличній та 1,5×1,2 см у правій лобній ділянці (рис. 7). Ураження головного мозку не супроводжувалось вогнищевою симптоматикою.
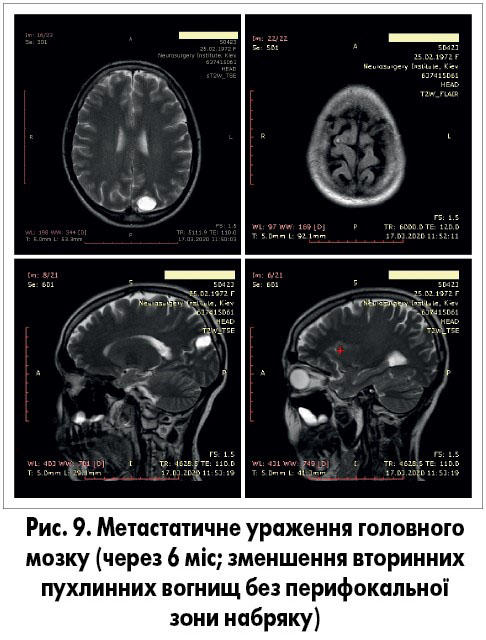
Лікування: пацієнтка отримала терапію осимертинібом 80 мг, бісфосфонатами, виконано радіохірургічне втручання на вогнища в головному мозку. Через 3 міс пацієнтка помітила часткове випадіння бокових полів зору. За даними магнітно-резонансної томографії відмічено зменшення метастатичного вогнища у лівій тім’яно-потиличній ділянці до 2,7×2,7×3,1 та перифокальну зону набряку 1,1 см (рис. 8). У зв’язку з цим пацієнтці додатково призначено терапію дексаметазоном протягом 1 міс без відміни осимертинібу. Через 6 міс розмір вторинного вогнища зменшився та становив 2,4×1,8×1,8 см, без набряку, а ураження у правій лобній ділянці майже не визначалось (рис. 9).
За даними комп’ютерної томографії зафіксована позитивна динаміка як щодо основного вогнища у легені, так і метастатичних вогнищ у ЦНС та кістках. За період терапії осимертинібом пацієнтка істотних побічних явищ не відмічала.
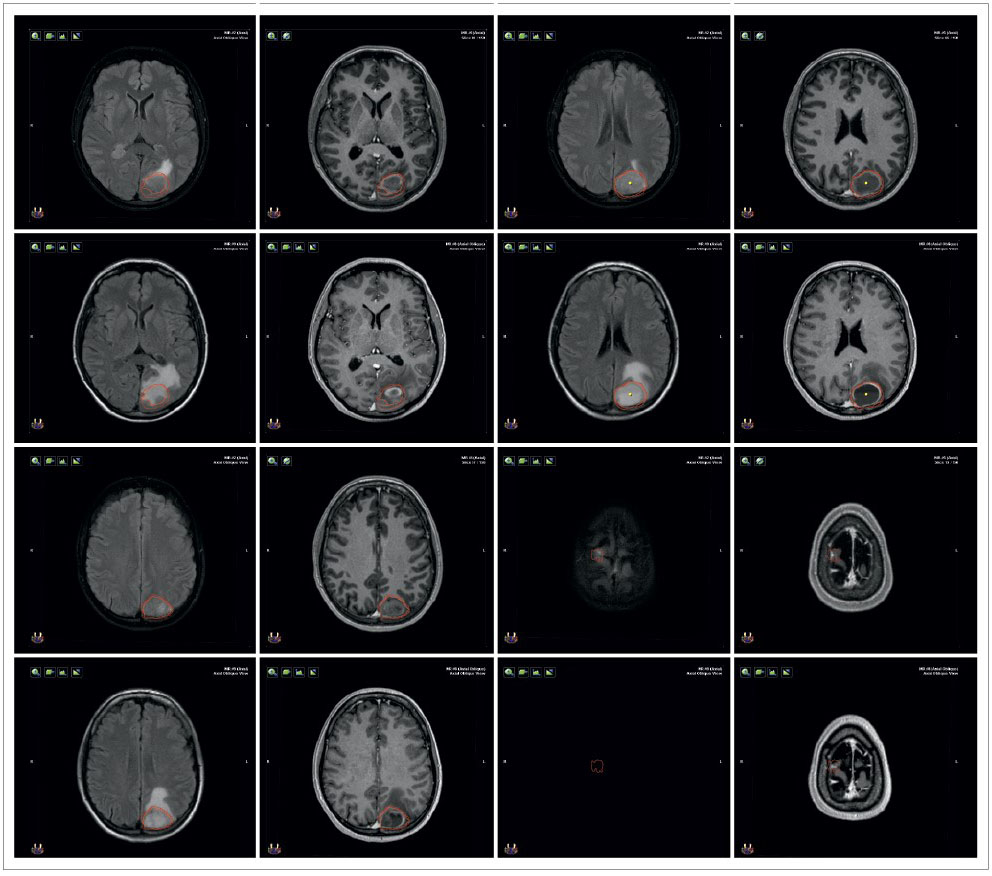 Рис. 8. Метастатичне ураження головного мозку (через 3 міс; верхні знімки – розмітка перед променевою терапією, нижні – після променевої терапії, з вираженою зоною набряку)
Рис. 8. Метастатичне ураження головного мозку (через 3 міс; верхні знімки – розмітка перед променевою терапією, нижні – після променевої терапії, з вираженою зоною набряку)
Висновки
 В експериментальних дослідженнях продемонстровано, що осимертиніб може проникати через ГЕБ і накопичуватися у спинномозковій рідині у концентрації, яка значно перевищує таку для ранніх поколінь ТКІ. Дослідження FLAURA та AURA показали високу терапевтичну ефективність осимертинібу як у першій лінії терапії у пацієнтів з НДРЛ і метастазами у ЦНС та драйверними мутаціями у гені EGFR, так і у хворих із мутацією резистентності Т 790М, які раніше отримували ТКІ першого покоління. У дослідженні FLAURA застосування осимертинібу у першій лінії терапії у пацієнтів із вторинним ураженням ЦНС при НДРЛ та мутаціями EGFR істотно подовжувало час до прогресування порівняно з ТКІ першого покоління, а також підвищувало частоту повної та об’єктивної відповіді на проведену терапію. У дослідженні AURA3 у підгрупі пацієнтів з НДРЛ та мутаціями EGFR і метастатичним ураженням головного мозку осимертиніб дозволив подвоїти медіану виживаності без прогресування порівняно з хіміотерапією. Можливість застосування осимертинібу при виникненні метастазів у ЦНС у пацієнтів з НДРЛ і мутаціями EGFR є проривом, оскільки розпочинає еру таргетної терапії для цих хворих.
В експериментальних дослідженнях продемонстровано, що осимертиніб може проникати через ГЕБ і накопичуватися у спинномозковій рідині у концентрації, яка значно перевищує таку для ранніх поколінь ТКІ. Дослідження FLAURA та AURA показали високу терапевтичну ефективність осимертинібу як у першій лінії терапії у пацієнтів з НДРЛ і метастазами у ЦНС та драйверними мутаціями у гені EGFR, так і у хворих із мутацією резистентності Т 790М, які раніше отримували ТКІ першого покоління. У дослідженні FLAURA застосування осимертинібу у першій лінії терапії у пацієнтів із вторинним ураженням ЦНС при НДРЛ та мутаціями EGFR істотно подовжувало час до прогресування порівняно з ТКІ першого покоління, а також підвищувало частоту повної та об’єктивної відповіді на проведену терапію. У дослідженні AURA3 у підгрупі пацієнтів з НДРЛ та мутаціями EGFR і метастатичним ураженням головного мозку осимертиніб дозволив подвоїти медіану виживаності без прогресування порівняно з хіміотерапією. Можливість застосування осимертинібу при виникненні метастазів у ЦНС у пацієнтів з НДРЛ і мутаціями EGFR є проривом, оскільки розпочинає еру таргетної терапії для цих хворих.
Від редакції
Нещодавно в рамках ASCO‑2020 R.S. Herbst та співавт. представили результати подвійного сліпого плацебо-контрольованого дослідження ІІІ фази ADAURA. Призначення осимертинібу як ад’ювантної терапії у пацієнтів з НДРЛ Ib-IIIA стадії після радикального хірургічного втручання та за наявності EGFR-мутації істотно покращувало медіану безрецидивної виживаності (відношення ризику = 0,17; 95% ДІ 0,12-0,23; p<0,0001), яка в групі осимертинібу не була досягнута, а в контрольній групі становила 20,4 міс. При застосуванні осимертинібу трирічна виживаність без ознак захворювання становила 80% у порівнянні з 28% у группі плацебо.
Підготувала Олена Поступаленко
Тематичний номер «Онкологія, Гематологія, Хіміотерапія» № 4 (65) 2020 р.