1 листопада, 2020
Підвищення неспецифічного імунного захисту у дітей: які інструменти в руках педіатра?
.jpg) Осінь є піковим періодом професійного навантаження на педіатрів, адже зростає частота звернень з приводу гострих респіраторних інфекцій (ГРІ). Особливої уваги потребують діти, які часто та тривало хворіють (діти з рекурентними застудними захворюваннями), адже рутинне симптоматичне (за потреби – етіотропне) лікування забезпечує короткий ефект, а не тривалий результат і запобігання повторним інфекціям. Тому важливо зосередитися на профілактиці подальших епізодів ГРІ шляхом підвищення захисних механізмів організму, які будуть ефективно протидіяти інфекційним збудникам.
Осінь є піковим періодом професійного навантаження на педіатрів, адже зростає частота звернень з приводу гострих респіраторних інфекцій (ГРІ). Особливої уваги потребують діти, які часто та тривало хворіють (діти з рекурентними застудними захворюваннями), адже рутинне симптоматичне (за потреби – етіотропне) лікування забезпечує короткий ефект, а не тривалий результат і запобігання повторним інфекціям. Тому важливо зосередитися на профілактиці подальших епізодів ГРІ шляхом підвищення захисних механізмів організму, які будуть ефективно протидіяти інфекційним збудникам.
У рамках XXІІ Всеукраїнської науково-практичної конференції «Актуальні питання педіатрії», присвяченої пам’яті члена-кореспондента НАН, НАМН України, професора В.М. Сідельникова, завідувачка відділення медичних проблем здорової дитини та преморбідних станів ДУ «Інститут педіатрії, акушерства і гінекології імені академіка О.М. Лук’янової НАМН України», доктор медичних наук, професор Людмила Вікторівна Квашніна увагу слухачів зосередила на питаннях підвищення функціональних можливостей неспецифічного імунітету у дітей.
– У батьків часто виникає запитання: чому при однакових епідемічних обставинах одні члени сім’ї мають виражені клінічні прояви вірусної інфекції, а інші – легкі або навіть залишаються здоровими після контакту з хворим. Основна роль у захисті людського організму від патогенів належить імунітету, стан якого залежить від великої кількості факторів. В умовах пандемії COVID-19 дітей не включають до групи ризику інфекції, що не зовсім раціонально в аспекті анатомо-фізіологічних особливостей імунної системи. У дітей виділяють 5 критичних періодів розвитку імунної системи, коли організм найбільш чутливий до дії зовнішніх факторів (Л.А. Щеплягина и соавт., 2013):
- від народження до 28-го дня життя – імунна система не сформована, через що новонароджений чутливий до усіх вірусних і бактеріальних інфекцій;
- 3-6 міс – відбувається руйнування материнських антитіл, а власна реакція на інфекцію, що супроводжується формуванням імуноглобуліну (Ig) M, не залишає пам’яті; sIgA недостатньо для забезпечення місцевого захисту; дитина схильна до гострих респіраторних вірусних інфекцій (ГРВІ), гострих кишкових інфекцій;
- 2-3 роки – період формування первинної імунної відповіді на інфекції, кількість яких зростає з появою нових контактів (відвідування дошкільного закладу), починає синтезуватися IgG, рівень sIgA залишається низьким; виникають повторні епізоди ГРВІ;
- 6-7 років – рівень IgM, IgG відповідають нормі, sIgA – нижчий за норму, IgЕ досягає рівня дорослого; у цей період формуються хронічні хвороби, наростає частота алергічної патології;
- 12-13 років у дівчаток та 14-15 років у хлопчиків – період гормональної перебудови, разом з чим зменшується об’єм лімфоїдних органів; у цьому віці збільшується частота розвитку хронічної патології та лімфопроліферативних утворень.
У ході нашого дослідження клітинного, гуморального та місцевого імунітету у дітей віком 5-6 років, які хворіють більше 5-8 разів на рік (1-ша група), та тих, що хворіють 2-4 рази на рік (2-га група), найбільш значуща різниця зафіксована між показниками місцевого імунітету. Так, рівень загального IgG у слині учасників 1-ї групи склав 2,42±0,36 мг/мл, 2-ї – 3,92±0,90 мг/мл, sIgA у слині – 262,10±53,38 мг/мл та 371,82± 13,36 мг/мл відповідно, загальний ІgA у слині – 1,17±0,04 мг/мл та 1,98±0,02 мг/мл відповідно.
При оцінці основних показників здоров’я (стан імунної системи, пероксидного окиснення ліпідів (ПОЛ) та антиоксидантного захисту (АОЗ), енергетичного обміну тощо) у дітей віком 7-10 років виявлено значну гетерогенність даних, що і стало приводом до формування 2 груп здоров’я. До 1-ї групи (без відхилень) належать діти з 2 типами показників імунної системи: стабільним і компенсованим. Дітей з незначними відхиленнями показників імунної системи включають до 2-ї групи здоров’я (субкомпенсований тип).
При стабільному типі діти не мають відхилень показників ПОЛ-АОЗ, енергетичного метаболізму та лізосомального апарату імунокомпетентних клітин.
Компенсований тип характеризується відсутністю відхилень показників імунної системи, але наявністю змін ПОЛ-АОЗ без активації ПОЛ, а також змін показників мітохондріального окиснення й анаеробного гліколізу без ознак вторинної тканинної гіпоксії (за станом лізосомального апарату). При субкомпенсованому типі у дітей є незначні відхилення показників імунної системи, зміни стану ПОЛ-АОЗ (з/без активації ПОЛ) та відхилення показників мітохондріального окиснення й анаеробного гліколізу без ознак вторинної тканинної гіпоксії (за станом лізосомального апарату; А.В. Костенко та ін., 2008).
Таким чином, незначні відхилення показників імунної системи, стану ПОЛ-АОЗ, енергетичного обміну у здорових дітей є визначальними факторами більшої схильності до вірусних інфекцій. Для профілактики частих епізодів ГРІ велике значення має покращення неспецифічного імунітету. Базовими заходами, які сприяють цьому, є грудне вигодовування (при можливості матері його забезпечити) з подальшим підбором індивідуальної дієти, раціональний режим дня та харчування, здоровий спосіб життя сім’ї, загартовування, загальнозміцювальна та лікувальна фізкультура, консультація психолога для вироблення правильної реакції родичів на часті захворювання дитини, санація хронічних вогнищ інфекції, лікування патології травної системи та гельмінозів, у дітей зі схильністю до алергії – консультація алерголога, фізіотерапія, вакцинація (не слід здійснювати раніше ніж через 14 днів після перенесеної ГРІ з високою температурою тіла та інтоксикацією). Важливе місце у зміцненні неспецифічного імунного захисту посідає застосування засобів з імунотропною дією.
В основі піраміди імунотропних засобів (рис.) лежать імуномікронутрієнти (поліненасичені жирні кислоти (ПНЖК), вітаміни, мікронутрієнти), застосування яких не завдасть шкоди організму навіть у критичні періоди становлення імунітету, але сприятиме адекватному росту та дозріванню дитини. Імуномікронутрієнти й імунобіотики використовують у дітей із рекурентними інфекційними захворюваннями, у тих, що тривало хворіють, та реконвалесцентів.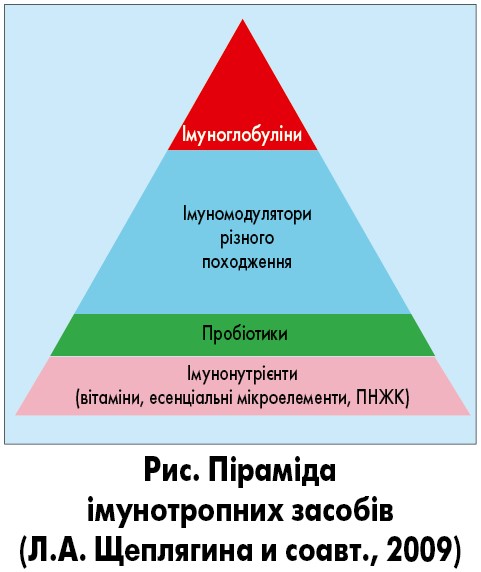
ПНЖК – це речовини, які мають важливе значення для нормальної роботи серцево-судинної системи, дозрівання нервової системи, ліпідного обміну, а також забезпечення неспецифічного імунного захисту. Виділяють омега-3, омега-6 та омега-9 ПНЖК. Часто увага педіатрів спрямована на пошук комбінованих засобів, які б містили усі ці компоненти. Проте при визначенні середніх показників довголанцюгових ПНЖК у дітей віком 5-6 років не виявлено дефіциту омега-6 та омега-9 ПНЖК. Для більш коректної інтерпретації нестачі чи надлишку ПНЖК слід оцінювати співвідношення омега-3 та омега-6 ПНЖК. Відповідно до сучасних міжнародних рекомендацій, співвідношення омега-6 до омега-3 має становити 5-10:1. У ході власного дослідження, метою якого було вивчення рівня довголанцюгових омега-3, омега-6 ПНЖК і показників ліпідного обміну у здорових дітей дошкільного віку (3-6 років), отримано такі результати:
- у здорових дітей переважають насичені жирні кислоти (39,6%), рівень поліненасичених становить 32,6%, а мононенасичених – 25,6%, тобто виявлено дефіцит важливих для дитячого організму складових;
- поряд із високим рівнем довголанцюгових омега-6 ПНЖК у здорових дітей відзначено достатньо високий рівень мононенасичених жирних кислот і виражений дефіцит довголанцюгових омега-3 ПНЖК;
- виявлено виражений дисбаланс омега-3/ омега-6 (від 1:6 до 1:85, середнє значення – 1:23).
Сьогодні накопичена велика доказова база про вплив омега-3 ПНЖК на імунітет. Омега-3 ПНЖК ферментативно беруть участь у забезпеченні функціонування різних біологічно активних медіаторів. Ці посередники протизапальної спрямованості включають резольвіни, протектини і марезини, вони особливо важливі для швидшого регресування гострого запалення, а також, імовірно, відіграють важливу роль у підвищенні захисних можливостей дитячого організму. B. Imhoff-Kunsch та співавт. (2011) дійшли висновку, що вживання матір’ю дієтичних добавок із вмістом докозагексаєнової кислоти (ДГК) сприяє зниженню ризику застудних захворювань у дітей до 1 міс, а також зменшує тривалість клінічної симптоматики застудних захворювань у 1, 3, 6 міс. T. Carlo та співавт. (2010) виявили пряму кореляцію між збільшенням споживання омега-3 ПНЖК і зниженням ризику розвитку пневмонії, а M. Uddin та співавт. (2011) зазначили, що завдяки протизапальним властивостям омега-3 ПНЖК їх вживання пацієнтами з тяжкою пневмонією сприяло зменшенню ушкодження тканин шокового органа. У 2006 р. N. Pastor та співавт. провели велике дослідження за участю 1342 дітей віком 5-9 міс із повторними епізодами гострого бронхіту та бронхіоліту, яким додатково до харчування був призначений 0,32% розчин ДГК. Доповнення раціону ДГК сприяло значному зниженню захворюваності. Цікаві дані представили J.F. Fenguson та співавт. (2014): при ендотоксемії застосування ейкозапентаєнової кислоти та ДГК у дозі 3600 мг/добу сприяло зниженню температури тіла та плазмової концентрації маркерів запалення.
Таким чином, результати досліджень показують важливе значення омега-3 ПНЖК у збереженні здоров’я дитини, що обґрунтовує необхідність адекватного надходження цих речовин в організм. Основними джерелами омега-3 ПНЖК є скумбрія, оселедець, анчоус, сардина, форель, лангуст та інші морепродукти. При достатній кількості рибних страв у раціоні можна забезпечити потребу дитини в омега-3 ПНЖК. Але існують ситуації, коли не вдається досягти адекватного забезпечення організму омега-3 ПНЖК лише шляхом корекції харчування: при непереносимості морепродуктів, категоричній відмові дитини від вживання морепродуктів, через економічні причини тощо. У таких випадках раціонально використовувати дієтичні добавки, наприклад Смарт Омега – додаткове джерело незамінних омега-3 ПНЖК для різних вікових категорій, починаючи з 6 міс.
Підготувала Ілона Цюпа
Тематичний номер «Педіатрія» №4 (55) 2020 р.



