16 лютого, 2026
Рання гематологічна відповідь на пероральну терапію залізом у дорослих з помірною залізодефіцитною анемією
Анемія, котру визначають як зниження рівня гемоглобіну (Hb) нижче 12,0 г/дл у жінок і 13,0 г/дл у чоловіків [1, 2], залишається однією з наймасштабніших проблем глобальної охорони здоров’я: на неї страждають близько 1,92 млрд людей у світі [3]. У понад половині випадків причиною є дефіцит заліза. Його запаси оцінюють за рівнем феритину, що в нормі становить 20-200 мкг/л у жінок і 30-300 мкг/л у чоловіків [4]. Основні чинники дефіциту – недостатнє надходження або порушення всмоктування заліза, підвищені потреби під час вагітності чи періодів росту, втрати через кровотечі (зокрема, рясні менструації), хронічні запальні процеси, гельмінтози тощо [4].
Для корекції залізодефіцитної анемії (ЗДА), крім обов’язкового пошуку й усунення першопричини, існують три основні підходи: пероральна терапія, парентеральне введення заліза та переливання крові [5]. Останнє незалежно від форми (алогенна, автологічна, рестриктивна трансфузія) пов’язане з низкою обмежень, протипоказань і потенційних ризиків [6]. Тому в переважній більшості випадків, за винятком невідкладних ситуацій, перевагу віддають пероральним або внутрішньовенним формам з метою поступового відновлення запасів заліза [7]. Вибір між ними залежить не стільки від рівня Hb, скільки від клінічного впливу анемії, потреби в швидкому ефекті та профілю безпеки кожного з методів.
Пероральна терапія зазвичай є методом першої лінії: вона проста в застосуванні, доступна й ефективна, хоча й може спричиняти шлунково-кишкові побічні ефекти, як-от закрепи, діарею або біль у животі. Метааналітичний огляд 21 дослідження за участю 4745 пацієнтів продемонстрував, що на тлі ЗДА така терапія достовірно підвищує рівень Hb і, ймовірно, знижує потребу в переливаннях [8].
Внутрішньовенне введення заліза є доцільним, коли потрібне швидке поповнення дефіциту, але воно істотно дорожче та не позбавлене ризиків, зокрема інфекційних ускладнень [9], інфузійних реакцій [10-12], гіпофосфатемії [13], а також рідкісних, але потенційно небезпечних реакцій гіперчутливості [14]. З огляду на це Французьке агентство з безпеки лікарських засобів (ANSM) оприлюднило оновлені заходи з мінімізації ризиків щодо гіперчутливості й анафілаксії [15].
У щоденній практиці ефективність пероральної терапії зазвичай оцінюють через місяць від початку. Проте з клінічного погляду рання оцінка відповіді на лікування була би значно кориснішою: вона дає змогу як підтвердити ефективність призначеної терапії, так і оперативно змінити підхід у разі відсутності результату.
У результатах 5 досліджень було показано: вже через 14 днів від початку приймання препаратів заліза (здебільшого сульфату заліза) 72,8% пацієнтів демонстрували приріст Hb ≥1 г/дл, що давало змогу вважати їх «відповідачами на терапію» [16]. Стосовно глюконату заліза таких даних досі бракує. Попри те що дослідження в дітей засвідчило профілактичну ефективність глюконату, зіставну із сульфатом заліза [17], для дорослих осіб інформації про динаміку відповіді на лікування небагато. Наявні праці здебільшого зосереджені або на біодоступності заліза після разового приймання [18, 19], або на ефективності тривалої терапії за рівнем феритину та Hb [20, 21], без аналізу швидкості відповіді. Для повноцінного оцінювання кінетики ефективності терапії залізом потрібні послідовні біохімічні вимірювання, особливо протягом першого тижня лікування.
У цьому контексті було проведено дослідження FAST (Assessments of the eFficacy, the onset-of-Action and the Safety of Tot’héma in adults with moderate iron deficiency anaemia). Метою стало вивчення динаміки ключових біомаркерів ефективності на ранніх етапах прийому перорального розчину глюконату заліза з додаванням міді та марганцю у пацієнтів з помірною ЗДА, а також оцінювання швидкості початку дії.
Матеріали та методи
Відкрите проспективне дослідження FAST проводили з листопада 2020 року до жовтня 2023 року у 20 клінічних центрах у Європі (Франція, Болгарія) й Африці (Кенія). Курс лікування тривав 12 тижнів і передбачав 5 візитів: скринінговий (V1, за 1-7 днів до залучення), візит залучення (V2/D0), два контрольні візити на 14-й (V3/D14) і 28-й день (V4/D28), а також завершальний візит на 84-й день (V5/D84). Загалом за період дослідження було проведено 11 лабораторних обстежень крові.
Пацієнтам призначали пероральний розчин, що містив глюконат заліза (50 мг Fe), глюконат міді (0,70 мг Cu) та глюконат марганцю (1,33 мг Mn) – препарат Тотема (Laboratoire Innotech International, Франція). Протягом 84 днів учасники приймали по 1 ампулі тричі на день, що відповідало добовій дозі 150 мг заліза у формі глюконату.
У дослідження залучали дорослих пацієнтів з помірною анемією (рівень Hb – 8-10 г/дл) і зниженим рівнем феритину (нижче референтного значення для відповідної лабораторії). Основними критеріями вилучення були активна кровотеча шлунково-кишкового тракту (ШКТ), гострий або хронічний запальний процес, нещодавній епізод малярії (в межах 15 днів до залучення), порушення з боку ШКТ, що унеможливлювали дотримання режиму лікування, а також рівень С-реактивного білка >10 мг/л на етапі скринінгу.
На кожному візиті лікар проводив загальноклінічний огляд і оцінював рівень утоми за візуальною аналоговою шкалою (ВАШ) – від 0 (відсутність втоми) до 10 (максимальна втома). Якість життя оцінювали за опитувальником SF‑36, але лише в європейських учасників і тільки на момент залучення та завершення дослідження [22]. Цей валідований інструмент охоплює 8 доменів здоров’я й формує два інтегровані індекси – фізичне та психоемоційне здоров’я, з балами від 0 (найгірший стан) до 100 (оптимальний).
Забір крові проводили на етапі скринінгу та в дні D0, D3, D5, D7, D10, D14, D21, D28, D56 і D84. Визначали рівні гемоглобіну, сироваткового заліза, ретикулоцитів, насичення трансферину (T-SAT) і середній об’єм еритроцитів (MCV). Рівень феритину оцінювали в ті самі дні, за винятком D3, D5 і D10. Усі лабораторні тести виконувалися в акредитованих місцевих лабораторіях, водночас біоматеріал кожного учасника аналізували в одній і тій самій лабораторії задля забезпечення порівнюваності результатів.
Головною метою дослідження було визначення часу, необхідного для підвищення рівня Hb щонайменше на 0,5 г/дл відносно вихідного. Первинною кінцевою точкою був день, на який уперше зафіксовано середнє підвищення Hb ≥0,5 г/дл. Серед вторинних кінцевих точок оцінювали на кожному контрольному етапі: частку пацієнтів із приростом Hb ≥0,5; ≥1 і ≥2 г/дл; частку учасників з досягненням нормального рівня Hb (≥12 г/дл для жінок і ≥13 г/дл для чоловіків); зміну рівнів Hb, феритину, сироваткового заліза, T-SAT, MCV і ретикулоцитів із часом; а також динаміку показників утоми та якості життя.
В аналіз безпеки залучали всіх пацієнтів, які отримали хоча б одну дозу препарату. Повна вибірка для аналізу ефективності охоплювала цю саму групу, але лише тих учасників, щодо яких були наявні дані після залучення.
Статистичний аналіз проводили з використанням програмного забезпечення Statistical Analysis Systems (SAS), версія 9.4.
Результати
У дослідження FAST залучили 97 учасників, з яких дані 95 пацієнтів увійшли до фінального аналізу. Повний курс лікування пройшла 91 особа; ще четверо вибули до завершення. Більшість учасників становили жінки (87,4%), середній вік пацієнтів – 41,9 року (діапазон – від 18,7 до 83,9 року). На момент залучення середній рівень Hb становив 9,13 г/дл, сироваткового заліза – 29,88 мкг/дл, феритину – 17,85 нг/мл, відсоток ретикулоцитів – 1,38.
Переважна частина учасників мали типові клінічні прояви ЗДА: блідість кон’юнктив (73,4%), утома (середнє значення за ВАШ – 4,71) і знижена якість життя (середні інтегральні показники SF‑36: фізичний компонент – 46,19; психоемоційний – 46,39).
Динаміка гематологічних показників
На підставі послідовних лабораторних досліджень і математичного моделювання було встановлено, що підвищення Hb ≥0,5 г/дл від базового рівня досягалося вже через 9-10 днів від початку терапії (оцінка на D10: 0,51 г/дл; 95% довірчий інтервал (ДІ) 0,45-0,57; p<0,0001) з високою статистичною значущістю (p<0,0001). Результати були подібними для всіх географічних регіонів.
На рисунку 1 наведено повну динаміку Hb, сироваткового заліза, феритину та ретикулоцитів. Уже з перших днів терапії спостерігали зростання рівня заліза в сироватці з піком на D7. Середній рівень Hb підвищився з 9,13 до 12,46 г/дл до завершення дослідження. Вироблення ретикулоцитів зростало паралельно з піком на D10 (середній приріст: +1,09% від D0). Рівень феритину підвищився із 17,85 до 42,76 нг/мл.
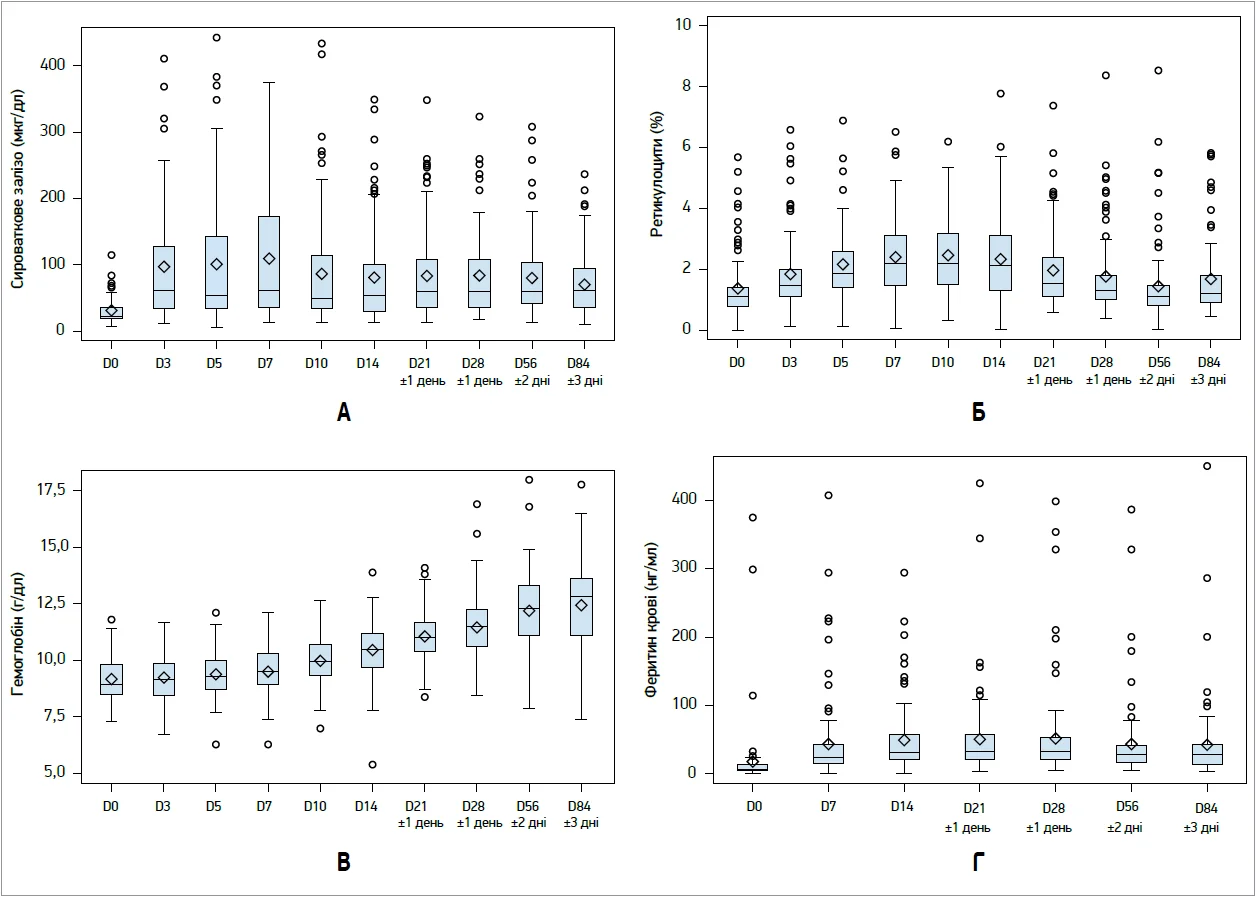 Рис. 1. Динаміка лабораторних показників за візитами (А – сироваткове залізо, Б – ретикулоцити, В – гемоглобін, Г – феритин)
Рис. 1. Динаміка лабораторних показників за візитами (А – сироваткове залізо, Б – ретикулоцити, В – гемоглобін, Г – феритин)
Примітка: в кожному прямокутнику горизонтальні лінії позначають медіанні значення, ромби – середні значення. Межі прямокутників відповідають 25-му та 75-му процентилям розподілу в групі; вертикальні лінії, що виходять за межі прямокутників, позначають крайні значення в межах 1,5 міжквартильного розмаху. Кружечки за межами – це нетипові значення, що виходять за межі діапазону крайніх значень.
Клінічна відповідь і прогностична цінність раннього приросту Hb
Після 12 тижнів терапії переважна більшість учасників досягли суттєвої відповіді:
- приріст Hb ≥0,5 г/дл – у 90,9%;
- приріст Hb ≥1 г/дл – у 85,2%;
- приріст Hb ≥2 г/дл – у 69,3%;
- нормалізація Hb – у 63,6%.
Географічних відмінностей у відповіді теж не зафіксовано.
Уже на D10 приріст Hb ≥0,5 г/дл відзначався в 72,3% пацієнтів. Цей показник виявився високочутливим предиктором подальшого підвищення Hb ≥1 г/дл на D14 (чутливість – 95,24%, специфічність – 74,19%, позитивна прогностична цінність – 88,24%, негативна прогностична цінність – 88,46%).
Медіана часу до досягнення приросту Hb ≥0,5 г/дл становила 8 днів (95% ДІ 6-11), а для приросту ≥1 г/дл – 15 днів (95% ДІ 11-15).
Зменшення симптомів і покращення якості життя
На завершення лікування всі основні симптоми, зафіксовані на старті, зменшилися. Середнє зниження показника втоми за ВАШ становило –2,76. Загальні оцінки за опитувальником SF‑36 зросли: +8,20 для фізичного компонента та +6,72 для психоемоційного. В усіх сферах опитувальника SF‑36 спостерігали покращення щонайменше на 10 балів (рис. 2).
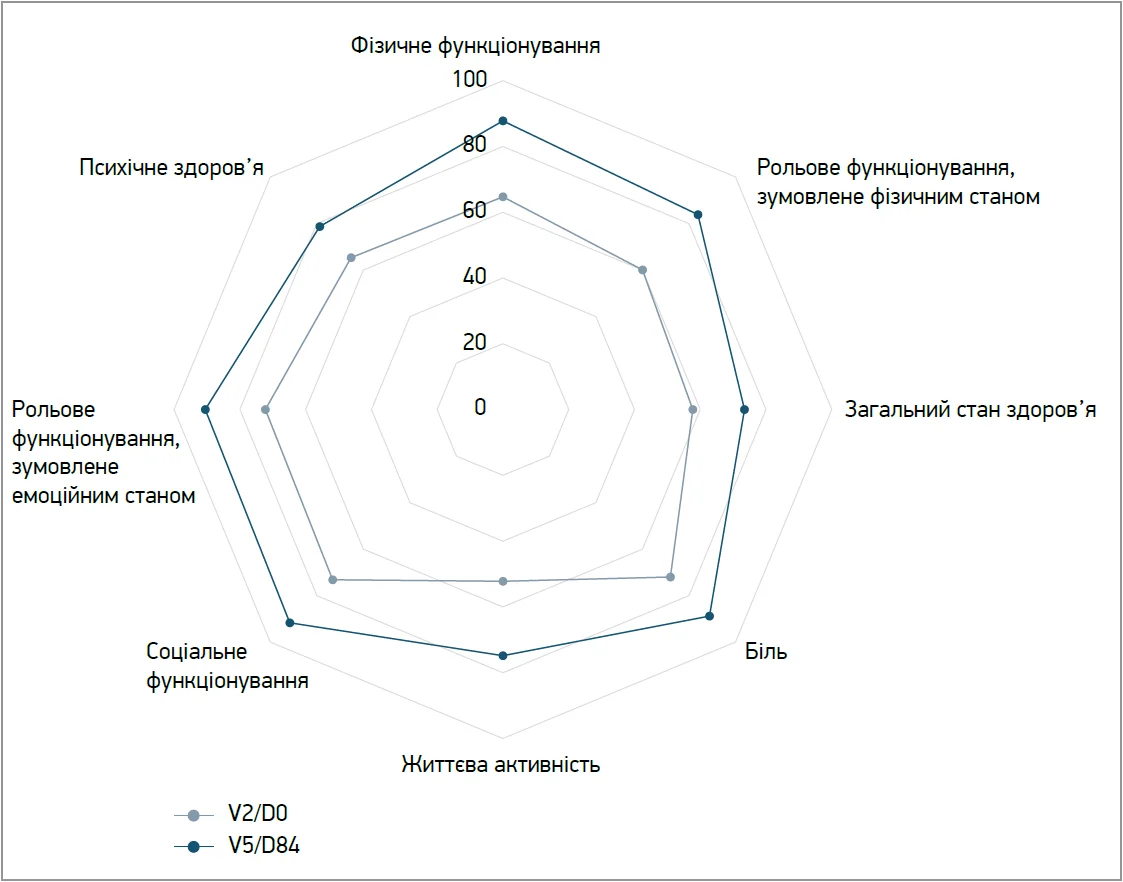 Рис. 2. Показники за доменами опитувальника SF‑36 на момент залучення (V2/D0) та після завершення лікування (V5/D84)
Рис. 2. Показники за доменами опитувальника SF‑36 на момент залучення (V2/D0) та після завершення лікування (V5/D84)
Примітка: опитувальник SF‑36 охоплює 8 доменів здоров’я за 36 запитаннями, відповіді на які перетворюються на бали від 0 (найгірший стан здоров’я) до 100 (оптимальний стан здоров’я).
Прихильність до лікування та безпека
Прихильність до лікування була надзвичайно високою: середній показник становив 99,29±4,04%. Лише троє європейських учасників мали комплаєнс <100%.
Загалом 97 пацієнтів отримали щонайменше одну дозу Тотеми. Під час дослідження було зафіксовано 34 небажані явища (НЯ) у 23 пацієнтів. Серед них – 6 серйозних НЯ в 1 пацієнта, які не були пов’язані з терапією та на момент завершення дослідження вже минали.
Сім НЯ стосувалися ШКТ. Три явища були визнані пов’язаними з лікуванням: один випадок нудоти та два випадки неприємного смаку розчину. Усі ці НЯ були легкими й несерйозними. В обох випадках неприємного смаку дозу було зменшено відповідно до протоколу. Загалом препарат продемонстрував дуже добру переносимість.
Обговорення
Наскільки нам відомо, це перше дослідження, в якому динаміку біомаркерів метаболізму заліза в пацієнтів з помірною анемією оцінювали вже з перших днів після початку терапії глюконатом заліза, з багаторазовими лабораторними вимірюваннями. Дослідження FAST підтвердило, що вже до 7-го дня терапії рівень сироваткового заліза зростає до пікових значень, а підвищення Hb на ≥0,5 г/дл досягається в середньому на 9-10-й день. Показовим є також швидке відновлення рівня феритину. Отже, статус «відповідача на терапію» потенційно можна виявити вже на 10-й день лікування.
Дані щодо порівняння початку дії різних солей заліза залишаються обмеженими. Хоча це дослідження не передбачало прямої порівняльної оцінки, отримана гематологічна відповідь узгоджується з літературними даними про високу ефективність глюконату заліза, зіставну з такою сульфату заліза. Зокрема, в рандомізованому дослідженні Falahati та співавт. було показано подібну профілактичну ефективність обох форм у дітей [17]. Наші результати доповнюють ці дані, надаючи реальні клінічні свідчення на дорослій популяції пацієнтів із ЗДА.
Раніше вважали, що збільшення Hb ≥1 г/дл на 14-й день можна використовувати як маркер відповіді на пероральну терапію залізом [16]. У дослідженні FAST було доведено: підвищення Hb ≥0,5 г/дл уже на 10-й день достовірно прогнозує відповідь на 14-й день. Цей підхід може стати новим орієнтиром для раннього оцінювання ефективності терапії. Отримана специфічність (74,19%) є зіставною з даними Okam і співавт. (79,3%) для 14-го дня [16] та вважається прийнятною, оскільки продовження терапії з подальшим моніторингом у разі відсутності відповіді не несе високого ризику. Перевагу віддали високій чутливості (95,24%), щоб не пропустити справжніх «відповідачів».
З погляду переносимості глюконат заліза потенційно має кращий профіль, аніж сульфат. Британське товариство гастроентерології [23] рекомендує розглядати альтернативні форми (глюконат, фумарат) для пацієнтів з побічними реакціями на сульфат заліза. У нашому дослідженні 3-місячна терапія глюконатом заліза продемонструвала дуже добру переносимість, з мінімальною кількістю побічних явищ. Це підтверджує доцільність його застосування в пацієнтів, які погано переносять інші форми заліза.
Попри помірну тяжкість ЗДА на старті сироваткове залізо почало зростати вже з 3-го дня лікування, досягаючи піку на 7-й день; це свідчить про ефективну абсорбцію препарату. Цьому, ймовірно, сприяють рідка форма препарату й наявність глюконату міді, відомого своєю здатністю покращувати кишкове всмоктування та метаболізм заліза, а також участю в синтезі Hb [24]. На моделі клітин Caco‑2 ex vivo доведено, що мідь сприяє проникненню заліза крізь кишковий епітелій [25]. Швидке зростання ретикулоцитів з піком на 10-й день додатково підтверджує ефективну абсорбцію.
Покращення біомаркерів супроводжувалося зменшенням відчуття втоми й покращенням фізичних і психоемоційних компонентів якості життя. Ці зміни узгоджуються з літературними даними про зв’язок дефіциту заліза з астенією та зниженням якості життя [26].
До умовного обмеження можна віднести вузькі критерії залучення – лише пацієнти з помірною анемією, що потребували ретельного скринінгу. Втім, ця стратегія є виправданою: середній рівень Hb на старті становив 9,13 г/дл. Співвідношення «жінки/чоловіки» серед учасників було вищим за глобальні показники поширеності ЗДА, проте повністю узгоджується з епідеміологічною ситуацією в регіонах проведення [27].
Висновки
Дослідження FAST уперше продемонструвало швидкий початок дії перорального розчину глюконату заліза в пацієнтів із ЗДА. Отримані результати свідчать, що підвищення рівня Hb на ≥0,5 г/дл, зафіксоване на 10-й день лікування, може слугувати раннім предиктором подальшої відповіді на терапію.
Попри обнадійливий характер цього спостереження воно потребує подальшої валідації та наразі не може розглядатися як остаточний клінічний поріг. Водночас така оцінка в динаміці може стати корисним орієнтиром для прийняття клінічних рішень і вибору шляху введення препаратів заліза в пацієнтів із ЗДА, особливо коли потрібне швидке відновлення залізодефіциту.
Cacoub P., Trichereau J., Gobert O., et al. Early haematologic response to oral iron treatment in adults with moderate iron-deficiency anaemia. Anemia. 2025 Nov 20; 2025: 8866390. doi: 10.1155/anem/8866390. PMID: 41277915; PMCID: PMC12634183.
Скорочений переклад підготував Олексій Терещенко
Від редакції
ЗДА – одна з найпоширеніших патологій у світі, що негативно впливає на самопочуття, розумову та фізичну працездатність, якість життя, а в окремих випадках і на виживаність пацієнтів. Водночас питання своєчасного оцінювання ефективності терапії досі залишається недостатньо висвітленим у щоденній клінічній практиці. Через це дослідження FAST, у якому вперше вивчалася динаміка біомаркерів метаболізму заліза у відповідь на пероральну терапію глюконатом заліза, є надзвичайно актуальним.
Тотема (Laboratoire Innotech International, Франція) – це оральний розчин двовалентного заліза глюконату і мікроелементів міді та марганцю. Завдяки такій формулі Тотема забезпечує швидке й ефективне всмоктування заліза, навіть за наявності супутніх порушень абсорбції. Результати дослідження FAST засвідчили: підвищення рівня Hb на ≥0,5 г/дл може фіксуватися вже на 10-й день лікування та слугувати раннім предиктором клінічної відповіді. Це відкриває перспективи для більш точного та персоналізованого вибору тактики корекції ЗДА.
Наукова значущість дослідження була визнана на міжнародному рівні. Його результати були представлені провідним дослідником, професором Патрісом Какубом (Patrice Cacoub) на 3-му Європейському конгресі з гематології та порушень системи крові (жовтень 2024 року, м. Рим, Італія), а також на міжнародному вебінарі «Дефіцит заліза й анемія: оптимізація стратегій замісної терапії на підставі нових клінічних даних», присвяченому Всесвітньому дню боротьби з анемією (листопад 2025 року).
Отже, Тотема постає як сучасний і добре переносимий варіант пероральної терапії ЗДА, особливо у випадках, коли важливо досягти швидкого клінічного ефекту з високою прихильністю до лікування та мінімальним ризиком побічних явищ.
Медична газета «Здоров’я України 21 сторіччя» № 23-24 (610-611), 2025 р



