10 липня, 2023
Оновлення рекомендацій ADA 2023: основні акценти
 У грудні 2022 року Американська діабетична асоціація (ADA) опублікувала оновлені «Стандарти надання медичної допомоги при цукровому діабеті 2023 р.». У них було враховано результати найсучасніших наукових і клінічних досліджень. До Стандартів увійшли важливі практичні рекомендації з менеджменту діабету і предіабету, у тому числі щодо: діагностики цукрового діабету (ЦД) 1 типу, ЦД 2 типу та гестаційного діабету в молоді та дорослих; стратегії профілактики або відстрочки ЦД 2 типу; терапевтичних підходів, які можуть зменшити кількість ускладнень, знизити серцево-судинні (СС) та ниркові ризики та поліпшити якість життя пацієнтів. Ще одне ключове оновлення стосується місця агоністів рецепторів глюкагоноподібного пептиду‑1 (арГПП‑1) в терапії ЦД, які наразі рекомендовано як першу ін’єкційну терапію для пацієнтів із ЦД 2 типу.
У грудні 2022 року Американська діабетична асоціація (ADA) опублікувала оновлені «Стандарти надання медичної допомоги при цукровому діабеті 2023 р.». У них було враховано результати найсучасніших наукових і клінічних досліджень. До Стандартів увійшли важливі практичні рекомендації з менеджменту діабету і предіабету, у тому числі щодо: діагностики цукрового діабету (ЦД) 1 типу, ЦД 2 типу та гестаційного діабету в молоді та дорослих; стратегії профілактики або відстрочки ЦД 2 типу; терапевтичних підходів, які можуть зменшити кількість ускладнень, знизити серцево-судинні (СС) та ниркові ризики та поліпшити якість життя пацієнтів. Ще одне ключове оновлення стосується місця агоністів рецепторів глюкагоноподібного пептиду‑1 (арГПП‑1) в терапії ЦД, які наразі рекомендовано як першу ін’єкційну терапію для пацієнтів із ЦД 2 типу.
Скринінг предіабету та діабету
Говорячи про скринінг діабету або предіабету в безсимптомних дорослих, треба підкреслити, що індекс маси тіла (ІМТ) сьогодні відіграє ключове значення у відборі пацієнтів для тестування та використовується для оцінки ризику розвитку ЦД 2 типу. Так, скринінгу діабету або предіабету підлягають усі безсимптомні дорослі з надмірною вагою або ожирінням (ІМТ 25 кг/м2), які мають один або більше з таких факторів ризику:
- родич першого ступеня з діабетом;
- расова приналежність високого ризику (наприклад, афроамериканці);
- серцево-судинні захворювання (ССЗ) в анамнезі;
- гіпертензія (артеріальний тиск (АТ) 140/90 мм рт. ст. або антигіпертензивна терапія);
- рівень ліпопротеїнів високої щільності (ЛПВЩ) <0,90 ммоль/л і/або рівень тригліцеридів >2,82 ммоль/л;
- жінки із синдромом полікістозних яєчників;
- відсутність фізичної активності / сидячий спосіб життя;
- інші клінічні стани, пов’язані з резистентністю до інсуліну (наприклад, морбідне ожиріння).
Осіб із предіабетом (рівнем глікованого гемоглобіну (НbА1с) ≥5,7%, порушенням толерантності до глюкози) потрібно перевіряти щороку. Жінки, в яких був діагностований гестаційний ЦД, мають проходити обстеження протягом усього життя принаймні кожні 3 роки. Для всіх інших осіб тестування має починатися у віці 35 років. Якщо результати нормальні, тестування повторюють щонайменше кожні 3 роки, проводячи його частіше залежно від початкових результатів і статусу ризику. Обов’язковому скринінгу також підлягають особи з ВІЛ-інфекцією.
Контроль маси тіла
Контролю ваги в ADA 2023 приділено набагато більше уваги, ніж у попередніх рекомендаціях.
Наголошується, що ожиріння є хворобою, яка потребує менеджменту, а також рекомендується перехід від глюкоцентричного лікування діабету до більш інтегрованих підходів, які розглядають контроль глікемії і лікування ожиріння як однаково важливі компоненти.
Контроль маси тіла вважають вагомою складовою цукрознижувального лікування в разі ЦД 2 типу, а динаміка зміни ваги – одним із критеріїв успішності лікування. Відповідно, щоб оцінити вплив лікування на вагу, потрібно вимірювати зріст і вагу та обчислювати IMT під час щорічних відвідувань або навіть частіше. Виходячи з клінічних міркувань, таких як наявність супутньої серцевої недостатності або значне незрозуміле збільшення або втрата ваги, може знадобитися частіший контроль та оцінка ваги (рівень доказовості В). Якщо погіршення медичного статусу пов’язане зі значним збільшенням або втратою ваги, треба розглянути обстеження в стаціонарі, особливо зосередившись на зв’язку між прийомом ліків, споживанням їжі та глікемічним статусом (рівень доказовості Е).
Особи з діабетом і надмірною вагою або ожирінням можуть отримати користь від помірної або більшої втрати ваги. Відносно невелика втрата ваги (приблизно 3-7% від початкової) поліпшує рівень глікемії та інших проміжних факторів СС ризику (рівень доказовості А). Більша втрата ваги (>10%) зазвичай дає більші переваги, зокрема впливає на захворювання, може спричинити ремісію ЦД 2 типу і позитивно вплинути на віддалені СС результати та зменшити смертність (рівень доказовості В).
Глікемічні цілі та контроль
Щодо глікемічних цілей лікування, то вони, загалом, не змінилися. Змінилися лише підходи до їх оцінювання. Безумовно, рівень НbA1c оцінюють у клінічній практиці і клінічних дослідженнях, він залишається важливим показником контролю глікемії.
Утім безперервний моніторинг глюкози (БМГ) відіграє важливішу роль у менеджменті ефективності та безпеки лікування багатьох пацієнтів із ЦД 1 типу та окремих категорій осіб із ЦД 2 типу.
Стандартизовані односторінкові звіти про рівень глюкози з БМГ з пристроїв із візуалізацією, таких як амбулаторний моніторинг глюкози (АМГ), треба розглядати як стандартний варіант для БМГ. Час у цільовому діапазоні (TIR) пов’язаний із ризиком мікросудинних ускладнень і може бути використаний для оцінки глікемічного контролю. Крім того, час нижче цільового діапазону та час вище цільового діапазону є корисними параметрами для оцінки плану лікування. Рекомендується більш розширене використання БМГ, який «слід пропонувати» тим, хто отримує базальну або базально-болюсну інсулінотерапію, що є кроком уперед у порівнянні з минулорічною рекомендацією, що БМГ «може використовуватися» в цій популяції.
Індивідуальний моніторинг рівня глюкози є корисним інструментом для самоконтролю діабету, який охоплює харчування, фізичну активність і коригування ліків, особливо в осіб, які приймають інсулін. Проте цей показник відіграє меншу роль в оцінці довгострокової ефективності лікування.
Цільові значення рівня НbА1с у різних груп пацієнтів не змінилися проти попередніх рекомендацій. Досягнення нижчих рівнів НbА1с, ніж цільове значення 7%, може бути прийнятним і навіть корисним, якщо цього можна досягти безпечно без розвитку значної гіпоглікемії чи інших побічних ефектів лікування (рівень доказовості В).
Менш суворі цільові рівні HbA1c (<8%) можуть бути прийнятними для пацієнтів з обмеженою очікуваною тривалістю життя або там, де шкода від лікування перевищує користь. Через підвищений обмін еритроцитів рівень HbA1c дещо знижується під час нормальної вагітності. В ідеалі цільовий рівень HbA1c під час вагітності становить <6%, якщо цього можна досягти без значної гіпоглікемії, але цільовий показник може бути зміщений до <7%, якщо необхідно запобігти розвитку гіпоглікемії (рівень доказовості В).
Незначно змінилися підходи до визначення індивідуальних глікемічних цілей, які наразі враховують особливості пацієнта та хвороби та можливість їх модифікації, що відображено на рисунку 1.
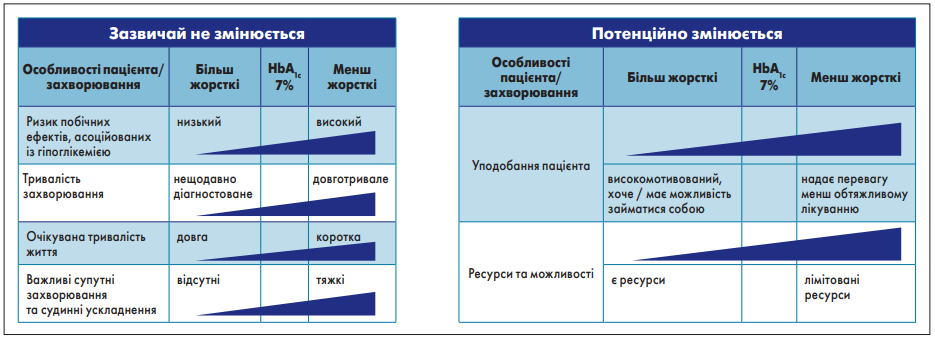 Рис. 1. Підхід до визначення індивідуальних глікемічних цілей
Рис. 1. Підхід до визначення індивідуальних глікемічних цілей
Таким чином, індивідуальні глікемічні цілі залежать не лише від характеристик захворювання, але й від комплаєнсу та уподобань хворого.
В оновлених рекомендаціях також наголошують на концептуальних відмінностях між поняттями «деінтенсифікація цілей» і «спрощення складних схем лікування». Так, поняття «деінтенсифікація» стосується цілей лікування, а саме – модифікації цілей лікування для зниження ризику гіпоглікемії, якщо цього можна досягти в рамках індивідуалізованого цільового рівня HbA1с. Термін «спрощення» стосується схем терапії і рекомендується для спрощення складних схем лікування (особливо інсулінотерапії), щоб зменшити ризик гіпоглікемії і поліпрагмазії та тягар захворювання, якщо цього можна досягти в рамках індивідуалізованого цільового рівня HbA1с (рівень доказовості B).
Лікування
Загальні принципи
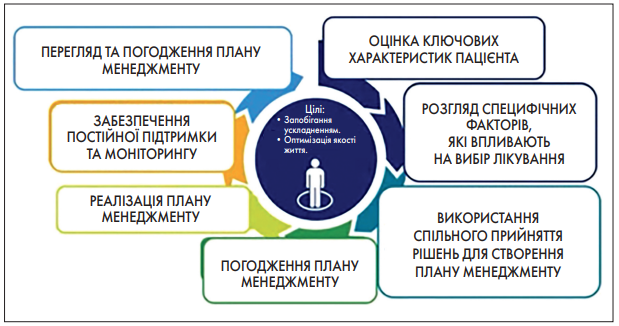
Ключова відмінність між попередніми та оновленими Стандартами ADA 2023, яка стосується лікування ЦД, полягає у використанні цілісного персофінікованого підходу, відображеного на рисунку 2.
Рис. 2. Цілісний персоніфікований підхід у лікуванні ЦД 2 типу
Необхідно зазначити, що менеджмент таких факторів ризику, як глікемія, маса тіла та ССЗ, разом із кардіоренальною протекцією однаково важливі та має проводитися постійно.
ССЗ залишаються провідною причиною смертності від ЦД, тому менеджмент СС-ризику не менш важливий, ніж інші компоненти лікування ЦД. Основні аспекти управління СС-ризиком на тлі ЦД відображені на рисунку 3.
Рис. 3. ССЗ та менеджмент ризиків
ADA 2023 рекомендує набагато агресивніше управління СС-факторами ризику, зокрема:
- цільовий АТ – <130/80 мм рт. ст. (а не <140/90 мм рт. ст., як було раніше);
- цільовий рівень ЛПНЩ – <70 мг/дл
- для людей із факторами ризику атеросклеротичного ССЗ (АС СС3) (раніше
- <100 мг/дл) і <55 мг/дл для осіб з АС ССЗ (раніше <70 мг/дл).
Особам із ЦД 2 типу та встановленим АС ССЗ або декількома факторами ризику АС ССЗ рекомендується призначати агоністи рецептора глюкагоноподібного пептиду-1 (арГПП-1) з продемонстрованою користю щодо ССС для зниження ризику серйозних коронарних подій (MACE). Особам із ЦД 2 типу та встановленим АС ССЗ або декількома факторами ризику АС ССЗ комбінована терапія інгібітором натрійзалежного котранспортера глюкози 2-го типу (іНЗКТГ2) та арГПП‑1 може бути розглянута для додаткового зниження ризику несприятливих СС і ниркових подій.
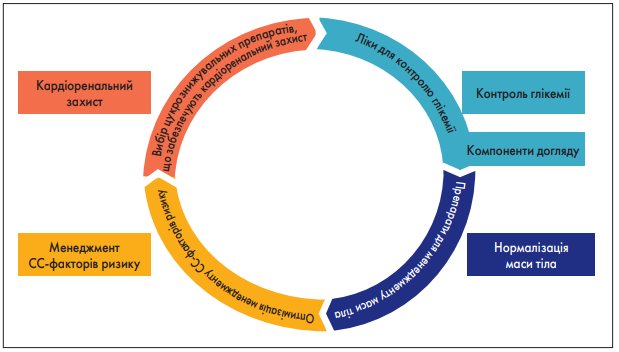
Таким чином, цілі лікування ЦД сьогодні все більше зміщують фокус із глюкозоцентричності до більш інтегрованих підходів, які враховують контроль глікемії і лікування ожиріння, що однаково важливо. Саме це дає можливість запобігти або відтермінувати ускладнення ЦД та оптимізувати якість життя пацієнтів. Цикл прийняття рішень для персоніфікованого менеджменту глікемії в разі ЦД 2 типу відображений на рисунку 4.
Рис. 4. Цикл прийняття рішень для персоніфікованого менеджменту глікемії в разі ЦД 2 типу
Ін’єкційна терапія
Зміни торкнулися і рекомендацій із застосування ін’єкційної терапії.
Передусім важливо, що в настанові застосовують термін саме «ін’єкційна», а не «інсулінотерапія». Це підкреслює пріоритетність застосування арГПП‑1 у пацієнтів із ЦД 2 типу в разі потреби ін’єкційної терапії для зниження рівня HbA1c (рівень доказовості А).
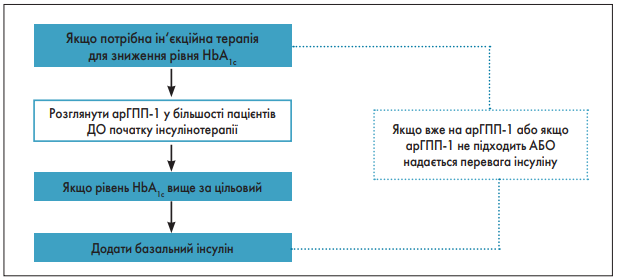
Алгоритм інтенсифікації ін’єкційної терапії відображений на рисунку 5.
Рис. 5. Алгоритм інтенсифікації ін’єкційної терапії
Рекомендації щодо застосування арГПП‑1 як першої ін’єкції пояснюються вищим співвідношенням користь-ризик у порівнянні з інсуліном. Зокрема, арГПП‑1 ефективно контролюють глікемію, не підвищуючи при цьому ризик гіпоглікемій, позитивно впливають на масу тіла та мають переваги щодо СС та ниркових наслідків.
Сучасні дослідження підтверджують доцільність застосування арГПП‑1 у людей, які не досягли цільового рівня глікемії. У клінічних дослідженнях додавання ін’єкційного арГПП‑1 або інсуліну особам, які потребують подальшого зниження рівня глюкози, глікемічна ефективність ін’єкційного арГПП‑1 була подібною або вищою за таку базального інсуліну. Застосування арГПП‑1 у цих дослідженнях супроводжувалося меншим ризиком гіпоглікемії та сприятливим впливом на масу тіла в порівнянні з інсуліном, хоча і з сильнішими шлунково-кишковими побічними ефектами. Отже, результати досліджень підтверджують, що арГПП‑1 є кращим варіантом для осіб, які потребують ефективної ін’єкційної терапії для контролю рівня глюкози.
Систематичний огляд доступних на сьогодні досліджень ефективності та безпеки застосування арГПП‑1 у разі діабету показав, що зниження рівня НbА1с від вихідного в разі використання арГПП‑1, як правило, було більшим або подібним порівняно з інсулінотерапією. При цьому застосування арГПП‑1 виявилося незмінно ефективнішим щодо зниження маси тіла, ніж більшість пероральних цукрознижувальних препаратів та інсуліну, і пов’язано з нижчим ризиком гіпоглікемії проти інсуліну або сульфонілсечовини. АрГПП‑1 також позитивно впливали на СС-фактори ризику.
Результати ще одного метааналізу, в якому порівнювали клінічні ефекти арГПП‑1 короткої або тривалої дії з інсуліном у хворих на ЦД 2 типу, показали, що порівняно з інсуліном арГПП‑1 ефективніше знижували рівень НbА1с (Δ -0,12%; р<0,0001). Базальний інсулін ефективніше знижував рівень глюкози в плазмі натще (Δ -1,8 ммоль/л; р<0,0001), тоді як арГПП‑1 ефективніше знижували масу тіла (Δ -3,71 кг; р<0,0001). Частка пацієнтів, в яких спостерігали епізоди гіпоглікемії, була на 34% нижчою в групі арГПП‑1 (р<0,0001), з подібною тенденцією стосовно розвитку тяжкої гіпоглікемії.
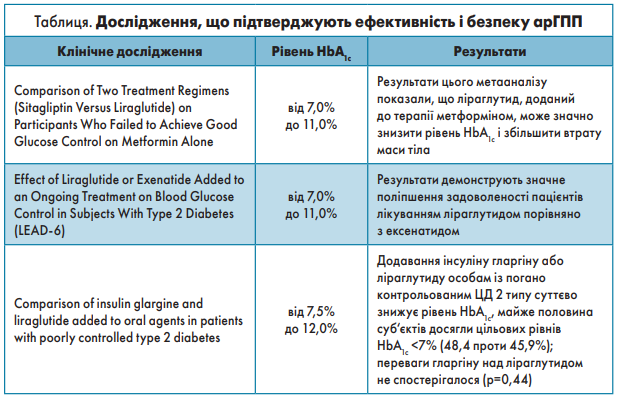
Щодо рівня НbА1с, на тлі якого доцільно призначати арГПП‑1, то результати клінічних досліджень, наведені в таблиці, підтверджують ефективність і безпеку арГПП‑1 у пацієнтів із рівнем HbA1c від 7% до 12%.
Висновки
Ключові оновлення «Стандартів надання медичної допомоги при цукровому діабеті 2023 р.» ADA:
- зростання ролі ІМТ у скринінгу ЦД 2 типу;
- зниження віку початку скринінгу ЦД серед загальної популяції до 35 років;
- перехід від глюкозоцентричного до цілісного персоніфікованого підходу, кожен із компонентів якого (менеджмент ваги, глікемії та кардіоренального ризику) є однаково важливим і безперервним;
- зростання ролі арГПП‑1 в інтенсифікації терапії ЦД 2 типу.
Реалізація усіх цих принципів у менеджменті пацієнтів із ЦД дає можливість більш ефективно та персоніфіковано досягати цілей лікування, підвищувати прихильність пацієнтів до терапії та забезпечувати особам із ЦД високу якість життя.
Адаптовано з Sayed E.l., Nuha A. et al. Classification and Diagnosis of Diabetes: Standards of Care in Diabetes‑2023. Diabetes care. V. 46, S.1 (2023): S19-S40. doi:10.2337/dc23-S002.
Тематичний номер «Діабетологія. Тиреоїдологія. Метаболічні розлади» № 2 (62) 2023 р.