17 квітня, 2026
Поза алгоритмами: клінічне судження у веденні алергічного риніту
Алергічний риніт (АР) уражає близько 10-40% населення світу й залишається одним з найпоширеніших станів у практиці алергологів і лікарів загальної практики – сімейної медицини. Міжнародні рекомендації, насамперед ARIA (Allergic Rhinitis and its Impact on Asthma), суттєво впорядкували підходи до діагностики та лікування АР завдяки алгоритмам, заснованим на доказах, що стало беззаперечним науковим кроком уперед [1]. Водночас повсякденна клінічна практика свідчить, що реальні пацієнти нерідко виявляються складнішими за будь-які стандартизовані схеми. Такий пацієнтоорієнтований погляд не є новим: він перегукується з гіппократівською традицією вивчати не лише хворобу, а передусім самого хворого, уважно спостерігати за перебігом його стану й не поспішати з висновками, особливо коли клінічні ознаки суперечливі [2].
У цьому матеріалі автори не ставлять під сумнів цінність клінічних настанов. Мета інша – звернути увагу на ті аспекти, яких неможливо повністю навчитися з алгоритмів: індивідуальну клінічну складність, діагностичну невизначеність, варіабельність відповіді на терапію та міжособистісний, комунікативний вимір медичної допомоги.
Фенотипова різнорідність АР, що виходить за межі класифікації ARIA
Класифікація ARIA з поділом АР на інтермітивний або персистивний, а також легкий чи середньотяжкий/тяжкий, безумовно, стала важливим досягненням порівняно з колишнім розмежуванням на сезонний і цілорічний риніт. Проте в реальній клінічній практиці така таксономія не завжди повною мірою відображає фенотипову різнорідність пацієнтів. Зокрема, лікарям добре знайомі хворі з переважанням назальної обструкції, пацієнти, в яких домінують ринорея та чхання, особи з провідними очними симптомами, а також ті, в кого симптоматика найвираженіша вночі.
Такі фенотипи не слід розглядати лише як різний ступінь тяжкості одного й того самого стану. Радше йдеться про відмінні клінічні патерни, яким можуть відповідати різні терапевтичні відповіді. Наприклад, у пацієнтів з переважанням закладеності носа зазвичай кращий ефект забезпечують інтраназальні кортикостероїди, тоді як пероральні антигістамінні засоби в цій ситуації часто є менш результативними.
У практичному вимірі це підкреслює важливість дуже простого, але клінічно вирішального запитання: «Який симптом турбує вас найбільше?». Відповідь на нього нерідко дає лікарю більше для вибору оптимальної терапії, ніж формальне віднесення пацієнта до тієї чи іншої категорії тяжкості.
Діагностична невизначеність і роль клінічного судження
Одним з найпідступніших викликів у практиці є пацієнти, в яких клінічна картина цілком відповідає АР, але результати алергологічного тестування залишаються негативними. Не менш складною є й протилежна ситуація, коли тести демонструють слабкопозитивні результати, проте клінічні прояви не узгоджуються з ними. Одним з можливих пояснень таких розбіжностей є локальний АР – форма захворювання, за якої продукція IgE обмежується слизовою оболонкою носа й може бути виявлена лише за допомогою специфічного назального провокаційного тестування. За сучасними уявленнями, саме ця форма може пояснювати до чверті випадків, які раніше відносили до неалергічного риніту [3].
Практична складність полягає в тому, що специфічне назальне провокаційне тестування недоступне в більшості рутинних клінічних умов. Тому лікареві нерідко доводиться вирішувати непросту дилему: орієнтуватися насамперед на негативні результати тестів чи все ж довіряти клінічній оцінці, якщо сезонність симптомів, чіткі провокувальні чинники та відповідь на протиалергічну терапію переконливо вказують на алергічний механізм.
У таких випадках діагностика виходить за межі суто алгоритмічного підходу й потребує послідовної клінічної інтерпретації, що формується в діалозі між об’єктивними даними, клінічною картиною, анамнезом пацієнта та результатами пробної терапії.
Від хвороби до переживання хвороби
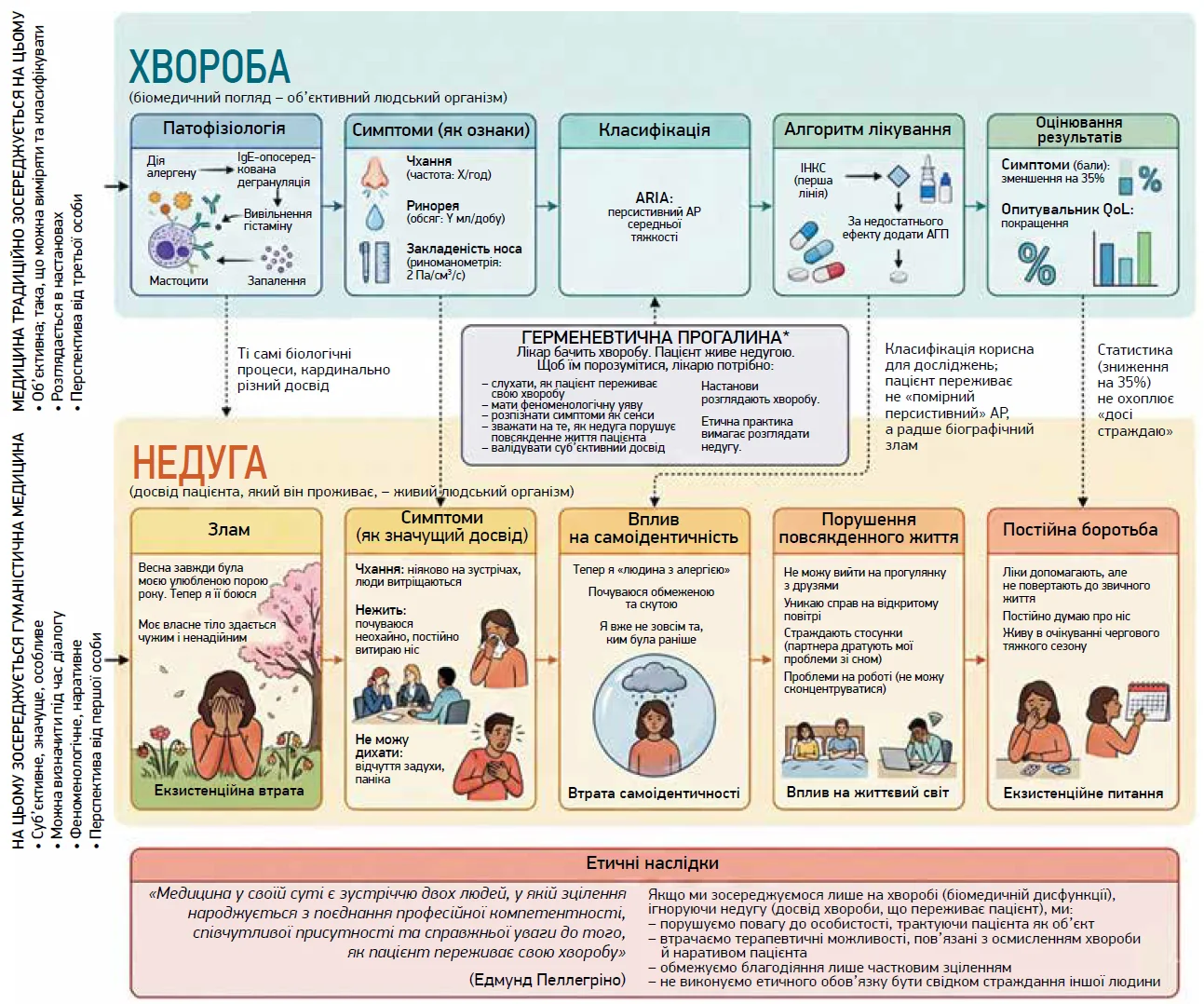
Розмежування між хворобою (англ. disease) як біомедичною сутністю та недугою (англ. illness) як індивідуально пережитим досвідом захворювання є особливо важливим у контексті АР (рис.). Підхід, зосереджений на хворобі як нозології, акцентує увагу на патофізіології, класифікації, терапевтичних алгоритмах і кількісно вимірюваних результатах. Натомість перспектива недуги дає змогу побачити суб’єктивний вимір стану пацієнта: яке значення він надає своїм симптомам, як вони впливають на його самоідентичність, повсякденну активність і якість життя [4].
Рис. Клінічне судження у веденні АР
Примітки. * Герменевтичний – такий, що стосується тлумачення й осмислення. У клінічному контексті означає інтерпретацію симптомів і даних обстеження з огляду на індивідуальний досвід пацієнта. ІНКС – інтраназальні кортикостероїди; АГП – антигістамінні препарати.
Саме тому навіть об’єктивно позитивний результат лікування не завжди означає реальне полегшення для пацієнта. Наприклад, зниження сумарного бала симптомів на 35% може розцінюватися як успіх за критеріями клінічних досліджень, але для самого хворого цього буває недостатньо: весна й надалі асоціюється з погіршенням самопочуття, перебування надворі залишається обмеженим, а сон – порушеним.
Сучасні публікації дедалі виразніше підкреслюють потребу активного залучення пацієнтів до програми лікування, щоб подолати розрив між наявними знаннями та реальною клінічною практикою в алергології. Такий підхід передбачає участь пацієнтів і осіб, які здійснюють догляд, на всіх етапах упровадження лікувальних стратегій [5]. Показово, що нині розроблення стандартизованих наборів клінічних наслідків також дедалі частіше відбувається за безпосередньої участі пацієнтів, зокрема в межах ініціатив на кшталт програми COMET. Це дає змогу враховувати не лише показники, важливі для дослідників, а й ті результати, що справді мають значення для самих хворих у клінічних дослідженнях і повсякденній практиці.
У цьому контексті промовистою є позиція Едмунда Пеллегріно1, який наголошував, що медицина – це не просто технічне застосування наукових знань до біологічної проблеми, а передусім зустріч двох людей, у якій професійна компетентність невіддільна від міжособистісного, екзистенційного й інтерпретаційного вимірів медичної допомоги [6].
Варіабельність терапевтичної відповіді
Антигістамінні препарати другого покоління рекомендовані як терапія першої лінії при легкому та середньотяжкому АР, а дані метааналізів переконливо підтверджують їхню перевагу над плацебо. Водночас середні показники ефективності не відображають усієї клінічної реальності, оскільки відповідь на лікування істотно варіюється між пацієнтами: повного контролю симптомів на тлі монотерапії антигістамінними засобами вдається досягти лише в 40-60% хворих. Аналогічно й інтраназальні кортикостероїди, попри високу ефективність, не забезпечують достатньої відповіді приблизно в 15-30% пацієнтів.
Якщо хворий повідомляє про недостатній ефект антигістамінної терапії, лікар має розглядати одразу кілька можливих причин. Це може бути недостатня прихильність до лікування, фенотип з домінуванням назальної обструкції, за якого антигістамінні засоби менш дієві, завищені очікування від терапії, неповна чи неточна діагностика з недооціненим неалергічним компонентом, а також супутня патологія, зокрема хронічний риносинусит.
Отже, оцінка недостатньої терапевтичної відповіді потребує складного клінічного аналізу й не зводиться до простого лінійного алгоритму.
Алергенспецифічна імунотерапія: чи ефективна в реальній практиці?
Алергенспецифічна імунотерапія (АСІТ) є єдиним методом лікування АР, що здатен модифікувати перебіг хвороби. Її застосування асоціюється зі зниженням вираженості симптомів на 30-40%, причому клінічні переваги можуть зберігатися й після завершення терапії [7]. Водночас між ефективністю, продемонстрованою в клінічних дослідженнях, і результативністю в умовах повсякденної практики існує помітний розрив.
Головним чинником такої невідповідності є недостатня тривалість лікування: повний рекомендований трирічний курс АСІТ завершує лише 40-60% пацієнтів. Саме тому успіх цього підходу визначається не лише біологічною дією терапії, а й здатністю забезпечити довготривалу прихильність пацієнта до лікування.
Підвищенню прихильності можуть сприяти ретельний добір пацієнтів, структуроване консультування до початку терапії, формування реалістичних очікувань, спільне ухвалення рішень і заплановане динамічне спостереження. Хоча ефективність таких стратегій підтверджується наявними даними, їх складно формалізувати у вигляді жорстких рекомендацій, оскільки вони значною мірою залежать від комунікативних навичок лікаря, чутливості до мотивації пацієнта та часу, який можна приділити поясненню й супроводу лікування.
Інтеграція доказів і клінічного досвіду
Майкл Поланьї2 розрізняв знання про щось, тобто явне, формалізоване знання, котре можна чітко описати й передати, та знання про те, як діяти, тобто практичне, досвідне знання [8]. Клінічні настанови належать до першої площини: вони перетворюють наявні наукові дані на чітко сформульовані рекомендації. Однак реальна медицина потребує й другого типу знання – клінічного судження, уміння розпізнавати патерни, що не завжди вкладаються в стандартизовані категорії, готовності працювати в умовах діагностичної невизначеності й інтуїтивного клінічного мислення, котре формується лише завдяки багаторічному досвіду ведення великої кількості пацієнтів.
Як свого часу визначили Sackett і співавт., доказова медицина – це сумлінне, чітке та виважене використання найкращих наявних доказів для ухвалення рішень щодо допомоги конкретному пацієнтові [9]. У такому розумінні вона передбачає не механічне застосування рекомендацій, а поєднання зовнішніх наукових доказів із клінічною експертизою лікаря та цінностями самого пацієнта.
Дуже влучною тут є метафора, згідно з якою клінічні настанови – це ніби мапа. Мапа необхідна для орієнтування, але вона не є самою місцевістю. А місцевість, тобто конкретний пацієнт, завжди виявляється складнішою, багатшою й неоднозначнішою, ніж будь-яка схема здатна повністю відобразити.
Висновки
Клінічна майстерність народжується не з протиставлення доказів і клінічного судження, стандартизації та персоналізації, науки й людяності, а з їх усвідомленого поєднання. Клінічні настанови слід знати, поважати й застосовувати, але водночас – інтерпретувати в контексті конкретної клінічної ситуації та, за потреби, вдумливо адаптувати до особливостей окремого пацієнта.
Саме в цьому полягає один із ключових викликів як для лікарів-практиків, так і для системи медичної освіти: формувати фахівців, які поєднують технічну компетентність і наукову строгість з рефлексивністю, уважністю до пацієнта та здатністю працювати в умовах невизначеності.
При АР, як і в багатьох інших галузях клінічної медицини, сутність справді якісної медичної допомоги розкривається саме в цьому проміжку – «між мапою та місцевістю», між правилом і клінічним судженням.
Література
- Bousquet J., Schünemann H.J., Togias A., et al. Next-generation Allergic Rhinitis and Its Impact on Asthma (ARIA) guidelines for allergic rhinitis based on Grading of Recommendations Assessment, Development and Evaluation (GRADE) and real-world evidence. Journal of Allergy and Clinical Immunology. 2020; 145 (1): 70-80.
- Jouanna J. Hippocrates. Johns Hopkins University Press, 1999.
- Rondón C., Campo P., Togias A., et al. Local allergic rhinitis: concept, pathophysiology, and management. Journal of Allergy and Clinical Immunology. 2012; 129 (6): 1460-1467.
- Di Lorenzo G., Pacor M.L., Amodio E., et al. Differences and similarities between allergic and nonallergic rhinitis in a large sample of adult patients with rhinitis symptoms. International Archives of Allergy and Immunology. 2011; 155 (3): 263-270.
- Warner J.O., Spitters S.J.I.M. Integrating patients into programmes to address the allergy knowledge practice gap. Clinical and Experimental Allergy. 2024; 54 (10): 723-733.
- Pellegrino E.D., Thomasma D.C. The virtues in medical practice. Oxford University Press, 1993.
- Roberts G., Pfaar O., Akdis C.A., et al. EAACI guidelines on allergen immunotherapy: allergic rhinoconjunctivitis. Allergy. 2018; 73 (4): 765-798.
- Polanyi M. The tacit dimension. University of Chicago Press, 1966.
- Sackett D.L., Rosenberg W.M., Gray J.A., Haynes R.B., Richardson W.S. Evidence based medicine: what it is and what it isn’t. BMJ. 1996; 312 (7023): 71-72.
Di Lorenzo G., Melluso M., Seidita A. Beyond algorithms: clinical judgement in the management of allergic rhinitis. Clin. Exp. Allergy. 2026 Feb 17. doi: 10.1111/cea.70254. Epub ahead of print. PMID: 41700315.
Переклав з англ. Олексій Терещенко
Від редакції
Стаття від колег з Італії, яку щойно прочитав читач, ненав’язливо нагадує про важливу річ: у клінічній медицині лікують не нозологію, а людину, яка щодня живе зі своїми симптомами. При АР це особливо відчутно, адже навіть формально легкий перебіг може істотно порушувати сон, денну активність, працездатність, здатність до концентрації та саму свободу звичного життя. Саме тому вибір антигістамінного препарату не зводиться лише до факту блокади H1-рецепторів. У реальній практиці ще потрібно, щоб терапія не створювала для пацієнта нової проблеми замість тієї, яку покликана усунути.
У цьому контексті на увагу заслуговує біластин (Ніксар®, «Берлін-Хемі») – антигістамінний препарат другого покоління, що поєднує клінічну ефективність з характеристиками, важливими для пацієнтоорієнтованого ведення АР. Біластин належить до неседативних H1-антигістамінних засобів і характеризується практично нульовою окупацією H1-рецепторів у головному мозку, що пояснює відсутність клінічно значущого седативного ефекту й мінімальний вплив на когнітивні та психомоторні функції. Це має не лише фармакологічне, а й глибоко практичне значення: пацієнт очікує від лікування не просто зменшення ринореї чи чхання, а збереження ясності мислення, звичної денної активності, працездатності та контролю над власним життям.
Не менш показово, що серед антигістамінних препаратів другого покоління саме біластин відповідає найбільшій кількості критеріїв ідеального антигістамінного засобу, сформульованих у документах EAACI/ARIA: йдеться про поєднання ефективності, селективності, швидкого початку дії, достатньої тривалості ефекту, доброї переносимості, а також відсутності значущої седації, негативного впливу на психомоторні функції, клінічно важливих антихолінергічних ефектів, кардіотоксичності та суттєвих CYP450-опосередкованих лікарських взаємодій. Окрім того, клінічні дані свідчать про ефективний контроль як назальних, так і очних симптомів, а також про нижчу частоту сонливості та втоми порівняно із цетиризином за зіставної антигістамінної ефективності.
У певному сенсі вибір сучасного антигістамінного препарату – це теж простір «між мапою та місцевістю», про який пишуть автори статті. Настанови вказують напрямок, але остаточна цінність терапії розкривається там, де фармакологічна точність зустрічається з реальним життям пацієнта. Коли препарат не лише зменшує симптоми, а й не обтяжує людину сонливістю, когнітивною загальмованістю чи зниженням повсякденної активності, лікування перестає бути просто технічним утручанням – воно стає способом повернути пацієнтові відчуття внутрішньої рівноваги, ясності та свободи дихати не тільки носом, а й повним життям.
1 Edmund Daniel Pellegrino (1920-2013) – американський лікар, філософ та один із засновників сучасної біоетики. Багато писав про моральну природу медицини, відносини між лікарем і пацієнтом, а також про те, що клінічна практика є не лише технічною, а й глибоко людською й етичною діяльністю.
2 Michael Polanyi (1891-1976) – угорсько-британський науковець і філософ науки, який розпочав кар’єру як фізичний хімік, а згодом став одним з найвпливовіших мислителів ХХ століття в галузі епістемології та філософії науки. Найбільше відомий концепцією tacit knowledge – неявного, або мовчазного, знання, тобто такого практичного знання, котрим людина користується, але не завжди може повністю його формалізувати чи висловити.
Медична газета «Здоров’я України 21 сторіччя» № 4 (615), 2026 р