12 травня, 2026
Доброякісна гіперплазія передміхурової залози з недостатньою відповіддю на медикаментозну терапію: ідентифікація нереспондентів
За матеріалами конференції
 Відомо, що до 30-40% пацієнтів із діагнозом доброякісної гіперплазії передміхурової залози (ДГПЗ) мають недостатню клінічну відповідь на медикаментозну терапію, що може бути зумовлено гетерогенністю симптомів нижніх сечових шляхів (СНСШ), різними ступенями тяжкості обструкції вихідного отвору сечового міхура, детрузорної дисфункції та супутніх станів. У рамках науково-практичної конференції «Реконструктивні рішення в урології та гінекології “UroGyn Synergy 2026”», що відбулася 5-8 лютого у змішаному форматі, доповідь «Доброякісна гіперплазія передміхурової залози з недостатньою відповіддю на медикаментозну терапію: ідентифікація нереспондентів» представив лікар уролог, онкохірург, трансплантолог, завідувач відділу урології, нефрології та трансплантації нирки КНП «Клінічний центр онкології, гематології, трансплантології та паліативної допомоги Черкаської обласної ради», доцент кафедри хірургії та екстреної медицини Черкаської медичної академії, доктор філософії (PhD) з медицини Роман Петрович Морару-Бурлеску. Він, зокрема, висвітлив причини неефективності a-адреноблокаторів та інгібіторів 5a-редуктази у цієї категорії пацієнтів та сучасні можливості їх ведення з використанням фітотерапевтичних засобів із доведеними профілями ефективності та безпеки.
Відомо, що до 30-40% пацієнтів із діагнозом доброякісної гіперплазії передміхурової залози (ДГПЗ) мають недостатню клінічну відповідь на медикаментозну терапію, що може бути зумовлено гетерогенністю симптомів нижніх сечових шляхів (СНСШ), різними ступенями тяжкості обструкції вихідного отвору сечового міхура, детрузорної дисфункції та супутніх станів. У рамках науково-практичної конференції «Реконструктивні рішення в урології та гінекології “UroGyn Synergy 2026”», що відбулася 5-8 лютого у змішаному форматі, доповідь «Доброякісна гіперплазія передміхурової залози з недостатньою відповіддю на медикаментозну терапію: ідентифікація нереспондентів» представив лікар уролог, онкохірург, трансплантолог, завідувач відділу урології, нефрології та трансплантації нирки КНП «Клінічний центр онкології, гематології, трансплантології та паліативної допомоги Черкаської обласної ради», доцент кафедри хірургії та екстреної медицини Черкаської медичної академії, доктор філософії (PhD) з медицини Роман Петрович Морару-Бурлеску. Він, зокрема, висвітлив причини неефективності a-адреноблокаторів та інгібіторів 5a-редуктази у цієї категорії пацієнтів та сучасні можливості їх ведення з використанням фітотерапевтичних засобів із доведеними профілями ефективності та безпеки.
Ключові слова: доброякісна гіперплазія передміхурової залози, симптоми нижніх сечових шляхів, медикаментозна терапія, a-адреноблокатори, клінічні нереспонденти, фітотерапія, екстракт Serenoa repens, Простамол® Уно.
Чинники, що визначають симптоми та відповідь на лікування
ДГПЗ – це гістологічно встановлений діагноз, який описує ріст тканини передміхурової залози (ПЗ) і є поширеною причиною СНСШ у чоловіків. Доведено, що ця патологія виникає внаслідок порушення балансу між клітинною проліферацією та загибеллю, у результаті чого збільшується кількість епітеліальних і стромальних клітин ПЗ. При цьому СНСШ найчастіше проявляються за доброякісної обструкції ПЗ. Клінічні дані свідчать, що частина пацієнтів із СНСШ не відповідають на стандартні схеми терапії через відмінні домінуючі механізми їх розвитку (обструкція вихідного отвору сечового міхура, гіперактивний сечовий міхур, гіпоактивність детрузора, запалення, нічна поліурія, поведінкові фактори тощо). Тому наріжним каменем менеджменту ДГПЗ виступає фенотипування пацієнтів і перегляд діагнозу в разі невдачі лікування (Американська урологічна асоціація – AUA, 2021; Європейська асоціація урології – EAU, 2025).
Низька ефективність α1-адреноблокаторів може спостерігатися за вираженої анатомічної обструкції (інтравезикальна простатична протрузія та великий об’єм ПЗ), а також за домінування детрузорної слабкості (Chia S.J. et al., 2003; Park H.Y. et al., 2016). Незважаючи на те що інгібітори 5α-редуктази знижують ризик прогресування ДГПЗ і гострої затримки сечі, їхній ефект формується повільно і є обмеженим в осіб із низьким рівнем простат-специфічного антигену (ПСА) та малим об’ємом ПЗ (McConnell J.D. et al., 2003; Roehrborn C.G. et al., 2010).
На думку доповідача, особливої уваги з боку практикуючого уролога потребує когорта чоловіків віком 50-65 років із невеликим об’ємом ПЗ, невираженими СНСШ, із категорією PI-RADS 3 та рівнем загального ПСА в діапазоні 4-10 нг/мл (так звана сіра зона). Цим пацієнтам, як правило, проводять fusion-біопсію ПЗ і за відсутності злоякісних змін призначають лікування з урахуванням превалювання іритативної або обструктивної симптоматики. Оперативне лікування не є терапією першого вибору. У приблизно 30% таких хворих через 10-15 років потенційно розвинеться клінічно значущий рак ПЗ, і вони підлягатимуть радикальному хірургічному лікуванню, притому що вже матимуть нетримання сечі після, наприклад, гольмієвої лазерної енуклеації або лапароскопічних простих простатектомій, виконаних із приводу ДГПЗ. Отже, пріоритетною в даному випадку є медикаментозна терапія.
Serenoa repens у довготривалому застосуванні: ключові клінічні спостереження
За даними клінічних досліджень, фітотерапія СНСШ/ДГПЗ не поступається традиційним препаратам за відсутності негативного впливу на статеву функцію (Carraro J.C. et al., 1996; Debruyne F. et al., 2002; Ryu Y.W. et al., 2015). Комітет з лікарських засобів рослинного походження (HMPC) Європейського агентства з лікарських засобів (EMA) видав монографію (2013), яка визначає гексановий екстракт із плодів пальми пилкоподібної Serenoa repens (HESr) як добре вивчений засіб для симптоматичного лікування ДГПЗ. Згідно з документом, рекомендована доза екстракту становить 320 мг/добу. HESr покращує об’ємну швидкість потоку сечі (Qmax) і сприяє скороченню кількості сечовипускань за ніч (0,64 [95% довірчий інтервал 0,98-0,31]) порівняно з плацебо. Крім того, він має сприятливий профіль безпеки з дуже обмеженою дією на статеву функцію. Згідно з настановами EAU, екстракт Serenoa repens показаний чоловікам із СНСШ, які хочуть уникнути будь-яких потенційних побічних ефектів лікування, особливо пов’язаних зі статевою функцією (рівень доказовості – 2, сила рекомендацій – слабка).
Терапевтичний ефект при ДГПЗ забезпечується комплексом активних фіторечовин екстракту Serenoa repens. При цьому склад, відсоток і зберігання останніх (поліненасичені жирні кислоти та фітостероли) в екстракті безпосередньо залежать від надійності виробника та якості виробництва. Так, згідно зі звітом EMA, добова доза жирних кислот значно відрізнялася (до 500 разів) від одного препарату до іншого: різниця між їх вмістом, заявленим на упаковці, та виміряною кількістю коливалася від 9,9 до 460,4% (Bartram W., 2015).
На вітчизняному фармацевтичному ринку оригінальний стандартизований спиртовий екстракт плодів Serenoa repens представлений фітопрепаратом Простамол® Уно (виробництво «Берлін-Хемі АГ», Німеччина), який за своїми характеристиками повністю відповідає вимогам EMA та HMPC. Згідно з базою даних Nicholas Hall’s global CHC DB6, Простамол® Уно лідирує з продажів безрецептурних препаратів для лікування ДГПЗ у Європі.
Відкрите непорівняльне спостережне дослідження довгострокової ефективності лікування екстрактом Serenoa repens (Простамол® Уно) у пацієнтів із легкими та помірними СНСШ, викликаними ДГПЗ (за Міжнародною шкалою оцінки простатичних симптомів [IPSS] <20 балів), продемонструвало, що тривалий прийом (протягом 24 міс) 320 мг спиртового екстракту Serenoa repens позитивно впливав на їхню сексуальну функцію, що підкріплювалося статистично значущим підвищенням Міжнародного індексу еректильної дисфункції (IIEF) (на 6,4 бала) (Sinescu I. et al., 2011) (рис. 1).
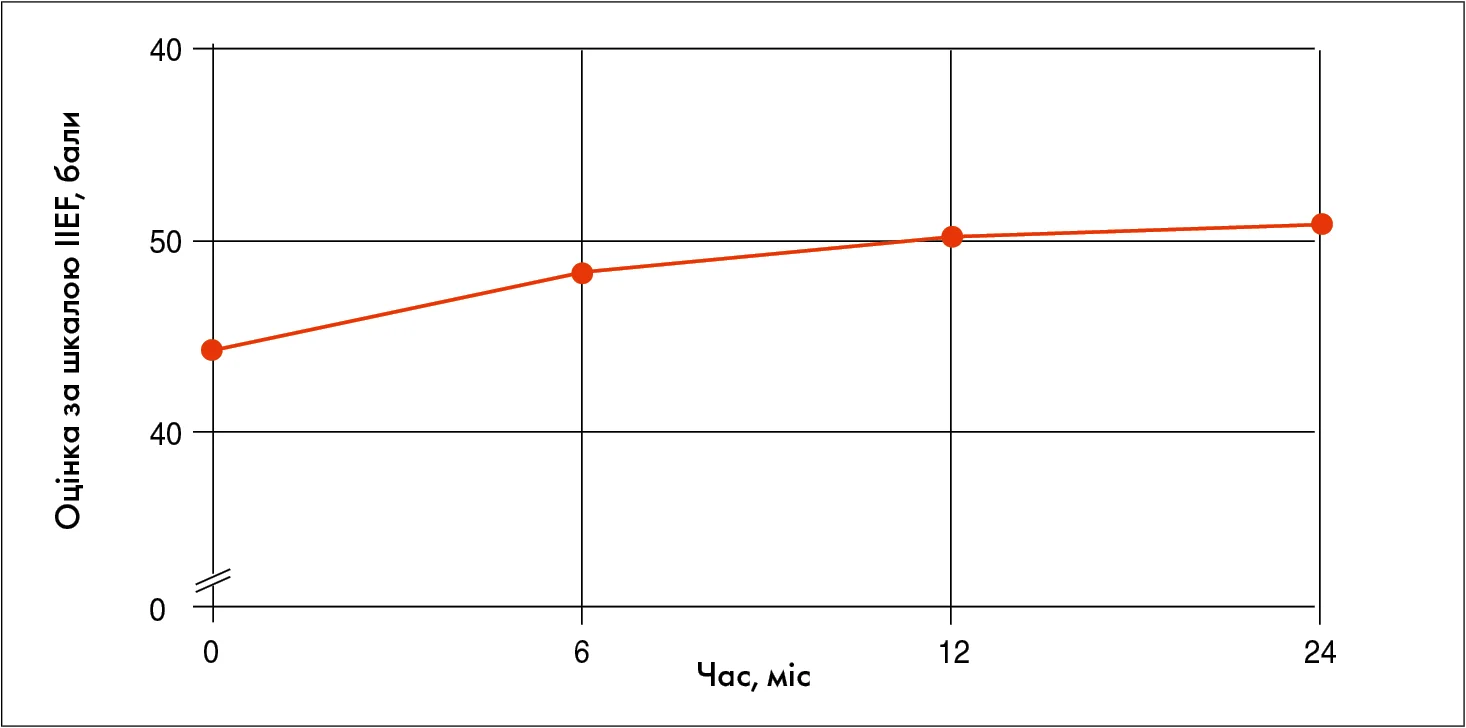 Рис. 1. Ефективність Простамол® Уно щодо покращення статевої функції у 24-місячному клінічному дослідженні (Sinescu I. et al., 2011)
Рис. 1. Ефективність Простамол® Уно щодо покращення статевої функції у 24-місячному клінічному дослідженні (Sinescu I. et al., 2011)
Згідно з результатами спостережного дослідження (Breza J. et al., 2005), прийом спиртового екстракту Serenoa repens (Простамол® Уно) 320 мг/добу впродовж 12 міс не лише полегшував суб’єктивні скарги пацієнтів із ДГПЗ (оцінка за шкалою IPSS >10 балів), а й зупиняв прогресування захворювання (рис. 2).
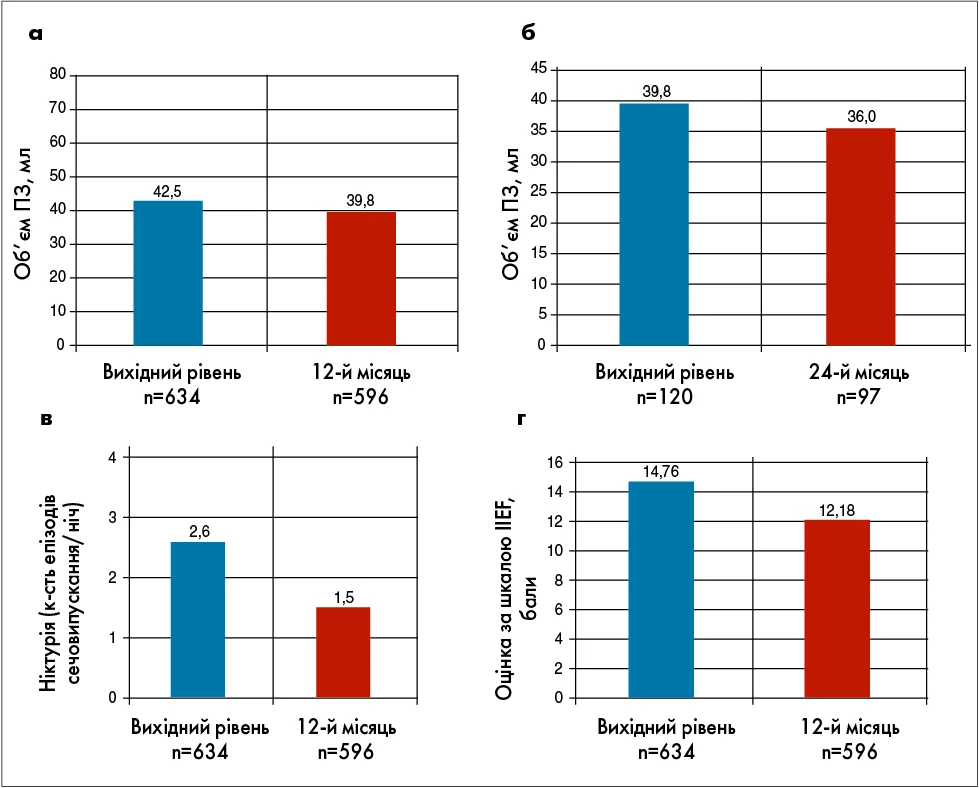 Рис. 2. Ефективність спиртового екстракту Serenoa repens (Простамол® Уно) у 12-місячному спостережному дослідженні (Breza J. et al., 2005):
Рис. 2. Ефективність спиртового екстракту Serenoa repens (Простамол® Уно) у 12-місячному спостережному дослідженні (Breza J. et al., 2005):
а – запобігання збільшенню об’єму ПЗ через 12 міс (об’єм змінився незначно – з 42,5 мл до лікування до 39,8 мл після лікування); б – запобігання подальшому збільшенню об’єму ПЗ через 24 міс (об’єм ПЗ змінився незначно – з 39,8 мл
на 12-му тижні до 36,0 мл на 24-му тижні); в – зниження частоти ніктурії на фоні фітотерапії протягом 12 міс; г – відсутність негативного впливу фітотерапії на сексуальну функцію протягом 12 міс (оцінка за шкалою IIEF змінилася незначно – з 14,76 бала до лікування до 12,18 бала після лікування)
Недостатня відповідь на терапію: причини, маркери, подальші кроки
Повертаючись до питання недостатньої відповіді на медикаментозну терапію ДГПЗ, спікер дав визначення поняттю «клінічний нереспондент»: це пацієнт, у якого після лікування належної тривалості адекватною дозою за високого комплаєнсу зберігаються клінічно значущі симптоми. При цьому він зауважив, що невдача консервативної терапії не є показанням до оперативного лікування.
До факторів, що підвищують ймовірність нереспонсивності, відносять великий об’єм залишкової сечі (ОЗС), низьку Qmax, рівень ПСА >1,5 нг/мл, об’єм ПЗ >40 см3, протрузію ПЗ. Отже, практичними маркерами невдачі медикаментозної терапії є недостатнє зменшення кількості балів за шкалою IPSS, великий ОЗС, низька Qmax, наявність епізодів затримки сечі та прогресування ускладнень (Roehrborn C.G. et al., 2008; EAU, 2024).
У разі недостатньої клінічної відповіді на медикаментозне лікування слід виключити так звану псевдонереспонсивність, що може мати місце в наступних випадках:
- поганий комплаєнс: пропуски прийому препаратів, самовільна їх відміна через побічні ефекти, неналежний час застосування;
- невиправдані очікування пацієнта: сподівання на «зникнення симптомів за три дні» при схемі лікування, де ефект проявляється через місяці;
- некоректний діагноз/коморбідність: гіперактивний сечовий міхур, нічна поліурія, інфекції сечовивідних шляхів, камені, стриктури, неврологічні порушення, діабетична цистопатія;
- фармакологічні чинники: застосування діуретиків увечері, прийом деконгестантів, антихолінергічних препаратів, споживання алкоголю/кофеїну, закрепи.
Нереспондентам медикаментозної терапії показане детальне обстеження:
- оцінка за шкалою IPSS, включаючи індекс якості життя (QoL), за опитувальником щодо нетримання сечі ICIQ, за шкалою ніктурії;
- об’єктивізація стану пацієнта: заповнення щоденника сечовипускань за три дні, урофлоуметрія (Qmax), визначення ОЗС при ультразвуковому дослідженні (УЗД), аналіз сечі;
- оцінка ПЗ: пальцеве ректальне дослідження, вимірювання рівня ПСА (за показаннями), трансректальне УЗД (об’єм ПЗ, наявність середньої частки);
- за підозри на ускладнення: креатинін, розрахункова швидкість клубочкової фільтрації, УЗД нирок/сечового міхура;
- уродинамічне дослідження/уретроцистоскопія показані за підозри на гіпоактивність детрузора, стриктуру, невідповідність симптомів і досліджуваних показників.
За відсутності клінічного покращення через 6-12 міс медикаментозної терапії, за прогресування симптомів або розвитку ускладнень слід змінити стратегію лікування та розглянути інвазивні методи (AUA, 2024; EAU, 2024).
Оперативне втручання показане в більш короткі строки в таких випадках:
- рецидивуюча гостра затримка сечі або значуще зростання ОЗС попри лікування;
- ускладнення – повторні інфекції сечовивідних шляхів, камені сечового міхура, макрогематурія, гідронефроз/погіршення функції нирок;
- симптоми, які суттєво знижують QoL, тоді як оптимізована схема медикаментозної терапії неефективна/непереносима;
- високий анатомічний фактор обструкції (інтравезикальна простатична протрузія/середня частка) + «обструктивний» профіль урофлоуметрії;
- користь від інтервенції переважає ризики з урахуванням уподобань пацієнта.
Таким чином, відсутність відповіді на медикаментозну терапію часто зумовлена не призначуваним препаратом, а неправильним відбором хворих. Пацієнти з великим ОЗС, низькою Qmax, об’ємом ПЗ >40 см3 та інтравезикальною простатичною протрузією є малоймовірними респондентами. Перед зміною терапії слід виключити псевдонереспондентів. Відсутність покращення через 6-12 міс має бути приводом для перегляду лікувальної стратегії, але не зміни препарату; разом із тим невдача терапії не є показанням до оперативного втручання.
Фітопрепарати, що містять екстракт із плодів Serenoa repens, можуть бути ефективними лише як стандартизовані екстракти, зокрема Простамол® Уно, що показаний для тривалої терапії пацієнтів із помірними симптомами ДГПЗ, без ознак вираженої обструкції. Настанови EAU 2025 року рекомендують екстракт Serenoa repens чоловікам із СНСШ, які хочуть уникнути будь-яких потенційних побічних ефектів, особливо пов’язаних зі статевою функцією. Простамол® Уно усуває основні прояви ДГПЗ, запобігаючи прогресуванню симптомів, збільшуючи швидкість потоку сечі та покращуючи якість життя. Високий контроль виробництва й відповідність вимогам EMA та HMPC щодо стандартизації рослинних екстрактів забезпечують якість і добру переносимість препарату Простамол® Уно.
Підготувала Марина Малєй
Тематичний номер «Урологія. Нефрологія. Андрологія» № 1 (40), 2026 р.



 Морару-Бурлеску Р.П.
Морару-Бурлеску Р.П.
