18 липня, 2019
Пазопаніб у лікуванні сарком м’яких тканин: досвід мультидисциплінарних центрів

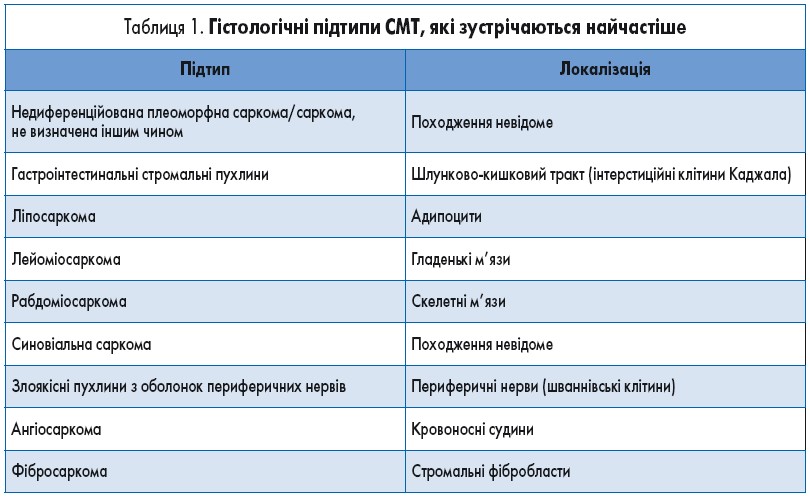
Саркоми м’яких тканин (СМТ) – це дуже неоднорідна група рідкісних злоякісних пухлин, що походять з мезенхімальних тканин – м’язів, сухожиль, жирової тканини, кровоносних і лімфатичних судин, нервів і навколосуглобових тканин. Гістологічний підтип СМТ визначається тканиною походження; загалом ідентифіковано понад 50 гістологічних підтипів цих пухлин (табл. 1). Найчастіше локалізаціями первинної пухлини є кінцівки (43%), внутрішні органи (19%), заочеревинний простір (15%), тулуб (10%), голова та шия (9%). СМТ становлять близько 1% усіх злоякісних пухлин у дорослих. У США у 2015 р. було діагностовано 11 930 випадків СМТ. Проте справжня захворюваність на СМТ, імовірно, точно не визначена, частково через те, що пацієнтів з гастроінтестинальними стромальними пухлинами (GIST) до 2001 р. не включали в онкологічні реєстри, а також через відсутність відповідного коду в Міжнародній класифікації хвороб 9-го перегляду, який дозволив би точно визначати всі випадки.
Локалізовані резектабельні СМТ лікують шляхом хірургічного втручання, часто в поєднанні з променевою терапією та хіміотерапією (ХТ), при цьому 5-річна виживаність становить 83%. Водночас рецидивні СМТ часто є неоперабельними або метастатичними і характеризуються поганим прогнозом. Приблизно в 50% пацієнтів, у яких на момент встановлення діагнозу наявна лише первинна пухлина, згодом розвиваються віддалені метастази і зрештою дисеміноване захворювання. Медіана виживаності після виявлення метастазів становить 12-14 міс, 5-річна виживаність при СМТ з метастазами – 16-18%. Деякі дослідники вказують на певне покращення виживаності пацієнтів з метастатичними СМТ (за винятком GIST) протягом останніх 20 років, проте загальний прогноз у таких хворих залишається поганим.
Традиційно стандартною першою лінією лікування пацієнтів з пізніми стадіями СМТ була системна цитотоксична ХТ. Перші схеми ХТ складалися з антрацикліну (доксорубіцин, епірубіцин) та алкілувального агента (іфосфамід або циклофосфамід і/або дакарбазин). Лікування при СМТ пізніх стадій має бути індивідуалізованим. Пацієнти, які не є кандидатами на проведення комбінованої ХТ, зазвичай отримують монотерапію антрацикліном (доксорубіцином). Нещодавно у ретроспективному дослідженні підходів до лікування СМТ у Північній Америці та Європі було встановлено, що найчастіше застосовувані схеми першої лінії терапії при рецидивних і метастатичних СМТ включають антрациклін (доксорубіцин або епірубіцин) у комбінації з іфосфамідом ± дакарбазин (37%) та доксорубіцин як монотерапію (34%). Монотерапія доксорубіцином є прийнятною, якщо метою лікування є контроль хвороби, проте в разі необхідності зменшення розмірів пухлини більш ефективна комбінована терапія. Ще донедавна доксорубіцин залишався єдиним препаратом, схваленим Управлінням з контролю якості харчових продуктів і лікарських препаратів США (FDA) для застосування при більшості підтипів СМТ пізніх стадій; докази ефективності інших часто застосовуваних агентів були отримані переважно у дослідженнях ІІ фази.
Частота відповіді на лікування за різними схемами варіює у широких межах – від 25 до 66% для комбінованої ХТ та від 4 до 45% для монотерапії. Імовірно, це пов’язано з неоднорідністю підтипів СМТ, а також застосовуваними препаратами, інтенсивністю їх дози та досвідом купірування токсичності. Інші хіміотерапевтичні агенти зазвичай використовують у наступних лініях лікування і, за даними досліджень ІІ фази, забезпечують частоту відповіді 25-49%. Трабектидин – алкілувальний агент, схвалений для лікування дорослих пацієнтів з СМТ пізніх стадій у разі прогресування захворювання після терапії антрациклінами й іфосфамідом, а також пацієнтів, які не є кандидатами на призначення цих препаратів. У більшості пацієнтів з СМТ ефективні наступні лінії терапії зрештою вичерпуються, що свідчить про необхідність впровадження більш ефективних методів лікування.
Часто обмежувальним фактором ХТ є токсичність, особливо при застосуванні високодозових схем. Проявами токсичності можуть бути нудота і блювання, алопеція, нейро- та нефротоксичність, мієлосупресія й анемія, при якій необхідне проведення гемотрансфузії. Застосування комбінації доксорубіцину й іфосфаміду асоціюється з високою частотою відповіді, але частіше порівняно з монотерапією викликає тромбоцитопенію, анемію та нейтропенію. Введення доксорубіцину в кумулятивних дозах вище 700 мг/м2 площі поверхні тіла у вигляді 72-годинної інфузії чи болюсно може призводити до кардіоміопатії. Додавання дексразоксану знижує цей ризик, але не усуває його повністю і, крім того, сприяє мієлосупресії.
Саркома м’яких тканин є порівняно рідкісним захворюванням, тож у клінічні дослідження зазвичай включали пацієнтів із різними гістологічними підтипами СМТ та лікували їх однаково. Утім з’являється все більше даних про те, що відповідь на ХТ різних гістологічних підтипів відрізняється. Зокрема краща відповідь на ХТ досягається у пацієнтів з рабдоміосаркомою, мікофібросаркомою, міксоїдною/круглоклітинною ліпосаркомою, синовіальною саркомою, ангіосаркомою та лейоміосаркомою, натомість у пацієнтів з альвеолярною м’якотканинною саркомою (АМС), світлоклітинною саркомою (меланомою м’яких тканин) та GIST зазвичай наявна резистентність до стандартної цитотоксичної ХТ. У випадку GIST, які найчастіше розвиваються внаслідок мутацій генів KIT або PDGFRA (кодують рецептор фактора росту мастоцитів/стовбурових клітин і поліпептид PDGFR-(α) відповідно), ефективність демонструють інгібітори цих сигнальних шляхів (іматиніб, сунітиніб, регорафеніб). При АМС перспективним є застосування мультитаргетного інгібітора тирозинкінази цедиранібу. Іншим типам СМТ також властиві певні генетичні зміни, проте таргетні препарати в цих випадках рутинно не застосовуються.
У 2012 р. cхвалення FDA пазопанібу для лікування пацієнтів з СМТ пізніх стадій, які раніше отримували ХТ (за винятком пацієнтів з адипоцитарною СМТ та GIST) істотно розширило можливості терапії цієї тяжкої хвороби. Пазопаніб, який є мультитаргетним низькомолекулярним інгібітором тирозинкінази, продемонстрував ефективність при багатьох гістологічних підтипах СМТ у разі прогресування після ХТ.
Коли інноваційний препарат впроваджують у клінічну практику, постають питання про відбір пацієнтів, які найімовірніше отримають користь від терапії, та про купірування побічних ефектів. У цій статті ми ділимося власним досвідом застосування пазопанібу в пацієнтів з СМТ пізніх стадій і даємо рекомендації для досягнення найкращих результатів лікування.
Огляд дослідження PALETTE
Схвалення FDA пазопанібу ґрунтувалося на доказах, отриманих у рандомізованому подвійному сліпому плацебо-контрольованому дослідженні ІІІ фази PALETTE у пацієнтів з СМТ пізніх стадій і прогресуванням хвороби після попередньої ХТ. Первинною кінцевою точкою дослідження була виживаність без прогресування (ВБП); вторинні кінцеві точки включали загальну виживаність (ЗВ), частоту відповіді, безпеку та якість життя.
До включення у дослідження пацієнти могли отримати до 4 ліній системної терапії, але не більше 2 ліній з комбінованими схемами; крім того, не дозволялася попередня терапія інгібіторами ангіогенезу чи модуляторами VEGF. Спектр гістологічних підтипів охоплював більшість типів СМТ, за винятком адипоцитарної саркоми (на підставі результатів дослідження ІІ фази, які вказували на недостатню ефективність препарату при цьому підтипі).
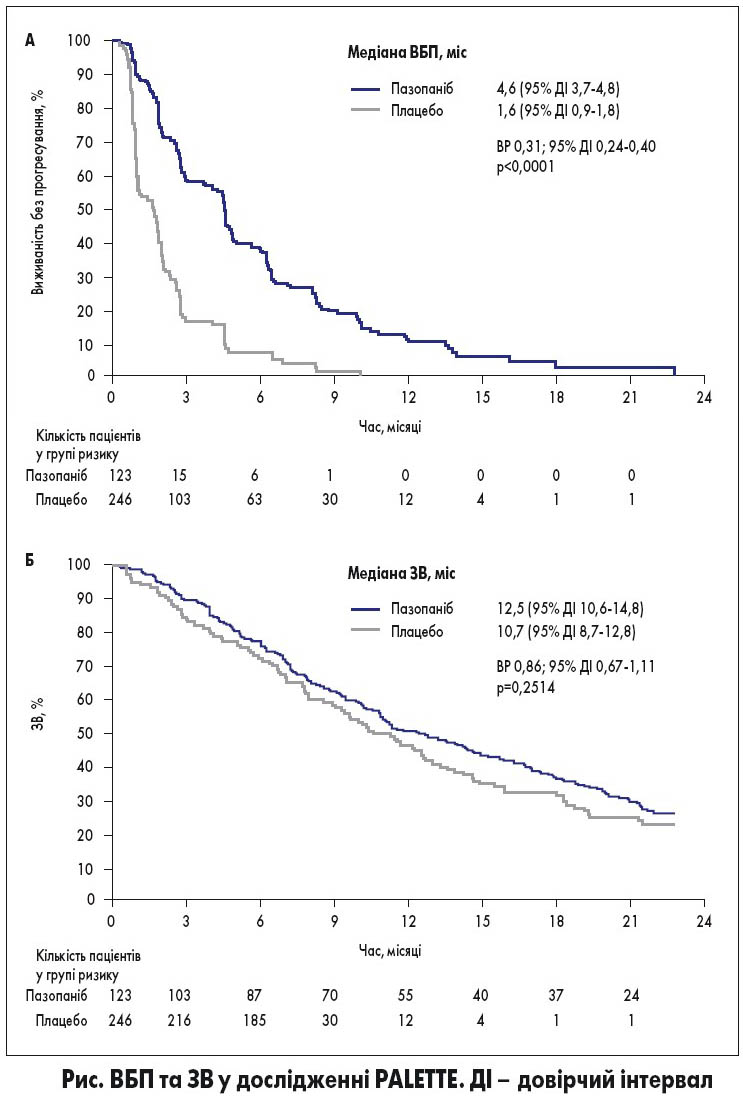
Пазопаніб значно покращив ВБП порівняно з плацебо (медіана 4,6 vs 1,6 міс; відносний ризик – ВР – 0,31; р<0,0001; рис. А). У групі пазопанібу також подовжувалася ЗВ, хоча різниця не досягла статистичної значимості (медіана 12,5 vs 10,7 міс; ВР 0,86; р=0,2514; рис. Б). При лікуванні пазопанібом у 6% пацієнтів було отримано часткову відповідь, у 67% – стабілізацію хвороби. Прогностичними факторами більшої ВБП були висока або проміжна диференціація пухлини, менша кількість попередніх ліній системної терапії та хороший функціональний стан пацієнта.
Характеристики пазопанібу
Пазопаніб є мультитаргетним низькомолекулярним інгібітором тирозинкінази. Препарат пригнічує рецептори судинного фактора росту (VEGFR1-3), рецептори тромбоцитарного фактора росту (PDGFR)-α і -β, KIT, рецептори фактора росту фібробластів (FGFR‑1, 3), лейкоцитспецифічну тирозинкіназу (Lck), IL‑2R-індуцибельну кіназу Т-клітин (Itk) та ін. Ріст і метастазування СМТ залежать від ангіогенезу, а експресія ангіогенних маркерів, як-от VEGF та PDGFR, асоціюється з нижчою диференціацією, більш пізньою стадією пухлини і вищим ризиком розвитку рецидиву. Отже, інгібування цих сигнальних шляхів є раціональною стратегією лікування СМТ.
Пазопаніб має більш сприятливий профіль токсичності щодо мієлосупресії, ніж часто застосовувані хіміопрепарати, зокрема доксорубіцин, іфосфамід, дакарбазин, гемцитабін і трабектидин; тяжка мієлосупресія при лікуванні пазопанібом розвивається дуже рідко. Ще одна рідкісна небажана подія при застосуванні пазопанібу – дисфункція міокарда – зазвичай є безсимптомною і зворотною.
Наш клінічний досвід свідчить, що пазопаніб переноситься краще, ніж будь-які інші препарати чи схеми для системного лікування пацієнтів із саркомами, включно з доксорубіцином, іфосфамідом, дакарбазином/темозоломідом, гемцитабіном і доцетакселом. Загалом профіль переносимості пазопанібу схожий на такий трабектидину.
Більшість низькомолекулярних інгібіторів тирозинкінази не є селективними щодо своїх мішеней; це викликає позацільові ефекти, які можуть спричиняти розвиток небажаних реакцій. Порівняно із сунітинібом пазопаніб інгібує меншу кількість кіназ, що може пояснювати відмінності у профілях безпеки цих препаратів. Із власного досвіду відомо: у пацієнтів, які отримували пазопаніб з приводу СМТ, виникало менше побічних ефектів, ніж у хворих, що приймали сунітиніб для лікування з приводу GIST.
Власний клінічний досвід застосування пазопанібу при СМТ
Наш досвід свідчить, що пазопаніб є ефективним і добре переноситься. Основні побічні ефекти препарату – нудоту, діарею і гіпертензію – можна порівняно легко й ефективно контролювати. Побічним ефектом, що найбільше турбує пацієнтів, є втома, але її також можна контролювати за допомогою фармакологічних і нефармакологічних підходів.
Хоча пазопаніб є ефективним при більшості підтипів СМТ, певні гістологічні підтипи є більш чутливими до препарату. Ми спостерігали вражаючу відповідь у пацієнтів із синовіальною саркомою, солітарною фіброзною пухлиною, лейоміосаркомою, АМС, позаскелетною міксоїдною хондросаркомою та міксофібросаркомою. Більшість із цих пацієнтів раніше отримували цитотоксичну ХТ, попри це у них не спостерігалася дозолімітуюча мієлосупресія при лікуванні пазопанібом. У нашій практиці пазопаніб є стандартною першою лінією терапії для пацієнтів з АМС.
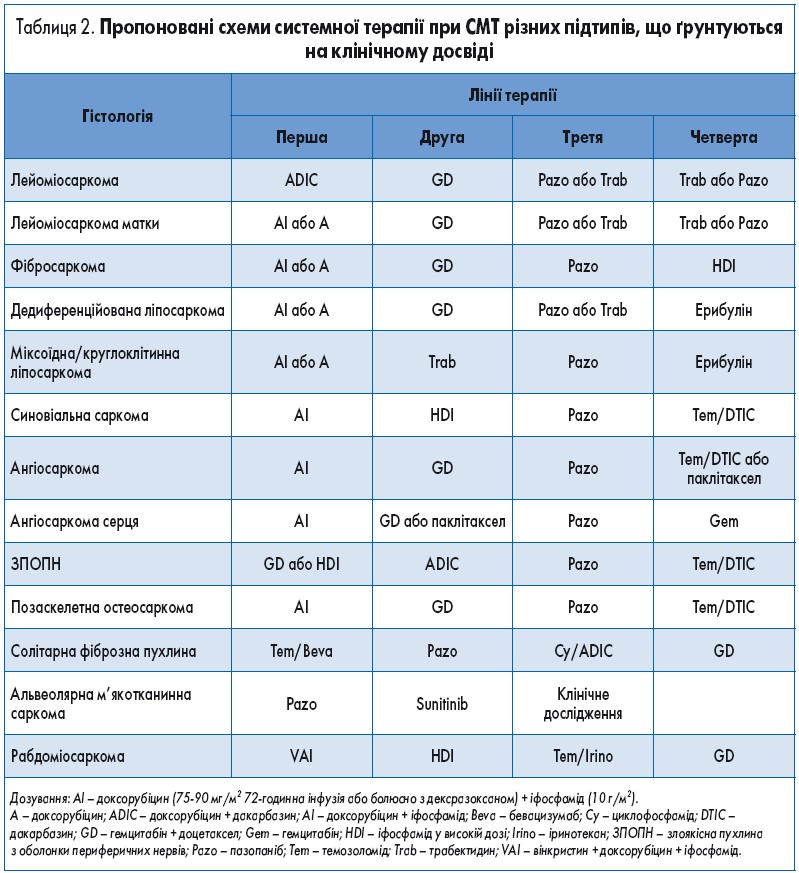
У таблиці 2 наведені варіанти системної терапії, які ми використовуємо при різних підтипах СМТ. Стосовно злоякісної пухлини з оболонок периферичних нервів, наш досвід лікування пацієнтів з нейрофіброматозом 1 типу свідчить про вищу активність іфосфаміду у високій дозі (14 мг/м2) та комбінації гемцитабін + доцетаксел порівняно з іншими варіантами лікування, зазначеними в рекомендаціях. Позаскелетна остеосаркома клінічно поводиться як СМТ, є відносно резистентною до платиновмісної ХТ і відповідає на лікування комбінацією доксорубіцин (75 мг/м2) + іфосфамід (10 г/м2); як другу лінію терапії доцільно призначати пазопаніб. АМС є хіміорезистентною, проте може відповідати на лікування сунітинібом та іншими інгібіторами MEK та VEGFR. Пазопаніб також може пригнічувати проліферативні сигнали при АМС; загалом він розглядається як препарат третьої лінії терапії, проте існують докази про доцільність його застосування у другій лінії. У дослідженні PALETTE пацієнти групи пазопанібу, які отримували цей препарат у першій або другій лінії, мали кращий прогноз порівняно з хворими, яким пазопаніб призначали у третій або наступних лініях терапії (ВР 0,72; р=0,0404).
Обговорення
Накопичений клінічний досвід свідчить, що пазопаніб загалом переноситься краще, ніж інші препарати чи схеми лікування СМТ. При застосуванні пазопанібу можливий розвиток побічних ефектів, але їх легко контролювати. Стратегії ведення пацієнтів з проявами токсичності включають профілактичні заходи, зменшення дози, вчасне лікування з приводу небажаної події, навчання пацієнтів і належне спостереження.
У клінічний практиці ми застосовуємо пазопаніб переважно у другій і третій лініях терапії у пацієнтів з різними підтипами СМТ, які раніше отримували ХТ. Ми віддаємо перевагу інтенсивному веденню побічних ефектів замість зменшення дози. У пацієнтів похилого віку іноді застосовуємо ескалацію дози з 200 до 800 мг протягом декількох тижнів, що допомагає мінімізувати побічні ефекти. Решта пацієнтів, за нашими спостереженнями, дозу 400 мг 2 р/добу переносять краще, ніж 800 мг 1 р/добу.
Можливості пазопанібу в лікуванні хворих з СМТ вивчають у поточних дослідженнях, зокрема в рандомізованому дослідженні ІІ фази, в якому порівнюють ефективність введення пазопанібу і доксорубіцину у першій лінії терапії у пацієнтів віком старше 60 років з СМТ пізніх стадій. Сьогодні доксорубіцин є основним препаратом для паліативного лікування цієї категорії хворих. Припускають, що застосування пазопанібу дозволить зменшити частоту гематологічної токсичності, нейтропенічної лихоманки й інфекцій. В інших дослідженнях, що тривають, оцінюють ефективність пазопанібу в першій лінії терапії у пацієнтів з СМТ, які не переносять ХТ, в ад’ювантній та неоад’ювантній терапії при резектабельних СМТ пізніх стадій, а також у складі комбінованих схем з іншими препаратами для системної терапії.
Van Tine B.A., Trent J.C. How we use pazopanib in treating soft-tissue sarcoma: experience atour multidisciplinary sarcoma centers. Curr Med Res Opin. 2019 Apr; 35 (4): 623-629.
Переклав з англ. Олексій Терещенко
Тематичний номер «Онкологія. Гематологія. Хіміотерапія» № 2 (58), 2019 р