13 квітня, 2018
Ехокардіографічна діагностика дисфункції протезованих клапанів серця як можливої причини серцевої недостатності
Особи з протезованими клапанами серця становлять особливу категорію пацієнтів, лікування котрих потребує спеціальних знань. Одна з проблем, з якою стикаються лікарі й пацієнти, – це виникнення симптомів або поглиблення явищ серцево-судинної недостатності. Частою причиною погіршення стану хворого може бути дисфункція клапанного протеза, що часто виникає гостро, але часом розвивається й поступово. Крім того, погіршення стану хворого може бути зумовлене незалежними від клапанного протеза причинами, а саме: ліво- чи правошлуночкова недостатність, що прогресує, аритмія, легенева гіпертензія, ішемія міокарда тощо.
Найпоширенішим способом оцінювання функції протезованих клапанів серця в щоденній клінічній практиці є ехокардіографія (ЕхоКГ). Однак у значній частині випадків це завдання не є простим. Частково це зумовлено великим розмаїттям клапанних протезів. Починаючи з 1950 року у світі впроваджено понад 100 моделей штучних клапанів серця. Мало того, кожен із чотирьох клапанів серця може бути замінений на штучний, а в одного й того самого пацієнта може бути два, ба навіть три клапанні протези [1].
 Нині маємо справу з трьома основними типами механічних протезів, які відрізняються між собою за будовою замикального елемента (оклюдера): коливальний диск, двопелюстковий елемент, кульковий оклюдер. Однопелюсткові коливальні дискові клапани складаються з круглого плоского замикального пристрою, що зазвичай відкривається під кутом 60-80°. Двопелюсткові клапани мають оклюдери, які представляють собою два напівкруглі диски, що прикріплюються до жорсткого кільця за допомогою маленьких петель (рис. 1). Кут відкриття дисків відносно площини кільця протеза досягає 75-90°, а отвір такого клапана має три частини: найменша розташована по центру між двома відкритими пелюстками, а дві більші – це напівкруглі отвори по боках. Кульковий клапан складається з пластмасової кулі й металевого круглого кільця, на якому розташовані металеві дужки, що втримують кулю [2].
Нині маємо справу з трьома основними типами механічних протезів, які відрізняються між собою за будовою замикального елемента (оклюдера): коливальний диск, двопелюстковий елемент, кульковий оклюдер. Однопелюсткові коливальні дискові клапани складаються з круглого плоского замикального пристрою, що зазвичай відкривається під кутом 60-80°. Двопелюсткові клапани мають оклюдери, які представляють собою два напівкруглі диски, що прикріплюються до жорсткого кільця за допомогою маленьких петель (рис. 1). Кут відкриття дисків відносно площини кільця протеза досягає 75-90°, а отвір такого клапана має три частини: найменша розташована по центру між двома відкритими пелюстками, а дві більші – це напівкруглі отвори по боках. Кульковий клапан складається з пластмасової кулі й металевого круглого кільця, на якому розташовані металеві дужки, що втримують кулю [2].
Крім механічних протезів у кардіохірургічній практиці застосовують три різні типи біологічних штучних клапанів: стентові, безстентові та гомографти. Ці протези виготовляють із біологічних тканин, а тому вони менш тромбогенні, ніж механічні клапани [3]. Клапанні біопротези складаються з еластичних стулок, які, відкриваючись, утворюють єдиний отвір, площа котрого відчутно більша за ту, що мають механічні клапани. Стентові біопротези складаються з трьох стулок, які взяті зі свинячого аортального клапана чи зроблені з бичачого перикарда. Ці стулки закріплені на металевому чи полімерному кільці. Безстентові біопротези також виготовлені зі свинячих або бичачих тканин, однак у своїй конструкції не мають ригідного кільця. Гомографти ж продукують шляхом кріопрезервації людських клапанів.
Протягом останнього десятиліття дедалі частіше застосовують транскатетерні клапани, котрі фактично є біопротезами зі спеціальною конструкцією, що дає можливість імплантувати їх в аортальну чи легеневу позицію, використовуючи черезшкірний стегновий або верхівковосерцевий доступ [4, 5].
Протези клапанів можуть мати різні розміри, що впливає на ЕхоКГ-показники, які характеризують роботу клапана. Розмір протеза визначають за зовнішнім (а не внутрішнім) діаметром його кільця й позначають у міліметрах. Тому треба мати на увазі, що цей розмір не є власне діаметром отвору штучного клапана.
Дисфункція клапанного протеза – це особлива патологія, що потребує від лікаря, котрий проводить дослідження, спеціальних знань про функціонування протезованих клапанів, методи їх обстеження та причини розладів їх нормальної роботи [6].
Основна причина дисфункції протезованих клапанів серця – їх тромбоз. За різними даними, він стається в 0,1-5,7% хворих за 1 рік. Окрім того, розлади функціонування протеза можуть виникати внаслідок розростання вегетацій, виникнення абсцесу кільця, наростання пануса (сполучнотканинний валик, який затягує отвір протеза) [7]. На клапанному протезі можна виявити зворотний потік (регургітацію), що відбувається або через отвір протеза, або поза клапанним кільцем (параклапанна регургітація). Надзвичайно рідко може виникнути деформація замикального елемента штучного клапана з порушенням його роботи.
Через те що лікарського об’єктивного обстеження недостатньо, щоб оцінити, чи протезований клапан функціонує нормально, запропоновано різні інструментальні діагностичні методи. Основні ЕхоКГ-характеристики функції протезованого клапана – градієнт тиску, визначений доплерівським методом, й ефективна площа отвору (EOA) [8]. Градієнт тиску залежить не лише від нормального відкриття замикального елемента клапана, а й від інших факторів, зокрема гемодинамічних, тому до отриманих при обстеженні підвищених показників у пацієнта з нормальним самопочуттям потрібно ставитися уважно, але без надмірної тривоги. Швидкості потоків через протези клапанів і, відповідно, розраховані за цими швидкостями градієнти є істотно вищими, ніж через здорові клапани [9]. Вони залежать від об’єму кровоплину, серцевого викиду, частоти серцевих скорочень, наявності супутньої регургітації, розміру й типу протеза, розміру камери чи судини, в яку протез відкривається. Навіть до «нормальних» показників треба ставитися з певною обережністю [10]. Найкраще порівнювати отримані цифри з результатами попередніх обстежень. Для цього всім пацієнтам треба визначати показники функції протезів одразу після імплантації та перед виписуванням зі стаціонару, вказуючи отримані значення в медичній документації, яку хворий забирає із собою [11].
Ліпше визначати середній градієнт тиску, ніж піковий, на який відчутно впливають гемодинамічні фактори. Середній градієнт тиску, отриманий при доплерівському оцінюванні, добре корелює із середнім градієнтом, отриманим при катетеризації серця. Це стосується як мітрального, так і аортального клапанних протезів [12, 13].
Ще один кількісний параметр, який застосовують із метою оцінювання протезованих клапанів, – DVI (Doppler velocity index – доплерівський швидкісний показник). Його розраховують як співвідношення швидкісно-часового інтегралу (VTI) потоку через штучний клапан і VTI у вихідному тракті лівого шлуночка, ЛШ (LVOT): DVI=VTIPrV/VTILVOT. Дисфункцію протезованого клапана запідозрюють тоді, коли співвідношення DVI знижене (<0,3) у випадку протеза аортального клапана чи підвищене (>2,2) у випадку мітрального протеза [13].
 Площу отвору мітрального протеза розраховують за часом напівпадіння тиску (PHT, pressure half-time) так само, як це роблять при мітральному стенозі. Називають цю розраховану величину «ефективна площа отвору» (EOA), бо вона відображає той просвіт протеза, через який відбувається кровоплин, з урахуванням того факту, що відкриті замикальні диски та дужки, котрі їх підтримують, створюють певну перешкоду потоку крові [14, 15]. EOA протезованого мітрального клапана не має бути меншою за 2,0 см2. Двопелюсткові механічні протези мають більшу площу, ніж однопелюсткові. Біологічні протези мають площу отвору більшу, ніж механічні протези. Мінімально допустима в нормі ефективна площа протезованого аортального клапана, розрахована за рівнянням безперервності, не має бути меншою за 1 см2. Основні ЕхоКГ-ознаки, що свідчать про обструкцію протеза мітрального клапана, вказано в таблиці 1.
Площу отвору мітрального протеза розраховують за часом напівпадіння тиску (PHT, pressure half-time) так само, як це роблять при мітральному стенозі. Називають цю розраховану величину «ефективна площа отвору» (EOA), бо вона відображає той просвіт протеза, через який відбувається кровоплин, з урахуванням того факту, що відкриті замикальні диски та дужки, котрі їх підтримують, створюють певну перешкоду потоку крові [14, 15]. EOA протезованого мітрального клапана не має бути меншою за 2,0 см2. Двопелюсткові механічні протези мають більшу площу, ніж однопелюсткові. Біологічні протези мають площу отвору більшу, ніж механічні протези. Мінімально допустима в нормі ефективна площа протезованого аортального клапана, розрахована за рівнянням безперервності, не має бути меншою за 1 см2. Основні ЕхоКГ-ознаки, що свідчать про обструкцію протеза мітрального клапана, вказано в таблиці 1.
Тромбоз штучних клапанів найчастіше стається внаслідок того, що пацієнт порушує режим прийому антикоагулянтів [16]. Найважливішими інструментальними діагностичними критеріями тромбозу механічного клапанного протеза є такі:
1) обмеження рухомості пелюсток замикального елемента при рентгеноскопії;
2) підвищені доплерівські градієнти на протезі при трансторакальній ЕхоКГ;
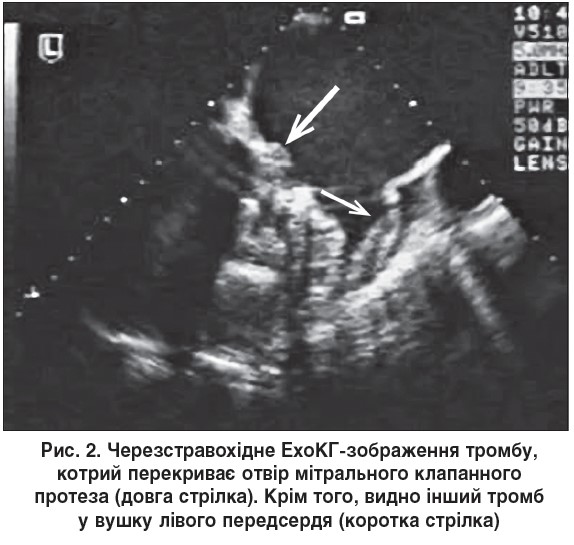 3) виявлення тромбу при черезстравохідній ЕхоКГ (рис. 2).
3) виявлення тромбу при черезстравохідній ЕхоКГ (рис. 2).
Тромб на протезі при трансторакальній ЕхоКГ вдається візуалізувати рідко через наявність інтенсивних артефактів і реверберації ультразвукового сигналу [17]. Зазвичай тромбоз протеза стається гостро зі швидким наростанням проявів серцевої недостатності. Якщо в такого пацієнта при трансторакальному обстеженні виявляють підвищений градієнт тиску на протезі та зменшену EOA, то з метою візуалізації тромбів, які перешкоджають руху крові через клапан, вдаються до черезстравохідного обстеження [18].
Протезну мітральну недостатність (регургітацію) часто важко розпізнати при ЕхоКГ-обстеженні, тому що ультразвуковий промінь проходить крізь протез, металеві структури якого дають інтенсивні артефакти. Потрібно використовувати нестандартні перетини [19]. Під час трансторакального обстеження можна запідозрити тяжку, клінічно суттєву мітральну протезну недостатність у разі таких знахідок: розширений і гіперкінетичний ЛШ; систолічна конвергенція потоку зі шлуночкового боку протеза; підвищена швидкість мітральної діастолічної швидкості E (≥2 м/с); середній градієнт тиску >6 мм рт. ст.; DVI >2,2; незрозуміла та/або така, що наростає, легенева артеріальна гіпертензія.
Коли якість зображення при трансторакальному обстеженні недостатня, вдаються до черезстравохідної ЕхоКГ. За допомогою цього методу з більшим успіхом можливо виявити місце та причину зворотного потоку, зокрема відходження кільця протеза, а також наростання пануса, утворення тромбів, вегетацій, виникнення абсцесів або парапротезних нориць [20, 21].
У режимі кольорової доплерографії часто вдається виявити зворотний потік через протез мітрального клапана на перетині по довгій осі ЛШ. Безперервно-хвильова доплерографія (CW) може дати уявлення про наявність зворотного потоку, але треба бути обережним, щоб не сплутати його з потоком через аортальний клапан. Кольорова доплерографія допомагає виявити, чи зворотний потік виникає на самому протезі, чи поза його кільцем (парапротезна недостатність).
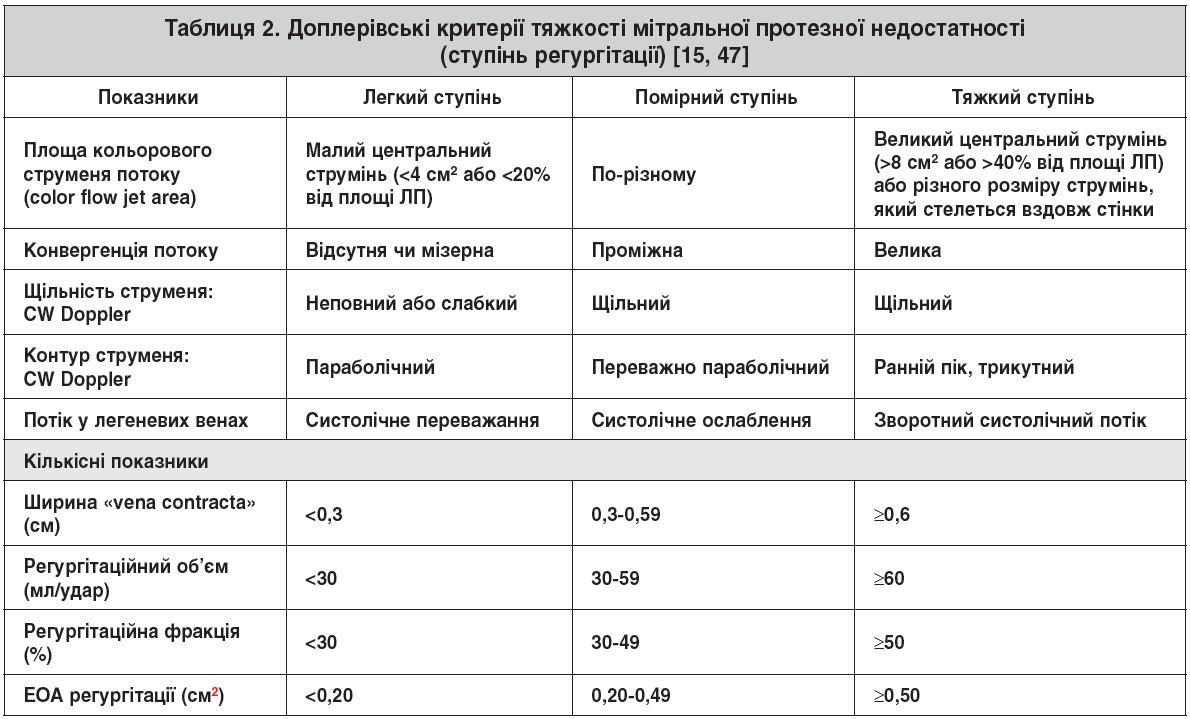
Ступінь мітральної протезної й парапротезної регургітації оцінюють найчастіше напівкількісним методом за відношенням максимальної площі регургітаційного струменя в лівому передсерді (ЛП) до площі перетину ЛП: легкий ступінь – <20%; середній ступінь – 20-40%; тяжкий ступінь – >40%. Це простий, однак досить часто неточний спосіб. Загалом оцінку клапанної протезної недостатності здійснюють за тими самими принципами, що й у разі нативних клапанів [22]. Основні кількісні доплерівські показники мітральної протезної недостатності представлено в таблиці 2. Проте нині не маємо достатньо переконливих даних, які впевнено засвідчували би точність різних кількісних ЕхоКГ-показників у контексті клапанних протезів, зокрема таких як EOA регургітації, ширина регургітаційного струменя чи «vena contracta», а також розраховані регургітаційні об’єми [23]. Ось чому доцільно використовувати багато різних параметрів, а не якийсь один або два, трактуючи їх порівняно з клінічними проявами.
У літературі трапляється чимало повідомлень про те, що 3D-EхоКГ має переваги перед двовимірним способом у виявленні мітральних біляклапанних фістул і регургітаційних струменів, забезпечуючи лікаря надійною інформацією щодо точного розміщення патологічних отворів і кількісно оцінюючи розміри шпаринок та їхні обриси [24, 25].
 Основні ЕхоКГ-показники, що вказують на тяжкість аортальної клапанної протезної обструкції, наведено в таблиці 3.
Основні ЕхоКГ-показники, що вказують на тяжкість аортальної клапанної протезної обструкції, наведено в таблиці 3.
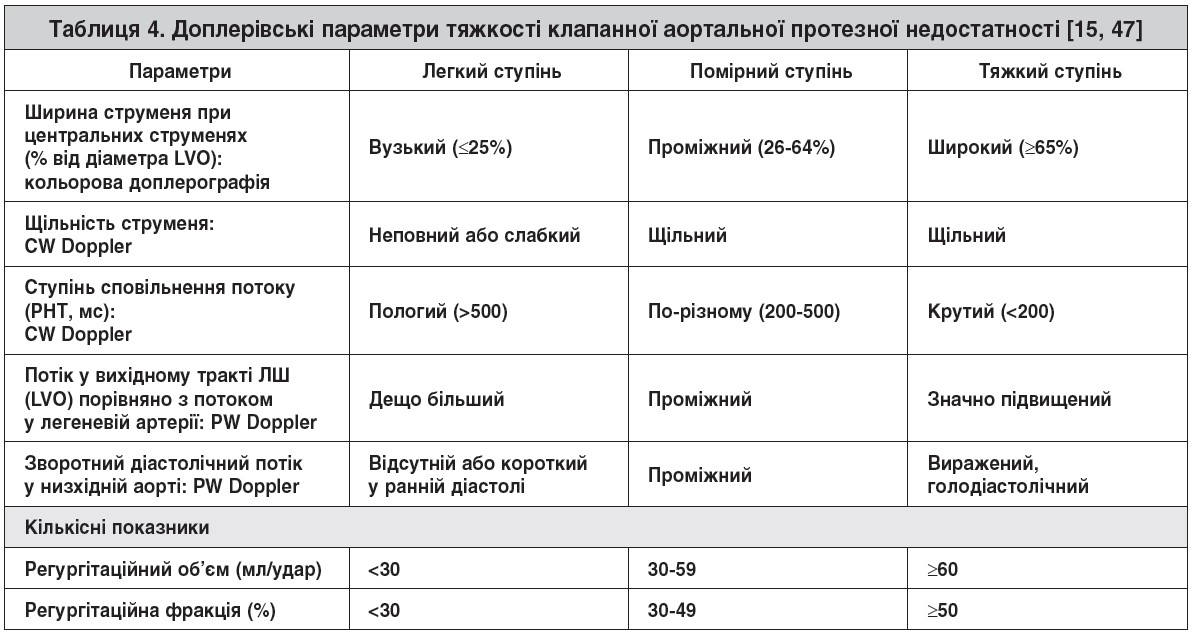
Аортальну протезну й парапротезну регургітацію часто оцінюють за відношенням проксимальної ширини струменя регургітації до ширини вихідного відділу ЛШ на тому самому рівні: легкий ступінь – 1-24%; помірний ступінь – 25-46%; помірно тяжкий ступінь – 47-64%; тяжкий ступінь – >65%. Зворотний потік через протез аортального клапана може бути добре видно в режимі колір-доплер при перетині по короткій осі на рівні вихідного тракту ЛШ. Візуалізація шийки зворотного потоку по короткій осі дає можливість визначити поперечну площину паравальвулярної регургітації в її найвужчому місці. Довжина шийки регургітаційного потоку, що становить <10% від периметру шовного кільця чи клапанного стента, відповідає легкому ступеню, 10-20% – помірному, a >20% – тяжкому зворотному потоку. Хитання чи коливання протеза, які видно на двовимірному зображенні, зазвичай відповідають відходженню кільця протеза більш ніж на 40% [26, 27]. У разі множинних зворотних струменів оцінка тяжкості загального об’єму регургітації є непростим завданням. Рекомендовані доплерівські параметри, котрі переважно застосовують із метою визначення тяжкості аортальної клапанної недостатності, наведено в таблиці 4.
Найпоширенішим недоліком імплантованого через катетер протеза аортального клапана є виникнення потоків регургітації. Насамперед паравальвулярне протікання може бути наслідком неповного прилягання клапанного протеза до аортального кільця. А черезклапанний зворотний потік може статися внаслідок обмеження рухомості стулок протеза чи їх руйнування, а також унаслідок неправильно підібраного розміру чи перерозтягнення клапанного протеза під час імплантації. Якщо протез був імплантований занадто низько в аортальну позицію, то може розвинутися особлива форма регургітації, котру називають надмуфтовою (supraskirtal) [28-31].
 Досить частою причиною дисфункції протезованих клапанів серця є інфекційний ендокардит (рис. 3). Його основними ЕхоКГ-проявами є такі: вегетації та тромби на структурах протеза, відходження кільця протеза від фіброзного кільця клапана, абсцеси, псевдоаневризми, фістули й перивальвулярна (параклапанна) регургітація [32, 33]. Треба мати на увазі, що незначна перивальвулярна недостатність досить часто трапляється й за відсутності ендокардиту. У разі дисфункції протезованого аортального клапана внаслідок інфекційного ендокардиту об’ємні ураження (тромби й вегетації) за допомогою черезстравохідної ЕхоКГ вдається візуалізувати більш ніж у 90% випадків, тоді як за допомогою трансторакального методу – лише в 40% [34-36].
Досить частою причиною дисфункції протезованих клапанів серця є інфекційний ендокардит (рис. 3). Його основними ЕхоКГ-проявами є такі: вегетації та тромби на структурах протеза, відходження кільця протеза від фіброзного кільця клапана, абсцеси, псевдоаневризми, фістули й перивальвулярна (параклапанна) регургітація [32, 33]. Треба мати на увазі, що незначна перивальвулярна недостатність досить часто трапляється й за відсутності ендокардиту. У разі дисфункції протезованого аортального клапана внаслідок інфекційного ендокардиту об’ємні ураження (тромби й вегетації) за допомогою черезстравохідної ЕхоКГ вдається візуалізувати більш ніж у 90% випадків, тоді як за допомогою трансторакального методу – лише в 40% [34-36].
Іншою причиною дисфункції клапанних протезів є розростання пануса. Панус – сполучнотканинний валик, який наростає на отвір протезованого клапана, поступово його перекриваючи [1, 37]. З патофізіологічного погляду це – хронічний запальний процес; клінічні прояви обструкції отвору, що повільно прогресує, наростають поступово, а виражені симптоми з’являються пізно й нагадують тромбоз. Правильна діагностика пануса має важливе значення для вибору методу лікування дисфункції клапанного протеза, адже тромбоз піддається дії фібринолітичних засобів, тоді як на панус фібринолітики не впливають [38]. 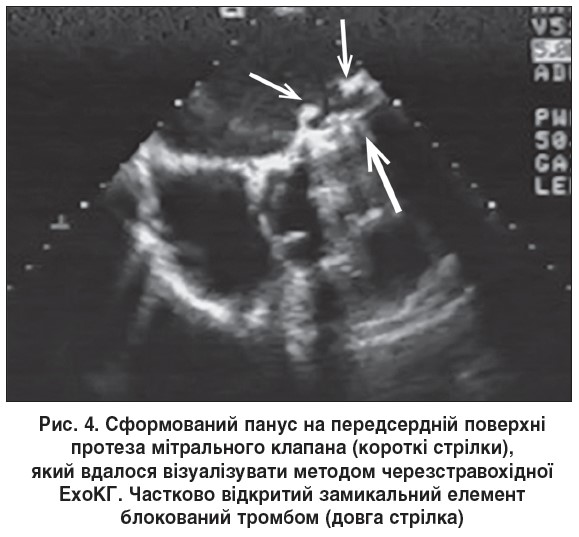 Здебільшого виявити панус вдається, провівши черезстравохідне обстеження (рис. 4). Згідно з опублікованими даними в різних серіях спостережень, частота цього ускладнення становить 1,6-2%. Панус розвивається винятково на механічних протезах, частіше в аортальній позиції [39, 40].
Здебільшого виявити панус вдається, провівши черезстравохідне обстеження (рис. 4). Згідно з опублікованими даними в різних серіях спостережень, частота цього ускладнення становить 1,6-2%. Панус розвивається винятково на механічних протезах, частіше в аортальній позиції [39, 40].
Стеноз протезованого трикуспідального клапана можна запідозрити в разі виявлення морфологічних змін і обмеженої рухомості його стулок у поєднанні з такими показниками: пікова швидкість трансвальвулярного потоку >1,7 м/с, середній градієнт тиску >6 мм рт. ст., час напівпадіння тиску >230 мс [41].
У переважній більшості випадків клапан легеневої артерії замінюють у педіатричних пацієнтів із вродженими вадами серця. Зазвичай із цією метою хірурги використовують різні гомо- й гетерографти. Коли ж виникає стеноз протезованого клапана, то за допомогою ЕхоКГ вдається виявити значне потовщення й різке зменшення рухомості стулок, високу черезклапанну пікову швидкість, пригнічення функції правого шлуночка та значно підвищений тиск у ньому. Якщо ж виникає тяжка недостатність протезованого клапана легеневої артерії, то крім широкого регургітаційного потоку вдається виявити ознаки об’ємного перевантаження правого шлуночка [15].
У хворого з протезованим аортальним клапаном високий піковий систолічний градієнт тиску на ньому може свідчити про невідповідність розмірів протеза величині серцевого викиду (занадто малий діаметр протеза – patient-prosthesis mismatch, PPM). У цих випадках черезстравохідна ЕхоКГ дає змогу з’ясувати, що сам протез функціонує звичайно й немає ознак його тромбування, наростання пануса чи інфекційного ураження. Показником, який свідчить про РРМ, є індексована EOA (розрахована EOA протеза, поділена на площу поверхні тіла хворого). Значення індексованої EOA <0,6 cм2/м2 у випадку протезованого аортального клапана й <0,9 cм2/м2 у випадку мітрального клапана свідчить про тяжку протезну невідповідність [42, 43].
У хворих із вузьким діаметром висхідної аорти (<3 cм) помірно підвищений градієнт тиску, визначений доплерівським методом, може бути пояснений феноменом відновлення тиску (pressure recovery phenomenon) [44]. Насправді загальний градієнт тиску в таких випадках є нижчим, і це вдається підтвердити, якщо підрахувати індекс втрати енергії [45]. Саме тому в осіб із вузькою аортою можна хибно запідозрити стеноз протезованого аортального клапана [46].
Погіршення клінічного стану хворого з протезованим клапаном серця може статися не лише через дисфункцію протеза, а й унаслідок інших серцевих причин. Тому ЕхоКГ-обстеження хворого з клапанним протезом має включати оцінювання нативних клапанів, розмірів камер серця, функції шлуночків, тиску в легеневій артерії, наявності тромбозу ЛП і рідини в порожнині перикарда.
Черезстравохідна ЕхоКГ показана в усіх випадках, коли є підозра на дисфункцію клапанного протеза. Цей метод є високочутливим у виявленні малих тромбів і вегетацій, окрім того, за його допомогою вдається добре локалізувати регургітаційні струмені й ліпше оцінити тяжкість регургітації [47].
Отже, комбінована ЕхоКГ-оцінка протезованих клапанів включає:
1) двовимірне обстеження, котре хоч і не дає достатньо інформації, але добре показує відрив протеза;
2) спектральне доплерівське обстеження, що дає можливість визначити градієнти тиску при стенозуванні (тромби, панус, великі вегетації) та розрахувати EOA;
3) кольорову доплерографію, що допомагає виявити клапанну й параклапанну регургітацію;
4) черезстравохідну ЕхоКГ, яка є особливо цінним методом, що дає змогу з високою чутливістю візуалізувати тромби, вегетації, панус і регургітаційні струмені.
Література
- Baumgartner H., Falk V., Bax J.J., De Bonis M., et al. 2017 ESC/EACTS Guidelines for the management of valvular heart disease. The Task Force for the Management of Valvular Heart Disease of the European Society of Cardiology (ESC) and the European Association for Cardio-Thoracic Surgery (EACTS). European Heart Journal, 2017; 38: 2739-2791.
- Pibarot P., Dumesnil J.G. Prosthetic heart valves: Selection of the optimal prosthesis and long-term management. Circulation, 2009; 119: 1034-1048.
- Cheung D.Y., Duan B., Butcher J.T. Current Progress in Tissue Engineering of Heart Valves: Multiscale Problems, Multiscale Solutions. Expert Opin. Biol. Ther. 2015; 15 (8): 1155-1172.
- Lichtenstein S.V., Cheung A., Ye J., Thompson C.R., Carere R.G., Pasupati S., et al. Transapical transcatheter aortic valve implantation in humans: Initial clinical experience. Circulation, 2006; 114: 591-596.
- Walther T., Simon P., Dewey T., Wimmer-Greinecker G., Falk V., Kasimir M.T., et al. Transapical minimally invasive aortic valve implantation: Multicenter experience. Circulation, 2007; 116: I240-245.
- Tanis W., Budde R.P.J., van der Bilt I.A.C., Delemarre B., Hoohenkerk G., van Rooden J.-K., Scholtens A.M., Habets J., Chamuleau S. Novel imaging strategies for the detection of prosthetic heart valve obstruction and endocarditis. Neth. Heart J. 2016; 24 (2): 96-107.
- Salamon J., Munoz-Mendoza J., Liebelt J.J., Taub C.C. Mechanical valve obstruction: Review of diagnostic and treatment strategies. World J. Cardiol. 2015; 7 (12): 875-881.
- Sordelli C., Severino S., Ascione L., Coppolino P., Caso P. Echocardiographic Assessment of Heart Valve. J. Cardiovasc. Echogr. 2014; 24 (4): 103-113.
- Jamieson W.R., Cartier P.C., Allard M., Boutin C., Burwash I.G., Butany J., et al. Surgical management of valvular heart disease 2004. Can. J. Cardiol. 2004; 20: 7E‑120E.
- Vesey J.M., Otto C.M. Complications of prosthetic heart valves. Curr. Cardiol. Rep. 2004; 6: 106-111.
- Wei-Guo Ma, Bin Hou, Adiljan Abdurusul, Ding-Xu Gong, et al. Dysfunction of mechanical heart valve prosthesis: experience with surgical management in 48 patients. J. Thorac. Dis. 2015; 7 (12): 2321-2329.
- Dumesnil J.G., Honos G.N., Lemieux M., Beauchemin J. Validation and applications of mitral prosthetic valvular areas calculated by Doppler echocardiography. Am. J. Cardiol. 1990; 65: 1443-1448.
- Chambers J.B. The echocardiography of replacement heart valves. Echo Res. Pract. 2016; 3 (3): R35-R43.
- Butchart E.G., Gohlke-Barwolf C., Antunes M.J., Tornos P., De Caterina R., Cormier B., et al. Working Groups on Valvular Heart Disease, Thrombosis, and Cardiac Rehabilitation and Exercise Physiology, European Society of Cardiology. Recommendations for the management of patients after heart valve surgery. Eur. Heart J. 2005; 26: 2463-2471.
- Zoghbi W.A., Chambers J.B., Dumesnil J.G., Foster E., Gottdiener J.S., Grayburn P.A., et al. Recommendations for evaluation of prosthetic valves with echocardiography and Doppler ultrasound: A report from the American society of echocardiography’s guidelines and standards committee and the task force on prosthetic valves, developed in conjunction with the American College of Cardiology Cardiovascular Imaging Committee, Cardiac Imaging Committee of the American Heart Association, the European Association of Echocardiography, a registered branch of the European Society of Cardiology, the Japanese Society of Echocardiography and the Canadian Society of Echocardiography, endorsed by the American College of Cardiology Foundation, American Heart Association, European Association of Echocardiography, a registered branch of the European Society of Cardiology, the Japanese Society of Echocardiography, and Canadian Society of Echocardiography. J. Am. Soc. Echocardiogr. 2009; 22: 975-1014.
- Cannegieter S.C., Rosendaal F.R., Briet E. Thromboembolic and bleeding complications in patients with mechanical heart valve prostheses. Circulation, 1994; 89: 635-641.
- Gursoy M.O., Kalcik M., Yesin M., Karakoyun S., Bayam E., Gunduz S., Ozkan M. A global perspective on mechanical prosthetic heart valve thrombosis: Diagnostic and therapeutic challenges. Anatol. J. Cardiol. 2016; 16 (12): 980-989.
- Tanis W., Budde R.P.J., van der Bilt I.A.C., Delemarre B., et al. Novel imaging strategies for the detection of prosthetic heart valve obstruction and endocarditis. Neth. Heart J. 2016; 24 (2): 96-107.
- Ionescu A., Fraser A.G., Butchart E.G. Prevalence and clinical significance of incidental paraprosthetic valvar regurgitation: a prospective study using transoesophageal echocardiography. Heart, 2003; 89 (11): 1316-1321.
- Vitarelli A., Conde Y., Cimino E., Leone T., D’Angeli I., D’Orazio S., Stellato S. Assessment of severity of mechanical prosthetic mitral regurgitation by transoesophageal echocardiography. Heart, 2004; 90 (5): 539-544.
- Kliger C., Eiros R., Isasti G., Einhorn B., Jelnin V., Cohen H., et al. Review of surgical prosthetic paravalvular leaks: Diagnosis and catheter-based closure. Eur. Heart J. 2013; 34: 638-649.
- Zoghbi W.A., Enriquez-Sarano M., Foster E., Grayburn P.A., Kraft C.D., Levine R.A., et al. American Society of Echocardiography. Recommendations for evaluation of the severity of native valvular regurgitation with two-dimensional and Doppler echocardiography. J. Am. Soc. Echocardiogr. 2003; 16: 777-802.
- Hahn R. Mitral prosthetic valve assessment by echocardiographic guidelines. Cardiol. clinic. 2013; 31: 287-309.
- Shiota T. Role of modern 3D echocardiography in valvular heart disease. Korean J. Intern. Med. 2014; 29 (6): 685-702.
- Kronzon I., Sugeng L., Perk G., Hirsh D., Weinert L., Garcia Fernandez M.A., et al. Real-time 3-dimensional transesophageal echocardiography in the evaluation of post-operative mitral annuloplasty ring and prosthetic valve dehiscence. J. Am. Coll. Cardiol. 2009; 53: 1543-1547.
- Roudaut R., Serri K., Lafitte S. Thrombosis of prosthetic heart valves: Diagnosis and therapeutic considerations. Heart, 2007; 93: 137-142.
- Vitarelli A., Conde Y., Cimino E., Leone T., D’Angeli I., D’Orazio S., et al. Assessment of severity of mechanical prosthetic mitral regurgitation by transoesophageal echocardiography. Heart, 2004; 90: 539-544.
- Mohammadi S., Tchana-Sato V., Kalavrouziotis D., Voisine P., Doyle D., Baillot R., et al. Long-term clinical and echocardiographic follow-up of the Freestyle stentless aortic bioprosthesis. Circulation, 2012; 126: S198-204.
- Gotzmann M., Korten M., Bojara W., Lindstaedt M., Rahlmann P., Mugge A., et al. Long-term outcome of patients with moderate and severe prosthetic aortic valve regurgitation after transcatheter aortic valve implantation. Am. J. Cardiol. 2012; 110: 1500-1506.
- Di Martino L.F.M., Vletter W.B., Ren B., Schultz C., et al. Prediction of paravalvular leakage after transcatheter aortic valve implantation. Int. J. Cardiovasc. Imaging. 2015; 31 (7): 1461-1468.
- Capodanno D., Petronio A.S., Prendergast B., Eltchaninoff H., et al. Standardised definitions of structural deterioration and valve failure in assessing long-term durability of transcatheter and surgical aortic bioprosthetic valves – a consensus statement from the European Association of Percutaneous Cardiovascular Interventions (EAPCI) endorsed by the European Society of Cardiology (ESC) and the European Association for Cardio-Thoracic Surgery (EACTS). Eur. Heart J. 2017; DOI: https://doi.org/10.1093/eurheartj/ehx303.
- Baddour L.M., Wilson W.R., Bayer A.S., et al. Infective Endocarditis in Adults: Diagnosis, Antimicrobial Therapy, and Management of Complications: A Scientific Statement for Healthcare Professionals From the American Heart Association. Circulation, 2015; 132 (15): 1435-1486.
- Vered Z., Mossinson D., Peleg E., Kaplinsky E., Motro M., Beker B. Echocardiographic assessment of prosthetic valve endocarditis. Eur. Heart J. 1995; 16, suppl_B: 63-67.
- Jessurun C., Mesa A., Wilansky S. Utility of transesophageal echocardiography in infective endocarditis. A review. Tex. Heart Inst. J. 1996; 23 (2): 98-107.
- Rap M.I., Chacko A. Optimising the use of transoesophageal echocardiography in diagnosing suspected infective endocarditis. Acta Cardiol. 2015; 70 (4): 487-491.
- Tanis W., Budde P.J.R., van der Bilt I.A.C., Delemarre B., et al. Novel imaging strategies for the detection of prosthetic heart valve obstruction and endocarditis. Neth. Heart J. 2016; 24 (2): 96-107.
- Aoyagi S., Nishimi M., Kawano H., Tayama E., Fukunaga S., Hayashida N., Akashi H., Kawara T. Obstruction of St. Jude Medical valves in the aortic position: significance of a combination of cineradiography and echocardiography. J. Thorac. Cardiovasc. Surg. 2000; 120: 142-147.
- Rizzoli G., Guglielmi C., Toscano G., Pistorio V., Vendramin I., Bottio T., Thiene G., Casarotto D. Reoperations for acute prosthetic thrombosis and pannus: an assessment of rates, relationship and risk. Eur. J. Cardiothorac. Surg. 1999; 16: 74-80.
- Barbetseas J., Nagueh S.F., Pitsavos C., Toutouzas P.K., Quinones M.A., Zoghbi W.A. Differentiating thrombus from pannus formation in obstructed mechanical prosthetic valves: an evaluation of clinical, transthoracic and transesophageal echocardiographic parameters. J. Am. Coll. Cardiol. 1998; 32: 1410-1417.
- Vitale N., Renzulli A., Agozzino L., Pollice A., Tedesco N., de Luca Tupputi Schinosa L., Cotrufo M. Obstruction of mechanical mitral prostheses: analysis of pathologic findings. Ann. Thorac. Surg. 1997; 63: 1101-1106.
- Zoghbi W.A., Enriquez-Sarano M., Foster E., Grayburn P.A., Kraft C.D., Levine R.A., et al. American Society of Echocardiography. Recommendations for evaluation of the severity of native valvular regurgitation with two-dimensional and Doppler echocardiography. J. Am. Soc. Echocardiogr. 2003; 16: 777-802.
- Lam B.K., Chan V., Hendry P., Ruel M., Masters R., Bedard P., et al. The impact of patient-prosthesis mismatch on late outcomes after mitral valve replacement. J. Thorac. Cardiovasc. Surg. 2007; 133: 1464-73.
- Ruel M., Rubens F.D., Masters R.G., Pipe A.L., Bedard P., Hendry P.J., et al. Late incidence and predictors of persistent or recurrent heart failure in patients with aortic prosthetic valves. J. Thorac. Cardiovasc. Surg. 2004; 127: 149-159.
- Baumgartner H., Khan S., DeRobertis M., Czer L., Maurer G. Discrepancies between Doppler and catheter gradients in aortic prosthetic valves in vitro: A manifestation of localized gradients and pressure recovery. Circulation, 1990; 82: 1467-1475.
- Levine R.A., Jimoh A., Cape E.G., McMillan S., Yoganathan A.P., Weyman A.E. Pressure recovery distal to a stenosis: Potential cause of gradient “overestimation” by Doppler echocardiography. J. Am. Coll. Cardiol. 1989; 13: 706-15.
- Vandervoort P.M., Greenberg N.L., Powell K.A., Cosgrove D.M., Thomas J.D. Pressure recovery in bileaflet heart valve prostheses. Localized high velocities and gradients in central and size orifices with implications for Doppler-catheter gradient relation in aortic and mitral position. Circulation, 1995; 92: 3464-3472.
- Lancellotti P., Pibarot P., Chambers J., et al. Recommendations for the imaging assessment of prosthetic heart valves. A report from the European Association of Cardiovascular Imaging endorsed by the Chinese Society of Echocardiography. Eur. Heart J.: Cardiovascular Imaging, 2016; 17: 589-590.
Журнал "Серцева недостатність та коморбідні стани" № 1, квітень 2018 р.