13 квітня, 2018
67-ма щорічна наукова сесія Американської колегії кардіологів (10-12 березня): що нового по проблемі серцевої недостатності?
Дослідження VEST: носимий кардіовертер-дефібрилятор запобігає смертельним випадкам у перші місяці після інфаркту
J. Olgin від імені колективу дослідників VEST
Згідно з останньою настановою Американської колегії кардіологів / Американської асоціації серця (АСС/АНА/HRS) щодо лікування пацієнтів зі шлуночковими аритміями (JACC, 2017) встановлення постійного імплантованого кардіовертера-дефібрилятора (ІКД) показано хворим на постінфарктну симптомну серцеву недостатність (СН) із фракцією викиду лівого шлуночка (ФВ ЛШ) ≤35%, яка лишається зниженою, незважаючи на оптимальне медикаментозне лікування, але не раніше ніж через 40 днів після перенесеного інфаркту міокарда (ІМ) або 90 днів після реваскуляризації. Разом із тим відомо, що певна частка випадків ранньої смерті зумовлена аритміями, які виникають не безпосередньо після ІМ, а дещо пізніше й від яких іще не захищає ІКД. Окрім того, ФВ ЛШ може відновитись і через 3 міс після ІМ, що потребує перегляду показань до встановлення ІКД.
У багатоцентровому рандомізованому відкритому дослідженні VEST вивчалося, чи зможе тимчасовий носимий кардіовертер-дефібрилятор (НКД) у вигляді зовнішнього пристрою на жилеті зменшити частоту випадків раптової серцевої смерті в перші 90 днів після ІМ у пацієнтів зі зниженою ФВ ЛШ, слугуючи «мостом» до можливого встановлення імплантованого пристрою.
Пацієнтів, які перенесли ІМ та мали ФВ ЛШ ≤35%, протягом 7 днів після виписки розподіляли в 2 групи: НКД + оптимальна медикаментозна терапія (n=1524) та оптимальна медикаментозна терапія (n=778). Скринінг і залучення пацієнтів відбувалися з 2008 по 2017 рік у 76 клінічних центрах США, 6 – Німеччини, 24 – Польщі та 2 – Угорщини (середній вік вибірки становив 61 рік; 27% учасників – жінки). У чверті учасників ІМ був не першим у житті; 84% пацієнтів із приводу індексного ІМ перенесли черезшкірне коронарне втручання, 10% – кардіогенний шок, 10% були реанімовані після фібриляції шлуночків або зупинки серця. Середня ФВ ЛШ після індексного ІМ становила 28,2%.
Середній час носіння НКД в основній групі становив 14,1±9,3 год/добу. За 3 міс спостереження у 13 пацієнтів (0,9%) НКД завдав принаймні 1 дефібриляційний розряд за призначенням, у 7 пацієнтів – ≥2 розряди. Частота первинної кінцевої точки «раптова серцева смерть або смерть від шлуночкової аритмії» становила 1,6% у групі НКД і 2,4% – у контрольній групі (p=0,18; відмінності недостовірні). Проте відмінності за вторинною кінцевою точкою «смерть від будь-яких причин» виявилися достовірними на користь НКД: її частота становила 3,1 проти 4,9% у контрольній групі (p=0,04).
Отже, НКД не забезпечує статистично значущого зниження частоти раптової серцевої смерті, проте достовірно знижує загальну смертність у перші 90 днів у постінфарктних пацієнтів із низькою ФВ ЛШ (зниження відносного ризику (ВР) на 35,5%). Призначення НКД доцільне для тимчасового захисту пацієнтів високого ризику з низькою ФВ ЛШ перед тим, як розглядати питання встановлення постійного ІКД через 40-90 днів після перенесеного ІМ.
OUTSMART-HF: дослідження діагностичної цінності рутинної магнітно-резонансної томографії серця за наявності неішемічної СН
I. Paterson, F. Erthal, L. Garrard і співавт.
СН неішемічної етіології досить поширена та в усьому світі переважає над ішемічною СН. Неішемічна СН може бути спричинена багатьма чинниками, й для кожного підтипу передбачене специфічне лікування. Клінічне й ультразвукове обстеження не дають змоги надійно розрізнити підтипи неішемічної СН. Магнітно-резонансна томографія (МРТ) серця допомагає в діагностиці неішемічних кардіоміопатій, але вартість цього методу значно вища, а доступність значно менша порівняно з ехокардіографією (ЕхоКГ). ACC/AHA та Європейське товариство кардіологів дають рекомендації класу I-IIa щодо застосування МРТ серця в пацієнтів із СН, хоча й із низьким рівнем доказів С.
Метою дослідження OUTSMART-HF було визначити, чи допомагає рутинна МРТ серця краще визначити специфічну причину неішемічної СН порівняно з вибірковою МРТ. Рандомізоване дослідження з двома гілками у співвідношенні 1:1 проводили на базі 9 канадських і 3 фінських клінік. До нього були залучені симптомні пацієнти з щойно діагностованою СН або декомпенсацією раніше діагностованої СН і з робочими діагнозами неішемічної кардіоміопатії (з будь-якою ФВ ЛШ) або СН зі збереженою ФВ ЛШ. Протокол передбачав 3 фази: спочатку проводили клінічне обстеження хворих і встановлювали попередній діагноз, потім хворих рандомізували в групи для виконання візуалізаційних досліджень (ЕхоКГ, МРТ), після чого продовжували їх спостерігати до формулювання клінічного діагнозу. Первинною кінцевою точкою слугувало встановлення специфічної етіології СН протягом наступних 3 міс спостереження після проведення візуалізаційних досліджень.
 Усього було рандомізовано 258 пацієнтів в основну групу (ЕхоКГ + рутинна МРТ) і 260 пацієнтів – у групу контролю (ЕхоКГ + МРТ серця в окремих пацієнтів). Групи були добре збалансовані за вихідними характеристиками пацієнтів: середній вік – 59 і 58 років відповідно, анамнез гіпертензії в 53% хворих в обох групах, 25 і 28% відповідно мали цукровий діабет (ЦД), 6 і 4% перенесли ІМ; середня ФВ ЛШ становила 29±12 та 29±15% відповідно в основній і контрольній групах. В основній групі МРТ виконували всім пацієнтам, у контрольній групі вибірково за рішеннями лікарів МРТ було виконано 54 хворим із підозрою на інфільтративну, спадкову патологію чи захворювання перикарда.
Усього було рандомізовано 258 пацієнтів в основну групу (ЕхоКГ + рутинна МРТ) і 260 пацієнтів – у групу контролю (ЕхоКГ + МРТ серця в окремих пацієнтів). Групи були добре збалансовані за вихідними характеристиками пацієнтів: середній вік – 59 і 58 років відповідно, анамнез гіпертензії в 53% хворих в обох групах, 25 і 28% відповідно мали цукровий діабет (ЦД), 6 і 4% перенесли ІМ; середня ФВ ЛШ становила 29±12 та 29±15% відповідно в основній і контрольній групах. В основній групі МРТ виконували всім пацієнтам, у контрольній групі вибірково за рішеннями лікарів МРТ було виконано 54 хворим із підозрою на інфільтративну, спадкову патологію чи захворювання перикарда.
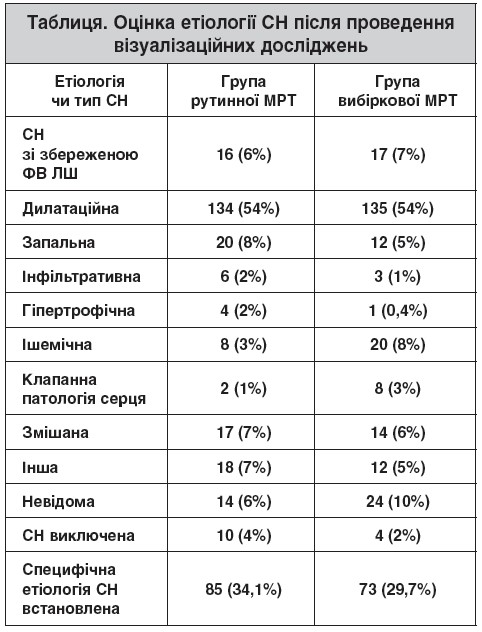
Як і очікувалося, початкова клінічна оцінка етіології СН була неточною й не мала достовірних відмінностей між групами. Після проведення візуалізаційних досліджень в основній групі специфічну етіологію СН (табл.) вдалося встановити у 85 (34,1%) пацієнтів, а в контрольній – у 73 (29,7%), без статистично значущих відмінностей (р=0,27).
Отже, в пацієнтів із попереднім діагнозом неішемічної СН не знайдено відмінностей у встановленні клінічних діагнозів специфічної етіології під час рутинного чи вибіркового застосування МРТ серця, хоча рутинна МРТ частіше виявляла специфічну етіологію СН порівняно з ЕхоКГ (35,7 та 20,1% відповідно; р<0,001). Також між групами не було значущих відмінностей щодо виживання пацієнтів без подій. Проте пацієнти зі специфічними причинами СН, визначеними за допомогою методів візуалізації, мали гірші наслідки порівняно з тими, в кого етіологію не вдалося уточнити. Таким чином, виконання МРТ серця в усіх пацієнтів із неішемічною СН підвищує точність візуалізації специфічних причин, але не впливає на точність клінічних діагнозів.
Дослідження CVD-REAL 2: початок терапії цукрового діабету інгібіторами натрій-глюкозного котранспортеру‑2 асоціюється зі зниженням частоти серцево-судинних подій і смертності
M. Kosiborod від імені колективу дослідників CVD-REAL
Метою цього масштабного міжнародного дослідження було вивчити взаємозв’язки між початком терапії інгібіторами натрій-глюкозного котранспортеру‑2 (SGLT‑2) та широким спектром серцево-судинних подій – госпіталізаціями з приводу СН, ІМ, інсультами, а також загальною смертністю в пацієнтів із ЦД 2 типу з трьох великих регіонів світу – Азійсько-Тихоокеанського, Середнього Сходу та Північної Америки. У дослідження залучали пацієнтів із національних баз даних Австралії, Канади, Ізраїлю, Японії, Сінгапуру й Південної Кореї за такими критеріями включення:
- нещодавно призначені SGLT‑2 чи інші оральні цукрознижувальні препарати;
- встановлений діагноз ЦД 2 типу;
- вік ≥18 років;
- наявні дані анамнезу за більш як 1 рік до дати включення в дослідження.
Після залучення 249 348 пацієнтів, які отримали призначення SGLT‑2, та 3 668 203 пацієнтів, яким було призначено інші цукрознижувальні препарати, було сформовано дві попарно підібрані когорти по 235 064 пацієнти в кожній, які були добре збалансовані за демографічними та клінічними характеристиками. Статистику кожної з досліджуваних подій у когортах описували за допомогою метода пропорційних моделей Кокса. Первинний аналіз здійснювали для популяції intent-to-treat (ITT), тобто незалежно від того, продовжувалося призначене лікування ЦД 2 типу чи припинялося.
Середній вік пацієнтів становив 57 років; 45% когорти SGLT‑2 та 46% когорти інших цукрознижувальних препаратів – жінки; 27 і 26% відповідно мали серцево-судинні захворювання; 53 та 52% відповідно – мікросудинні ускладнення. У двох когортах 63 та 62% пацієнтів відповідно отримували антигіпертензивну терапію; по 9% у кожній когорті – інгібітори АПФ, по 47% – блокатори рецепторів ангіотензину ІІ, по 19% – β-блокатори, по 65% – статини. За лікуванням ЦД 2 типу учасники розподілилися таким чином: 74 та 75% у двох когортах відповідно приймали метформін, 52 та 51% відповідно – похідні сульфонілсечовини, 56 і 55% – інгібітор ДПП‑4, по 13% у кожній когорті – тіазолідіндіони, 20 і 19% – інсулін. З ініційованих SGLT‑2 переважав дапагліфлозин (75% часу експозиції), значно рідше призначали емпагліфлозин (9%), канагліфлозин (4%), лише в Кореї та Японії – іпрагліфлозин (8%), лише в Японії – лузеогліфлозин (1%) і тофогліфлозин (3%).
За результатами аналізів у пропорційних моделях Кокса для популяції ІТТ визначено такі співвідношення частоти подій між когортами терапії SGLT‑2 та терапії іншими цукрознижувальними препаратами:
- загальна смертність – ВР 0,51 (95% довірчий інтервал, ДІ 0,37-0,70); p<0,001;
- госпіталізації з приводу СН – ВР 0,64 (ДІ 0,50-0,82); p<0,001;
- комбінована кінцева точка «смерть від усіх причин / госпіталізація з приводу СН» – ВР 0,60 (ДІ 0,47-0,76); p<0,001;
- ІМ – ВР 0,81 (ДІ 0,74-0,88); p<0,001;
- інсульт – ВР 0,68 (ДІ 0,55-0,84); p<0,001.
За результатами додаткових аналізів жодне із супутніх або перенесених серцево-судинних захворювань не впливало на загальні результати на користь терапії SGLT‑2.
Отже, це велике дослідження, засноване на результатах понад 400 тис. пацієнтів із ЦД 2 типу та з достатньою кількістю подій для кожної кінцевої точки, щоб вважати його статистично значущим, виявило, що ініціація терапії діабету препаратами класу SGLT‑2 асоціюється зі зниженням ризиків смерті, госпіталізації з приводу СН, ІМ та інсульту. Ці результати також вказують на те, що сприятливі серцево-судинні ефекти SGLT‑2 поширюються за межі етнічних груп і географічних регіонів.
Дослідження INDIE-HFpEF: неорганічні нітрити не виправдали сподівань щодо покращення якості життя пацієнтів із СН зі збереженою ФВ
B.A. Borlaug від імені мережі клінічних досліджень СН Національного інституту серця, легенів і крові США
Непереносимість фізичних навантажень, яка маніфестує у вигляді задишки та втомлюваності, є однією з характерних рис СН зі збереженою ФВ. Є докази того, що в патофізіології цього типу СН ключову роль відіграє порушення сигнального шляху оксиду азоту (NO). Попередні спроби підвищити доступність NO за допомогою органічних нітратів провалилися: ізосорбіду динітрат і мононітрат погано переносяться чи обмежують активність хворих. Неорганічні нітрити розглядалися як нове альтернативне джерело NO для таких пацієнтів. У невеликих одноцентрових дослідженнях вони покращували гемодинаміку й толерантність до навантажень.
У дослідженні INDIE-HFpEF перевірялася гіпотеза, чи зможе неорганічний нітрит при інгаляційному введенні за допомогою небулайзера протягом 4 тиж підвищити пікове споживання кисню під час навантажень у пацієнтів із СН зі збереженою ФВ. Окрім цього, були заплановані такі вторинні кінцеві точки, як денна активність пацієнтів за показами акселерометрів; якість життя, пов’язана із СН (за Канзаським опитувальником – KCCQ); рівні натрійуретичного пептиду NT-proBNP; зміни функціонального класу (ФК) СН за NYHA, ЕхоКГ-ознак застою.
Популяція дослідження складалася з пацієнтів середнього віку (68 років) із II-IV ФК СН, середньою ФВ ЛШ (61%), переважно гіпертензивною й ішемічною етіологією СН. Дослідження проводилося за подвійним сліпим рандомізованим плацебо-контрольованим перехресним дизайном. Після первинного скринінгу та рандомізації на групи пацієнти отримували впродовж 4 тиж терапію нітритом або плацебо, потім навпаки. Нітрит дозували починаючи із 46 мг і до 80 мг за умови задовільної переносимості. Статистичний аналіз проводили для популяції ITT.
Початкове пікове споживання кисню становило в середньому 13,8 мл/кг/хв у групі першого призначення плацебо та 13,9 мл/кг/хв у групі першого призначення нітриту. За 4 тиж цей показник дещо покращувався в обох групах (до 18 мл/кг/хв), але між групами не було достовірних відмінностей (p=0,27). Їх також не було щодо жодної зі вторинних кінцевих точок. За переносимості нітрит майже не відрізнявся від плацебо: для всіх небажаних ефектів p>0,05.
Дослідники зробили висновок, що порівняно з плацебо інгаляційний небулізований неорганічний нітрит не покращує толерантність до фізичних навантажень, не впливає на якість життя, рівні натрійуретичного пептиду та інші показники клінічного статусу хворих на СН зі збереженою ФВ. Ці дані не підтримують доцільність застосування неорганічних нітритів для симптоматичної терапії пацієнтів із СН зі збереженою ФВ, але актуалізують нагальну потребу пошуку альтернативних втручань для відновлення дефіциту NO в цієї категорії хворих.
Раптова смерть серед пацієнтів із СН зі збереженою ФВ: аналіз дослідження TOPCAT
M. Vaduganathan, B.L. Claggett, N.A. Chatterjee і співавт.
У цьому дослідженні вивчалися частота та предиктори раптової смерті (РС) або зупинки серця з успішною реанімацією в пацієнтів із СН зі збереженою ФВ. Когорту становили 1767 пацієнтів із СН зі збереженою ФВ (ФВ ≥45%), які брали участь у дослідженні ТОРСАТ на території Американського континенту. РС визначали як несподівану смерть стабільного пацієнта. Медіана терміну спостереження становила 3 роки (від 1,9 до 4,4 року). За цей час померли 385 пацієнтів: 72 пацієнти – від РС (19%), 313 осіб – від інших причин окрім РС (81%). Зареєстровано 6 підтверджених випадків зупинки серця з успішною реанімацією, після яких 4 пацієнти вижили, 1 хворий помер від РС і 1 – унаслідок інфекції. Розрахована частота комбінованої кінцевої точки «РС / реанімована зупинка серця» становила 1,4 (1,1-1,8) на 100 пацієнто-років, частота смертельних випадків з інших причин окрім РС – 5,8 (5,1-6,4) на 100 пацієнто-років. Частота випадків РС / реанімована зупинка серця була чисельно меншою, але статистично недостовірною в пацієнтів, рандомізованих у групу спіронолактону: 1,2 (0,9-1,7) проти 1,6 (1,2-2,2) подій / 100 пацієнто-років; ВР 0,74; 95% ДІ 0,47-1,16; p=0,19. Пацієнти, які померли від РС або перенесли зупинку серця, були молодшими за тих, що померли від інших причин (70±9 проти 75±9 років). Серед них було більше чоловіків (68 проти 54% відповідно), вони мали вищий індекс маси тіла (35±9 проти 32±9 кг/м2 відповідно), а також частіше мали ЦД (58 проти 45% відповідно); p≤0,05 для всіх порівнянь. ФВ ЛШ була зіставною в пацієнтів, які померли від РС або перенесли зупинку серця, та в тих, що померли від інших причин: 56±8 та 57±8% відповідно; p=0,20. За часткою перенесених ІМ (29 проти 24% відповідно) та наявністю ішемічної хвороби серця (ІХС) (57 проти 49% відповідно) ці підгрупи також не мали статистично значущих відмінностей (p>0,05 для обох порівнянь).
Чоловіча стать і діабет, лікований інсуліном, були визначені як незалежні предиктори комбінованої кінцевої точки «РС / реанімована зупинка серця» з помірною дискримінацією (C-statistic 0,65). Інші коваріати, включно з віком, ФВ ЛШ, ІХС, блокадою лівої ніжки пучка Гіса та вихідною терапією, не асоціювалися з РС / зупинкою серця. Стать і ЦД залишилися незалежними предикторами РС / реанімованої зупинки серця після проведення аналізу чутливості результату з виключенням пацієнтів з ІКД, а також залишилися предикторами в окремому аналізі лише для РС. Хоча в дослідженні TOPCAT спіронолактон зменшував частоту клінічних подій, включно з серцево-судинною смертю, за даними цього аналізу, спіронолактон не зменшував ризик РС / зупинки серця порівняно з плацебо.
Автори дійшли висновку, що на РС припадає близько 20% у структурі смертності пацієнтів із СН зі збереженою ФВ. Пацієнти чоловічої статі та з ЦД, який лікують інсуліном, мають підвищений ризик РС або зупинки серця. Хоча загальна кількість подій була невеликою, цей аналіз вказує на значний тягар РС для популяції. Пошук інших предикторів РС допоможе краще зрозуміти природний перебіг СН зі збереженою ФВ, тому при плануванні нових клінічних досліджень треба розглядати РС як важливу кінцеву точку.
Підготував Дмитро Молчанов
Журнал "Серцева недостатність та коморбідні стани" № 1, квітень 2018 р.



