23 грудня, 2020
Порушення енергетичного обміну міокарда і мозку як спільна терапевтична мішень у пацієнтів похилого віку
Основою майже будь-якого патологічного процесу є порушення енергетичного обміну в клітині, не виняток і серцево-судинні захворювання (ССЗ). Серцева недостатність (СН) – складна патологія, для якої характерні численні системні ураження, зокрема ЦНС, адже зменшення серцевого викиду призводить до порушення перфузії головного мозку та когнітивної дисфункції. Іншими словами, чим тяжчий перебіг СН, тим глибше ушкодження функції мозку. Про модуляцію енергетичного обміну міокарда як мету лікування СН та можливості екзогенного креатинфосфату розповідає Юрій Степанович Рудик, д. мед. н., завідувач відділу клінічної фармакології та фармакогенетики неінфекційних захворювань ДУ «Національний інститут терапії iменi Л.Т. Малої» НАМН України (м. Харків).
Серце в умовах СН є своєрідним «мотором без палива». Задля розуміння цього патологічного процесу варто розібратися з механізмами енергоутворення у кардіоміоциті. На першому етапі відбуваються посилена утилізація невуглеводних субстратів та транспортування їх у мітохондрії. На другому – синтез аденозинтрифосфорної кислоти (АТФ), далі енергія переноситься у місця використання, і наприкінці АТФ перетворюється на механічну енергію.
Цікаво, що при СН часто спостерігається підвищений синтез енергії, але при цьому вона не досягає місця локального використання. У кардіоміоциті 70‑80% синтезованого АТФ йде на акт скорочення, 10‑15% – перенесення Са2+ в саркоплазматичному ретикулумі та мітохондріях для релаксації, 5‑10% – процеси активного транспорту Na+ проти градієнта концентрації через саркоплазму, а залишок – на забезпечення потреб біосинтетичних процесів, що підтримують цілісність структури клітини.
Так званий човниковий механізм транспортування енергії у кардіоміоциті полягає в тому, що молекула АТФ передає свою енергію креатину, який під дією ізоферменту креатинфосфокінази трансформується в фосфокреатин (ФКр), що мігрує до місць локальних креатинкіназних реакцій, де інші ферменти забезпечують ресинтез АТФ із ФКр та аденозиндифосфату (реакція Ломана). Креатин, що при цьому вивільняється, повертається до мітохондрії, а енергія АТФ застосовується, наприклад, для м’язового скорочення.
Таким чином, фізіологічна роль ФКр полягає в ефективному забезпеченні внутрішньоклітинного транспорту енергії від місць її утворення до використання.
У клітині майже ніколи не відбувається різкого падіння рівня АТФ. Він залишається практично незмінним як за ішемії, зокрема, з навантаженням. Однак при цьому патологічному стані значно знижується рівень ФКр, що є головним джерелом клітинної енергії (De Feyter et al., 2000).
У контексті фармакокінетики екзогенного ФКр (препарат Неотон) варто зазначити, що найефективнішим є внутрішньовенне (в/в) введення лікарського засобу, адже при пероральному прийманні сполука нестійка та одразу розпадається. Приблизно через хвилину спостерігається максимальна концентрація препарату, а через годину – збільшення АТФ у еритроцитах. Чому ж акцентують увагу саме на них? Бо вони є віддзеркаленням того, що відбувається у клітинах інших тканин. Швидкість поглинання ФКр еритроцитами є відносно низькою, але її цілком достатньо для збереження субсарколемних пулів ФКр та АТФ (Zou et al., 2011).
Так, використання екзогенного ФКр у комплексній терапії гострого інфаркту міокарда (ГІМ) супроводжується поліпшенням клінічного перебігу захворювання. Раннє призначення кардіопротектора Неотону в пацієнтів із ГІМ приводить до зменшення маси некротизованого міокарда (на 32,9%). Застосування ФКр при ГІМ попереджає розвиток ранньої систолічної та діастолічної дилатації порожнини лівого шлуночка в динаміці спостереження, сприяє поліпшенню загальної та сегментарної скоротливості міокарда – збільшенню фракції викиду (ФВ) на 12,8%. Також відбувається зменшення екстрасистоли високих градацій (ІІІ і ІV класу) в перші дні захворювання (66,7 vs 86,3% у групі контролю) (Пархоменко та співавт., 2014). Крім того, застосування Неотону сприяє зниженню частоти аритмій, що загрожують життю (Landoni et al., 2016).
Серед інших ефектів Неотону необхідно виділити його позитивний вплив на скоротливу функцію міокарда (Ferraro et al., 1990). Він розвивається протягом години та супроводжується зменшенням об’ємних структур серця і покращенням його насосної функції (Яворовський, 2015).
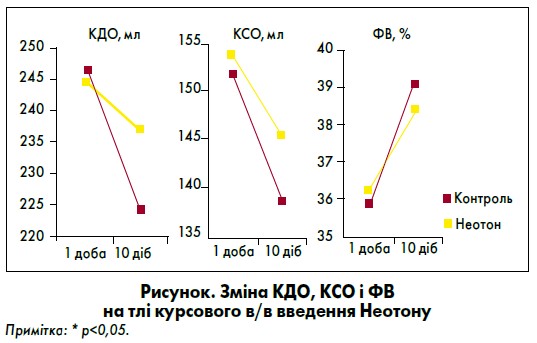 Показовими є результати дослідження щодо зміни кінцевого діастолічного об’єму (КДО), кінцевого систолічного об’єму (КСО) та ФВ на тлі лікування Неотоном. При лікуванні Неотоном у дозі 3 г/добу протягом 10 днів було виявлено, що розмір камер серця зменшився, а насосна функція покращилася, про що свідчило суттєве збільшення ФВ (рисунок) (Недошивін, Перепеч, 1996).
Показовими є результати дослідження щодо зміни кінцевого діастолічного об’єму (КДО), кінцевого систолічного об’єму (КСО) та ФВ на тлі лікування Неотоном. При лікуванні Неотоном у дозі 3 г/добу протягом 10 днів було виявлено, що розмір камер серця зменшився, а насосна функція покращилася, про що свідчило суттєве збільшення ФВ (рисунок) (Недошивін, Перепеч, 1996).
Не менш цікавим є багатоцентрове контрольоване дослідження застосування ФКр, в якому взяли участь більш як 1 тис. осіб із хронічною СН І‑ІV функціонального класу за критеріями Нью-Йоркської асоціації серця (NYHA). Серед хворих 499 отримували традиційну терапію, а 508 – додатково Неотон. Спостереження тривало 45 діб, два тижні хворим вводили по 1 г ФКр в/в крапельно два рази на добу, потім упродовж місяця доза становила 500 мг/добу внутрішньом’язово. За отриманими даними, кількість пацієнтів із високими функціональними класами хронічної СН значно зменшилася порівняно з контрольною групою, що отримувала стандартне лікування (Grazioli et al., 1992).
Підсумовуючи, Юрій Степанович зазначив, що ФКр стабілізує сарколему завдяки трьом механізмам. Насамперед це його електростатична взаємодія з полярними голівками фосфоліпідів сарколеми, що забезпечує перехід клітинної мембрани з рідкого в гелеподібний стан і, як наслідок, попереджає руйнацію мембранних фосфоліпідів, гальмує накопичення лізофосфогліцеридів та інгібує ліпідну пероксидацію. Дія ФКр на реакції сарколемної 5-нуклеотидази пригнічує розпад аденінових нуклеотидів до аденозину та неорганічного фосфату, забезпечуючи таким чином збереження клітинних запасів високоенергетичних фосфатів.
Підготувала Ольга Маковецька
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 5 (72) 2020 р.



