2 лютого, 2021
COVID-19 і психоемоційні розлади: роль нейротрансмітерів, можливості профілактики та лікування
 Одночасно з поширенням пандемії коронавірусної хвороби (COVID‑19) зростає кількість осіб, які відчули на собі тягар довготривалих наслідків для здоров’я після одужання. Не всі реконвалесценти з негативним тестом на SARS-CoV‑2 повністю позбулися симптомів. У багатьох відзначаються залишкові явища, зокрема виснаження, біль у кістках і суглобах, серцебиття, головний біль, запаморочення та безсоння. Страх перед ускладненнями хвороби, вимушена соціальна ізоляція й невпевненість у майбутньому роблять свій внесок, спричиняючи тривожні та стресові розлади. Крім психосоціального стресу, пов’язаного з пандемією, науковці вивчають прямі ефекти вірусу SARS-CoV‑2 на центральну нервову систему (ЦНС) [1, 2].
Одночасно з поширенням пандемії коронавірусної хвороби (COVID‑19) зростає кількість осіб, які відчули на собі тягар довготривалих наслідків для здоров’я після одужання. Не всі реконвалесценти з негативним тестом на SARS-CoV‑2 повністю позбулися симптомів. У багатьох відзначаються залишкові явища, зокрема виснаження, біль у кістках і суглобах, серцебиття, головний біль, запаморочення та безсоння. Страх перед ускладненнями хвороби, вимушена соціальна ізоляція й невпевненість у майбутньому роблять свій внесок, спричиняючи тривожні та стресові розлади. Крім психосоціального стресу, пов’язаного з пандемією, науковці вивчають прямі ефекти вірусу SARS-CoV‑2 на центральну нервову систему (ЦНС) [1, 2].
Досить поширеним наслідком COVID‑19 є зниження когнітивних функцій, що відзначають навіть ті, хто переніс інфекцію в легкій формі. Британські науковці [3] проаналізували результати когнітивних тестів 84 285 учасників програми Great British Intelligence Test, які мали підозрювану чи підтверджену COVID‑19. Серед людей, які одужали, включно з тими, хто більше не відзначав симптомів захворювання, тестування виявило суттєвий дефіцит у когнітивній сфері, котрий залишався значущим після поправки на вік, стать, рівень освіти, доходу, расово-етнічну приналежність і фонові проблеми зі здоров’ям.
Фактори ризику тяжкого перебігу COVID‑19 включають похилий вік, гіпертензію, цукровий діабет, надмірну масу тіла, куріння. Разом із тим зазначені чинники є факторами ризику цереброваскулярних захворювань і когнітивних порушень. Отже, особи з високим ризиком несприятливого перебігу COVID‑19 водночас схильні до уражень ЦНС, тому потребують особливої уваги [1].
Інфекція нещадна й до тих, хто надає медичну допомогу, ризикуючи власним життям і здоров’ям. У ранню фазу епідемії в Китаї було проведене анкетування медичних працівників для вивчення гострих психологічних наслідків коронавірусної інфекції [4]. Депресія, тривога та посттравматичний стресовий розлад були виявлені з частотою 15,0; 27,1 та 9,8% відповідно. Серед чинників тривоги й депресії медики зазначали роботу безпосередньо з інфікованими хворими та невпевненість в ефективності засобів захисту.
У період із 18 березня по 18 квітня 2020 року, в ранню фазу поширення інфекції та росту смертності, в Сполучених Штатах Америки досліджували гострий стрес і симптоми депресії в репрезентативній національній вибірці (загалом 6514 респондентів) [5]. Встановлено, що рівні стресу та депресії серед населення корелювали з частотою повідомлень засобів масової інформації про кількість померлих від COVID‑19, а також посилювалися розбіжностями даних із різних джерел.
Поряд із панічними настроями розвиток психоемоційних і когнітивних порушень при COVID‑19, імовірно, спричинений прямим впливом вірусу на функціонування нейронів, метаболізм нейротрансмітерів, а також опосередкованим ураженням нервової тканини внаслідок системного запалення, тромбоутворення й ішемії [6] (рис.).
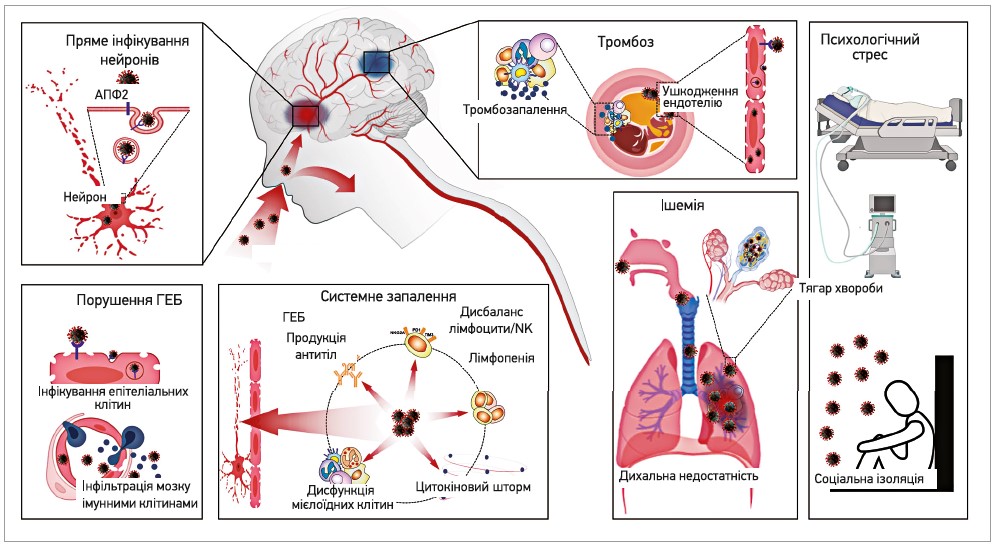 Рис. Вплив інфекції SARS-CoV‑2 на нервові клітини (Verkhratsky A. et al., 2020)
Рис. Вплив інфекції SARS-CoV‑2 на нервові клітини (Verkhratsky A. et al., 2020)
Примітки: ГЕБ – гематоенцефалічний бар’єр; NK – натуральні кілери.
Один із механізмів когнітивних і психоемоційних порушень при COVID‑19 пов’язують із дисфункцією шлунково-кишкового тракту. Біль у животі, діарея, втрата апетиту є частими клінічними проявами інфекції, що можуть спричиняти порушення засвоєння прекурсорів нейротрансмітерів [7, 8]. За моноаміновою теорією, знижені рівні дофаміну, норадреналіну та серотоніну є найважливішим чинником розвитку депресії. Амінокислотні нутрієнти – глутамін, глутамат, триптофан і тирозин – є попередниками синтезу нейротрансмітерів, зокрема гамма-аміномасляної кислоти (ГАМК), норадреналіну, адреналіну, дофаміну, серотоніну та мелатоніну. Різке припинення надходження цих амінокислот супроводжується падінням рівня відповідних нейротрансмітерів, що пов’язано з появою психіатричних симптомів у пацієнтів із COVID‑19 [9].
Цікаво, що стрес від соціальної ізоляції також супроводжується зниженням рівнів нейротрансмітерів і чутливості рецепторів у різних ділянках ЦНС. Попередні дослідження показали, що ізоляція людини на понад 10 днів призводить до пригнічення вивільнення дофаміну, серотоніну, адреналіну, ГАМК і глутамату [11]. Отже, як і сам перебіг захворювання, спричиненого вірусом SARS-CoV-2, так і пов’язана з пандемією COVID-19 необхідність у тривалій самоізоляції здатні спричинити значні розлади в роботі нейромедіаторних систем. Що можна запропонувати для корекції цих порушень? Раніше терапія амінокислотними прекурсорами виявилася досить ефективною при лікуванні деяких видів болю та психосоматичних розладів [9, 12]. Нещодавно Rozga та співавт. [13] проаналізували доказову базу нутритивної терапії при лікуванні пацієнтів із COVID‑19 і дійшли висновку, що призначення деяких амінокислот може полегшувати наслідки інфекції.
Перспективним вважається також застосування ГАМК, яка є основним гальмівним нейротрансмітером у корі головного мозку людини. ГАМК широко використовується як безрецептурний заспокійливий засіб у формі харчових добавок, але серед науковців тривають дискусії щодо її біодоступності й ефективності [14]. За даними одних досліджень, ГАМК проникає крізь гематоенцефалічний бар’єр (ГЕБ), натомість інші експерименти спростовують цей факт. Невизначеність зумовлена й тим, що фармакокінетику ГАМК вивчали переважно на гризунах, а метаболізм нейротрансмітерів у тварин і людини може суттєво відрізнятися. Цікаво, що на початку століття в ГЕБ був відкритий специфічний транспортер ГАМК. Експресія цього білка вказує на те, що ГАМК може надходити в мозок і виводитися з нього шляхом активного транспортування крізь ГЕБ. Але, за даними інших авторів, у мишей ефлюкс ГАМК у 17 разів вищий за вхідний потік. Це ускладнює визначення концентрації ГАМК у мозку та, можливо, призводить до заниженої оцінки здатності ГАМК проникати крізь ГЕБ.
Отже, наявна доказова база, отримана переважно в дослідах на тваринах, не дає підстав рекомендувати застосування натуральної ГАМК із метою отримання клінічно значущих ефектів на психоемоційний стан людини. Натомість анксіолітичний ефект можна отримати від застосування вдосконаленої молекули ГАМК, відомої як фенібут.
Фенібут: вплив на нейротрансмітери та клінічні ефекти
Фенібут (β-феніл-гамма-аміномасляна кислота) є похідним ГАМК і фенілетиламіну. Фенільне кільце в молекулі покращує її проникність крізь ГЕБ. Сполука була синтезована, вивчена та впроваджена в клінічну практику в 60-х роках минулого століття науковцями відділу органічної хімії Університету ім. Герцена в Санкт-Петербурзі (РФ). Механізми впливу на психоемоційну сферу пов’язані здебільшого з ГАМК-міметичним ефектом. Фенібут має переважну спорідненість до ГАМК-рецепторів типу В та певною мірою до рецепторів типу А. Крім того, фенібут стимулює дофамінові рецептори та є антагоністом β-фенетиламіну (РЕА) – потужного ендогенного медіатора тривоги [15]. Пізніше була виявлена спорідненість фенібуту до α2δ-субодиниці потенціалозалежних кальцієвих каналів, що забезпечує антиноцицептивний і нейропротекторний ефекти препарату [16].
Як було встановлено в численних експериментах на тваринах і клінічних дослідженнях, фенібут чинить анксіолітичну та ноотропну дії (підсилює когнітивні функції). Плацебо-контрольовані дослідження з подвійним засліпленням проводилися за участю пацієнтів із невротичними та психотичними розладами. Фенібут призначали в дозах від 0,25 до 0,5 г тричі на день упродовж 1-2 тиж. Терапія сприяла активації інтелектуальних здібностей, підвищувала фізичну витривалість, мотивацію, зменшувала прояви астенії [15, 16].
Найбільший обсяг інформації стосується клінічного використання фенібуту при неврозах, психічних розладах, які характеризуються тривогою. Зокрема, при лікуванні геріатричних пацієнтів фенібут перевершив транквілізатори та нейролептики. Подібно до баклофену, фенібут зменшує спастичність, успішно застосовується в лікуванні посттравматичного стресового розладу, «астенічно-депресивного» синдрому, логоспазму та вестибулярних розладів [15].
Важливою властивістю фенібуту є його висока безпека, про що свідчать дані нещодавнього систематичного огляду латвійських науковців (11 клінічних досліджень за участю 583 пацієнтів).
У клінічних дослідженнях фенібуту частота всіх побічних ефектів становила лише 5,66%, із них найчастішим була сонливість (1,89%). Автори дійшли висновку, що в терапевтичних дозах 0,25-2 г/день фенібут безпечний і добре переноситься [16].
Висновки
- Когнітивні та психоемоційні порушення при COVID‑19 спричинені як прямим впливом вірусу на функціонування нейронів і метаболізм нейротрансмітерів, так і соціальними наслідками пандемії, зокрема соціальною ізоляцією, панікою та невпевненістю в майбутньому.
- Особливої уваги потребують люди похилого віку із супутніми серцево-судинними захворюваннями та факторами ризику, котрі одночасно підвищують схильність до тяжкого перебігу COVID‑19 і до розвитку когнітивних/психічних розладів.
- Заходи, спрямовані на нормалізацію функціонального стану нейромедіаторних систем, є ефективним методом корекції психоемоційних розладів різного генезу.
- Фенібут як удосконалене та безпечне джерело ГАМК чинить анксіолітичну й ноотропну дії, при своєчасному профілактичному застосуванні допомагає зберегти когнітивне здоров’я та запобігти довгостроковим ускладненням.
Список літератури знаходиться в редакції.
UA-BIFR-PUB-012021-029
Медична газета «Здоров’я України 21 сторіччя» № 1 (494), 2021 р.



