9 березня, 2021
Німесулід при гострих респіраторних захворюваннях: безпека й ефективність
 Гострі респіраторні захворювання (ГРЗ) є одними з найпоширеніших патологічних станів у світі. Втім, незважаючи на значну розповсюдженість, постає багато запитань під час їх лікування, крім того, з’являється чимало помилок, які насамперед пов’язані з невиправданим призначенням антибактеріальних препаратів. Оскільки переважна більшість ГРЗ мають вірусну природу (ГРВІ), вони не потребують проведення антибактеріальної терапії. Це положення виправдане в разі як патології верхніх відділів респіраторного тракту, так і гострих бронхітів. За допомогою численних досліджень доведено, що призначення системних антибіотиків при ГРВІ не спричиняє зменшення тривалості захворювання й частоти ускладнень. З огляду на те, що можливості патогенетичної терапії ГРВІ обмежені, терапевтичні зусилля варто спрямувати на полегшення симптомів і проявів надмірної запальної реакції. Препаратами вибору в такому разі є нестероїдні протизапальні препарати (НПЗП), але лікарі часто ігнорують їх призначення, побоюючись небажаних побічних явищ і можливого ослаблення імунної відповіді. Щоби спростувати це припущення, слід розглянути патогенез запалення, спричиненого респіраторними патогенами, та звернутися до результатів клінічних досліджень.
Гострі респіраторні захворювання (ГРЗ) є одними з найпоширеніших патологічних станів у світі. Втім, незважаючи на значну розповсюдженість, постає багато запитань під час їх лікування, крім того, з’являється чимало помилок, які насамперед пов’язані з невиправданим призначенням антибактеріальних препаратів. Оскільки переважна більшість ГРЗ мають вірусну природу (ГРВІ), вони не потребують проведення антибактеріальної терапії. Це положення виправдане в разі як патології верхніх відділів респіраторного тракту, так і гострих бронхітів. За допомогою численних досліджень доведено, що призначення системних антибіотиків при ГРВІ не спричиняє зменшення тривалості захворювання й частоти ускладнень. З огляду на те, що можливості патогенетичної терапії ГРВІ обмежені, терапевтичні зусилля варто спрямувати на полегшення симптомів і проявів надмірної запальної реакції. Препаратами вибору в такому разі є нестероїдні протизапальні препарати (НПЗП), але лікарі часто ігнорують їх призначення, побоюючись небажаних побічних явищ і можливого ослаблення імунної відповіді. Щоби спростувати це припущення, слід розглянути патогенез запалення, спричиненого респіраторними патогенами, та звернутися до результатів клінічних досліджень.
Патогенез запалення при ГРВІ
На початкових етапах розвитку ГРВІ в результаті безпосередньої інвазії вірусу в епітеліоцити слизової оболонки дихальних шляхів або короткочасної вірусемії запускаються неспецифічні механізми захисту у вигляді продукції прозапальних цитокінів, простагландинів і гістаміну. Ці речовини активують запальний процес, який проявляється лихоманкою, зниженням апетиту, нездужанням, ознобом, головним і м’язовим болем тощо (Eccles R., 2005).
Запалення являє собою еволюційно створену захисну реакцію, спрямовану на локалізацію та подальшу ліквідацію збудника. Проте надлишок запальних компонентів може зумовлювати виражене погіршення стану пацієнта, збільшення тривалості захворювання, а іноді – значні порушення функції дихальної системи й інших органів.
Варто враховувати, що запалення характеризується стадійним перебігом, у якому послідовно змінюють одна одну альтерація, ексудація та проліферація.
На стадії альтерації відбувається ушкодження клітин і тканин із виходом лізосом і лізосомальних ферментів у позаклітинний простір. Активні ферменти та вільні радикали продовжують ушкоджувати навкружні тканини (вторинна альтерація). Тривалість цієї стадії становить приблизно 1-2 дні. На стадії ексудації спостерігається вихід рідкої частини крові, електролітів, білків і клітин через судинну стінку в запалену тканину, що провокує появу набряку. Через 4-5 днів спостерігається стадія проліферації (стимуляція синтетичної функції фібробластів, що забезпечує відновлення структури тканини).
Призначення НПЗП є ефективним на стадіях альтерації й ексудації, тобто в перші 4-5 днів від початку появи запальних симптомів. Епізодичний прийом системних НПЗП не забезпечує адекватного знеболювального та протизапального ефекту.
НПЗП мають також низку додаткових ефектів, які посилюють їхні протизапальні й аналгетичні властивості в пацієнтів із ГРЗ:
- антигіалуронідазна активність (сприяє зменшенню проникності судин і клітинних мембран у вогнищі запалення – протинабряковий ефект);
- зниження рівня вільних радикалів, що ушкоджують клітинні мембрани в місці запалення, перешкоджає його поширенню;
- інгібування утворення аденозинтрифосфату у вогнищі запалення, що сприяє зменшенню енергозабезпечення запальної реакції;
- зменшення набряку забезпечує зниження тиску на барорецептори та додатково сприяє ослабленню больових відчуттів (Burian M., Geisslinger G., 2005).
Якому НПЗП віддати перевагу?
Під час обрання лікарського засобу ми завжди розглядаємо його крізь призму ефективності та безпеки. Серед великої кількості НПЗП вигідним співвідношенням зазначених показників характеризується німесулід; його терапевтичний ефект як представника класу НПЗП зумовлений впливом на метаболізм арахідонової кислоти та синтез простагландинів шляхом пригнічення циклооксигенази (ЦОГ).
Слід зазначити, що німесулід чинить переважну інгібувальну дію на ЦОГ‑2, тому меншою мірою впливає на синтез простагландинів, які забезпечують цитопротекторний вплив на клітини слизової оболонки шлунка та кишечнику. У терапевтичних концентраціях німесулід пригнічує 88% активності ЦОГ‑2 і 45% активності ЦОГ‑1. Така збалансована дія препарату на ізоформи ЦОГ пояснює нижчий ризик ускладнень із боку шлунково-кишкового тракту порівняно з традиційними НПЗП за відсутності вираженої кардіоваскулярної токсичності, що характерна для коксибів.
Окрім того, німесулід знижує синтез прозапальних цитокінів (TNF, інтерлейкіну-6 – IL‑6), які стимулюють секрецію білків гострої фази запалення й активність прозапальних клітин, зокрема макрофагів і нейтрофілів; здатен пригнічувати виділення гістаміну, що забезпечує протинабряковий ефект.
Згідно з даними W. Wober, переносимість німесуліду є кращою порівняно з такою диклофенаку (препарат, який розглядають як загальновизнаний еталон при вивченні терапевтичного потенціалу та безпеки НПЗП) за однакової ефективності.
За даними J. R. Laporte та співавт., показники гастроінтестинальної безпеки німесуліду виявилися зіставними з такими ібупрофену та значно кращими порівняно з піроксикамом, кетопрофеном і кеторолаком.
Доказова база ефективності німесуліду при ГРЗ
Сьогодні існує досить багато доказів ефективності німесуліду в лікуванні ГРЗ. У подвійному сліпому 4-денному дослідженні в паралельних групах за участю пацієнтів із гострим запаленням верхніх дихальних шляхів (n=51) протизапальну, антиексудативну та жарознижувальну дії німесуліду порівнювали з плацебо. У пацієнтів, які отримували німесулід, спостерігалося полегшення таких проявів і симптомів ГРЗ, як почервоніння глотки, почервоніння та набряк мигдалин, осиплість голосу, біль у горлі, головний біль й артралгія. Різниця між німесулідом і плацебо була очевидною та статистично значущою для всіх зазначених симптомів. У групі німесуліду 92% (22 із 24 пацієнтів) оцінили користь від призначеного лікування, тоді як у групі плацебо лише 16% (4 із 25 пацієнтів) визнали лікування корисним (р<0,01). Побічних ефектів, пов’язаних із прийомом німесуліду, не відзначено (Nouri M. E. et al., 1984).
В іншому дослідженні порівняли жарознижувальну та протизапальну ефективність німесуліду й парацетамолу, котрі призначають як симптоматичне лікування ГРЗ у дітей. До випробування залучили 40 пацієнтів віком від 3 до 12 років із гострими інфекціями нижніх дихальних шляхів, які не потребували системної антибіотикотерапії в перші 3 дні спостереження. Учасників дослідження рандомізували на дві однорідні групи для прийому німесуліду по 1,5 мг/кг/добу 3 р/день або парацетамолу від 120 до 288 мг 3 р/день упродовж 3-7 діб. На початку та після завершення лікування проводили стандартні лабораторні дослідження, а також рентгенографію органів грудної клітки. Крім того, регулярно реєстрували показники температури тіла, артеріального тиску та частоти серцевих скорочень. Протизапальну ефективність обох препаратів оцінювали на основі нормалізації швидкості осідання еритроцитів, значень С-реактивного білка (СРБ) та кількості лейкоцитів. Водночас оцінювали загальну тривалість захворювання. Результати дослідження продемонстрували, що німесулід був ефективнішим за парацетамол щодо нормалізації температури тіла (р<0,05) та зменшення показників запалення (р<0,05). Пацієнти групи німесуліду потребували коротшого періоду лікування, ніж пацієнти групи парацетамолу (Gianiorio P. et al., 1993).
M. Reiner провів подвійне сліпе плацебо-контрольоване дослідження ефективності лікування серед 45 госпіталізованих дорослих пацієнтів із ГРЗ, яким була показана антибіотикотерапія. Пацієнтам, розподіленим на дві групи, паралельно з антибіотиком призначали німесулід по 100 мг 2 р/день або плацебо впродовж 15-23 днів. Результати дослідження довели, що в пацієнтів групи німесуліду спостерігалося значно швидше покращення таких проявів і симптомів захворювання, як біль у грудях, кашель, гіперемія ротоглотки, астенія, а також артралгія. Лікування в групі німесуліду переносилося добре.
Роль НПЗП у лікуванні COVID‑19
Важливим питанням є безпека та доцільність призначення НПЗП хворим на коронавірусну хворобу (COVID‑19). Європейське агентство з лікарських засобів (EMA) заявило: наразі немає наукових доказів того, що НПЗП можуть погіршити перебіг COVID‑19.
Як відомо, в розвитку та патогенезі тяжких форм COVID‑19 центральне значення має неконтрольована гіперпродукція цитокінів, яка дістала назву «цитокіновий шторм». Суть цієї реакції імунної системи полягає в неконтрольованій гіперпродукції широкого спектра прозапальних цитокінів: інтерлейкінів, TNF тощо, що зумовлює системну активацію клітин запальної відповіді (макрофагів, нейтрофілів, лімфоцитів). Отже, застосування НПЗП, які здатні пригнічувати розвиток надмірної запальної реакції при COVID‑19, є цілком обґрунтованим.
Німесулід має низку фармакологічних ефектів, які не залежать від клас-специфічного впливу на ЦОГ‑2 і можуть зменшувати цитокіновий шторм при COVID‑19. Зокрема, препарат пригнічує гіперпродукцію головних прозапальних цитокінів (IL‑6, TNF), знижує активність металопротеїназ, чинить антигістамінну дію. До не-ЦОГ‑2-асоційованих ефектів німесуліду також належить здатність пригнічувати фермент фосфодіестеразу‑4, завдяки чому знижувати активність макрофагів і нейтрофілів, які мають визначну роль у патогенезі гострої запальної реакції.
Всесвітня організація охорони здоров’я рекомендує призначення НПЗП пацієнтам із COVID‑19 як симптоматичну терапію (для досягнення жарознижувальної й аналгетичної дій), але не уточнює, яким препаратам цього класу варто віддавати перевагу.
Застосовувати НПЗП рекомендовано й в оновленому італійському протоколі з лікування COVID‑19 у домашніх умовах, згідно з положеннями котрого в пацієнта з підозрою на COVID‑19 за наявності міалгії, артралгії, головного болю або інших больових синдромів першою рекомендацією є призначення німесуліду (ще до отримання результатів тестування). Препарат слід застосовувати перорально дозою 100 мг 2 р/день після прийому їжі протягом 15 діб (не довше). Водночас наголошується, що німесулід має потужний антипіретичний ефект. Альтернативою є селективний інгібітор ЦОГ‑2 целекоксиб: початкова доза 400 мг із подальшим прийомом 200 мг у перший день; згодом – до 400 мг/день (200 мг 2 р/день) за потреби.
Якщо в пацієнта підвищується температура тіла (≥38,6 °C) чи з’являються лабораторні ознаки гепатотоксичності, німесулід необхідно замінити на ацетилсаліцилову кислоту дозою 500 мг перорально 2 р/день після їди.
Отже, німесулід можна широко використовувати в лікуванні ГРЗ, адже він допомагає полегшити симптоми захворювання, покращити самопочуття пацієнта, а в деяких випадках і прискорити одужання. Необхідно враховувати, що призначення цього препарату протипоказане при лихоманці, тяжких порушеннях функції печінки та нирок, виразковій хворобі, вагітності тощо.
Ефективність німесуліду демонструють і власні клінічні випадки.
Клінічні випадки ефективності німесуліду при ГРЗ
Клінічний випадок 1
Пацієнт А., віком 42 роки, звернувся по медичну допомогу у зв’язку з проявами ГРВІ, котрі з’явилися гостро та зберігаються протягом 2 днів. Чоловік скаржиться на головний біль, нежить, закладеність носа, втрату нюху та смаку, біль у горлі, незначну задишку, що спостерігається під час фізичного навантаження (підйом сходами на 4-й поверх), загальну слабкість. Утім, хворого найбільше турбують постійний головний біль, ломота в тілі, виражений біль у м’язах і суглобах, що супроводжується порушенням сну (сон поверхневий із частими пробудженнями). Можливий контакт з особами, хворими на COVID‑19, заперечує.
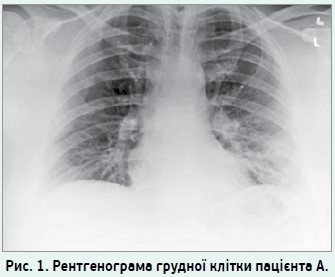 На момент звернення стан пацієнта був задовільним; скарги на задишку відсутні. Об’єктивно: насичення артеріальної крові киснем (SpO2) за даними пульсоксиметрії – 97%, частота серцевих скорочень – 78 уд./хв, температура тіла – 37,2 °C, над легенями прослуховується везикулярне дихання. На рентгенограмі грудної клітки відхилень не виявлено (рис. 1).
На момент звернення стан пацієнта був задовільним; скарги на задишку відсутні. Об’єктивно: насичення артеріальної крові киснем (SpO2) за даними пульсоксиметрії – 97%, частота серцевих скорочень – 78 уд./хв, температура тіла – 37,2 °C, над легенями прослуховується везикулярне дихання. На рентгенограмі грудної клітки відхилень не виявлено (рис. 1).
За даними лабораторних досліджень: концентрація СРБ – 44 мг/л, концентрація прокальцитоніну – 0,058 нг/мл, кількість лейкоцитів – 8,0×109/л. Результат імунохроматографічного тесту на грип А та В був негативним.
Проведено забір мазка з носоглотки та підтверджено інфекцію SARS-CoV‑2 за допомогою полімеразно-ланцюгової реакції (ПЛР).
З анамнезу відомо, що пацієнт не має захворювань печінки, нирок і патології з боку шлунково-кишкового тракту, алергологічні захворювання також заперечує.
Діагноз: підтверджена інфекція SARS-CoV‑2, легкий перебіг. У зв’язку з легким перебігом COVID‑19 і відсутністю дихальної недостатності вирішено проводити лікування амбулаторно в режимі самоізоляції. Крім того, пацієнт не належав до групи ризику тяжкого перебігу захворювання. Контроль стану проводили в телефонному режимі.
Лікування. За відсутності засобів специфічної терапії COVID‑19 не забороняється використання й інших лікарських препаратів, які можуть впливати на патогенетичні ланки розвитку захворювання та його ускладнень. Сьогодні значного поширення набув протокол лікування COVID‑19, розроблений під керівництвом голови відділення пульмонології та реаніматології Медичного інституту Східної Вірджинії Пола Маріка (Paul Marik), який містить положення з профілактики й лікування COVID‑19 та її ускладнень.
Відповідно до пункту «Лікування амбулаторних пацієнтів із гострою симптоматикою COVID‑19» пацієнту призначено:
- вітамін C – 500 мг 2 р/день;
- кверцетин – 250 мг 2 р/день;
- цинк – 75-100 мг/добу;
- мелатонін – 10 мг на ніч;
- вітамін D3 – 2000 ОД/добу.
Враховуючи гострі симптоми ГРВІ, що непокоять пацієнта (головний біль, виражені міалгія й артралгія, загальна слабкість), було вирішено призначити препарат німесуліду Найз дозою 100 мг 2 р/день перорально протягом 5 діб.
Пацієнт відзначав поліпшення загального самопочуття вже з першого дня лікування. Біль у м’язах і суглобах майже не відчувався, також значно зменшилася вираженість головного болю. Температура тіла зберігалася в межах 36,8-37 °C.
Спостерігалися респіраторні симптоми та загальна слабкість, але вони поступово зменшувалися. На 8-й день після звернення пацієнт почував себе здоровим, тому призначене лікування припинив; йому було рекомендовано продовжувати дотримуватися режиму самоізоляції ще протягом тижня.
Клінічний випадок 2
Пацієнт Б., віком 25 років, звернувся зі скаргами на сухий надсадний кашель, біль у грудній клітці, що посилюється під час кашлю та глибокого вдиху, головний біль, біль у горлі. Хворий відчуває задишку під час ходьби. Захворів гостро (на наступний день після короткочасного переохолодження).
Хронічних захворювань не має, алергологічний анамнез не обтяжений.
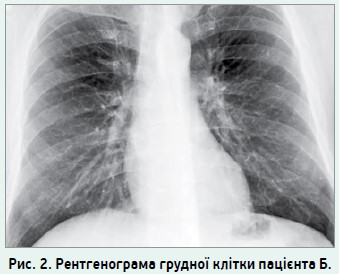 Об’єктивно: насичення артеріальної крові киснем (SpO2) за даними пульсоксиметрії – 98%, частота серцевих скорочень – 75 уд./хв, температура тіла – 37,1 °C. При аускультації легень прослуховуються сухі розсіяні хрипи. При рентгенологічному дослідженні грудної клітки відзначаються посилення легеневого малюнка та нечіткість коренів легень (рис. 2).
Об’єктивно: насичення артеріальної крові киснем (SpO2) за даними пульсоксиметрії – 98%, частота серцевих скорочень – 75 уд./хв, температура тіла – 37,1 °C. При аускультації легень прослуховуються сухі розсіяні хрипи. При рентгенологічному дослідженні грудної клітки відзначаються посилення легеневого малюнка та нечіткість коренів легень (рис. 2).
ПЛР-тест на SARS-CoV‑2 показав негативний результат.
Можливий діагноз пневмонії за даними рентгенографії й аускультації також було виключено. Встановлено діагноз: гострий бронхіт.
Лікування. Медикаментозне лікування гострого бронхіту має бути спрямоване на усунення симптомів ураження дихальних шляхів у максимально стислі терміни (полегшення тяжкості кашлю, зменшення його тривалості), зниження ступеня вираженості клінічних проявів інтоксикації. Стартова антибіотикотерапія в разі гострого бронхіту не показана.
Для пригнічення непродуктивного кашлю пацієнту призначено протикашльовий засіб центральної дії глауцин дозою 40 мг 2 р/день. Із метою купірування больових відчуттів призначено Найз дозою 100 мг 2 р/день перорально протягом 5 днів.
Водночас надано рекомендацію вживати достатню кількість рідини (до 2-2,5 л/добу), що сприяє розрідженню мокротиння та полегшує його відходження.
На 4-й день захворювання кашель став вологим із виділенням мокротиння білуватого забарвлення, у зв’язку з чим протикашльовий засіб було замінено на муколітик ердостеїн 300 мг 2 р/добу перорально. На 10-й день лікування пацієнт почувався добре. Кашель усе ще спостерігався (нечастий, майже не турбував). Температура тіла – в межах норми.
Клінічний випадок 3
Пацієнтка, віком 32 роки, звернулася зі скаргами на біль у ділянці проєкції лівої гайморової пазухи, стікання слизу задньою стінкою глотки, слизові виділення з носа, закладеність носа. Зі слів хворої, такі симптоми з’явилися на 4-й день перебігу ГРВІ, що супроводжувалася рясними виділеннями з носа та його закладеністю; для покращення дихання використовувала краплі ксилометазоліну. З анамнезу відомо, що хронічних захворювань пацієнтка не має; можливість вагітності заперечує.
Об’єктивно: температура тіла – 37,3 °C, слизова оболонка порожнини носа набрякла та гіперемована, наявні слизово-гнійні виділення. Відзначається біль при перкусії передньої стінки лівої гайморової пазухи. Було встановлено попередній діагноз гострого риносинуситу, ймовірно, вірусної етіології та призначено консультацію оториноларинголога. Після консультації діагноз було уточнено.
Діагноз: гострий бактеріальний риносинусит.
Пацієнтці було призначено:
- амоксицилін / клавуланова кислота 875/125 мг по 1 таблетці 2 р/день протягом 7 діб;
- краплі ксилометазоліну (інтраназально);
- назальну іригаційну терапію із застосуванням сольового розчину;
- Найз по 100 мг 2 р/день упродовж 5 діб.
На 2-й день після початку лікування пацієнтка відзначила покращення самопочуття та значне зменшення болю в проєкції гайморової пазухи. Під час контрольного огляду через 3 доби спостерігалося поліпшення загального самопочуття, біль у проєкції лівої гайморової пазухи не турбував. Носові виділення слизового характеру, температура тіла – 36,8 °C. Через 5 днів антибіотикотерапію було припинено.
Наведені клінічні приклади демонструють високу ефективність симптоматичного лікування проявів ГРВІ за допомогою препаратів німесуліду. Слід ураховувати, що не кожен НПЗП підходить для лікування зазначених захворювань. «Ідеальний» препарат має не лише характеризуватися високою протизапальною та знеболювальною активністю, а й мати оптимальний профіль переносимості та безпеки.
Медична газета «Здоров’я України 21 сторіччя» № 3 (496), 2021 р.



