15 березня, 2021
COVID‑19 та артеріальна гіпертензія: що відомо на початок 2021 року?
Серед усіх захворювань глобальний внесок артеріальної гіпертензії (АГ) у втрату років здорового життя є найбільшим. Ще на початку пандемії коронавірусної хвороби (COVID‑19) було отримано свідчення того, що пацієнти з АГ мають тяжчий перебіг коронавірусної інфекції, та висловлювалася думка, що цей зв’язок може бути зумовлений застосуванням деяких антигіпертензивних препаратів (АГП). Відтоді були виконані численні дослідження та метааналізи, котрі дали змогу краще зрозуміти роль АГ й АГП у пацієнтів із COVID‑19. У цьому огляді наведено останні докази, що відповідають на важливі запитання щодо ведення АГ у контексті COVID‑19.
Чи є АГ фактором ризику тяжчих наслідків коронавірусної інфекції?
Перші невеликі серії випадків не свідчили про надлишок АГ у пацієнтів із COVID‑19. У лютому 2020 року Епідеміологічна група з реагування на надзвичайну ситуацію з новою коронавірусною пневмонією опублікувала аналіз великої вибірки з Китаю; загальний коефіцієнт летальності (CFR) становив 2,3% (1023 із 44 672 підтверджених випадків) проти 6,0% у пацієнтів з АГ. Утім, цей аналіз провели без поправки на вік. Відомо, що CFR COVID‑19 і поширеність АГ збільшуються з віком, досягаючи 8,0% і понад 50% відповідно для вікової групи 70-79 років (Clark C. E. et al., 2021). У дослідженні OpenSAFELY, що охопило >17 млн мешканців Великої Британії, наявність АГ після поправки на вік й інші супутні фактори асоціювалася з підвищенням внутрішньогоспітальної смертності від COVID‑19 на 7% (Williamson E. та співавт., травень 2020). Надалі було проведено кілька систематичних оглядів і метааналізів, які надали такі результати:
- у госпіталізованих хворих на COVID‑19 АГ асоціюється з підвищенням смертності на 157% (р<0,001; без поправки на вік) (19 досліджень, 12 243 пацієнти; Whiteman E., травень 2020);
- після поправки на вік й інші супутні фактори АГ є незалежним фактором ризику тяжкого перебігу (відносний ризик (ВР) 1,82) та смерті від COVID‑19 (ВР 2,27) (24 дослідження, 99 918 пацієнтів; Du Y. та співавт., грудень 2020);
- АГ є більш значущим фактором ризику смерті від COVID‑19 у чоловіків й осіб віком >55 років (19 досліджень, 21 684 пацієнти; Ghosh P. K. і співавт., грудень 2020);
- після поправки на вік АГ не асоціюється з підвищеною внутрішньогоспітальною смертністю від COVID‑19 (ВР 1,0) (45 досліджень, 18 300 пацієнтів; Silverio A. та співавт., січень 2021).
Станом на початок 2021 року Центри з контролю та профілактики хвороб США (CDC) відносять АГ до факторів, які можуть підвищувати ризик тяжчого перебігу COVID‑19 (на відміну, приміром, від ішемічної хвороби серця, серцевої недостатності, цукрового діабету 2 типу й ожиріння з індексом маси тіла ≥40 кг/м2, які підвищують цей ризик). Натомість Всесвітня організація охорони здоров’я, Британська фундація серця та Виконавча служба охорони здоров’я Ірландії вважають АГ значущим фактором підвищеного ризику тяжкого перебігу COVID‑19 і відносять пацієнтів з АГ до категорії пріоритетної вакцинації від COVID‑19.
Чи здатні деякі АГП знижувати пов’язані з COVID‑19 ризики?
Вірус SARS-CoV‑2 використовує ангіотензинперетворювальний фермент-2 (АПФ‑2) як рецептор для потрапляння всередину клітини. Через це вважали, що блокатори ренін-ангіотензинової системи (РАС), а саме інгібітори АПФ і блокатори рецепторів ангіотензину ІІ (БРА), котрі підвищують експресію АПФ‑2, можуть сприяти інфікуванню SARS-CoV‑2 і погіршувати перебіг COVID‑19. Однак численні повідомлення, зокрема два великі ретроспективні дослідження (червень 2020 року), засвідчили, що пацієнти з АГ можуть безпечно продовжувати лікування цими препаратами без підвищеного ризику тяжкої COVID‑19 (Mancia G. et al., 2020; Reynolds H. et al., 2020).
На сьогодні велика кількість когортних досліджень і метааналізів підтвердила відсутність зв’язку між застосуванням інгібіторів РАС і тяжкістю COVID‑19, включно з опублікованим у вересні метааналізом 7 досліджень високої якості (n=164 064) (Chan C. K. et al., 2020). Однак більшість досліджень проводилася в госпіталізованих пацієнтів із позитивним тестом на COVID‑19, і багато з цих пацієнтів мали супутні захворювання, асоційовані з підвищеним ризиком COVID‑19, що могло спричинити певну упередженість висновків.
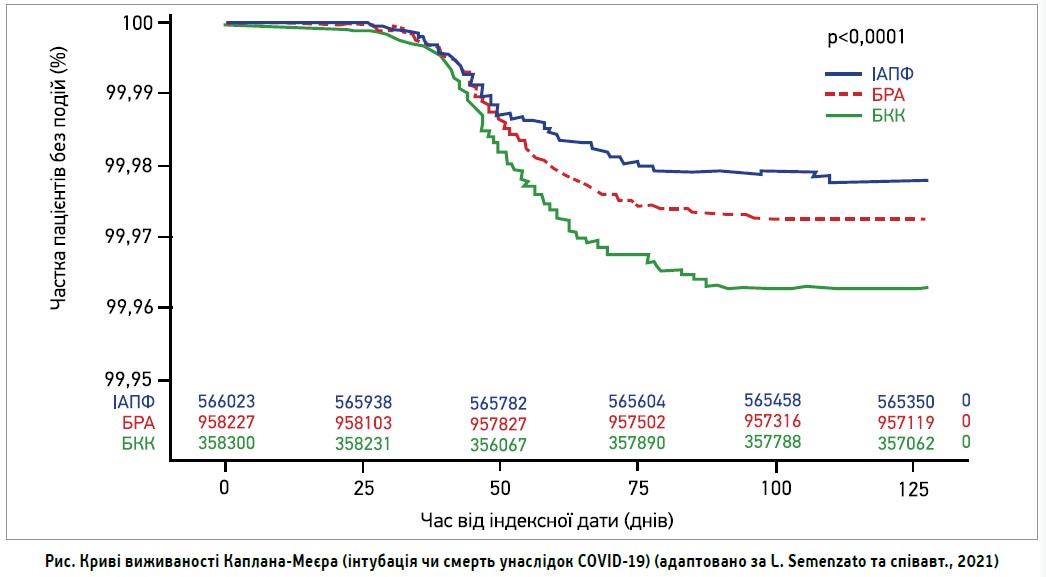
У січні 2021 року L. Semenzato та співавт. представили результати найбільшого когортного дослідження, котре охопило все доросле населення Франції (67 млн осіб), з яких 2 млн дорослих із неускладненою АГ розподілили на 3 взаємовиключні групи: тих, хто приймав ІАПФ, БРА чи блокатори кальцієвих каналів (БКК). При цьому з аналізу виключили пацієнтів із діабетом, кардіоваскулярними захворюваннями, хронічними хворобами нирок і легень, діагностованими в останні 5 років. Унікальність цього дослідження полягає в тому, що воно ґрунтується на порівнянні класів АГП в амбулаторних пацієнтів, які перебувають на довгостроковій антигіпертензивній терапії (тоді як у більшості інших робіт оцінювали зв’язок класів АГП із тяжкістю COVID‑19 у госпіталізованих хворих). Пацієнтів спостерігали протягом 16 тиж; кінцевими точками були час до госпіталізації та час до інтубації чи смерті. Результати показали: порівняно з БКК, терапія ІАПФ або БРА асоціювалася зі зниженням ризику госпіталізації через COVID‑19 на 26 і 16% відповідно, а також зі зниженням ризику інтубації чи смерті на 34 та 21% відповідно (рис.).
Як можна пояснити захисний ефект ІАПФ і БРА проти COVID‑19?
Наведене французьке дослідження спростовує гіпотезу про потенційно шкідливий вплив інгібіторів РАС і висуває нові гіпотези. Так, інгібітори РАС продемонстрували значну перевагу над «метаболічно нейтральними» БКК, водночас ІАПФ асоціювалися приблизно з у 1,5 раза нижчими ризикам госпіталізації/інтубації/смерті від COVID‑19 порівняно з БРА.
Імовірне пояснення захисного впливу ІАПФ/БРА може бути таким. Як уже згадувалося, вірус SARS-CoV‑2 використовує мембранний рецептор АПФ‑2 як «ворота» для потрапляння в клітини. АПФ‑2 є ключовим ферментом РАС, який забезпечує перетворення октапептиду Ang II (ангіотензину ІІ) на гептапептид Ang (1-7) – ангіотензин (1-7). Ang II шляхом дії на АТ1R (рецептори Ang II 1 типу) спричиняють низку потенційно шкідливих ефектів, як-от вазоконстрикція, затримка натрію, запалення, фіброз, окислювальний стрес, апоптоз і проліферація клітин. Натомість Ang (1-7) через рецептор mas (masR) протидіє сигнальному шляху Ang II – AT1R і забезпечує вазодилатацію, протизапальний, антифібротичний, антиапоптотичний та антипроліферативний ефекти.
Після того, як вірус зв’язується з позаклітинним доменом АПФ‑2, він разом з АПФ‑2 інтерналізується – потрапляє всередину клітини, при цьому активність АПФ‑2 знижується. У результаті посилюється дія Ang II на АТ1R із відповідними шкідливими ефектами, знижуються утворення Ang (1-7) й активність masR – корисного контррегуляторного рецептора РАС. Власне, саме втрату клітинами АПФ‑2 вважають головною рушійною силою системних проявів COVID‑19. В експериментальних дослідженнях було встановлено, що ІАПФ і БРА підвищують експресію АПФ‑2 у тканинах, а отже, можуть протидіяти системному прогресуванню COVID‑19. При цьому збільшення кількості АПФ‑2 не супроводжується підвищенням тяжкості COVID‑19 завдяки поєднанню пригнічення Ang II / AT1R й активації захисного сигнального шляху АПФ‑2 – Ang (1-7) – masR під впливом ІАПФ/БРА (Carey M. R., 2021).
Чому ІАПФ продемонстрували кращий результат порівняно з БРА?
Щодо істотної переваги ІАПФ над БРА, котру спостерігали французькі вчені, нещодавно отримано дані про теоретичну пряму дію ІАПФ проти SARS-CoV‑2. Для пошуку «нових старих» препаратів проти COVID‑19 дослідники з Італії використали мережевий алгоритм для «перепрофілювання» лікарських засобів SaveRUNNER (Searching off-lAbel dRUg aNd NEtwoRk), створений для передбачення асоціацій «препарат – хвороба» шляхом оцінки взаємодії між мішенями ліків і хворобоспецифічними білками в людському інтерактомі. Алгоритм виявив, що серед 282 препаратів і комбінацій, включно із застосованими офлейбл засобами для лікування COVID‑19 (хлорохіном, гідроксихлорохіном, тоцилізумабом, гепарином тощо), в топі анти-SARS-CoV‑2-препаратів були ІАПФ (поряд із моноклональними антитілами проти TNF, IFN-γ, IL‑12, IL‑1β, IL‑6 й інгібіторами тромбіну), а серед ІАПФ найбільший потенціал для «перепрофілювання» як анти-SARS-CoV‑2-препарат мав еналаприл (Fiscon G. і співавт., лютий 2021).
Загалом слід зазначити, що еналаприл на сьогодні є найкраще вивченим ІАПФ. Його клінічна ефективність і безпека при АГ і хронічній серцевій недостатності були продемонстровані у великих рандомізованих контрольованих дослідженнях (CONSENSUS I, CONSENSUS II, SOLVD, ABCD та ін.). В Україні широко застосовується Берліприл – еналаприл виробництва німецької фармацевтичної компанії «Берлін-Хемі». Для пацієнтів з АГ, які потребують інтенсивнішого контролю артеріального тиску, створено Берліприл Плюс – фіксована комбінація еналаприлу та гідрохлортіазиду. Берліприл і Берліприл Плюс доступні в різних дозуваннях, що дає змогу легко підібрати необхідну терапію для кожного пацієнта. Крім того, важливими перевагами цих препаратів є інноваційна система внутрішньої стабілізації, котра захищає активні речовини від гідролізу в шлунку й завдяки цьому забезпечує високу біодоступність.
Отже, на початок 2021 року більшість досліджень і метааналізів (але не всі) свідчать, що АГ є фактором ризику тяжчого перебігу COVID‑19. Теорія про потенційну небезпеку інгібіторів РАС спростована, натомість з’явилися переконливі докази про захисний ефект цих препаратів, насамперед ІАПФ й особливо еналаприлу. Як зазначила нещодавно Американська медична асоціація, АГ є найважливішим фактором ризику інфаркту міокарда й інсульту, котрий можна модифікувати, тому контроль артеріального тиску має залишатися пріоритетом в умовах пандемії, що триває.
Підготував Олексій Терещенко
Медична газета «Здоров’я України 21 сторіччя» № 3 (496), 2021 р.