28 вересня, 2021
Прогностична роль електролітних порушень у розвитку серцево-судинних захворювань та можливості їх корекції
 Натепер існують переконливі докази зв’язку вмісту деяких макроелементів, зокрема калію та магнію, із серцево-судинними захворюваннями. Про механізми електролітних порушень, їх прогностичне значення та важливість досягнення цільових рівнів розповідає старший науковий співробітник ННЦ «Інститут кардіології імені академіка М.Д. Стражеска» НАМН України, к. мед. н. Таісія Вячеславівна Гетьман.
Натепер існують переконливі докази зв’язку вмісту деяких макроелементів, зокрема калію та магнію, із серцево-судинними захворюваннями. Про механізми електролітних порушень, їх прогностичне значення та важливість досягнення цільових рівнів розповідає старший науковий співробітник ННЦ «Інститут кардіології імені академіка М.Д. Стражеска» НАМН України, к. мед. н. Таісія Вячеславівна Гетьман.
Поширені електролітні розлади
Загрозливими щодо виникнення аритмій є як гіпер-, так і гіпокаліємія. Рутинне застосування діуретиків та нейрогуморальна активація роблять гіпокаліємію (вміст калію <3,5 ммоль/л у сироватці крові) поширеним електролітним розладом серед пацієнтів із серцевою недостатністю (СН). Зокрема, при дефіциті калію блокуються натрій-калієві канали та відбувається накопичення натрію всередині клітин, що призводить до порушення обміну кальцію.
Останні експериментальні дослідження показали, що спричинені гіпокаліємією аритмії ініціюються через зниження активності Na+/K+-АТФази, що згодом спричиняє перевантаження Ca2+, активацію Ca2+/кальмодулін-залежної кінази II та деполяризацію. У кінцевому підсумку це зумовлює зростання ризику шлуночкових аритмій та раптової кардіальної смерті при СН (Scogestad, Aronsen, 2018).
В осіб із гіпокаліємією за принципом зворотного зв’язку подовжується рефрактерний період, що також здатні робити антиаритмічні препарати. Отже, відбувається подвійна стимуляція, наслідком якої є поява проаритмогенних ефектів (Weiss, 2017).
Тяжка гіпокаліємія може погіршити тенденцію та прогноз аритмії (Mattsson et al., 2016). Від цільових рівнів калію залежить кількість суправентрикулярних тахікардій та пароксизмів фібриляції передсердь (ФП). Те саме стосується шлуночкових групових порушень ритму: що нижчий вміст даної речовини, то більша ймовірність виникнення шлуночкових аритмій. У пацієнтів із тяжкою гіпокаліємією (рівень калію ≤3,1 ммоль/л) спостерігається підвищений ризик надшлуночкової аритмії та ектопії шлуночків (Mattsson et al., 2016; Bird et al., 2017).
У дослідженні, проведеному в Норвегії (n=1074), в 17,2% осіб із гіпокаліємією та 7,5% – із нормокаліємією виникли шлуночкові порушення ритму серця. При цьому найбезпечнішими були рівні калію від 4,1‑4,5 та 4,6‑5,1 ммоль/л, що вказувало на ризик розвитку шлуночкових порушень ритму 5,4 та 7,1% відповідно. Натомість при його концентрації >5,2 ммоль/л ризик становив 12,5%, а у разі ˂3,0 ммоль/л сягав 33,3% (Nordrehaug et al., 1983).
Встановлено, що пов’язаний із гіпокаліємією ризик асоційований із вищою імовірністю летальних випадків, тоді як нормалізація калію незалежно корелювала з нижчим ризиком смерті (Nunes et al., 2018). Зокрема, гіпокаліємія призводить до зростання смертності на 25‑36% та частоти госпіталізацій серед осіб із хронічною СН (Ahmed et al., 2007). Відповідно, пацієнти кардіологічного профілю мають уникати гіпокаліємії.
Ризик розвитку серцево-судинних подій також залежить від споживання магнію. Загалом, чим менше споживає людина магнію, тим вища ймовірність розвитку цукрового діабету (ЦД), інсульту та смерті від кардіоваскулярної патології (Fang et al., 2016).
Після інфаркту міокарда спостерігається значне зниження вмісту калію та магнію у тканинах серця (Speich et al., 1980). Встановлено, що жінки, курці й пацієнти із ЦД, гіпертонією або низьким рівнем загального холестерину частіше мають низький вміст сироваткового магнію. Зокрема, у США в кожної четвертої жінки рівень магнію становить <0,8 ммоль/л (Zhang et al., 2017).
На додаток, зростання ризику розвитку депресії у 2,6 раза через три місяці після інсульту асоційоване з рівнем магнію в плазмі крові <0,84 ммоль/л (Yingying et al., 2016).
Отже, ризики електролітних порушень також пов’язані з коморбідною патологією. Зокрема, наявність ЦД та артеріальної гіпертензії у 3,32 і 2,73 раза підвищує ймовірність гіпомагніємії та гіпокаліємії відповідно, тоді як застосування тіазидних діуретиків – як гіпомагніємії, так і гіпокаліємії (Liamis et al., 2013).
Цільові рівні калію та магнію
Так звана нормальна концентрація калію та магнію у плазмі крові становить 3,5‑5,5 і 0,66‑1,07 ммоль/л відповідно. Та чи завжди нормальний рівень є цільовим? Було проведене дослідження щодо вмісту калію у крові та виживаності осіб із хронічною СН (Hoss et al., 2016). За результатами, серед пацієнтів із рівнем даної речовини <3,5 та ≥6 ммоль/л значно зменшувалася виживаність, водночас при 4‑5,5 ммоль/л вона різко покращувалася протягом тривалого періоду часу.
Таким чином, цільовим рівнем калію або магнію є їх оптимальний вміст у плазмі крові. Тож досягнення плазмової концентрації цих мікроелементів >4,0 і >0,84 ммоль/л відповідно допомагає звести до мінімуму ризик інсульту, порушень серцевого ритму, зниження артеріального тиску (АТ), смерті тощо.
Гомеостаз калію
Добова кількість калію становить біля 2,5 г (<100 ммоль/л). Основне надходження мікроелемента в організм відбувається разом з їжею, а основним органом, що регулює його рівень, є нирки (Weir et al., 2015). У нормальному стані це відбувається за принципом зворотного зв’язку, але нирки регулюють вміст калію протягом декількох годин, тож важливим аспектом є також вплив інших органів. Відомо, що близько 90% калію мають позаклітинне зберігання (у м’язах, печінці, еритроцитах тощо), тоді як у клітинах міститься лише 2% від його загальної кількості.
Калій є природним сечогінним засобом, високий рівень якого знижує АТ шляхом вироблення альдостерону та регуляції натрій- і калійурезу (Burnier, 2018). Натомість при зниженні концентрації калію АТ підвищується.
Отже, у пацієнтів без високого ризику гіперкаліємії показане збільшення споживання калію для зниження АТ.
Фактори ризику гіперкаліємії
Перш ніж рекомендувати пацієнтові збільшити споживання калію, слід оцінити ризик розвитку гіперкаліємії та ретельно контролювати його вміст за потреби. Зокрема, до групи ризику належать:
- хворі, які приймають інгібітори ренін-ангіотензин-альдостеронової системи або інші препарати (триметоприм, сульфаметоксазол, амілорид, триамтерен);
- особи із хронічною хворобою нирок (ШКФ ˂45 мл/хв/1,73 м2);
- пацієнти, що мають базовий рівень калію в сироватці >4,5 ммоль/л.
Диференціальна діагностика гіперкаліємії ґрунтується на типах і причині дисбалансу калію (як-то хвороба Аддісона, β-адренергічна блокада, гіперглікемія, приймання інгібіторів ангіотензинперетворювального ферменту, β-блокаторів, низькомолекулярних гепаринів, дигіталісу тощо). Також до розвитку гіперкаліємії можуть призводити інші зовнішні фактори, що пов’язані з аритмією: дигіталісна інтоксикація, брадикардія, електролітний дисбаланс, зокрема натрію та кальцію (Udensi, Tchounwou, 2017).
Причини розвитку гіпокаліємії
Серед причин розвитку гіпокаліємії зустрічаються наступні:
- втрата калію через порушення у шлунково-кишковому тракті, як-то хронічна діарея, аденома товстої кишки тощо;
- внутрішньоклітинний зсув: введення інсуліну, тиреотоксикоз, сімейний періодичний параліч та ін.;
- ниркові втрати калію на тлі синдрому Іценка – Кушинга, вродженої гіперплазії надниркових залоз, первинного гіперальдостеронізму, гіпомагніємії тощо;
- фармакотерапія: тіазидні, петльові та осмотичні діуретики, проносні засоби, амфотерицин В, пеніцилін у високих дозах, теофілін тощо.
Електрокардіографічними ознаками гіпокаліємії є депресія сегмента ST, сплощення зубця Т чи його інверсія, подовження інтервалу QT, поява зубця U.
Дефіцит калію та магнію: фактори ризику й симптоми
Факторами ризику гіпокаліємії та гіпомагніємії є жіноча стать, застосування діуретиків, ЦД, зловживання алкоголем, інфаркт міокарда, порушення серцевого ритму, АГ, хронічна СН, «швидке»/нераціональне харчування (Schartum-Hansen et al., 2015).
Симптомами дефіциту калію можуть бути обмінні порушення в міокарді, зниження скоротливої функції міокарда, зміни серцевого ритму, м’язова слабкість, тремор, спазми, парестезії, згасання сухожильних рефлексів, ерозивний гастрит, виразкова хвороба, метеоризм, закреп, а також втома та зниження працездатності. Натомість дефіцит магнію проявляється симптомами нестачі калію, коливаннями АТ, підвищеною стомлюваністю, втратою апетиту, головним болем, порушеннями сну, труднощами із пробудженням, відчуттям недосипання, м’язовими посмикуваннями, тремором, судомами, парестезіями, субфебрилітетом, ознобом, нудотою, сухістю в роті, диспепсією, діареєю/закрепом, метеоризмом тощо (Баришнікова та співавт., 2019).
Корекція електролітних порушень
Вочевидь, електролітні порушення потребують корекції. При цьому відомо, що ймовірність розвитку інсульту зменшується на 13% за умов високого споживання лише магнію, та на 11% – лише калію. Своєю чергою споживання комбінації цих речовин у жінок сприяє зниженню на 28% частоти усіх видів інсульту, на 22% – ішемічного та на 20% – геморагічного (Adebamowo et al., 2015).
Чи можна скорегувати рівні даних мікроелементів завдяки їжі? Як відомо, у чоловіків високе споживання лише магнію із продуктами харчування сприяє зниженню ризику інсульту на 13%, а лише калію – на 11%, тоді як їх поєднання – на 21%. Натомість у разі приймання добавок магнію та калію імовірність інсульту зменшується на 26 та 34% відповідно. Отже, не зажди можна скорегувати рівні зазначених речовин при їх споживанні лише з іжею.
ФП досить часто виникає в ранній післяопераційний період та не пов’язана із кардіологічними втручаннями. Тож перед хірургічним втручанням важливо відкорегувати електролітний баланс, зокрема рівень магнію. Також у пацієнтів із ФП, особливо тих, які отримують соталол, рекомендований ретельний контроль інтервалу QT, вмісту калію в сироватці крові, кліренсу креатиніну та інших факторів ризику аритмії (ESC/EACTS, 2020).
Варто зауважити, що вміст електролітів впливає на когнітивні функції. Встановлено, що сіль магнію порівняно з сіллю натрію значно покращувала неврологічні параметри пацієнтів після інсульту. Передбачається, що невелику кількість добавок магнію та калію можна розглядати як недорогу допоміжну терапію для полегшення неврологічного відновлення у пацієнтів з інсультом навіть після виписки (Pan et al., 2017).
Перевагою препарату Панангін є комбінація калію та магнію в одній таблетці, оскільки у 61% випадків гіпокаліємія поєднується із гіпомагніємією (Crop et al., 2007). До того ж калій та магній у вигляді аспарагінату мають такі переваги (Manz, Susilo, 2002; Громова, 2006; Zhi et al., 2007):
- вища біодоступність порівняно з неорганічними сполуками: 35 vs 8% відповідно;
- сіль (аспарагінат) нейтралізує аміак до сечовини, знижуючи ступінь ураження міокарда при ішемії;
- низька токсичність (LD50 >400 мг/кг);
- разом калій, магній та аспарагінат-аніон сприяють захисту міокарда й запобігають розвитку аритмії.
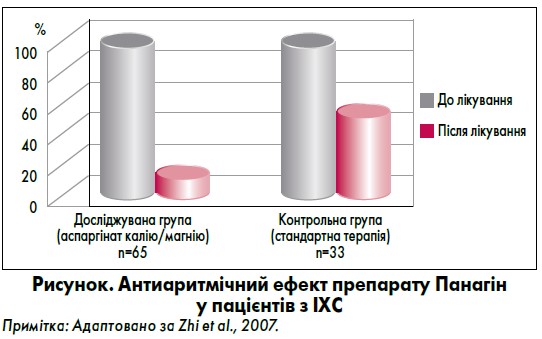 Використання аспарагінату калію та аспарагінату магнію (Панангіну) приводить до зменшення екстрасистолії у пацієнтів з ішемічною хворобою серця (ІХС) на 87% (рисунок) (Zhi et al., 2007).
Використання аспарагінату калію та аспарагінату магнію (Панангіну) приводить до зменшення екстрасистолії у пацієнтів з ішемічною хворобою серця (ІХС) на 87% (рисунок) (Zhi et al., 2007).
Динаміка естрасистолії
Варто також підкреслити, що Панангін – це препарат, тоді як більшість інших засобів, що містять калій та магній, переважно є дієтичними добавками. Додатковою зручністю препарату Панангін форте є приймання не двох, а однієї таблетки (яка містить 280 магнію аспарагінату та 316 мг калію аспарагінату) тричі на добу, що забезпечує добову дозу калію та магнію.
Висновки
- У пацієнтів із порушеннями ритму серця дефіцит калію спричиняє подовження періоду реполяризації з високим ризиком формування тяжких аритмій типу «пірует». Гіпокаліємія збільшує імовірність виникнення аритмій у пацієнтів з ІХС, СН або гіпертрофією лівого шлуночка.
- Рекомендовано моніторинг вмісту калію у плазмі крові та підтримання на рівні ≥4,0 ммоль/л.
- Разом калій, магній та аспарагінат-аніон у складі Панангіну та Панангіну форте сприяють захисту міокарда й запобігають аритмії.
Підготувала Олександра Демецька
Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 4 (77) 2021 р.




