19 липня, 2022
Біластин: антигістамінний препарат нового покоління для лікування алергічного риніту та кропив’янки
Останнім часом спостерігається постійне зростання захворюваності на алергічні хвороби. Наразі сукупна поширеність таких захворювань, як алергічний риніт (АР), харчова алергія, бронхіальна астма й анафілактичні реакції становить 25% у популяції, сягаючи максимуму серед підлітків і дорослих у промислово розвинених країнах. Важливий клас препаратів для лікування алергічних захворювань – антагоністи гістамінових H1-рецепторів, інноваційним представником яких є біластин. Препарат являє собою неседативний високоселективний антагоніст гістамінових H1-рецепторів II покоління, що пригнічує вивільнення гістаміну з мастоцитів; його схвалено для лікування АР, кропив’янки та свербежу, пов’язаного із захворюваннями шкіри. Цей огляд охоплює безпеку, ефективність і фармакологічні аспекти застосування біластину як важливого препарату для лікування зазначених захворювань.
Особлива увага приділятиметься саме АР у зв’язку з надзвичайно високою поширеністю цієї патології.
АР – це запальне захворювання слизової оболонки носа, спричинене алергеном, який індукує IgE-опосередковане запалення. В усьому світі ≈10-40% населення різних вікових груп страждають на АР, що значно впливає на якість життя. Лікарі часто не діагностують АР, а пацієнти не звертають на нього уваги. Втім, нелікований АР часто зумовлює розвиток кон’юнктивіту й астми [1, 2].
Класифікація АР згідно з рекомендаціями Allergic Rhinitis and its Impact on Asthma (ARIA, 2019)
Класифікацію АР було вперше запропоновано в Міжнародному погоджувальному документі «Алергічний риніт і його вплив на астму» (ARIA) в 1999 році з урахуванням тяжкості симптомів захворювання та їхньої тривалості. У 2019 році було опубліковано останнє оновлення класифікації ARIA, відповідно до якого розрізняють такі форми АР:
- за тривалістю симптомів:
- інтермітуючий АР – симптоми наявні <4 дні/тиж або <4 тиж/рік;
- персистуючий АР – симптоми наявні щонайменше 4 дні/тиж і щонайменше 4 тиж;
- за тяжкістю перебігу симптомів (порушення сну; негативний вплив на повсякденну активність, відпочинок, заняття спортом; негативний вплив на дієздатність і навчання в школі; виражені та нестерпні симптоми):
- легкий АР – не спостерігається жодного з вищезазначених симптомів;
- середньотяжкий/тяжкий – наявний щонайменше 1 із вищезазначених симптомів.
Лікування АР
Для лікування періодичних та постійних симптомів АР ARIA (2019) наполегливо рекомендує застосовувати пероральний H1-антигістамінний препарат, а також інтраназальний кортикостероїд (ІНКС).
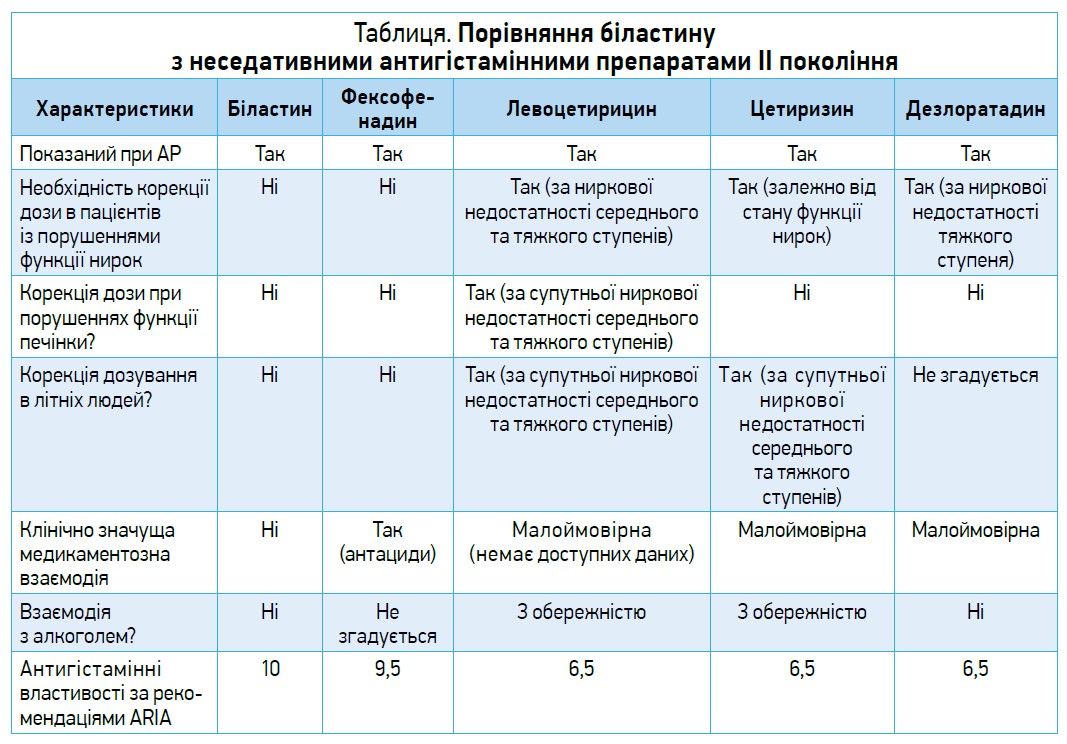
Антигістамінним препаратам II покоління віддається перевага порівняно із препаратами I покоління у зв’язку з їхньою високою ефективністю в лікуванні алергічних симптомів, відсутністю седативної дії та блокуванням мускаринових рецепторів. Біластин вважається кращим пероральним антагоністом H1-рецепторів у зв’язку з легкістю дозування та відсутністю міжмедикаментозної взаємодії (табл.) [8, 9].
Вплив антигістамінних препаратів на когнітивні, психомоторні функції та здатність керувати автомобілем
Безпека препарату при виконанні когнітивних і психомоторних функцій (наприклад, керування транспортним засобом) має вирішальне значення, тому під час обрання антигістамінного засобу II покоління необхідно обов’язково враховувати його седативні ефекти. Біластин є неседативним антигістамінним препаратом, що характеризується швидкою адсорбцією; він не метаболізується ферментами печінки, тому майже не взаємодіє з іншими антигістамінними препаратами та не посилює їхньої седативної дії. Отже, біластин можна розглядати як антигістамінний препарат вибору для водіїв транспортних засобів. Біластин рекомендований у Настанові щодо поводження з препаратами, які використовуються екіпажем літака, нещодавно підготовленій Міністерством землі, інфраструктури та транспорту Японії [10, 11].
Основні характеристики біластину
Під час алергічних реакцій сенсибілізовані імунні клітини вивільняють антитіла Ig-E, які зв’язуються з мастоцитами та дестабілізують їх, вивільняючи гістамін й інші медіатори запалення, що спричиняє появу симптомів АР. Біластин зв’язується з H1-рецепторами мастоцитів, запобігає їхній дестабілізації та вивільненню гістаміну, отже, забезпечує у такий спосіб полегшення симптомів АР [13]. Біластин є високоселективним блокатором периферичних H1-рецепторів, що не зв’язується з мускариновими рецепторами. Крім того, препарат пригнічує міграцію еозинофілів до джерела запалення, стабілізуючи в такий спосіб мастоцити. В дослідженнях in vitro біластин пригнічував вивільнення гістаміну, інтерлейкіну‑4, фактора некрозу пухлини-α з мастоцитів і гранулоцитів людини, демонструючи протизапальну активність. Біластин має високу специфічність до H1-рецепторів, котра в 3-6 разів перевищує спорідненість фексофенадину. Ефективність біластину (20 мг) є схожою та не поступається такій цетиризину (10 мг) і фексофенадину (120 мг) через 1 год після прийому. Біластин має тривалішу дію (до 26 год після прийому) порівняно із цетиризином, а також фексофенадином, характеризується швидким початком антигістамінного ефекту (через ≈30 хв після прийому). Максимальний ефект препарату розвивається в інтервалі часу від 0,5 до 8 год [8-12].
Фармакокінетика
Біодоступність біластину становить 61% з tmax 1,13 год; cmax знижується на 25-33% при прийомі їжі з низьким/високим умістом жиру порівняно зі станом натще. Біластин не проявляє клінічно значущих міжмедикаментозних взаємодій на відміну від багатьох інших антигістамінних препаратів II покоління, оскільки не взаємодіє із системою цитохрому Р450 [12]. Біластин виводиться переважно із фекаліями (66,5%) та сечею (28,3%) у незміненому вигляді.
Спосіб застосування та дози
Рекомендована доза біластину становить 20 мг 1 р/добу. Для досягнення більшої ефективності препарат слід приймати щонайменше за 1 год до або через 2 год після прийому їжі.
Для пацієнтів віком >65 років корекція дози не потрібна. Це стосується і хворих із порушенням функції нирок. Утім, слід уникати одночасного застосування біластину й інгібіторів Р-глікопротеїну (Pgр) пацієнтам із порушенням функції нирок середнього та тяжкого ступенів. Оскільки біластин не метаболізується в печінці, а його основний шлях виведення – нирки, малоймовірно, що печінкова недостатність може зумовити передозування препаратом. З огляду на це немає потреби коригувати дозу для пацієнтів із порушенням функції печінки. Біластин належить до препаратів категорії В при вагітності [14].
Безпека та переносимість
Висока безпека та переносимість біластину встановлені в усіх проведених клінічних дослідженнях. Найчастішими побічними ефектами, про які повідомляли пацієнти, були головний біль та слабкість. Біластин не подовжує інтервалу QT/QTc і не спричиняє суттєвих змін на ЕКГ у досліджуваних дозах, навіть у разі одночасного застосування із препаратами, що підвищують його рівень у плазмі (наприклад, кетоконазол). Біластин не проникає через гематоенцефалічний бар’єр, тому не спричиняє седації; у терапевтичних дозах він не має антихолінергічної дії, не впливає на психомоторну працездатність, не посилює дії алкоголю, бензодіазепіну, лоразепаму. Під час тестування водіїв транспортних засобів біластин не продемонстрував істотних відмінностей порівняно із плацебо [10-14].
Клінічні докази та перспективи застосування
P. Kuna та співавт. (2009) у рандомізованому подвійному сліпому плацебо-контрольованому дослідженні оцінювали безпеку й ефективність біластину 20 мг і цетиризину 10 мг у пацієнтів із сезонним АР віком від 12 до 70 років. Із відібраних 683 хворих на сезонний період рандомізовано призначали біластин 20 мг, цетиризин 10 мг або плацебо протягом 2 тиж. Пацієнти, які отримували біластин і цетиризин, продемонстрували значне покращення (р<0,001) середньої загальної шкали симптомів (TSS) порівняно із плацебо.
Продемонстровано, що біластин у дозі 20 мг 1 р/добу не поступається цетиризину в дозі 10 мг, але значно перевершував плацебо щодо полегшення симптомів сезонної АР. У пацієнтів, котрі отримували цетиризин, частіше спостерігалися епізоди сонливості та втоми [15].
Ефективність (для полегшення симптомів АР) біластину, цетиризину, фексофенадину було оцінено в подвійному сліпому дослідженні F. Horak і співавт. (2010). Хворим з алергією на пилок одноразово призначали біластин 20 мг, цетиризин 10 мг, фексофенадин 120 мг або плацебо перорально через 2 год після початку провокації. Оцінку ефективності лікування визначали за шкалою загальної оцінки симптомів (TSS) на 1-й і 2-й дні. Біластин і цетиризин довели найшвидший (протягом 1 год) початок дії та тривалий ефект (>26 год). Фексофенадин був не гіршим на 1-й день, але менш ефективним на 2-й, що свідчить про коротшу тривалість дії. Безпека та переносимість біластину, цетиризину, фексофенадину були схожими.
Відповідно до чинних рекомендацій Європейської академії алергії та клінічної імунології (EAACI), Глобальної європейської мережі з алергії й астми (GA2LEN), Європейського дерматологічного форуму (EDF), антигістамінні препарати ІІ покоління є першою лінією симптоматичного лікування хронічної спонтанної кропив’янки (ХСК). Утім, контролю ХСК вдається досягти далеко не в усіх пацієнтів, які отримують стандартні дози антигістамінних препаратів ІІ покоління.
За відсутності ефекту від призначення зазначених препаратів у звичайних дозах можливі дві стратегії подальшого лікування: збільшити дозу того самого лікарського засобу вище стандартної або застосувати комбінацію антигістамінних препаратів.
Метою нещодавнього дослідження B. Shah та співавт. (2022) було визначити ефективність і переносимість подвійної дози біластину, а також фексофенадину; комбінації різних антигістамінних препаратів ІІ покоління; комбінації левоцетиризину й антигістамінних препаратів І покоління (гідроксизину) в пацієнтів із ХСК.
До випробування залучили пацієнтів вікової групи 18-60 років із клінічною історією ХСК упродовж щонайменше 6 тиж протягом останніх 3 міс без ідентифікованої причини захворювання, а також із показником активності кропив’янки за шкалою UAS7 (Urticaria Activity Scоre) ≥7 балів. Найвираженіше зниження середнього бала за опитувальником UAS7 через 4 тиж лікування спостерігалося в групі біластину (58,6%). Підвищення дози біластину було не лише ефективним, а й спричиняло менш виражену седацію, ніж збільшення дози фексофенадину чи комбінування антигістамінних препаратів І та ІІ поколінь (левоцетиризин + гідроксизин). Отже, збільшення дози біластину є кращою альтернативою, ніж комбінація антигістамінних препаратів І та ІІ поколінь.
A. M. Abdelshafy та співавт. (2022) провели систематичний огляд і метааналіз рандомізованих контрольованих досліджень щодо вивчення впливу біластину на симптоми АР та хронічної кропив’янки. Були зібрані дані за загальною оцінкою симптомів АР (TSS), загальною оцінкою назальних симптомів (TNSS), дискомфорту, пов’язаного із цими алергічними станами, визначеного за візуально-аналоговою шкалою (VAS), а також за оцінкою якості життя (QOL) для АР та ХСК. Метааналіз довів, що біластин перевершує плацебо за показниками TSS, TNSS, VAS, QOL у пацієнтів з АР та ХСК у разі зіставної з плацебо частоти побічних ефектів. Біластин виявив схожу ефективність щодо зазначених результатів порівняно з такими антигістамінними препаратами, як цетиризин, фексофенадин і лоратадин, а також виявився безпечнішим.
Висновки
Біластин є антагоністом H1-рецепторів II покоління, показаним при АР і хронічній кропив’янці в дорослих і дітей віком від 6 років, або з масою тіла >20 кг. Препарат здатен забезпечити швидку, ефективну та тривалу дію. Висока безпека біластину передбачає відсутність седативного ефекту порівняно із цетиризином і мінімальну лікарську взаємодію порівняно із фексофенадином.
Підготував В’ячеслав Килимчук
Медична газета «Здоров’я України 21 сторіччя» № 5-6 (522-523), 2022 р.