27 жовтня, 2022
Нові можливості в лікуванні алергічного риніту
Алергічний риніт (АР) негативно впливає на повсякденне функціонування і якість життя пацієнтів, отже, потребує обов’язкового терапевтичного втручання. Запорукою ефективного лікування є ретельно підібрана персоналізована терапія. Сучасний алгоритм терапії АР, представлений у настанові ARIA (Allergic Rhinitis and its Impact on Asthma), базується на оцінці стану пацієнта за допомогою візуальної аналогової шкали (ВАШ) та відповідно до неї посиленні (step up) або ослабленні (step down) фармакологічного лікування. До препаратів першого ряду належать Н1-антигістамінні препарати II покоління, інтраназальні кортикоїди (ІНК) і комбінація ІНК з азеластином. Комбінація ІНК з інтраназальними антигістамінними препаратами дозволяє пацієнтам отримати вигоду від терапевтичних переваг обох груп препаратів, тому вважається універсальною стратегією лікування. Цей огляд присвячено одній з найновіших терапевтичних опцій для лікування АР – комбінації мометазону фуроату з олопатадину гідрохлоридом.
Основні відомості про АР
АР визначається як клінічний синдром, спричинений IgE-залежною реакцією слизової оболонки носа на сенсибілізуючі алергени. Симптоми АР характеризуються водянистими виділеннями з носа, пароксизмальним чханням, свербежем і відчуттям закладеності носа. Назальні симптоми часто супроводжуються алергічним кон’юнктивітом, тобто набряком і почервонінням кон’юнктиви, сльозотечею та свербінням очей.
АР є одним із найпоширеніших захворювань людини. В європейських країнах частота підтверджених випадків АР у дорослих коливається від 17 до 28,5% (Brożek J. L. et al., 2017). У випробуванні ECAP це захворювання діагностували у 28,9% обстежених в амбулаторних умовах, у т. ч. інтермітуюча форма у 47,7% і персистуюча – в 52,3% (Samoliński B. et al., 2014). За інтермітуючої форми АР симптоми спостерігаються <4 днів/тиж протягом загального періоду <4 тиж, перевищуючи зазначені часові рамки в разі персистуючої форми.
При класифікації АР також ураховуються тяжкість симптомів та їхній вплив на якість життя пацієнта. Тяжкість симптомів залежить насамперед від впливу сенсибілізуючого алергену, а також, наприклад, від ступеня забруднення повітря. Симптоми легкого АР не такі неприємні, щоб мати значний вплив на якість життя та повсякденне функціонування пацієнтів. Проте помітне погіршення якості життя спостерігається за АР середнього та тяжкого ступенів. При такій інтенсивності хвороба зумовлює труднощі у професійному житті та навчанні, спорті й соціальному житті, а також порушення сну.
ВАШ є дуже корисним інструментом для оцінки вираженості симптомів АР; вона використовується для діагностики АР, оцінки якості життя пацієнта, визначення схеми лікування та моніторингу його ефективності. ВАШ – це 10-сантиметрова шкала, яку пацієнт застосовує для визначення інтенсивності симптомів від 0 (немає симптомів) до 10 (дуже серйозні симптоми). Шкала характеризується високою чутливістю та відтворюваністю. Електронні щоденники, наприклад, у формі мобільних додатків, полегшують оцінку контролю симптомів АР та допомагають визначати обставини появи симптомів, у т. ч. сезонність і дотримання рекомендацій щодо фармакотерапії.
Нелікований або неправильно лікований АР може сприяти розвитку таких ускладнень, як параназальний синусит або гнійний середній отит. Окрім того, АР є потужним фактором ризику розвитку бронхіальної астми, яка діагностується в 15-38% пацієнтів з АР (Brożek J. L. et al., 2017), при цьому >85% хворих на бронхіальну астму також мають діагноз АР (Samoliński B. et al., 2019). Неконтрольовані симптоми середнього та тяжкого АР впливають на контроль симптомів бронхіальної астми (Taramarcaz P. et al., 2003).
Алгоритм лікування АР
Відповідно до останнього оновлення рекомендацій ARIA (2019) метою лікування АР є контроль захворювання для покращення якості життя пацієнта та запобігання можливим ускладненням. Обрання схеми терапії АР залежить від численних факторів, пов’язаних з пацієнтом, тому має бути персоналізованим. До факторів, які слід брати до уваги під час ухвалення терапевтичних рішень, належать вік пацієнта, його побажання щодо лікування, кількість і тяжкість симптомів, мультиморбідність, історія відповідей на попередню терапію, поточне лікування та його ефективність, безпека і своєчасність запропонованого лікування.
Нові рекомендації ARIA-GRADE (2019) щодо обрання лікування АР, які ґрунтуються на результатах клінічних досліджень, містять такі положення:
- ефект пероральних Н1-антигістамінних препаратів слабший, ніж ІНК, хоча багато пацієнтів надають перевагу пероральним препаратам;
- ефективність назальних Н1-антигістамінних препаратів нижча за таку ІНК;
- початок дії назальних Н1-антигістамінних препаратів спостерігається вже через декілька хвилин; початок дії ІНК – через декілька годин або днів;
- комбінація ІНК із пероральними H1-антигістамінними препаратами не надає додаткових переваг порівняно з монотерапією ІНК;
- комбінації ІНК із назальними H1-антигістамінними препаратами є ефективнішими (ніж ІНК окремо) в пацієнтів із помірним та тяжким АР;
- початок дії комбінації ІНК із назальними H1-антигістамінними препаратами спостерігається протягом декількох хвилин;
- антагоністи лейкотрієнів менш ефективні за ІНК.
Для початку терапії пацієнта з АР, який раніше не лікувався, слід обрати один із трьох препаратів першого вибору:
- H1-антигістамінний препарат;
- ІНК;
- комбінація ІНК із назальним H1-антигістамінним препаратом.
Для пацієнта з персистуючим АР зі ступенем тяжкості за ВАШ не менше 5 балів першим вибором є ІНК або комбінація ІНК із назальним H1-антигістамінним препаратом. Щоденна оцінка контролю симптомів у пацієнта за шкалою ВАШ використовується як основа для продовження або посилення / послаблення терапії на 3-й та 7-й дні.
В хворих, які вже отримували адекватне лікування (одним із трьох препаратів першої лінії), терапевтичний вибір також буде залежати від тяжкості симптомів, оцінених за допомогою ВАШ. У разі тяжкості симптомів за ВАШ <5 балів рішення має ґрунтуватися на формі АР та впливі сенсибілізуючих алергенів на даний час. У разі інтермітуючого АР та відсутності впливу сенсибілізуючих алергенів лікування можна зменшити чи припинити. За персистуючого АР та постійного впливу сенсибілізуючого алергену лікування варто продовжити в попередньому обсязі чи посилити. В обох ситуаціях повторна оцінка контролю захворювання проводиться на 3-й день після зміни лікування на основі щоденних показників ВАШ.
Коли тяжкість симптомів у пацієнта, котрий уже отримує лікування одним із трьох препаратів першого вибору, оцінюється в ≥5 балів, слід ухвалити рішення про посилення лікування. Вибір передбачає ІНК і комбінацію ІНК із назальним H1-антигістамінним препаратом. Повторний контроль терапії слід проводити на 7-й день на основі щоденних оцінок ВАШ. За потреби здійснюють корекцію лікування.
Характеристика доступних методів лікування
H1-антигістамінні препарати
Антигістамінні препарати II покоління широко застосовуються для лікування АР. Пероральні H1-антигістамінні засоби I покоління пов’язані з численними небажаними явищами, в т. ч. із седативними ефектами, тому їх слід уникати.
Механізм дії цих лікарських засобів полягає у конкуренції з гістаміном за зв’язування гістамінових рецепторів. Препарати зворотно зв’язуються з H1-рецепторами, що зумовлює зменшення гістамінзалежних симптомів АР (водянисті виділення з носа, свербіж і пароксизмальне чхання). Представники II покоління мають високу селективність до периферичних H1-рецепторів, хорошу здатність проникати до периферичних тканин, а також низьку проникність через гематоенцефалічний бар’єр. Антигістамінні препарати II покоління характеризуються широким терапевтичним вікном і низькою токсичністю. Додаткова нерецептивна активність цих препаратів пов’язана із впливом на медіатори алергії та запалення, блокуванням надходження прозапальних клітин до вогнища запалення і пригніченням експресії молекул адгезії.
Група пероральних H1-антигістамінних препаратів II покоління містить дезлоратадин, лоратадин, левоцетиризин, цетиризин, фексофенадин, біластин і рупатадин.
Місцеві антигістамінні препарати, нанесені на слизову оболонку носа чи кон’юнктиви, здатні створювати вищі локальні концентрації порівняно з пероральним застосуванням, не виявляючи системних ефектів. Група містить азеластин, левокабастин, олопатадин і емедастин.
ІНК
Характерними рисами цих препаратів є сильна місцева протизапальна дія та низький системний вплив. Така властивість значно скорочує спектр побічних ефектів цієї групи лікарських засобів. Механізм їх дії полягає у зв’язуванні молекули препарату з розташованим у цитоплазмі рецептором глюкокортикоїду. Після перенесення до ядра клітини препарат зв’язує послідовності регулятора ДНК у промоторах генів, впливаючи на їхню експресію. В цього класу препаратів також спостерігаються екстрарецепторні ефекти.
Глюкокортикоїди пригнічують експресію генів, відповідальних за розвиток і підтримку запалення, продукцію прозапальних цитокінів та хемокінів, а також експресію молекул адгезії. Вони ущільнюють і звужують кровоносні судини, зменшуючи в такий спосіб набряк слизової оболонки й ексудацію, а також виділення слизу. Їхня активність пригнічує ранні та пізні стадії алергічної реакції. Отже, ІНК зменшують усі симптоми АР, особливо закладеність носа, що значно покращує якість життя пацієнтів з АР.
До групи ІНК належать беклометазон, будесонід, флутиказону пропіонат, флутиказону фуроат і мометазону фуроат. Певні особливості мають препарати фуроатної групи. Бічний ланцюг у молекулі фуроатного ефіру сприяє його високій ліпофільності, полегшуючи його всмоктування слизовою оболонкою носа та поглинання фосфоліпідами в клітинних мембранах. Ця властивість зменшує системні ефекти при максимальному збільшенні місцевої активності.
Фармакокінетичні властивості ІНК забезпечують дуже сприятливі значення терапевтичного індексу, тобто максимальний терапевтичний ефект за мінімуму побічних реакцій (терапевтичний індекс для мометазону фуроату – 7). Мометазону фуроат має найнижчу системну біодоступність у цій групі препаратів, що означає його високу безпеку. Дослідження доводять, що мометазону фуроат і флутиказону фуроат також зменшують вираженість кон’юнктивальних симптомів, пов’язаних з АР.
Комбінація назального глюкокортикоїду з назальним H1-антигістамінним препаратом
Оптимальне терапевтичне рішення при АР полягає у поєднанні ІНК із назальним H1-антигістамінним препаратом в одному препараті. За окремого застосування обидва препарати мають свої обмеження – відтермінований початок дії ІНК і відсутність чіткого протизапального ефекту для антигістамінних препаратів.
Відповідно до оновлених рекомендацій ARIA комбіноване лікування у вигляді одного інгаляційного пристрою рекомендовано при інтермітуючому та персистуючому АР як терапія першого вибору. В пацієнтів із помірним і тяжким АР така схема лікування є ефективнішою (порівняно із застосуванням лише ІНК). Окрім того, комбіноване лікування з використанням однієї інгаляційної форми замість декількох монотерапевтичних засобів може покращити прихильність до лікування.
Комбінація флутиказону пропіонату й азеластину гідрохлориду донедавна була єдиним доступним продуктом у цьому класі препаратів і отримала високу оцінку серед методів лікування АР. Нещодавно пацієнтам стала доступна нова комбінація ІНК і назального H1-антигістамінного засобу – мометазону фуроату з олопатадину гідрохлоридом. Олопатадин є високоселективним антагоністом H1-гістамінових рецепторів, який добре переноситься, має додаткові протизапальні властивості. При назальному введенні олопатадин зменшує виділення з носа, свербіж і чхання. Мометазону фуроат – ІНК із добре задокументованим профілем безпеки, який завдяки сильній протизапальній дії ефективно зменшує симптоми закладеності носа та свербіж, чхання і виділення з носа. Ефективність і безпеку цієї комбінації досліджували як при інтермітуючому, так і при персистуючому АР.
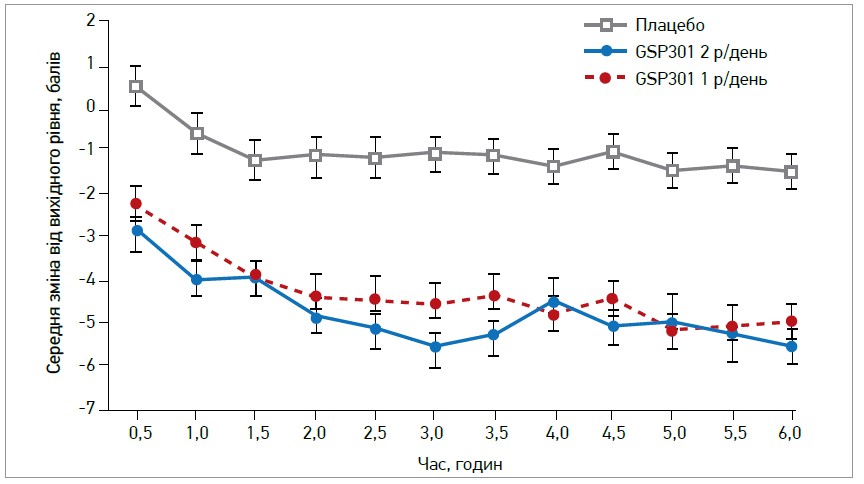
У рандомізованому подвійному сліпому плацебо-контрольованому дослідженні Patel та співавт. (2019) оцінили ефективність і безпеку GSP301 (комбінація фіксованих доз олопатадину гідрохлориду, а також мометазону фуроату в назальному спреї) у групі зі 180 дорослих із сезонним АР, які піддавалися впливу пилку амброзії в алергенній камері під час серії візитів протягом 2 тиж. Прийом GSP301 2 р/день (у вигляді комбінації олопатадину гідрохлориду 665 мкг із мометазону фуроату 25 мкг) або 1 р/день (у вигляді комбінації олопатадину гідрохлориду 665 мкг із мометазону фуроату 50 мкг) забезпечив достовірне та клінічно значуще покращення симптомів АР, а також значне покращення супутніх очних симптомів порівняно із плацебо (рис. 1). Обидві схеми лікування GSP301 добре переносилися. Клінічно значуще покращення назальних симптомів (порівняно із плацебо) спостерігалося протягом 10 хв після прийому.
Рис. 1. Середня зміна рефлексивної загальної оцінки носових симптомів (rTNSS) від початкового рівня
до завершення курсу лікування препаратом GSP301 (порівняно із плацебо) в дорослих із сезонним АР,
які зазнали впливу пилку амброзії в алергенній камері (Patel et al., 2019)
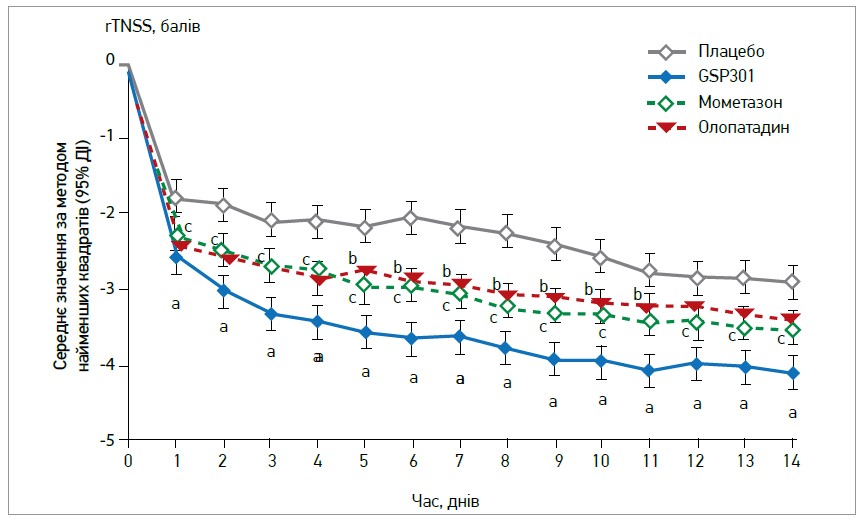
У подвійному сліпому дослідженні Gross і співавт. (2019) у 43 центрах США групу з 1176 дорослих і підлітків віком від 12 років із сезонним АР рандомізували у співвідношенні 1:1:1:1 до груп, що отримували GSP301 (олопатадину гідрохлорид 665 мкг + мометазону фуроат 25 мкг), олопатадину гідрохлорид (665 мкг), мометазону фуроат (25 мкг) або плацебо 2 р/день протягом 14 днів. Первинною кінцевою точкою була середня зміна ранкового та вечірнього середнього 12-годинного рефлексивного загального балу назальних симптомів (rTNSS) порівняно з базовим значенням. GSP301 забезпечив статистично та клінічно значущі поліпшення rTNSS порівняно із плацебо (p<0,001), олопатадином (p<0,03) і мометазоном (p<0,02) (рис. 2). Він також довів ефективність в усуненні кон’юнктивальних симптомів АР. GSP301 характеризувався швидким початком дії, адже його ефект спостерігався протягом 15 хв. Препарат виявився безпечним і добре переносився, частота його побічних ефектів була схожою на частоту таких монотерапії та плацебо.
Рис. 2. Порівняння середніх ранкових і вечірніх результатів 12-годинної рефлексивної загальної
оцінки носових симптомів (rTNSS) протягом 14-денного лікування в пацієнтів із сезонним
АР: a) достовірна різниця (p<0,05) для GSP301 проти плацебо; (b) достовірна різниця (p<0,05)
для олопатадину проти плацебо; c) достовірна різниця (p<0,05) для мометазону проти плацебо
(Gross et al., 2019)
Щоб оцінити довгострокову (52-тижневу) безпеку та ефективність GSP301 при персистуючому АР, Segall і співавт. провели рандомізоване подвійне сліпе плацебо-контрольоване дослідження за участю 601 дорослого та підлітка віком ≥12 років у 33 центрах США. Комбінація олопатадину гідрохлориду 665 мкг, а також мометазону фуроату 25 мкг, які застосовували 2 р/день, добре переносилася і забезпечувала статистично та клінічно значущу ефективність у зменшенні симптомів АР (порівняно із плацебо) протягом 52 тиж.
Висновки
Комбінації ІНК із назальними H1-антигістамінними препаратами є найуніверсальнішими препаратами проти АР і можуть застосовуватися як при інтермітуючій, так і при персистуючій формі захворювання. Вони отримали високу позицію в нових алгоритмах лікування АР і як препарати першого вибору, і як ліки для посилення терапії.
Довідка «ЗУ»
На українському фармацевтичному ринку комбінація ІНК із назальним H1-антигістамінним засобом представлена препаратом Ріалтріс®, який випускається у вигляді назального спрею. Одна доза Ріалтріс® містить олопатадину гідрохлориду 665 мкг (еквівалентно олопатадину 600 мкг) і мометазону фуроату моногідрату (еквівалентно мометазону фуроату 25 мкг). Препарат показаний для лікування АР у дорослих і дітей віком від 12 років. Рекомендована доза становить 2 впорскування в кожну ніздрю 2 р/добу.
Список літератури знаходиться в редакції.
Адаптований переклад з англ. В’ячеслава Килимчука
За матеріалами: Agnieszka Lipiec, Dariusz Jurkiewicz. A new therapeutic option in the management of allergic rhinitis. Otolaryngol Pol. 2021 Nov 2; 75 (5): 1-5.
Медична газета «Здоров’я України 21 сторіччя» № 11 (528), 2022 р.