24 лютого, 2023
Ліпітензія – новий погляд на відомі проблеми
 Відомо, що серцево-судинні захворювання (ССЗ) є головною причиною смерті в світі. У 2019 році 17,6 млн осіб померло внаслідок зазначених недуг, що склало 32% глобальної смертності; ¾ з них припадають на країни низького та проміжного економічного розвитку. Загалом кожну 1,7 с одна особа помирає від ССЗ [1]. Експерти Всесвітньої організації охорони здоров’я (ВООЗ) прогнозують зростання кардіоваскулярної смертності до >23 млн осіб у 2030 році та до >34 млн осіб до 2060 року [1].
Відомо, що серцево-судинні захворювання (ССЗ) є головною причиною смерті в світі. У 2019 році 17,6 млн осіб померло внаслідок зазначених недуг, що склало 32% глобальної смертності; ¾ з них припадають на країни низького та проміжного економічного розвитку. Загалом кожну 1,7 с одна особа помирає від ССЗ [1]. Експерти Всесвітньої організації охорони здоров’я (ВООЗ) прогнозують зростання кардіоваскулярної смертності до >23 млн осіб у 2030 році та до >34 млн осіб до 2060 року [1].
У 2022 році Американська асоціація кардіологів (ACC) оновила головні елементи ідеального кардіоваскулярного здоров’я: відсутність експозиції нікотину, нормальна маса тіла й показники артеріального тиску (АТ), ліпідограми та вуглеводного обміну (рівень глікованого гемоглобіну), здорова дієта, достатня фізична активність і повноцінний сон [2]. Водночас артеріальна гіпертензія (АГ) та дисліпідемія (поряд із курінням, цукровим діабетом (ЦД), ожирінням) нині визначені як головні модифіковані чинники ризику атеросклеротичних ССЗ, контроль яких дозволяє стримати прогресування атеросклеротичного процесу [3].
Ліпітензія – дефініція, епідеміологія
Уперше феномен поєднання АГ та дисліпідемії (дисліпідемічна гіпертензія) був описаний у 1988 році при проведенні популяційного дослідження в штаті Юта (США). У 12% обстежених пацієнтів з есенціальною АГ ідентифікували генетичний синдром родинної дисліпідемії, а серед кровних родичів – у 48% випадків [4]. Згодом було відмічено, що неродинні форми дисліпідемії частіше трапляються в разі АГ, ніж родинна дисліпідемія, а в 2012 році поєднання цих двох вагомих модифікованих кардіоваскулярних чинників ризику запропоновано називати терміном «ліпітензія» з метою кращого виявлення, діагностики та менеджменту [5].
Поширення ліпітензії, за даними різних епідеміологічних досліджень, складає 15-31%, зростає з віком та за умови супутнього ожиріння, метаболічного синдрому чи ЦД 2 типу [6]. Відзначено також певну расову відмінність у поширенні поєднання АГ та дисліпідемії: найвище серед темношкірого населення [6].
Взаємний вплив дисліпідемії та АГ на прогресування атеросклерозу
Прогресування атеросклерозу залежить від окислювального стресу, ендотеліальної дисфункції, запалення, а АГ та/або дисліпідемія можуть незалежно ініціювати ці процеси. Дисліпідемія й АГ є патологічними станами, за яких спостерігається ушкодження ендотелію; це зумовлює проліферацію клітин, ремоделювання судин, апоптоз і підвищення клітинної проникності з посиленою продукцією молекул адгезії, які зв’язують моноцити та Т‑лімфоцити, створюючи хибне коло патофізіологічних факторів. Під впливом хемоатрактантів і прозапальних цитокінів моноцити проникають до інтими судинної стінки, де диференціюються в макрофаги, які безконтрольно поглинають окислені ліпопротеїни низької щільності (ЛПНЩ), утворюючи пінисті клітини й атеросклеротичні ураження. Крім того, ушкодження ендотелію також спричиняє втрату вазомоторної активності, непропорційну скоротливість судин, підвищення АТ у пацієнтів із дисліпідемією, тоді як у хворих із гіпертензією відбувається подальше підвищення АТ, створюючи хибне коло, яке посилює розвиток і прогресування атеросклеротичних ушкоджень [7].
Взаємний вплив АГ та дисліпідемії на прогресування атеросклерозу показаний у великому епідеміологічному дослідженні MRFIT за участю 356 222 осіб чоловічої статі, які спостерігалися протягом 12 років. Результати випробування підкреслили, що навіть легкі та помірні рівні як гіпертензії, так і дисліпідемії мали мультиплікативний несприятливий вплив на ризик ішемічної хвороби серця (ІХС) [8]. Нещодавно проведено дослідження із залученням 117 056 дорослих осіб з 11 великих промислових центрів Китаю (термін спостереження – 6 років), під час якого вивчали низку атеросклеротичних індексів (коефіцієнт атерогенності, атерогенний індекс плазми, індекс ризику Castelli тощо), котре показало, що атеросклеротичні індекси були значно вищими в популяціях з АГ порівняно з такими в популяціях із нормальним тиском незалежно від рівня гіпертензії. Водночас систолічний (САТ) і діастолічний АТ (ДАТ) були лінійно та позитивно пов’язані з атеросклеротичними показниками. Крім того, індекс холестерину (ХС) і ХС неЛПВЩ (різниця між загальним ХС і ХС ліпопротеїнів високої щільності – ЛПВЩ) були незалежними факторами ризику поширення АГ [9].
Оцінка кардіоваскулярного ризику в пацієнтів із ліпітензією
Вищезазначений мультиплікативний вплив АГ та дисліпідемії на 10-річний кардіоваскулярний ризик пацієнта може бути показаний за допомогою таблиць SCORE‑2 на прикладі умовного пацієнта віком 60 років у первинній профілактиці, котрий не курить, мешкає в Україні (що належить до категорії найвищого в Європі рівня кардіоваскулярної захворюваності) (табл. 1).
Як показано, кожний із факторів окремо збільшує кардіоваскулярний ризик пацієнта менше ніж наполовину, тоді як існування ліпітензії призводить до понад дворазового зростання ризику порівняно з ідеальним профілем АТ та ХС.
Іншим інструментом оцінки кардіоваскулярного ризику в первинній профілактиці, також рекомендованим настановами Європейського товариства кардіологів (ESC) із превенції кардіоваскулярних захворювань, є калькулятор ризику кардіоваскулярних подій протягом життя (LIFE-CVD model, доступний онлайн https://u-prevent.com/calculators/description/lifeCvd). Зазначена модель дозволяє не лише оцінити ймовірність кардіоваскулярної події у практично здорової особи впродовж життя (умовно – до 90-річного віку), а й демонструє потенційне зниження ризику при застосуванні антигіпертензивної та ліпідознижувальної терапії. Продовжимо розглядати наведений приклад умовного пацієнта з ліпітензією: його індивідуальний ризик кардіоваскулярних подій протягом життя складає 48% без фармакологічного лікування, але може бути кардинально знижений понад ніж удвічі (на 28%) за умови призначення розувастатину 20 мг та антигіпертензивної терапії з досягненням цільового рівня САТ <130 мм рт. ст. [24].
Вищезазначені теоретичні розрахунки переконливо підтверджуються, зокрема, результатами дослідження >438 тис. учасників британського біобанку із застосуванням менделівської рандомізації, у якому одночасне зниження ХС ЛПНЩ та АТ відповідно на 1 ммоль/л і 10 мм рт. ст. були асоційовані із 78% зменшенням відносного ризику (ВР) кардіоваскулярних подій, 67% – кардіоваскулярної смерті, 30% – смерті від будь-якої причини. Варто зазначити, що описаний ефект зберігав високий рівень статистичної значущості для всіх досліджених компонентів кінцевої точки (р<0,001), а також не залежав від інших важливих коваріат (вік, стать, діабет, куріння, ожиріння) [25].
Ефективність комбінованого лікування АГ та дисліпідемії
Наявні наразі рандомізовані клінічні дослідження комбінованого лікування АГ та дисліпідемії не є численними. Одним із перших таких проєктів стало дослідження ASCOT, яке залучило >19 тис. гіпертензивних пацієнтів, рандомізованих до прийому β‑блокатора ± тіазидного діуретика або дигідропіридинового блокатора кальцієвих каналів (БКК) амлодипіну ± інгібітора ангіотензинперетворювального ферменту (ІАПФ) [26]. Одночасно >10 тис. учасників (≈54%) увійшли до ліпідознижувальної гілки дослідження та були рандомізовані до прийому 10 мг аторвастатину або плацебо. За результатами, аторвастатин знизив ризик первинної кінцевої точки (фатальна ІХС та нефатальний інфаркт міокарда, ІМ) на 36% (ВР 0,64, 95% довірчий інтервал (ДІ) від 0,5 до 0,83) із суттєвими відмінностями залежно від характеру антигіпертензивного лікування. Так, у групі терапії, що базувалася на амлодипіні, ефект аторвастатину проти плацебо щодо кінцевої точки досяг 53% (р<0,001) на відміну від відсутності достовірного впливу в групі атенололу (-16%; р=0,3).
Іншим дослідженням, що варте уваги в контексті лікування ліпітензії, є НОРЕ‑3 – випробування з 2х2 дизайном, у якому 12 705 пацієнтів проміжного кардіоваскулярного ризику були рандомізовані до прийому розувастатину або плацебо, фіксованої дози кандесартану чи плацебо або комбінації обох видів лікування проти подвійного плацебо [27]. Впродовж 5,6 року (медіана) спостереження первинна комбінована кінцева точка (кардіоваскулярна смертність, нефатальні ІМ і мозковий інсульт) констатована в 3,6% пацієнтів групи комбінованої терапії проти 5% – у групі подвійного плацебо, що відповідало 29% зниженню ВР (0,71, 95% ДІ від 0,56 до 0,9; р=0,005), без суттєвих проблем із безпекою та переносимістю терапії (нові випадки діабету, ниркова або печінкова дисфункція, захворювання ока, рак тощо).
З огляду на взаємний обтяжувальний вплив АГ та дисліпідемії на прогноз обов’язковим компонентом лікування хворих на гіпертензію, відповідно до чинних настанов ESC (2018), крім антигіпертензивної терапії, є призначення статинів у дозах, які відповідають кардіоваскулярному ризику, з метою досягнення цільових значень ХС ЛПНЩ у крові [10].
Відомо, що статини – це інгібітори 3-гідрокси‑3-метилглутарил коензиму А (ГМГ-КоА) редуктази, які ефективно знижують рівень загального ХС і ХС ЛПНЩ. За допомогою низки великих рандомізованих клінічних досліджень однозначно продемонстровано, що зниження рівня ХС ЛПНЩ, особливо за допомогою статинів, виразно зменшує ризик серцево-судинних смертей і небажаних подій. Показано, що інгібітори ГМГ-КоА‑редуктази запобігають початковим і подальшим серцево-судинним подіям у пацієнтів з ІХС незалежно від концентрації ХС.
На додаток до сприятливих ефектів зниження рівня ХС статини покращують ендотеліальну функцію, підвищують стабільність атеросклеротичних бляшок і пригнічують запальні, а також тромбогенні реакції у стінках артерій. Крім того, широке постмаркетингове спостереження довело, що тривала терапія статинами загалом добре переноситься [11].
Розувастатин є відносно гідрофільним членом родини статинів, хімічна структура якого містить фторовану фенільну та полярну метансульфонамідну групу. Наявність цих груп забезпечує кілька сайтів для взаємодії з цільовим ферментом (ГМГ-КоА‑редуктазою), що обумовлює потужніше пригнічення ферменту за нижчих концентрацій, отже, й виразніший вплив на ліпіди в менших дозах [12].
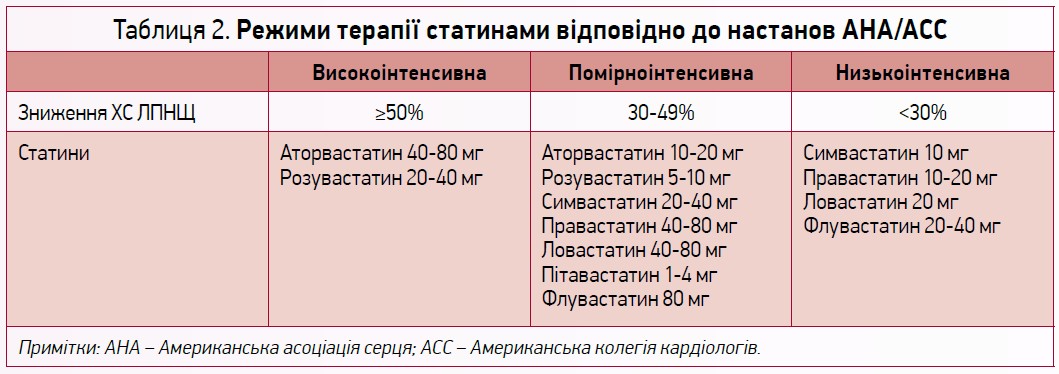
Численними дослідженнями доведені ефективність та безпека розувастатину в контролі показників ліпідограми, регресі атероми й поліпшенні прогнозу пацієнтів з атеросклеротичними ССЗ. Як найсильніша молекула розувастатин рекомендований для вторинної профілактики небажаних кардіоваскулярних подій у пацієнтів високого і дуже високого ризику в режимах інтенсивної та високоінтенсивної статинотерапії (табл. 2) [13].
Нещодавно проведений систематизований огляд та метааналіз клінічних досліджень порівняння еквівалентних доз розувастатину й аторвастатину щодо впливу на ліпідний профіль і об’єм атеросклеротичної бляшки показав, що терапія розувастатином призвела до більшого зменшення вмісту в плазмі крові ХС ЛПНЩ, збільшення рівня ХС ЛПВЩ, а також виразнішого зменшення об’єму атероми [14].
Крім вторинної профілактики, розувастатин продемонстрував відмінні результати в первинній профілактиці небажаних серцево-судинних подій. Post hoc аналіз дослідження JUPITER довів, що в пацієнтів із підвищеним рівнем C‑реактивного білка, які мали високий глобальний серцево-судинний ризик (10-річний бал ризику за шкалою Framingham >20% або ризик SCORE ≥5%) та рівень ХС ЛПНЩ, що не потребує фармакологічного лікування, розувастатин у дозі 20 мг значно знижував основні серцево-судинні події [15]. У дослідженні HOPE‑3 використання розувастатину в дозі 10 мг/добу в осіб високого ризику без атеросклеротичних ССЗ на 20% зменшувало ризик головних небажаних кардіоваскулярних подій: ІМ, інсульту та серцево-судинної смерті [16]. Крім того, нещодавно проведений об’єднаний метааналіз зазначених досліджень показав пропорційне зниження ризику венозних тромбоемболій (ВТЕ) під впливом розувастатину на 47%, причому цей ефект є постійним як за наявності, так і за відсутності пов’язаних із ВТЕ клінічних факторів ризику [17].
Окремі дослідження продемонстрували певну антигіпертензивну дію статинів, особливо в хворих на АГ. Метааналіз досліджень, наявних в електронних базах даних MEDLINE, EMBASE та Cochrane Library, довів, що розувастатин продемонстрував помірне значуще зниження ДАТ і тенденцію до зниження САТ, що можна розглядати як додаткове зниження ризику серцево-судинних подій у пацієнтів із ліпітензією [18].
Метаболічний синдром і ЦД на тлі ліпітензії
Поєднання ліпітензії із ЦД 2 типу, переддіабетом або центральним ожирінням являє собою маніфестний метаболічний синдром – стан, асоційований зі стрімким прогресуванням атеросклеротичного процесу та швидким зростанням ризику кардіоваскулярних подій.
В обсерваційному дослідженні амбулаторних пацієнтів первинної ланки майже чверть осіб із центральним ожирінням мала також АГ й дисліпідемію, при цьому ризик ліпітензії на тлі ожиріння збільшувався мало чи не вп’ятеро (ВР 4,75; 95% ДI 2,87-7,87) порівняно з відсутністю метаболічних порушень [28].
Дисліпідемія в осіб із ЦД та метаболічним синдромом характеризується підвищенням рівня тригліцеридів (ТГ) і зниженням ХС ЛПВЩ у сироватці крові [29]. Крім того, відбувається збільшення концентрації ХС ліпопротеїнів дуже низької щільності (ХС ЛПДНЩ) і ХС ЛПНЩ, причому рівні ХС ЛПНЩ можуть не відрізнятися від значень осіб без метаболічних порушень, проте збільшується кількість найбільш атерогенних дрібних щільних часток ЛПНЩ, спостерігається підвищення ХС неЛПВЩ, що в поєднанні зі збільшенням ЛПДНЩ і ліпопротеїну проміжної щільності зумовлює підвищення рівнів аполіпопротеїну B. Саме тому, на відміну від вторинного характеру в загальній популяції, ХС неЛПВЩ та аполіпропротеїн В набувають особливої актуальності як цілі ліпідознижувальної терапії саме в когортах ЦД і метаболічного синдрому.
Спільна експертна думка останнім часом невпинно схиляється до жорсткіших цільових рівнів ліпідів у пацієнтів із ЦД. Так, згідно з настановою ESC із профілактики кардіоваскулярних захворювань (2021), зниження ХС ЛПНЩ на 50% від початкового рівня та досягнення межі <1,8 ммоль/л рекомендовано як початкова ціль за наявності в хворого на діабет не лише перенесеної атеротромботичної події, а й уражень органів-мішеней (певні прояви діабетичної хвороби нирок або 3 прояви діабетичної мікроангіопатії), при цьому остаточною ліпідною ціллю для зазначеної популяції є 1,4 ммоль/л. Нещодавно оновлені рекомендації Американської діабетичної асоціації (ADA, 2023) визначають досягнення рівня ХС ЛПНЩ <1,8 ммоль/л при застосуванні статину високої інтенсивності для хворих на ЦД із високим кардіоваскулярним ризиком, до якого закономірно призведе наявність ліпітензії [30].
Схожі тенденції простежуються й щодо цільових рівнів АТ. Рекомендації ВООЗ із фармакотерапії АГ (2021) і вищезазначені рекомендації ADA (2023) формулюють необхідність зниження АТ <130/80 мм рт. ст. для будь-якого пацієнта із ЦД, якщо досягнення такого рівня АТ є безпечним та добре переноситься [31]. Основою антигіпертензивної терапії у пацієнта з АГ та ЦД або переддіабетом є блокатори ренін-ангіотензин-альдостеронової системи (РААС), причому вибір відбувається між ІАПФ і блокаторами рецепторів ангіотензину ІІ (БРА) (сартанами). Вибір конкретної молекули має ґрунтуватися не лише на антигіпертензивних властивостях, а й на доказовій базі зниження кардіоваскулярних подій, профілактики ураження органів-мішеней, сприятливому метаболічному профілі тощо. Висока антигіпертензивна ефективність і сприятливий профіль безпеки комбінації валсартану та гідрохлортіазиду (ГХТ) в умовах реальної клінічної практики доведені у великому обсерваційному дослідженні The MATCH (Abts M. et al., 2006). Лікування понад 17 тис. амбулаторних пацієнтів (середній початковий рівень АТ – 165,4/95,8 мм рт. ст.) зазначеною комбінацією в дозах 160/12,5 мг протягом 3 міс дозволило знизити середній систолічний і діастолічний АТ на 27 та 14 мм рт. ст. відповідно з досягненням цільових значень АТ в середньому в 78% пацієнтів, у тому числі у 87% серед тих, хто не отримував антигіпертензивної терапії раніше. Наднизький і зіставний із плацебо рівень відміни терапії внаслідок побічних ефектів (0,4%) підкреслює великі можливості використання комбінацій на основі валсартану в широкій практиці лікування АГ. Згідно з результатами метааналізу, до якого залучили >140 тис. пацієнтів з АГ, застосування сартанів асоційовано з найменшою кількістю нових випадків ЦД (ВР 0,57, 95% ДІ від 0,46 до 0,72; р<0,0001) [32]. Безумовно, чи не найбільший внесок до цих результатів зробили численні дослідження валсартану. Зокрема, субаналіз дослідження VALUE продемонстрував 23% зниження ризику діабету de novo в гіпертензивних пацієнтів високого кардіоваскулярного ризику для валсартану порівняно з амлодипіном – абсолютно нейтральним у метаболічному аспекті компаратором [33]. Окрім того, в рандомізованому клінічному дослідженні NAVIGATOR у когорті 9306 пацієнтів із переддіабетом валсартан у комбінації з модифікацією стилю життя протягом 5 років застосування призвів до 14% зниження ВР нових випадків ЦД 2 типу (ВР 0,86, 95% ДІ від 0,8 до 0,92; р<0,001) [34].
Тоді як комбінація валсартану з дигідропіридиновим БКК (зокрема, з амлодипіном) видається цілком безпечною в метаболічному контексті, поєднання блокаторів РААС із діуретиками в осіб із метаболічними розладами й досі залишається предметом дискусій. У певної кількості пацієнтів із тяжкою АГ досягнення цільових рівнів АТ неможливе без призначення тіазидних діуретиків – обов’язкового компонента потрійної антигіпертензивної комбінації. У зазначених ситуаціях лікар у своїх призначеннях має балансувати між безсумнівною користю внаслідок зниження кардіоваскулярних ризиків при зниженні АТ з одного боку та ймовірністю погіршення метаболічного профілю пацієнта – з іншого.
Досить популярна в певних колах медичної спільноти думка щодо метаболічної нейтральності тіазидоподібних діуретиків, порівняно зі «старими» тіазидами, на жаль, не підтверджується результатами клінічних досліджень. Так, у прямому порівнянні ГХТ з індапамідом та хлорталідоном у 883 гіпертензивних пацієнтів не було виявлено статистично значущих відмінностей у зіставних препаратів за частотою метаболічних й електролітних порушень [35]. Тотожні результати отримано під час метааналізу 12 досліджень із залученням >1,5 тис. пацієнтів, що застосовували ГХТ або тіазидоподібні діуретики [36]. Незважаючи на певну перевагу останніх за антигіпертензивним ефектом, частота гіпокаліємії, гіпонатріємії, а також зміни рівнів глюкози або ХС суттєво не відрізнялися при використанні досліджуваних препаратів. D. H. Zappe та співавт. у своїй роботі показали, що дійсно наявні дисметаболічні ефекти монотерапії ГХТ у вигляді зростання рівнів ТГ та глікованого гемоглобіну в хворих на переддіабет абсолютно нівелюються при комбінації ГХТ із валсартаном [37]. Комбінована терапія протягом 16 тижнів, тотожно до монотерапії валсартаном, не чинила суттєвого впливу на ключові маркери кардіометаболічного профілю (індекс НОМА, інсулінемія, глікемія натще, глікований гемоглобін, а також концентрації ТГ і неетерифікованих жирних кислот.
Прихильність до лікування
Серцево-судинні препарати, як-от ІАПФ / БРА, β-блокатори, антиагреганти та статини, залишаються найпоширенішими медичними втручаннями у всьому світі для профілактики ІХС. Хоча їхній сприятливий вплив встановлено в первинній і вторинній профілактиці ССЗ, їхня ефективність у реальних умовах поступається тому, що спостерігається в рандомізованих контрольованих дослідженнях, а це частково пояснюється низькою прихильністю до лікування. Згідно з результатами TRANSLATE-ACS study, майже 31% пацієнтів з ІМ більше не приймає призначені їм ліки через 6 міс після гострої серцевої події [19]. Метааналіз, який включав 1 978 919 пацієнтів, показав, що лише 60% хворих прихильні до призначених серцево-судинних препаратів. Окрім того, порівняно з дотриманням режиму лікування, ризик серцево-судинних подій або смертності в тих, хто погано дотримується режиму лікування, збільшився на 20 або 35% відповідно [20].
Метааналіз 18 клінічних досліджень (402 201 пацієнт) показав зворотний лінійний зв’язок між прихильністю до лікування ССЗ та серцево-судинними подіями: поліпшення на 20% прихильності до лікування серцево-судинними препаратами асоціювалося зі зниженням ризику смерті від усіх причин на 12% і зниженням ризику будь-яких серцево-судинних подій на 8% [21].
Відомо, що прихильність до лікування є ключовим компонентом лікування хронічних захворювань. Підвищення прихильності до лікування – один із головних пріоритетів порядку денного громадського здоров’я. Згідно з даними ВООЗ, здатність пацієнтів правильно дотримуватися рекомендацій щодо лікування залежить від низки факторів, а не від одного. Ці фактори взаємодіють і посилюють вплив один одного; їх можна об’єднати в 5 основних груп: соціально-економічні, пов’язані з системою охорони здоров’я, станом здоров’я, лікуванням і пацієнтом [22].
Зменшення економічних бар’єрів (зниження вартості, використання великих економних упаковок, застосування якісних генериків тощо) для призначених ліків також покращує рівень прихильності. Так, зниження вартості статинів і клопідогрелю в одній із програм корпорації Pitney Bowes (США) призвело до негайного збільшення прихильності до статинотерапії на 2,8 та на 4% до клопідогрелю, що забезпечило емпіричну основу для використання цього підходу з метою покращення якості медичної допомоги [23].
Одним із генеричних препаратів розувастатину, наявних на фармацевтичному ринку України, є Клівас. Відмінна особливість лікарського засобу – наявність у його складі 3 залужнювачів, які надають змогу значно збільшити його біодоступність, а спеціальна технологія виготовлення забезпечує рівномірний розподіл субстрату в таблетці. Рівень біоеквівалентності Клівасу відповідає оригінальному розувастатину, що дозволило віднести його до класу В1 довідника еквівалентності лікарських засобів Rx index.
Добре відомим для українських лікарів комбінованим препаратом валсартану для початкового і подальшого лікування АГ є Діокор® (валсартан 80/160 мг, гідрохлоротіазид 12,5 мг) компанії ACINO, який зберігає позицію № 1 у продажах 15 років поспіль і виробляється на українському заводі європейського рівня, що підтверджено Європейським сертифікатом GMP.
Список літератури знаходиться в редакції.
UA-CARD-PUB-012023-077
Медична газета «Здоров’я України 21 сторіччя» № 1-2 (537-538), 2023 р.