22 березня, 2026
DiabEyes: від складного до простого
16 грудня 2025 року в Києві з онлайн-трансляцією в прямому ефірі відбулася науково-освітня конференція «DiabEyes: від складного до простого», організована Всеукраїнським альянсом офтальмологів. Під час заходу до уваги спеціалістів-офтальмологів, ендокринологів, лікарів загальної практики, присутніх у залі, а також тих, котрі долучилися онлайн, було представлено доповіді провідних спікерів, які допомогли розставити всі крапки над «і» в темі сучасних можливостей ведення пацієнтів із діабетичною ретинопатією (ДР). Під час панельної дискусії слухачі мали можливість додати коментарі, поставити свої запитання й отримати відповіді фахівців. Щоб переглянути запис заходу, скористайтеся QR‑кодом: https://www.youtube.com/live/Nmk66VUhUFs?si=2zV5xEHyXIIKz502

ДР: типові портрети пацієнтів
 Захід відкрила професор кафедри офтальмології Національного медичного університету ім. О. О. Богомольця, голова правління ГО «Український альянс офтальмологів» (м. Київ), доктор медичних наук Оксана Петрівна Вітовська, до якої приєдналася керівник відділу клінічної діабетології ДУ «Інститут ендокринології та обміну речовин ім. В. П. Комісаренка НАМН України» (м. Київ), доктор медичних наук Любов Костянтинівна Соколова, щоб розглянути типові портрети пацієнтів із ДР.
Захід відкрила професор кафедри офтальмології Національного медичного університету ім. О. О. Богомольця, голова правління ГО «Український альянс офтальмологів» (м. Київ), доктор медичних наук Оксана Петрівна Вітовська, до якої приєдналася керівник відділу клінічної діабетології ДУ «Інститут ендокринології та обміну речовин ім. В. П. Комісаренка НАМН України» (м. Київ), доктор медичних наук Любов Костянтинівна Соколова, щоб розглянути типові портрети пацієнтів із ДР.
Нині алгоритм ведення пацієнта (рис. 1) розпочинається зі скринінгу. Діагноз ДР установлює офтальмолог, до якого звертається пацієнт за скеруванням лікаря-ендокринолога. На ранніх стадіях ДР завдання лікаря-ендокринолога передбачає оптимізацію контролю цукрового діабету (ЦД), призначення специфічного лікування і спостереження за пацієнтом. У разі наявності проліферативної ДР (ПДР) або діабетичного макулярного набряку (ДМН) офтальмолог розпочинає лікування із застосуванням анти-VEGF-терапії або лазерної фотокоагуляції з подальшим спостереженням за пацієнтом.
Професор О.П. Вітовська звернулася до аудиторії з низкою запитань. Чи так лікарі ведуть своїх пацієнтів? Чи дійсно такий алгоритм є оптимальним у сучасних умовах? Чи достатньо просто спостереження у випадку неПДР і що саме може бути тією специфічною терапією поряд з обов’язковою оптимізацією контролю ЦД у таких пацієнтів? У ході зустрічі на всі ці запитання було отримано відповіді.
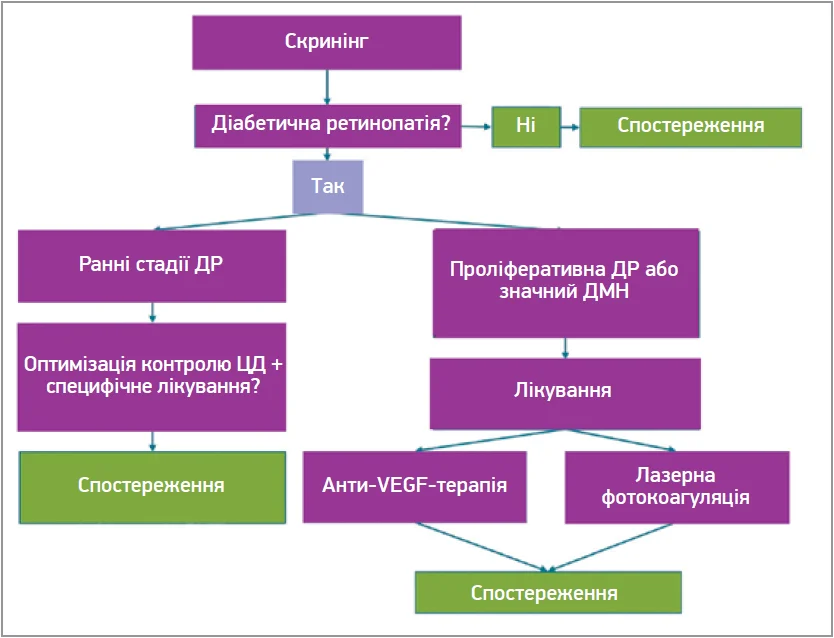 Рис. 1. Найпоширеніший алгоритм ведення пацієнтів із ДР
Рис. 1. Найпоширеніший алгоритм ведення пацієнтів із ДР
Типовий портрет пацієнта № 1: декомпенсований ЦД + неконтрольована неоваскуляризація
Пацієнтка з декомпенсованим ЦД, ускладненим ДР.
Без належного лікування в таких пацієнтів можуть виникнути серйозні ускладнення: ДМН, вітреальні крововиливи, тракційні відшарування, неоваскулярна глаукома, що значно погіршують зір або зумовлюють сліпоту. В разі лікування (анти-VEGF-терапія, лазерна фотокоагуляція, вітректомія) можлива стабілізація або значне зниження ризику втрати зору, однак уже встановлені ускладнення можуть залишати постійний дефіцит зору.
Офтальмологічний анамнез: останнє обстеження очей – 4 роки тому. Діагноз на той час: «Праве око: тяжка неПДР. Ліве око: легка неПДР». Найкраща коригована гострота зору 4 роки тому та під час поточного звернення: OD – 0,8 та 0,01, OS – 0,8 і 0,5 відповідно.
Під час поточного візиту при обстеженні переднього та заднього відрізків виявлено неоваскуляризацію райдужки біля зіничного краю в обох очах. За допомогою огляду очного дна виявлено ознаки проліферації: неоваскуляризацію в інших ділянках сітківки, «ватні» ексудати, інтраретинальні крововиливи, тверді ексудати.
Встановлено діагноз: «ПДР в обох очах. Клінічно значущий ДМН в обох очах».
Проведено консультацію з ретинальним хірургом. Призначено негайне лікування: інтравітреальні ін’єкції анти-VEGF в обидва ока.
! Анти-VEGF-препарати для інтравітреального введення безпосередньо зв’язуються з вже утвореним VEGF або його рецептором. Як синергічне лікування в цьому випадку також можна застосовувати фенофібрат, який активує РРАRα-рецептори, що знижують ретинальну експресію VEGF ядром клітини. Завдяки цьому безпосередньо знижується надмірне утворення VEGF [2]. Дослідження показують, що додавання фенофібрату до стандартного протоколу терапії ДМН сприяє зменшенню товщини макули в центрі та поліпшенню гостроти зору [3].
Типовий портрет пацієнта № 2: початковий ЦД + метаболічний синдром
Пацієнт, 52 роки. 5 років тому діагностовано ЦД 2 типу. Працює водієм великовантажного автомобіля. Звернувся в серпні 2023 р. для обстеження щодо перевірки придатності до роботи.
На момент початку дослідження: наявний метаболічний синдром, глікований гемоглобін – 9,7%, тригліцери – 1,8 ммоль/л, артеріальний тиск – 130/80 мм рт. ст.; ознак ДР не виявлено. Ускладнення відсутні, але наявний високий ризик розвитку ДР і серцево-судинних ускладнень. Стан очного дна – без патологічних змін, ознаки неоваскуляризації відсутні.
Без належного лікування в таких пацієнтів ризик прогресії ЦД і метаболічного синдрому високий. Можуть виникнути такі серйозні ускладнення, як ДР, ДМН, гіпертонічна ангіопатія, підвищення внутрішньоочного тиску, що зумовить погіршення зору. Крім того, значно зростає ризик інфаркту міокарда, інсульту, нефропатії. З лікуванням (контроль глікемії, корекція маси тіла, антигіпертензивна терапія, статини, зміна способу життя) можливі стабілізація стану, зниження ризику розвитку ретинопатії та системних ускладнень, збереження гостроти зору і профілактика серцево-судинних катастроф.
Для запобігання подальшому прогресуванню захворювання пацієнту призначено пероральні антигіперглікемічні препарати.
Під час другого візиту в лютому 2024 р. виявлено симптоми неПДР, але пацієнт не брав цього до уваги через побоювання, що може втратити роботу. В лютому 2025 р. діагностовано ПДР, пацієнт терміново госпіталізований; призначено інсулінотерапію. Гострота зору в правому оці в зазначений період знизилася з 1,0 до 0,05.
У наведеному випадку однією із причин стрімкого прогресування ДР міг стати професійний стрес. Дійсно, дослідження свідчать про можливий синергічний фактор, який часто ігнорують: тип професії та асоційований з ним стрес. Загроза втрати єдиного джерела доходу, недостатня соціальна підтримка становили фінансовий та емоційний тиск. Усе це супроводжувалося фізіологічним впливом стресу, адже хронічний стрес посилює системне запалення й ендотеліальну дисфункцію, що є доведеними механізмами прискорення мікросудинних ускладнень ЦД. Отже, професія пацієнта має значення. Крім того, у хворих із метаболічним синдромом збільшення вироблення кортизолу й адреналіну на тлі хронічного стресу в Україні в умовах війни спричиняє збільшення інсулінорезистентності та прогресування ожиріння. Тривала гіперглікемія в пацієнтів із ЦД 2 типу збільшує ризик мікроваскулярних ускладнень (нефропатія, ретинопатія) [1].
! Тип професії та пов’язаний з нею психоемоційний стрес є недооціненим, але потенційно вирішальним фактором у прогресуванні ПДР. Інтеграція цього фактора в клінічну оцінку може суттєво покращити прогнозування перебігу захворювання та результати лікування пацієнтів.
Типовий портрет пацієнта № 3: артеріальна гіпертензія + гіпертонічна ангіопатія
Пацієнтка з артеріальною гіпертензією, ускладненою змінами судин сітківки (звуження артерій, венозні перетини, підвищений ризик крововиливів). Стан очного дна: ознаки ангіопатії, без неоваскуляризації.
Без належного лікування в таких випадках ризик прогресії високий. Можуть виникнути такі серйозні ускладнення, як гіпертонічна ретинопатія, ДМН, тромбоз судин сітківки, крововиливи, що зумовлять значне погіршення зору. Крім того, в таких пацієнтів високий ризик подальших метаболічних змін із розвитком ЦД 2 типу, хронічної хвороби нирок і серцево-судинної патології. Лікування включає контроль АТ, корекцію способу життя, вплив на ліпіди, щоб попередити системні зміни та загальмувати розвиток ЦД.
ДР – головна причина погіршення і втрати зору в пацієнтів із ЦД. За наявними даними, 30% пацієнтів із ЦД страждають на ДР. На момент установлення діагнозу ЦД 2 типу вона наявна в 21% випадків [4]. Імовірність втрати зору в пацієнта із ЦД є у 29 разів вищою, ніж у людини без ЦД. Загрозливу для зору ДР мають 7% пацієнтів із ЦД; якщо хворий страждає на ЦД ≥10 років, цей показник підвищується до 16% [5-7]. Пацієнтів із ЦД слід інформувати про необхідність періодичного офтальмологічного скринінгу. Утім, навіть у розвинених країнах за консультацією до офтальмолога звертається лише 50% пацієнтів, які цього потребують, і лише половина з них у подальшому отримує адекватне лікування.
Фактори ризику ДР:
- тривалість ЦД – головний фактор ризику, що асоціюється з розвитком ДР;
- серед пацієнтів віком >30 років із ЦД 2 типу тривалістю <5 років у 40%, які приймають інсулін, і в 24%, котрі його не приймають, наявна ретинопатія;
- частота виявлення ДР збільшується до 84% і 53% відповідно за тривалості ЦД до 19 років;
- ПДР розвивається в 2% пацієнтів із ЦД 2 типу із тривалістю <5 років і в 25% хворих із тривалістю ЦД ≥25 років;
- глікемічний контроль – головний модифіковуваний фактор ризику. З моменту виникнення ДР тривалість ЦД стає менш важливим фактором ризику, ніж глікемічний контроль при прогнозі прогресування ДР [8].
Фактори ризику прогресування ДР: поганий глікемічний контроль, артеріальна гіпертензія, дисліпідемія (особливо специфічна з підвищенням рівня тригліцеридів), куріння, вік >60 років, тривалість ЦД >10 років, ожиріння, вагітність, хронічна хвороба нирок, інсулінотерапія.
Слід зазначити, що ДР прогресує навіть при контролі факторів ризику. Так, у дослідженні Steno‑2 показано, що ДР прогресує у кожного 2-го пацієнта із ЦД 2 типу через 8 років, незважаючи на інтенсивну багатофакторну терапію [9].
! Порушення метаболізму можуть розвинутися за багато років до того, як пацієнтам буде встановлено діагноз ЦД 2 типу [10, 11]. Саме тому пацієнти із ЦД 2 типу, які мали роки недіагностованого ЦД і мають значний ризик поширеної ДР на момент установлення діагнозу, повинні пройти первинне розширене та всебічне обстеження очей на момент установлення діагнозу [12]. Якщо при первинному огляді не виявлено діабетичних змін очей, подальші огляди проводять не рідше 1 разу на рік.
В офтальмологічних настановах щодо лікування ДР основним показником контролю рівня глюкози крові є глікований гемоглобін. Показано, що зниження його рівня щонайменше на 1% спричиняє зменшення:
- прогресування ДР на 17%;
- потреби в проведенні лазерної коагуляції на 29%;
- розвитку крововиливів у склоподібне тіло на 23%;
- ризику розвитку повної сліпоти на 16% [13].
Лікування ДР передбачає модифікацію факторів ризику прогресування ДР:
- антигіперглікемічну терапію;
- ліпідознижувальну терапію, асоційовану зі зниженням ризику розвитку ДР у пацієнтів із ЦД 2 типу на 33% [14];
- застосування фенофібрату, завдяки чому зменшується потреба в лазерному лікуванні та інтравітреальних введеннях анти-VEGF-препаратів у пацієнтів із ДР [15];
- антиагрегантну/антикоагулянтну терапію;
- лазерну фотокоагуляцію;
- інтравітреальні ін’єкції анти-VEGF-препаратів;
- вітректомію [8].
За останні десятиліття алгоритм ведення пацієнтів із ДР видозмінювався, до арсеналу лікаря-офтальмолога додавалися такі методи лікування, як лазерна фотокоагуляція та інтравітреальне введення анти-VEGF-препаратів, вітректомія. Але це все стосувалося здебільшого пізніх стадій – ПДР і такого грізного ускладнення, як ДМН. Водночас пацієнтів на ранніх стадіях найчастіше вели, використовуючи лише вичікувальну тактику або додавання симптоматичної неспецифічної терапії, що не мала доведеного впливу на сповільнення прогресування ДР. Це було пов’язано з різними причинами, в т. ч. з відсутністю специфічної патогенетичної терапії або інформації про її наявність. Але з плином часу підходи трансформувалися. Так, за останні кілька років змінилася сама парадигма лікування ДР – від реактивного спостереження та очікування до проактивного втручання (рис. 2). Мета – не просто лікувати ускладнення, а активно запобігати втраті зору.
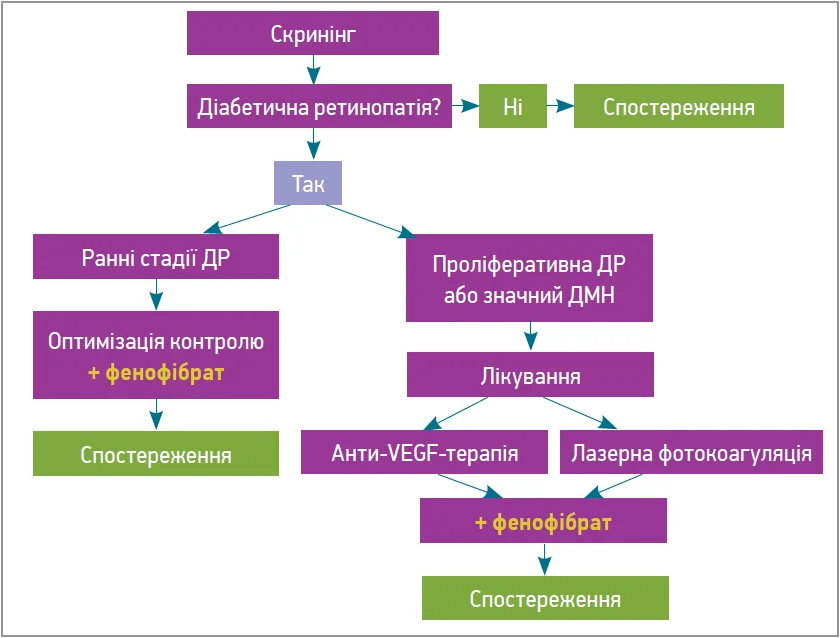 Рис. 2. Найдієвіший алгоритм ведення пацієнтів з ДР
Рис. 2. Найдієвіший алгоритм ведення пацієнтів з ДР
Це буде можливо завдяки:
- дотриманню графіку скринінгу;
- системному підходу – посиленому контролю системних факторів, включаючи глікемічний контроль, контроль АТ, рівнів ліпідів (і в цьому не обійтися без кооперації з ендокринологами або сімейними лікарями);
- проактивному втручанню на ранніх стадіях (раннє лікування неПДР);
- персоналізованій терапії у випадку ДМН та ПДР (у т. ч. використання комбінованих схем терапії із додаванням фенофібрату).
Початково фенофібрат використовувався лише як гіполіпідемічний засіб, але з роками досвіду і публікацією нових досліджень виявилося, що фенофібрат суттєво уповільнює прогресування ДР і цей ефект реалізується незалежно від контролю ліпідів. Тому зараз в інструкції до препарату є два незалежні один від одного показання: дисліпідемія та ДР. І вплив на ці стани реалізується через різні механізми.
Ліпідонезалежний:
- зниження активності VEGF;
- зниження апоптозу ендотеліальних клітин сітківки;
- зниження запалення;
- нейропротекція;
- антиоксидантна дія.
Ліпідозалежний:
- зниження рівня тригліцеридів;
- підвищення рівня ліпопротеїнів високої щільності (ЛПВЩ);
- зниження рівня ліпопротеїнів низької щільності;
- підвищення зворотного транспорту холестерину;
- підвищення ліполізу [16-20].
Інші терапевтичні напрями фенофібрату в пацієнтів із ЦД 2 типу передбачають вплив на перебіг:
- хронічної хвороби нирок (зменшення ризику появи мікроальбумінурії, регрес мікроальбумінурії до нормоальбумінурії, зменшення прогресування мікроальбумінурії у макроальбумінурію, запобігання зниженню швидкості клубочкової фільтрації);
- діабетичної нейропатії (зменшення частоти ампутацій нижніх кінцівок) [15].
Як показано в дослідженні D. Preiss і співавт. (LENS, 2024), фенофібрат зумовив зниження прогресування або необхідності лікування ДР. Ризик розвитку ДМН знизився на 50%, а макулопатії, що потребувала скерування до офтальмолога, – на 34% [21] (рис. 3).
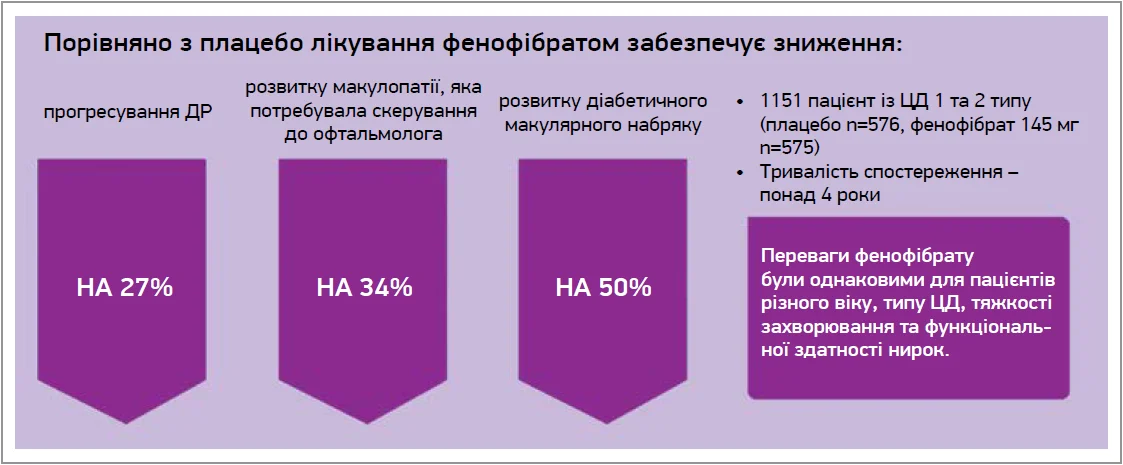 Рис. 3. Результати лікування фенофібратом у дослідженні D. Preiss і співавт. (2024)
Рис. 3. Результати лікування фенофібратом у дослідженні D. Preiss і співавт. (2024)
На фармацевтичному ринку України фенофібрат представлений оригінальним препаратом Трайкор® 145 мг. Його приймають по 1 таблетці 145 мг/добу. Для отримання позитивного клінічного ефекту термін застосування становить не менше 8 міс.
! Згідно з даними інструкції до медичного застосування, Трайкор® 145 мг показаний для зменшення прогресування ДР у пацієнтів із ЦД 2 типу та наявною ДР. Доведено, що препарат уповільнює прогресування ДР, особливо на ранніх стадіях, зменшує потребу в лазерній терапії та інтравітреальних введеннях, а також підвищує клінічну ефективність хірургічних методів лікування [17].
Отже, сучасне лікування ДР має бути більш проактивним, індивідуалізованим і заснованим на доказах, і це суттєво змінює підходи в менеджменті ДР, а саме додавання фенофібрату у вигляді специфічної терапії на ранніх стадіях ДР паралельно з контролем основних факторів ЦД, а у випадку ПДР – поєднання хірургічних методів лікування (інтравітреальні ін’єкції, лазерна фотокоагуляція) та фенофібрату задля досягнення оптимального результату для збереження зору пацієнта. Отже, фенофібрат має бути включений до базисної терапії пацієнтів із діагностованою ДР на будь-якій стадії, починаючи з легкої неПДР.
Шлях пацієнта із ДР – від бар’єрів до рішень
 Продовжила захід лікар-офтальмолог КНП «Житомирська обласна клінічна лікарня ім. О. Ф. Гербачевського» Оксана Василівна Гаврилюк, яка навела клінічні приклади ведення офтальмологічно та соматично тяжких пацієнтів із ДР.
Продовжила захід лікар-офтальмолог КНП «Житомирська обласна клінічна лікарня ім. О. Ф. Гербачевського» Оксана Василівна Гаврилюк, яка навела клінічні приклади ведення офтальмологічно та соматично тяжких пацієнтів із ДР.
Клінічний випадок № 1
Пацієнтка, 62 роки. ЦД 2 типу. На момент звернення в 2016 р. – стан після лазерної коагуляції сітківки, проведено лікування афліберсептом. Протягом декількох років спостереження в міру наростання ДМН вводили препарати анти-VEGF (2016, 2018, 2019). У 2021 р. через наявність ДМН вже на обох очах зроблено чергову ін’єкцію афліберсепту та до схеми лікування додано Трайкор® 145 мг. Протягом наступних 4 років пацієнтка по допомогу не зверталася і лише в 2025 р. прийшла на консультацію, оскільки це було вимогою лікаря-ендокринолога. Увесь цей час пацієнтка дотримувалася призначеного прийому Трайкор® 145 мг (фенофібрату). Картину очного дна під час візитів у 2021 та 2025 рр. представлено на рисунку 4. Оксана Василівна зазначила, що часто постає питання, як довго потрібно приймати призначене лікування. Однак пацієнти бачать результат, який дає фенофібрат, і самі не хочуть відмовлятися від подальшого прийому препарату. Тому лікування фенофібратом має бути тривалим.
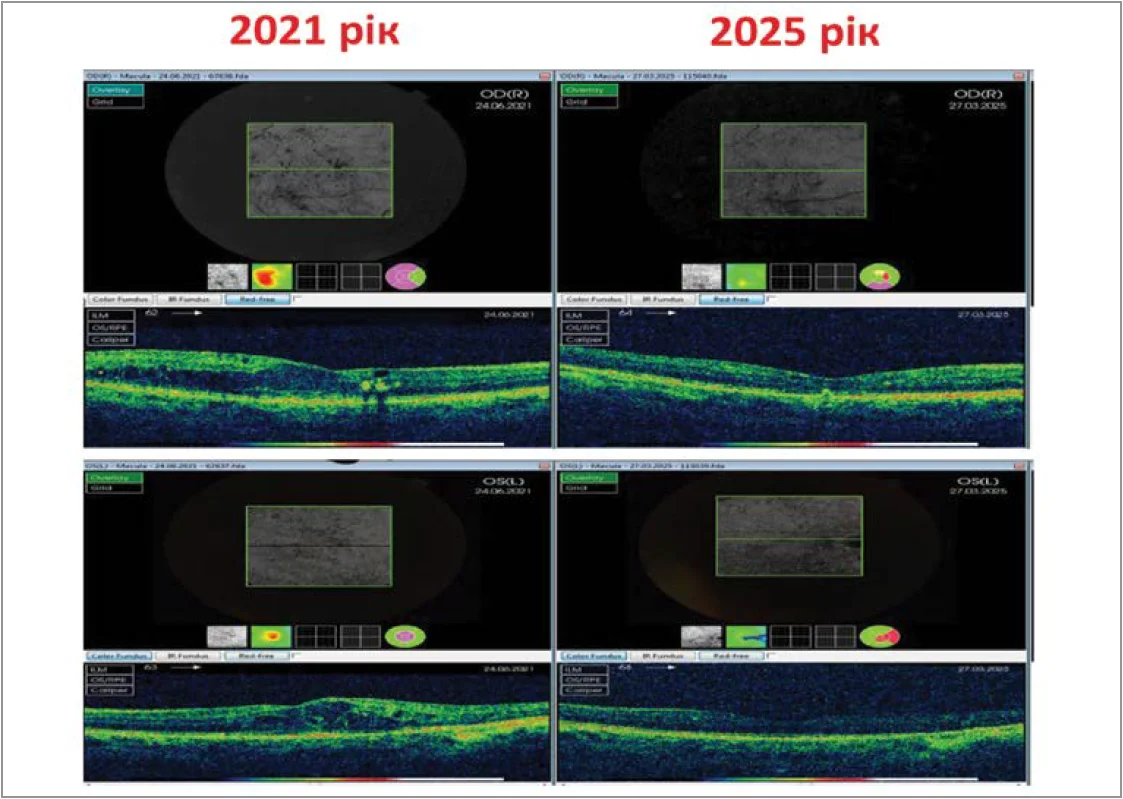 Рис. 4. Стан очного дна пацієнтки з клінічного випадку № 1 у 2021 та 2025 рр. (до та після 3,9 року застосування Трайкор® 145 мг)
Рис. 4. Стан очного дна пацієнтки з клінічного випадку № 1 у 2021 та 2025 рр. (до та після 3,9 року застосування Трайкор® 145 мг)
Клінічний випадок № 2
Пацієнт, 42 роки. ЦД 2 типу. Звернувся в 2015 р. Призначено лікування – інтравітреальні введення афліберсепту. Протягом наступних років неодноразово виконувалися повторні введення афліберсепту (2018, 2019), у 2019 р. також проведено лазерну фотокоагуляцію сітківки та до схеми лікування додано Трайкор® 145 мг (фенофібрат). Хворий ретельно дотримувався призначеного лікування, проходив регулярні обстеження, кинув курити. Останній візит був у 2024 р.: пацієнт повністю задоволений результатами лікування і навіть не відчував необхідності в повторному зверненні. У грудні 2025 р. у телефонному режимі пацієнт повідомив, що його стан стабільний, бачить добре, погіршення немає і він продовжує дотримуватися попередніх призначень.
Клінічний випадок № 3
Пацієнтка, 68 років. ЦД 2 типу, ожиріння, пересування значно утруднене. Під час звернення в 2023 р. – клінічно значущий ДМН. Від інтравітреальних ін’єкцій категорично відмовилася. Під час одного з наступних звернень у 2024 р. призначено Трайкор® 145 мг (фенофібрат), який пацієнтка приймала з перервами, курсами по 3 міс, самостійно скасовуючи та відновлюючи прийом. При цьому симптоматика і картина очного дна були без покращення. Під час візиту у 2025 р. було відмічено значне покращення картини очного дна (рис. 5). Пацієнтка спостерігала покращення загального стану, відзначала, що їй легше рухатися, і ці зміни відбулися на фоні переходу на постійний прийому препарату.
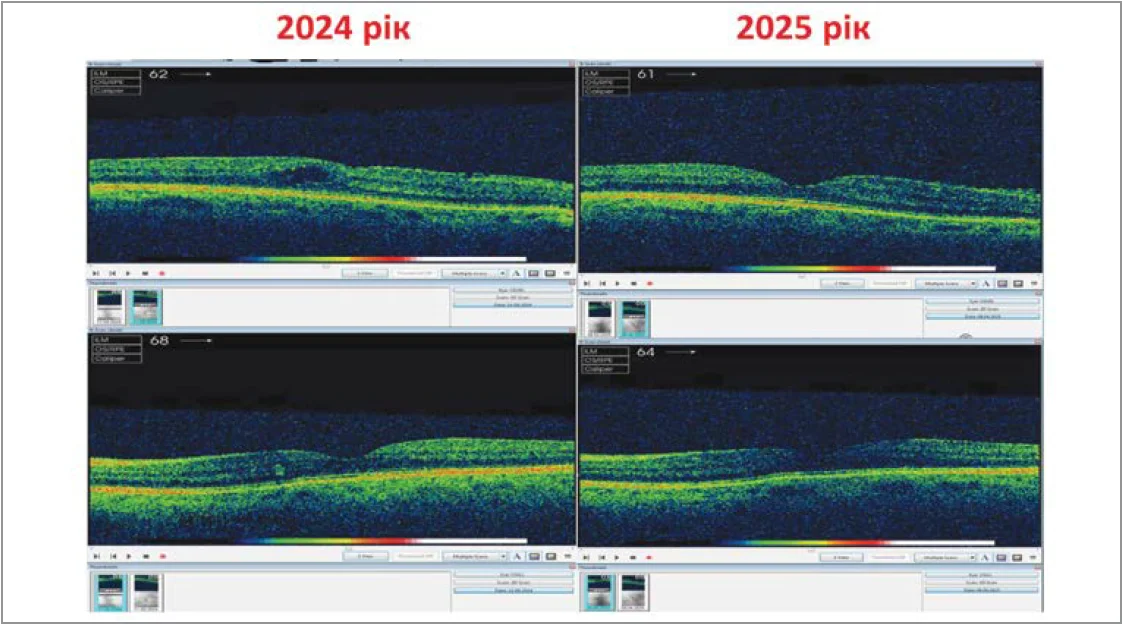 Рис. 5. Стан очного дна пацієнтки з клінічного випадку № 3 у 2024 та 2025 рр. (до та через 4 міс після переходу на постійний прийом Трайкор® 145 мг)
Рис. 5. Стан очного дна пацієнтки з клінічного випадку № 3 у 2024 та 2025 рр. (до та через 4 міс після переходу на постійний прийом Трайкор® 145 мг)
Клінічний випадок № 4
Пацієнт, 34 роки. ЦД 1 типу. Початкове звернення – в 2022 р. Протягом 2022-2024 рр. неодноразово проводилися анти-VEGF-терапія, лазерна коагуляція сітківки, проте тривалого ефекту таке лікування не дало. У 2024 р. спостерігали гемофтальм, було виконано введення інтравітреальних ін’єкцій в обидва ока та, після обговорення з пацієнтом й отримання від нього згоди (оскільки на момент призначення в інструкції препарату було відсутнє показання до застосування при ЦД 1 типу), до схеми лікування додано Трайкор® 145 мг (фенофібрат). Під час наступних візитів у 2024 та 2025 рр. – без погіршень, гемофтальму не спостерігали. Інтравітреальні ін’єкції більше не проводилися, пацієнт приймає Трайкор® 145 мг (фенофібрат) і перебуває під спостереженням.
Клінічний випадок № 5
Пацієнтка Б., 51 рік, ЦД 2 типу, тяжка форма, стан компенсації. Діабетична полінейропатія нижніх кінцівок. Діабетична мікроангіопатія нижніх кінцівок ІІ ст., ПДР обох очей. Хворіє на ЦД 2 типу >20 років.
Проведене лікування: анти-VEGF-терапія 5 завантажувальними дозами за протоколом і згодом кожні 6 міс. У 2016 р. виконано лазерну коагуляцію сітківки, але стабільність не спостерігалася ані в якості зору, ані в морфології сітківки; протягом 2018-2021 рр. продовжували введення анти-VEGF-препаратів.
У 2021 р. відбувся епіретинальний крововилив правого ока, введено останню дозу анти-VEGF-препарату, призначено Трайкор® 145 мг (фенофібрат). Через 6 міс хвора спостерігала значне покращення тактильної чутливості кінчиків пальців рук. З боку очного дна також відзначене суттєве покращення, яке було стабільним протягом наступних візитів у 2022-2023 рр.
! Отже, призначення пацієнтам фенофібрату (Трайкор® 145 мг) дозволило уповільнити прогресування ДР. Застосування фенофібрату разом з анти-VEGF-терапією дозволило посилити ефект останньої, збільшити інтервали між ін’єкціями, тобто зменшити потребу в них, а в окремих випадках навіть відмовитися від них взагалі. У період воєнного стану в Україні, епідеміологічних обмежень, нестабільної фінансової спроможності пацієнтів застосування фенофібрату також може бути альтернативою при тимчасовому відтермінуванні запланованої анти-VEGF-терапії.
Сучасні можливості ведення пацієнтів із ДР
 Лікар-офтальмолог, ретинолог, лазерний хірург медичного центру TopMedical Вадим Геннадійович Печерій (м. Дніпро), прокоментував виступи колег щодо сучасних можливостей ведення пацієнтів із ДР. Зі свого боку він також поділився позитивним досвідом застосування фенофібрату (Трайкор® 145 мг), зокрема в пацієнтів молодого віку із ЦД 1 типу з ознаками неоваскуляризації, яку спочатку купіювали за допомогою анти-VEGF-агентів, а потім виконували панретинальну лазерну коагуляцію. Незважаючи на це, неоваскуляризація прогресувала, а інтервали між ін’єкціями ставали меншими. Після додавання фенофібрату спостерігали стабілізацію, в деяких пацієнтів – припинення неоваскуляризації протягом років, отже, потреби в проведенні анти-VEGF-терапії не було.
Лікар-офтальмолог, ретинолог, лазерний хірург медичного центру TopMedical Вадим Геннадійович Печерій (м. Дніпро), прокоментував виступи колег щодо сучасних можливостей ведення пацієнтів із ДР. Зі свого боку він також поділився позитивним досвідом застосування фенофібрату (Трайкор® 145 мг), зокрема в пацієнтів молодого віку із ЦД 1 типу з ознаками неоваскуляризації, яку спочатку купіювали за допомогою анти-VEGF-агентів, а потім виконували панретинальну лазерну коагуляцію. Незважаючи на це, неоваскуляризація прогресувала, а інтервали між ін’єкціями ставали меншими. Після додавання фенофібрату спостерігали стабілізацію, в деяких пацієнтів – припинення неоваскуляризації протягом років, отже, потреби в проведенні анти-VEGF-терапії не було.
Експерт розповів про багаторічний шлях застосування фенофібрату в своїй практиці. Від початку препарат призначали фактично поза показанням, маючи суто патогенетичне підґрунтя до цього та дані кількох масштабних досліджень (FIELD, ACCORD), які згодом і стали основою для появи в інструкції показання «ДР при ЦД 2 типу», після чого препарат почали дуже активно застосовувати. Перший час було певне непорозуміння між офтальмологами, ендокринологами, терапевтами та сімейними лікарями щодо того, хто саме повинен призначати цей препарат, але доволі швидко комунікацію вдалося налагодити. Згодом фенофібрат почали призначати в т. ч. пацієнтам із ЦД 1 типу, що в деяких випадках надавало навіть кращого результату, ніж у хворих із ЦД 2 типу. Наразі доступні дані дослідження LENS [22], а також очікується оприлюднення результатів дослідження FAME1 EYE [23] за участю пацієнтів із ЦД 1 типу. Отже, найближчим часом очікується розширення показань в інструкції щодо застосування фенофібрату в цієї категорії пацієнтів.
Наприкінці виступу спікер зауважив, що багато його колег також спостерігають позитивний досвід застосування фенофібрату в своїх пацієнтів та із задоволенням діляться своїми кейсами, демонструючи позитивний ефект у реальній клінічній практиці.
Список літератури знаходиться в редакції.
Підготувала Віталіна Хмельницька
Медична газета «Здоров’я України 21 сторіччя» № 3 (614), 2026 р



