23 березня, 2023
Вплив симптоматичної фітотерапії на стан мікробіому та раціональне призначення антибіотиків
Епітеліальні поверхні тіла людини виконують бар’єрну функцію, а також мають вирішальне значення для захисту від патогенних мікроорганізмів. Зокрема, вони є своєрідною домівкою для мікробіому, який, своєю чергою, являє собою частину бар’єрної складової епітелію. За відсутності порушень існує добре збалансований та взаємовигідний симбіоз між мікробіомом і його хазяїном. Тоді як хазяїн забезпечує середовище проживання та поживні речовини для мікробіоти, вона, зі свого боку, сприяє підтримці гомеостазу, оскільки запобігає колонізації патогенними мікроорганізмами і впливає на стан імунної системи. Порушення стану біологічної рівноваги підвищує сприйнятливість до інфекцій та запалення.
Відомо, що основою для лікування бактеріальних інфекцій є антибіотикотерапія, але її часто призначають передчасно і невиправдано, оскільки багато бактеріальних інфекцій є самообмежувальними та минають без лікування. Однак застосування антибіотиків може наражати пацієнта на ризик розвитку несприятливих явищ, як-от збільшення імовірності вагінального кандидозу, підвищення ризику формування резистентності до протимікробних препаратів, а також порушення стабільності мікробіому. Вплив останнього може бути негативнішим і тривалішим, ніж самообмежувальних та некритичних інфекцій, для лікування яких призначалися антибіотики.
Фітопрепарати для лікування неускладнених інфекцій
Ефективною альтернативою для лікування неускладнених інфекцій є лікарські засоби на основі рослинних препаратів або їхніх екстрактів, які зазвичай мають позитивне співвідношення користь-ризик (Lee J.Y. et al., 2016). На відміну від антибіотиків або протизапальних засобів, фітопрепарати зазвичай не спрямовані на конкретні патогени чи сигнальні шляхи; їхня ефективність базується на багатоцільовому підході.
Для багатьох поширених та рецидивуючих інфекцій, як-от урогенітальні інфекції (Wawrysiuk S. et al., 2019) або інфекції верхніх і нижніх дихальних шляхів (Palm J., 2017; Kardos P. et al., 2021), доступні ефективні й безпечні варіанти фітотерапії. Наприклад, варіанти фітотерапії неускладнених інфекцій сечовивідних шляхів (ІСШ) включають фітокомпозицію із Centaurii herba, Levistici radix та Rosmarini folium (Канефрон® Н, компанія «Біонорика СЕ», Німеччина) (Wagenlehner F.M. et al., 2018). Важливо, що дослідження з такими препаратами демонструють таке: фітотерапія може бути ефективною для полегшення симптомів, а це, своєю чергою, спричиняє зменшення застосування пацієнтами антибіотиків, забезпечуючи водночас сприятливі профілі безпеки.
Ефективність фітотерапії у разі ІСШ
Для демонстрації ефективної та безпечної фітотерапії неускладнених ІСШ розглянуто фітопрепарат, який містить як активний фармацевтичний інгредієнт – фітокомбінацію BNO 2103, стандартизовану за вмістом ключових біологічно активних речовин лікарських рослин, з Rosmarini folium, Centaurii herba і Levistici radix (Канефрон®, компанія «Біонорика СЕ», Німеччина).
Ефективність препарату доведено в подвійному сліпому плацебо-контрольованому рандомізованому клінічному дослідженні з подвійною імітацією (Wagenlehner F.M. et al., 2018). У цій роботі 325 рандомно відібраних жінок отримували як лікування фітопрепарат і плацебо, що імітує фосфоміцин, а 334 учасниці – антибіотик фосфоміцину трометамол і плацебо, що імітує Канефрон® Н. Після аналізу результатів учені відзначили, що ефективність фітозасобу не поступалася такій антибіотикотерапії за неускладнених гострих ІСШ нижніх відділів (з огляду на необхідність додаткового лікування антибіотиками).
Крім того, ефективність препарату в умовах дійсної клінічної практики продемонстровано в нещодавно опублікованому дослідженні, яке ґрунтувалося на аналізі бази даних, що містить інформацію про 160 000 випадків лікування ІСШ антибіотиками або фітокомбінацією BNO 2103 (Höller M. et al., 2021). Висновки цієї роботи підтверджують результати вищезазначеного клінічного дослідження – відсоток хворих, котрі потребували додаткового призначення антибіотиків із 1-го по 30-й день, також був майже однаковим в обох групах, а ймовірність спорадичних або частих рецидивуючих епізодів ІСШ була нижчою після лікування лікарським засобом рослинного походження. Дивує те, що потреба в додатковій антибіотикотерапії з 31-го по 356-й день була вищою в групі пацієнтів, які отримували антибіотики як початкове лікування неускладнених випадків ІСШ. Потенційним поясненням цього може бути негативний вплив антибіотиків на специфічний мікробіом і стан локальної імунологічної реактивності. Вважається, що здорова мікрофлора кишечнику, піхви та сечовивідних шляхів захищає від ІСШ, отже, зміна складу мікробіому залучена до етіології ІСШ (Mestrovic T. et al., 2020).
Терапевтичний ефект фітопрепарату, який є багатокомпонентною сумішшю, що має більше одного механізму дії, можна пояснити іншими терапевтичними ефектами, крім антибактеріального. Так, його складники перешкоджають адгезії патогенних мікроорганізмів в урогенітальному тракті, чинять спазмолітичну, сечогінну, антиоксидантну (тобто протидіє фактору патогенності бактерій), протизапальну й антиноцицептивну дію, що перешкоджає реалізації інфекційного процесу та сприяє успішному лікуванню.
Збереження мікробіому кишечнику при застосуванні BNO 2103: результати дослідження на моделі мишей
Вважається, що лікарські засоби рослинного походження зберігають мікробіом і його захисну роль. У 2017 році K.G. Naber і співавт. опублікували попередні результати дослідження на моделі мишей, метою якого було вивчення впливу фітопрепаратів на мікробіом кишечнику. Під час роботи вчені проаналізували зразки випорожнень мишей за допомогою секвенування 16S рРНК. Миші отримували щоденні пероральні дози антибіотика нітрофурантоїну протягом 7 днів, воду (як розчинник без діючої речовини; контрольна група), фітокомбінацію BNO 2103 або одноразову дозу антибіотика фосфоміцину в 1-й день. Дози BNO 2103 становили 65 та 1333 мг/кг, що еквівалентно 1- та 20-кратній рекомендованій дозі препарату для людини. Зразки калу зібрали до початку лікування, на 2-й (для мишей, які отримували фосфоміцин) або на 7-й день (решта груп).
За результатами секвенування виявлено значні зміни в складі мікробіому кишечнику під впливом антибіотиків (рис.); такі зміни були виразнішими в групі фосфоміцину: при одноразовому введенні деякі родини бактерій повністю зникали з мікробіому кишечнику та не відновлювалися впродовж подальших днів, у які лікування не проводилося. В мишей, котрі отримували фітотерапевтичне лікування, різноманітність кишкових бактерій здебільшого не змінилася (як і в контрольній групі мишей, що отримували воду, без діючих речовин). Навіть за одержання 20-кратного еквівалента рекомендованої дози для людини мікробіом кишечнику мишей майже не зазнав змін. Ці висновки підтверджують мікробіотично-зберігальну дію фітокомбінації, а також доповнюють існуючі докази щодо сприятливого профілю безпеки фітозасобів.
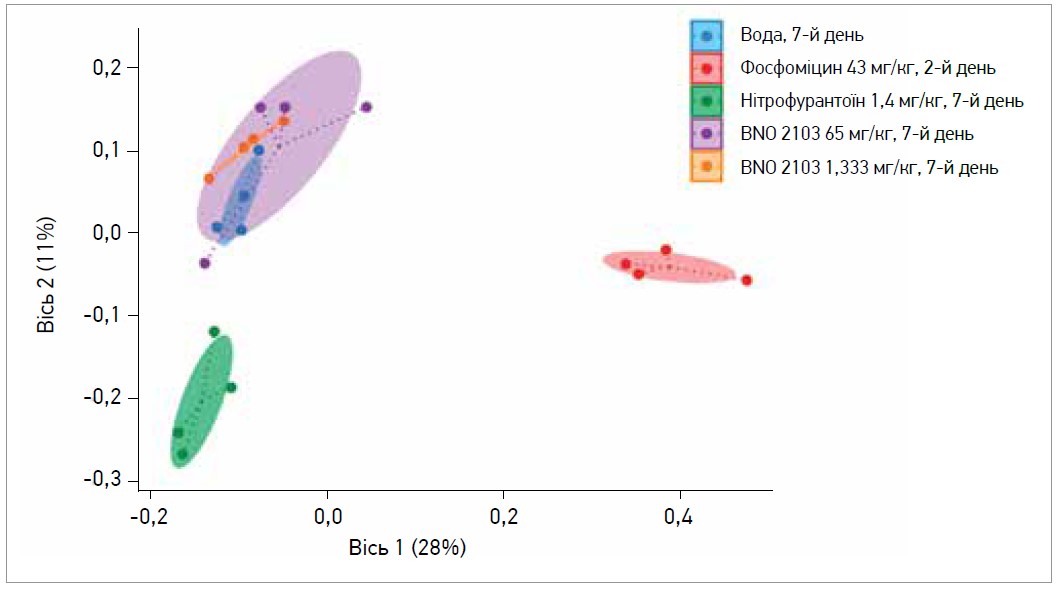
Рис. Зміни в мікробіомі після лікування мишей фосфоміцином (2-й день після 1 дози), нітрофурантоїном (7-й день) та BNO 2103 (7-й день) порівняно з контрольною групою (вода, 7-й день)
Схожість між окремими бактеріальними складами вивчали за допомогою методу головних компонент для даних секвенування 16S рРНК. Окремі зразки (кольорові крапки) добре кластеризуються відповідно до груп лікування. Еліпси представляють 95% довірчі інтервали, які базуються на багатовимірному t-розподілі для кожної групи. Диференційна кластеризація зразків після лікування фосфоміцином або нітрофурантоїном свідчить про зміни їхнього складу після лікування мишей антибіотиками, тоді як миші, котрі отримували BNO 2103 або контроль, кластеризуються разом, що свідчить про схожий бактеріальний склад. Координати представляють 28 та 11% загальної дисперсії набору даних.
Висновки
1. Терапія фітопрепаратами є доцільною за неускладнених гострих ІСШ. Її ефективність не поступається такій антибіотикотерапії, особливо в разі порівняння необхідності додаткового лікування антибіотиками.
2. Терапевтичний ефект фітопрепарату можна пояснити іншими терапевтичними ефектами, крім антибактеріального. Його складники перешкоджають адгезії патогенних мікроорганізмів в урогенітальному тракті, чинять спазмолітичну, сечогінну, антиоксидантну, протизапальну й антиноцицептивну дію.
3. Прийом фітозасобів не змінює бактеріального складу мікробіому кишечнику, що підтверджує їхню мікробіотично-зберігальну дію та потенційно попереджує розвиток ускладнень.
За матеріалами: Nausch B., Bittner C.B., Höller M. et al. Contribution of Symptomatic, Herbal Treatment Options to Antibiotic Stewardship and Microbiotic Health. Antibiotics 2022, 11, 1331.
https://doi.org/10.3390/antibiotics11101331
Підготувала Юлія Котикович
Медична газета «Здоров’я України 21 сторіччя» № 4-5 (540-541), 2023 р.