31 березня, 2023
Управління болем і запаленням у разі захворювань опорно‑рухового апарату: час змін?
Гостре запалення – це універсальна біологічно виправдана адаптивна реакція організму, спрямована на знищення (елімінацію) шкідливого чинника (антигена) та ліквідацію спричинених ним змін у тканинах. Порушення перебігу цього процесу може призвести до неоптимальних результатів. Для втамуваня болю та запалення часто застосовуються нестероїдні протизапальні засоби (НПЗЗ). Зазначені препарати швидко усувають симптоми запалення та мають потенційну цінність у розриві больового циклу, проте їх використання може зумовлювати шкідливе маскування болю, перешкоджати загоєнню тканин, спричиняти хронізацію запального процесу. Потенційно серйозні побічні ефекти НПЗЗ добре встановлені. Наразі є великий інтерес до потенційного переходу від пригнічення запалення до його розрішення, тобто завершення фізіологічним шляхом із повним відновленням структури та функції пошкодженої тканини, в рамках нової галузі наукових досліджень, яка називається «резолюційна фармакологія» (resolution pharmacology).
Гомеостаз у разі болю та запалення
Підтримання гомеостазу тканин, загоєння та відновлення функції під час запального процесу включають як прозапальну фазу, так і фазу розсмоктування (резолюції). Останні дослідження свідчать про складний, жорстко регульований процес, коли обидві фази починаються після травми чи інфекції, а потім перебігають паралельно, а не як лінійна послідовність кроків. Було припущення, що «початок програмує кінець», коли запальні клітини, залучені до активної фази запалення, зазнають функціональної реполяризації, а потім сприяють початку розсмоктування.
Багато прозапальних медіаторів можуть одночасно ініціювати програму активного розсмоктування. При пошкодженні тканини прозапальні макрофаги вивільняють медіатори, зокрема цитокіни, лейкотрієни та простагландини (наприклад, простагландин PGE2). Вони зумовлюють збільшення кровотоку, мікросудинну проникність і набряк. Поліморфноядерні нейтрофіли (ПМН) швидко проникають через капіляри, поглинають і розкладають патогени. Стадія розсмоктування ініціюється під час запалення апоптотичними ПМН, що вивільняють спеціалізовані медіатори SPM (specialized pro-resolving mediators), які пригнічують подальшу міграцію. Потім макрофаги поглинають апоптичні нейтрофіли (ефероцитоз), перетворюючи їх на макрофаги фази розсмоктування.
! Перемикання фенотипу макрофагів із прозапального на протизапальний сприяє імунній толерантності після розсмоктування та запобігає автоімунним процесам. Подібним чином зміна фенотипу нейтрофілів призводить до перепрограмування на протизапальний тип, що спричиняє зворотну міграцію нейтрофілів.
Усі ці процеси сприяють відновленню гомеостазу тканин і поверненню до нормального функціонування. Цікаво, що нещодавно було виявлено наступну фазу, яка виникає після зникнення запалення, вона включає третю хвилю лейкоцитів. Ідентифікація цих взаємопов’язаних етапів загоєння та медіаторів надає дослідникам нові терапевтичні можливості.
Показання, дія та ризики НПЗЗ
НПЗЗ широко рекомендуються для короткочасного лікування болю та симптомів остеоартриту (ОА). Основним механізмом їхньої дії є інгібування каскаду арахідонової кислоти, зокрема ізоферментів циклооксигенази (ЦОГ) 1 і 2, що перешкоджає утворенню медіаторів запалення, у тому числі пророзрішуючих. Тому застосування НПЗЗ може призвести до хронізації запального процесу.
НПЗЗ можуть стати в нагоді за наявності сильного гострого больового синдрому на тлі вираженого запалення. При цьому відомо, що близько 2% людей гіперчутливі до подібних препаратів. НПЗЗ спричиняють небажану токсичну дію на систему травлення, серцево-судинну систему, нирки. Особливо небезпечним є такий вплив на організм людей із груп ризику: дітей та осіб літнього віку. Однак багато медичних працівників не усвідомлюють важливості дози, способу введення, тривалості лікування, віку пацієнта та взаємодії ліків. Як наслідок, можуть бути не враховані всі ризики й переваги. Зокрема, часто не зважають, що широко доступні НПЗЗ, як-от ібупрофен і диклофенак, утричі підвищують ризик виникнення інсульту. Диклофенак також у 4 рази збільшує смертність від серцево-судинних захворювань, водночас подвоюючи смертність від різних причин. Призначення селективних інгібіторів ЦОГ-2 справді знижує ризик шлунково-кишкових розладів, але їх використання було затьмарене досвідом із рофекоксибом, що призвів до серйозних серцево-судинних подій.
! Дія НПЗЗ може перешкоджати відновленню кісток і сухожиль, що призводить до невдалого загоєння в місці пошкодження та підвищеного ризику ретравматизації.
В експериментальному дослідженні, опублікованому 2018 року Sauerschnig і співавт., селективні інгібітори ЦОГ-2 спричиняли порушення загоєння сухожиль, послаблювали механічну стабільність і знижували вміст PGE2 у синовіальній рідині. Perry та співавт., проаналізувавши рентгенограми пацієнтів, помітили зв’язок між регулярним застосуванням НПЗЗ та прогресуванням ОА колінного суглоба.
На відміну від вищезазначеного, систематичні огляди приблизно того самого часу Duchman і співавт., Ghosh і співавт. та Constantinescu та співавт. дійшли висновку, що немає достатніх доказів за чи проти НПЗЗ після гострої травми, доцільність їх використання має визначатися в кожному конкретному випадку. Проте вибір препарату може бути важливим у світлі даних Sauerschnig і співавт. стосовно того, що селективні інгібітори ЦОГ-2 можуть негативно впливати на загоєння м’яких тканин після хірургічного втручання як у тварин, так і в людей.
Наявні підходи до лікування болю можуть виявитися помилковими. Нещодавнє багатоцентрове клінічне дослідження свідчить про те, що лікування гострого запалення за допомогою НПЗЗ може бути контрпродуктивним для довгострокових результатів серед хворих на біль у попереку. Parisien і співавт. проаналізували транскриптоми в клітинах периферичного імунітету 98 пацієнтів із гострим болем у попереку.
Зникнення болю через 3 міс було пов’язане з тисячами динамічних транскрипційних змін, але жодних змін не виявлено в тих, хто мав постійний біль.
Інші підходи до нехірургічного лікування захворювань ОРА
Лікування захворювань опорно-рухового апарату (ОРА) ускладнюється неповним розумінням патофізіологічних процесів і механізмів дії багатьох сучасних методів терапії.
Відпочинок, лід, стиснення та підняття (Rest, Іce, Сompression and Еlevation – RICE) є традиційними стратегіями після травми кінцівки. Їх можна доповнити вправами на розтяжку, відновлення амплітуди рухів та ізометричними вправами, а також програмою підтримки фізичної форми.
Парацетамол корисний для лікування легкого та середнього ступеня гострого / загострення хронічного болю або лихоманки, але не має протизапальної дії. Вважається, що він діє централізовано, пригнічуючи ЦОГ-2 і канабіноїдні рецептори в мозку. Хоча загалом вважається безпечним у рекомендованих дозах, огляд Національного інституту здоров’я та вдосконалення медичної допомоги Великої Британії (NICE) показує, що парацетамол має «низьку ефективність» при ОА.
На вищій сходинці болю опіоїди мають потужний центральний болезаспокійливий і седативний ефекти, але пов’язані з такими побічними явищами, як сонливість і закреп. За тривалого застосування існує ризик звикання, й опіоїди самі по собі можуть бути менш ефективними для лікування хронічного болю з ушкодженнями ОРА чи без них, аніж неопіоїдні засоби.
Кортикостероїди в таблетках або ін’єкціях широко застосовуються при невиліковних хворобах ОРА й ревматичних захворюваннях. Їхня швидка протизапальна та знеболювальна дія опосередковується активацією глюкокортикоїдних рецепторів і пригніченням метаболізму в клітинах запалення. Кортикостероїди уповільнюють загоєння й зумовлюють місцеву атрофію тканин, а за тривалого застосування можуть призвести до остеопорозу, гіпертензії, діабету, збільшення ваги та схильності до інфекцій. ОА колінного і тазостегнового суглобів є поширеною проблемою, для котрої поодинокі внутрішньосуглобові ін’єкції кортикостероїдів вважаються безпечними й ефективними для короткочасного полегшення болю та покращення функції. Однак існує ризик, що повторні ін’єкції можуть призвести до хондротоксичності та прискореної втрати хряща.
Для пацієнтів із ревматичними захворюваннями тривале лікування протиревматичними засобами, як-от метотрексат, гідроксихлорохін і сульфасалазин, допомагає полегшити біль і запалення шляхом загального пригнічення імунної системи. Якщо таке лікування спричиняє ускладнення, може бути показаний перехід на біопрепарати та біосиміляри, які зменшують запалення шляхом дії на певні клітини й білки.
Побічні ефекти від використання імунодепресантів є поширеними та потенційно небезпечними для життя, а деякі нові препарати є дорогими.
Тобто поточне лікування захворювань ОРА є різним за ефективністю, але завжди з потенційними серйозними побічними ефектами.
Прорезолюційна терапія та прорезолюційні препарати
Наразі є великий інтерес до лікування запальних захворювань за допомогою підходу, спрямованого на вирішення проблеми «в зародку». Вже зареєстровано близько 1100 патентів на потенційні ліки, що сприяють оздоровленню, і щонайменше 13 великих фармацевтичних компаній виділяють ресурси на цю галузь.
! Прорезолюційний підхід передбачає посилення або стимуляцію чинників, необхідних для усунення спонукального стимулу, послаблення прозапальної сигналізації та стимулювання кліренсу лейкоцитів. Центральними для цього є SPM, які в низьких дозах впливають на специфічні імунні рецептори та ноцицептори, обмежуючи біль і запалення залежно від часу.
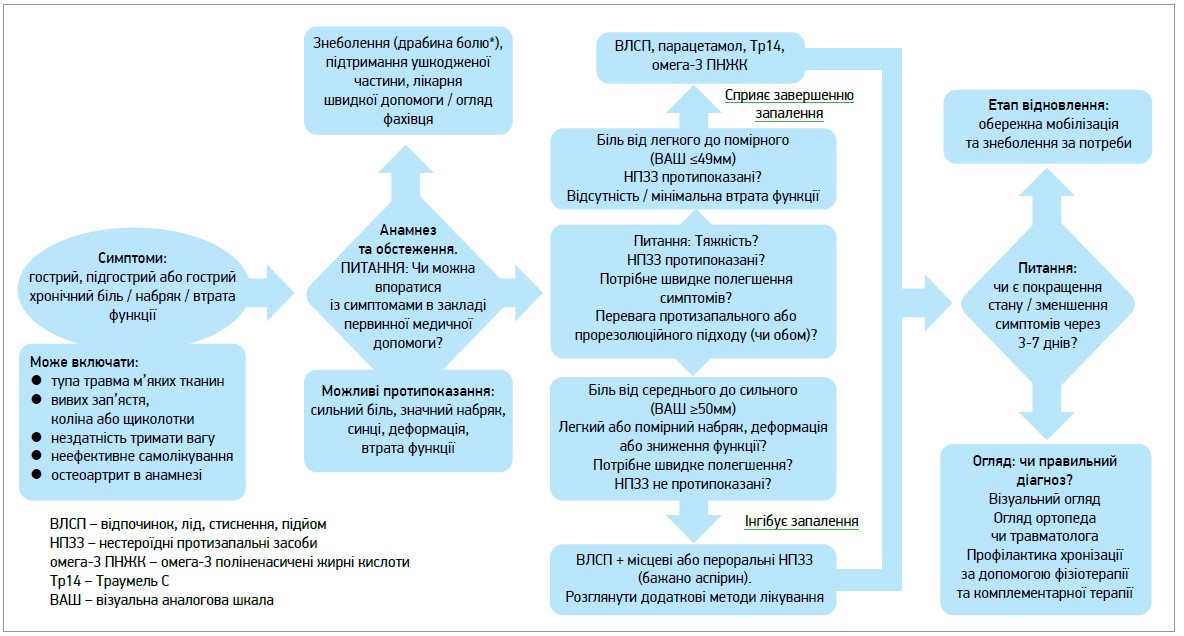
Наведений на рисунку алгоритм прорезолюційної терапії на етапі первинної медичної допомоги для гострого, підгострого або загострення хронічного болю при хворобах ОРА особливо важливий для пацієнтів із легкими та помірними симптомами, коли є бажання уникнути або доповнити дію НПЗЗ.
Рис. Прорезолюційний підхід до ведення болю і запалення, пов’язаних із захворюваннями ОРА
Примітка. «Драбина болю» Всесвітньої організації охорони здоров’я класифікує біль за ступенем тяжкості та рекомендує серію чимраз потужніших знеболювальних кроків залежно від реакції.
Оскільки SPM є ліпідними медіаторами, біосинтезованими з ω3-жирних кислот, є інтерес до ефектів відповідних добавок, уживання котрих може збільшити ендогенні рівні SPM і запобігти болю та запаленню при таких захворюваннях, як ревматоїдний артрит і діабетична нейропатія.
! Траумель С – природний засіб, що складається з 14 компонентів, розроблений приблизно 60 років тому. Він зареєстрований як комплексний гомеопатичний препарат, який має потужну доказову базу щодо ефективності та безпечності.
Наприклад, було показано, що він пригнічує секрецію цитокінів IL-1β, TNF та IL-8 у стані спокою, а також в активованих імунних клітинах. Порівняно з НПЗЗ Траумель С здатний модулювати різні запальні процеси. Диклофенак, наприклад, пригнічує ЦОГ-2, а отже, вироблення PGE2. Траумель С не пригнічує індукцію ЦОГ-2, що забезпечує нормальну активацію залежних від ЦОГ/5-ліпоксигенази шляхів на ранній стадії запалення.
Використовуючи модель мишачого перитоніту, Jordan і співавт. продемонстрували, що Траумель С сприяє біосинтезу SPM і залученню лейкоцитів і макрофагів, потрібних для очищення апоптичних PMN і «клітинного сміття» шляхом ефероцитозу. Результатом є скорочення індексу розсмоктування, що сприяє швидшому зникненню запалення.
Ці висновки підтверджуються Laurent і співавт., які продемонстрували, що Траумель С знижує рівні мРНК у шляху синтезу лейкотрієнів у моделі рани мишей, що може пояснити деякі з його протизапальних властивостей. Окрім того, Траумель С зумовив транскриптомні зміни в клітинах, присутніх у рані. Це відображає підвищений рівень регуляторних Т-клітин, виявлених у ранах, оброблених Траумелем С.
Ще один цікавий висновок цієї роботи полягає в тому, що механізми дії диклофенаку та Траумелю С відрізняються залежно від стадії запалення. Хоча на початкових етапах відбувається приблизно 50% перекриття, процеси, на які вони діють, потім розходяться. Laurent і співавт. виявили, що спільні молекулярні шляхи, які включають позаклітинний матрикс, уроджений імунітет, міграцію клітин і запалення, зазнають впливу диклофенаку відразу після травми. Введення Траумелю С дало ефект на пізніших стадіях загоєння рани.
Інші попередні доклінічні дані також указують на те, що Траумель С модулює сигнальні шляхи та поведінку багатьох типів імунних клітин, що сприяє зникненню запалення.
Рандомізовані клінічні випробування й обсерваційні дослідження загалом підтверджують ефективність і безпеку Траумелю С для лікування різних захворювань ОРА, включаючи гострі розтягнення зв’язок гомілковостопного суглоба, тендинопатію, епікондиліт і ОА колінного суглоба (в поєднанні з Zeel T). Виявляється, він такий же ефективний, як пероральні НПЗЗ у гострому стані. Подальші дослідження можливого ефекту Траумелю С у людей, здійснені Muders і співавт., виявили, що він може обмежити пошкодження м’язів, спричинене фізичними вправами, модулюючи певні сигнали, що регулюють запалення.
Висновки
НПЗЗ і кортикостероїди міцно закріплені в терапевтичному арсеналі більшості клініцистів. Вони є ефективними препаратами, але протипоказані за наявності певних супутніх захворювань.
Багато пацієнтів віддали б перевагу альтернативному підходу, зваживши ризики та вигоди. Якщо медичний працівник або пацієнт націлені на запобігання/зменшення хронізації запалення, застосування препарату Траумель С буде вдалою альтернативою НПЗЗ.
Він не має будь-яких значних побічних ефектів і може використовуватися окремо або в поєднанні з іншими методами лікування.
Перевагою застосування мультитаргетного засобу Траумель С також є можливість зменшення дози ліків, що призначаються разом, а отже, мінімізація їхніх побічних ефектів.
За матеріалами: Wolfarth B., Speed C., Raymuev K., Vanden Bossche L. & Migliore A. Managing pain and inflammation associated with musculoskeletal disease: time for a change? Current Medical Research and Opinion, 2022; 38: 10, 1695-1701. DOI: 10.1080/03007995.2022.2108618.
Підготувала Олена Костюк
Медична газета «Здоров’я України 21 сторіччя» № 4-5 (540-541), 2023 р.