6 квітня, 2023
Ефективність перорального застосування препаратів заліза у пацієнтів із серцевою недостатністю і залізодефіцитною анемією

Залізодефіцитна анемія (ЗДА) – поширений коморбідний стан серед пацієнтів із серцевою недостатністю (СН), пов’язаний зі зниженими рівнями функціональної здатності та якості життя. У низці досліджень зазначено, що лікування анемії може мати позитивний вплив на клінічний результат в осіб із СН. Щодо лікування ЗДА доведено ефективність внутрішньовенного (в/в) введення препаратів заліза, однак доступ до такого лікування є обмеженим із різних причин (Anker et al., 2009; Beck-da-Silva et al., 2013). Зокрема, застосування перорально препаратів заліза у формі таблеток є доступною та зручною альтернативою. До вашої уваги представлено огляд статті L.D. Suryani et al. «Oral Ferrous Sulphate Improves Functional Capacity on Heart Failure Patients with Iron Deficiency Anemia», опублікованої у Global Heart (2022;17(1):81). DOI: http://doi.org/10.5334/gh.1151.
Залізовмісні препарати для перорального застосування, наприклад сульфат заліза, є доступними засобами та коштують менше, ніж препарати для внутрішньовенного (в/в) використання. Однак вважається, що через запалення у пацієнтів із СН може підвищуватися рівень гормону гепсидину, який, своєю чергою, пригнічує абсорбцію заліза в шлунково-кишковому тракті (ШКТ) (Langer et al., 2017; Lakhal-Littleton et al., 2016; Nemeth, 2004; Franchini et al., 2010). Усупереч цій позиції Е. Niehaus et al. (2015) продемонстрували, що пероральне застосування сульфату заліза підвищує рівень заліза в пацієнтів із СН.
Метою рандомізованого подвійного сліпого плацебо контрольованого дослідження, яке проводили в Національному серцево-судинному центрі Харапан Кіта на базі клініки Університету Індонезії (Джакарта), стало визначення ефективності перорального застосування препаратів заліза, а саме сульфату заліза, для поліпшення рівня функціональних можливостей пацієнтів із СН зі зниженою фракцією викиду (СНзнФВ) лівого шлуночка (ЛШ) і ЗДА.
Учасників дослідження відбирали за такими критеріями: пацієнти віком від 18 до 75 років із ФВ ЛШ <45%, із функціональним класом II‑III за NYHA, які отримували лікування згідно з настановами, мали рівень гемоглобіну (Hb) <130 г/л (чоловіки) і <120 г/л (жінки), рівень феритину <100 нг/мл або 100‑300 нг/мл коефіцієнт насичення трансферину залізом <20%, швидкістю клубочкової фільтрації (ШКФ) >30 мл/хв/1,73 м2. Критеріями виключення були: активні кровотечі, інфекція, злоякісні процеси, гематологічна патологія, пептична виразка, непереносимість сульфату заліза, отримання заліза в/в упродовж останнього місяця, імплантований постійний водій ритму, внутрішньосерцевий дефібрилятор або пристрій для серцевої ресинхронізуючої терапії, рівень N-кінцевого пропептиду натрійуретичного гормону (NT-pro BNP) >4000 пг/мл, захворювання печінки з перевищенням нормального співвідношення печінкових трансаміназ аспартатамінотрансферази (АСТ)/аланінамінотрансферази (АЛТ) більше, ніж утричі, вроджені хвороби серця, клапанна хвороба серця, правостороння СН через легеневу гіпертензію, проведення первинного черезшкірного втручання або операції з аорто-коронарного шунтування впродовж останніх 3 місяців, інсульт або транзиторна ішемічна атака впродовж останніх 3 місяців.
Первинною кінцевою точкою була різниця рівня функціональної здатності, визначеного за допомогою тесту із 6-хвилинною ходьбою (6MWT), а вторинною – різниця клінічних результатів ФВ ЛШ і профілю заліза через 12 тижнів приймання сульфату заліза або плацебо. Зокрема, 54 учасники, які відповідали зазначеним критеріям, були рандомізовані у дві однакові за кількістю групи: перша отримувала перорально сульфат заліза (200 мг) тричі на добу, а друга – плацебо впродовж 12 тижнів. На початку дослідження учасники пройшли низку тестів: лабораторне визначення профілю заліза, функції нирок, рівня NT-pro BNP, а також ехокардіографію і 6MWT. Через 12 місяців терапії тести виконали повторно. На старті дослідження зазначені показники, а також частково в учасників, що мали певний функціональний клас за NYHA (переважно ІІ чи ІІІ), у двох групах були подібними. Рівень функціональної здатності, який визначали за допомогою 6MWT, на старті становив 300±85 м для групи сульфату заліза і 309±75 м для групи плацебо. Рівень Hb становив 116±18 г/л і 130±10 г/л відповідно, а феритину – >0,001 мг/л в обох групах. Учасники обох груп отримували подібну терапію СН згідно з настановою.
Через 12 тиж. у групі, яка отримувала сульфат заліза, порівняно з групою плацебо зафіксували суттєве збільшення: рівня функціональної здатності (46,23±35 м проти 13,7±46 м, p<0,001, 95% довірчий інтервал [ДІ] від -86,8 до -33,2); рівня Hb (127±18 г/л проти 113±10 г/л, p=0,004, 95% ДІ від -2,3 до -0,4); рівня феритину (207,3±104 нг/мл проти 111,7±81,4 нг/мл, p=0,001, 95% ДІ від -160 до -41,87); коефіцієнта насичення трансферину залізом (29,5±10,4% проти 20±10,6%, p=0,008, 95% ДІ від -16,3 до -2,6).
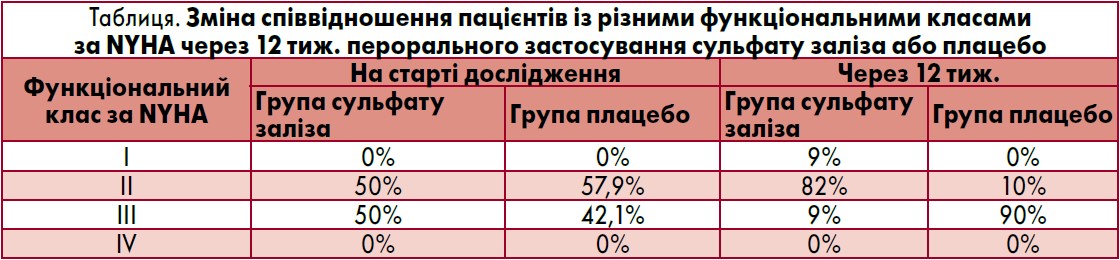
У дослідженні через 12 тижнів застосування сульфату заліза спостерігали поліпшення функціонального класу за NYHA порівняно з плацебо з p=0,01 (таблиця).
Значної різниці щодо частоти виникнення побічних ефектів в обох групах впродовж 12 тижнів не виявлено. У кожній із груп було по два випадки тяжких шлунково-кишкових побічних ефектів. Відомо, що у групі застосування сульфату заліза зафіксовано п’ять, а в групі плацебо – сім нетяжких шлунково-кишкових побічних реакцій. Не встановлено значущої різниці щодо рівня NT-pro BNP (зокрема, сульфат заліза –1625±1233 пг/мл проти плацебо – 2055±1931 пг/мл; p=0,3; 95% ДІ від -478 до 1682), а також щодо величини ФВ ЛШ (сульфат заліза 37+10,3% проти плацебо 34,8+12,2%; p=0,5; 95% ДІ від -9,8 до 5,4) через 12 тижнів дослідження.
У рандомізованому подвійному сліпому плацебо контрольованому дослідженні вивчали вплив перорального застосування препарату заліза в пацієнтів із СНзнФВ і ЗДА. За результатами 6MWT і функціонального класу за NYHA, підтверджено значне підвищення рівня функціональної здатності через 12 тижнів лікування сульфатом заліза порівняно з плацебо. Таку терапію пацієнти переносили добре, між групами застосування сульфату заліза і плацебо не виявлено значної різниці щодо частоти виникнення побічних ефектів. У дослідженні продемонстровано доцільність застосування сульфату заліза перорально по 200 мг тричі на добу впродовж 12 тижнів для підвищення рівня функціональної здатності і відновлення профілю заліза. Через 12 тижнів фіксували підвищення рівня Hb на 9 г/л, феритину – на 69%, трансферину – на 88%, що можна порівняти з результатами в/в застосування препаратів заліза, зокрема в дослідженнях FAIR-HF і CONFIRM-HF (Anker et al., 2009; Ponikowski et al., 2014).
Підвищення рівня функціональної здатності згідно з результатами тесту із 6-хвилинною ходьбою було порівнянним з отриманим у згаданих дослідженнях, що підтверджує переваги відновлення профілю заліза у пацієнтів із СН і ЗДА.
Поліпшення профілю заліза та відновлення гемоглобіну в пацієнтів в описаному дослідженні свідчать на користь всмоктування заліза в ШКТ. Отже, вплив високого рівня гепсидину на ефективність пероральних препаратів заліза у пацієнтів із СН і ЗДА залишається темою для дискусій. Щодо відсутності значущого впливу лікування сульфатом заліза на рівень NT-pro BNP у крові і ФВ ЛШ, то автори дослідження припускають, що 12 тижнів – замалий період часу для стійкого поліпшення функції міокарда.
Нормалізація лабораторних показників обміну заліза в дослідженні дає змогу припустити, що в ШКТ відбувається абсорбція заліза. Раніше вважали, що пероральне застосування препаратів заліза не є ефективним у пацієнтів із СН і ЗДА через високий рівень гормону гепцидину (von Haehling et al., 2011; Saxena et al., 2019; De Las Nieves et al., 2020; Jankowska et al., 2012). Втім, роль гепсидину в пацієнтів із СН і ЗДА досі обговорюється, оскільки отримані дані є суперечливими. Так, суперечливі результати щодо перорального застосування заліза пацієнтами із СНзнФВ і ЗДА були отримані в дослідженні IRONOUT HF (Lewis et al., 2017). Після 16 тижнів застосування препарату (по 150 мг двічі на добу), що містив комплекс заліза з полісахаридами, не спостерігали суттєвої зміни рівнів феритину, трансферину і функціональної здатності (у 6MWT). Отриманий результат можна пояснити різницею у препаратах заліза. Вважається, що комплекс заліза з полісахаридами переноситься краще, ніж сульфат заліза (Saha et al., 2007). Проте у зазначеному дослідженні не виявлено значної різниці щодо побічних ефектів між групами сульфату заліза і плацебо. Водночас в інших дослідженнях отримано вищі показники відновлення рівня заліза в разі приймання заліза Fe+2 порівняно з Fe+3 без суттєвих відмінностей щодо побічних ефектів (Zdravkovic et al., 2019; Powers et al., 2017).
У рандомізованому дослідженні BESTIRON, у якому порівнювали ефективність комплексу заліза з полісахаридами і сульфату заліза для лікування аліментарної ЗДА у дітей, за 12 тижнів застосування сульфату заліза забезпечило більше підвищення рівня гемоглобіну (Powers et al., 2017).
За даними дослідження IRON-HF, застосування як сульфату заліза, так і цукрату заліза в/в протягом 5 тижнів у пацієнтів із СНзнФВ і ЗДА підвищувало рівень феритину і трансферину (Beck-da-Silva et al., 2013).
У дослідженні IRON-HF не спостерігали поліпшення фізичного стану після 5 тижнів застосування сульфату заліза, тобто для підвищення рівня функціональної здатності пацієнтів із СН і ЗДА необхідно щонайменше 12 тижнів. Отже, вчені дійшли висновку, що пероральне застосування сульфату заліза можна використовувати як альтернативу в/в введення заліза для відновлення профілю заліза і поліпшення рівня функціональної здатності у пацієнтів із СНзнФВ і ЗДА.
Підготувала Тетяна Ткаченко