6 квітня, 2023
Ефективність тромбопрофілактики ривароксабаном у госпіталізованих пацієнтів із приводу COVID‑19 після виписки: результати дослідження MICHELLE
Пацієнти, госпіталізовані з приводу COVID‑19, мають підвищений ризик тромботичних подій після виписки з лікарні. Таким хворим рекомендовано проводити профілактику парентеральними антикоагулянтами. Також існує консенсус щодо використання гепарину як первинної тромбопрофілактики під час госпіталізації. Однак роль розширеної профілактики тромбозів у цій популяції достеменно не з’ясована. E. Ramacciotti et al. виконали дослідження з метою оцінити ефективність тромбопрофілактики ривароксабаном у пацієнтів групи високого ризику, виписаних після госпіталізації з приводу COVID‑19, порівняно з відсутністю антикоагулянтної терапії. Було продемонстровано, що тромбопрофілактика ривароксабаном у дозі 10 мг/добу протягом 35 днів покращувала клінічні результати хворих. Огляд отриманих у дослідженні даних опубліковано у виданні The Lancet (2022; 399: 50‑59).
Частота розвитку тромботичних подій на тлі COVID‑19 є вищою, ніж за гострого респіраторного синдрому, не пов’язаного з SARS-CoV‑2 (Helms et al., 2020). За результатами досліджень із залученням пацієнтів, виписаних після госпіталізації з приводу COVID‑19, поширеність симптомної венозної тромбоемболії (ВТЕ) становить від ˂1 до 2,5% (Patell et al., 2020). Згідно з даними великого проспективного реєстру, який включав 4906 осіб із коронавірусом після виписки зі стаціонару, частота подій ВТЕ, артеріальних тромбоемболій (АТЕ) або смерті від усіх причин склала 7,13%. При цьому показник виявився на 46% нижчим у хворих, яким було призначено профілактичну антикоагулянтну терапію (Giannis et al., 2020).
На сьогодні доступні дані низки робіт, присвячених ролі розширеної профілактики ВТЕ у хворих після виписки з лікарні (без COVID‑19). Так, у дослідженні MARINER оцінювали застосування ривароксабану в дозі 10 або 7,5 мг/добу (у пацієнтів із кліренсом креатиніну [КК] <50 мл/хв) порівняно із плацебо протягом 45 днів після виписки у 12 019 осіб із соматичними захворюваннями (Spyropoulos et al., 2020). При застосуванні ривароксабану спостерігалося статистично значуще зниження відносного ризику (ВР) симптомної нефатальної ВТЕ на 56%, на 27% – симптомної ВТЕ і смерті від усіх причин, а також на 28% – серйозних та фатальних тромбоемболічних подій. До того ж не було статистично достовірного зростання частоти великих кровотеч (Spyropoulos et al., 2018).
Рекомендації щодо ролі розширеної антитромботичної профілактики після виписки зі стаціонару в пацієнтів, госпіталізованих із приводу COVID‑19, дещо суперечливі (Gerotziafas et al., 2020; Tritschler et al., 2020). У цьому контексті E. Ramacciotti et al. (2022) вирішили дослідити, чи покращить клінічні результати (включно із великими та фатальними тромбоемболічними подіями) у даній популяції хворих профілактика ривароксабаном у дозі 10 мг/добу протягом 35 днів після виписки з лікарні.
Матеріали й методи дослідження
Дизайн дослідження та популяція хворих
MICHELLE – прагматичне відкрите багатоцентрове рандомізоване контрольоване дослідження з оцінкою результатів методом засліплення, що охоплювало пацієнтів, виписаних після госпіталізації з приводу COVID‑19, із 14 лікарень Бразилії. Науковці мали на меті визначити, чи матиме вплив тромбопрофілактика ривароксабаном на зниження частоти сукупності подій симптомних/безсимптомних ВТЕ, АТЕ та серцево-судинної (СС) смерті. Хворі були рандомізовані у співвідношенні 1:1 для лікування ривароксабаном у дозі 10 мг/добу (що розпочиналося протягом 24 год від моменту виписки з лікарні) або регулярного спостереження (без антикоагулянтної терапії) впродовж 35 днів. Із жовтня 2020 р. до червня 2021 р. загалом було обстежено 997 пацієнтів, із яких усім критеріям прийнятності відповідали 320 осіб (n=160 на групу).
Під час госпіталізації хворі отримували стандартні профілактичні дози парентерального еноксапарину, нефракціонованого гепарину або фондапаринуксу. Включені пацієнти також повинні були мати підвищений ризик ВТЕ, що визначався як 2‑3 бали за шкалою IMPROVE, та рівень D-димеру ˃500 нг/мл або ˃4 балів незалежно від показника D-димеру при виписці з лікарні.
Підозра або підтвердження тромботичної події були критеріями виключення, тому пацієнти з позитивними результатами, отриманими за допомогою ультразвукової доплерографії або комп’ютерно-томографічної (КТ) ангіографії легень до включення, не мали права на участь у дослідженні. Вазопресорна підтримка була дозволена для хворих, що перебували у відділенні інтенсивної терапії (ВІТ). Всі пацієнти надали письмову або підписану електронним підписом інформовану згоду на участь.
Обстеження пацієнтів
Базова оцінка хворих включала демографічні характеристики, фактори ризику, історію хвороби, внутрішньолікарняне застосування антикоагулянтів, перебування у ВІТ та лабораторні дані (D-димер і КК). Пацієнтів зобов’язали повідомляти про будь-який симптом, що вказував на наявність ВТЕ, АТЕ або кровотечі. Під час консультацій (на 7 і 35-й день) у хворих детально оцінювали задишку, біль у грудях, нижніх кінцівках, периферичні набряки, пульс та ознаки кровотечі, а також виконували двосторонню доплерографію вен нижніх кінцівок та КТ легень.
Оцінка результатів
Для оцінювання лікування були визначені такі первинні результати:
- первинна кінцева точка для встановлення ефективності: сукупність подій симптомної або фатальної ВТЕ, безсимптомної ВТЕ, симптомної АТЕ, включно з інфарктом міокарда (ІМ), негеморагічним інсультом і великою несприятливою подією з боку кінцівок, а також СС-смерті на 35-й день спостереження;
- первинний показник безпеки: велика кровотеча відповідно до критеріїв Міжнародного товариства тромбозу та гемостазу (ISTH) (Kaatz et al., 2015).
Вторинні результати передбачали наступне:
- вторинні кінцеві точки для визначення ефективності: сукупність подій симптомної та фатальної ВТЕ, сукупність симптомної ВТЕ і смерті від усіх причин та комбінація симптомної ВТЕ, ІМ, негеморагічного інсульту й летального випадку через СС-подію (смерть через підтверджене кардіоваскулярне захворювання або смерть, коли не можна виключити СС-причину);
- вторинний показник безпеки: сукупність подій великих, клінічно значущих невеликих та інших кровотеч відповідно до критеріїв ISTH (Kaatz et al., 2015).
Дослідники фіксували всі передбачувані або підозрювані тромбоемболічні події, незалежно від даних візуалізаційних досліджень. Якщо результат був підтвердженим, випадок класифікували як підтверджену тромбоемболію легеневої артерії (ТЕЛА), ВТЕ або АТЕ. Якщо результат був недоступним, але існувала значна клінічна ймовірність наявності тромбозу глибоких вен (ТГВ) або ТЕЛА, випадок класифікували як ймовірний ТГВ чи ТЕЛА. Якщо пацієнт помирав за невідомої причини, випадок класифікували як невиключену ТЕЛА.
Результати
Внаслідок відсіву до ІТТ-аналізу були включені по 159 пацієнтів у кожній групі. Базові характеристики були збалансовані між групами. Середній вік учасників становив 57 років, частка жінок – 40%, чоловіків – 60%, а середній індекс маси тіла – 29,7 кг/м². Середня тривалість госпіталізації склала вісім днів, 52% перебували у ВІТ, на момент виписки з лікарні 97% пацієнтів мали КК ≥50 мл/хв.
Еноксапарин у дозі 40 мг/добу як внутрішньолікарняну тромбопрофілактику отримували 86% хворих, антитромбоцитарну терапію – 5%; у 62% було зафіксовано 2‑3 бали за IMPROVE зі зростанням рівня D-димеру, і в 92% – збільшення рівня D-димеру (вище верхньої межі норми 500 нг/мл). У групі лікування досліджуваний препарат протягом 35 днів без перерви більш ніж на тиждень приймали 99% пацієнтів.
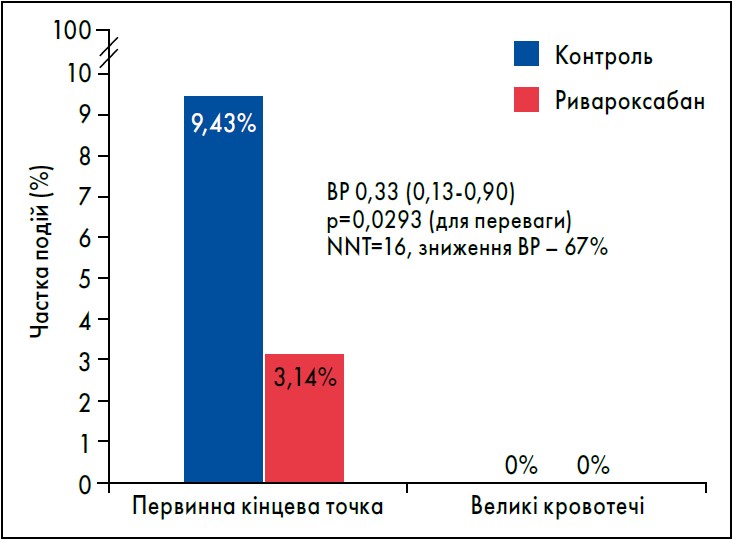
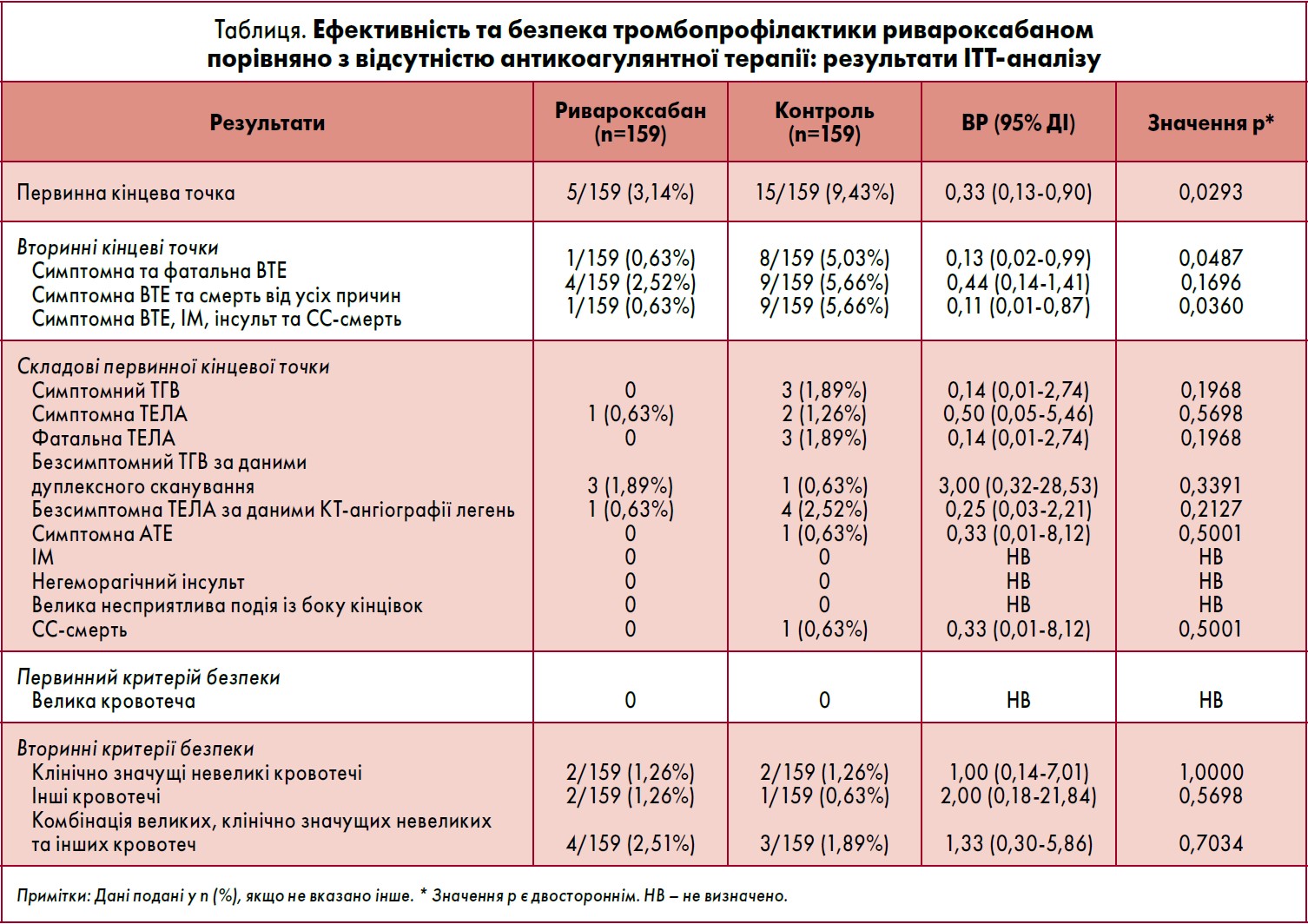
За отриманими даними, 9,43% пацієнтів групи контролю і 3,14% – ривароксабану досягли первинної кінцевої точки (ВР 0,33; 95% ДІ 0,13‑0,90) на 35-й день дослідження, при цьому зниження ВР становило 67% (рисунок). У жодній із груп не спостерігалося серйозних кровотеч за визначенням ІСТН. Що стосується вторинної кінцевої точки, симптомна/фатальна ВТЕ виникла в 1 хворого на тлі ривароксабану та у 8 – в групі контролю (ВР 0,13; 95% ДІ 0,02‑0,99), симптомна ВТЕ і смертність від усіх причин – у 4 та 9 хворих відповідно (ВР 0,44; 95% ДІ 0,14‑1,41), сукупність симптомної ВТЕ, ІМ, інсульту або СС-смерті – в 1 і 9 відповідно (ВР 0,11; 95% ДІ 0,01‑0,87).
Рисунок. Результати ефективності й безпеки тромбопрофілактики ривароксабаном порівняно з відсутністю антикоагулянтної терапії
Примітка. NNT – кількість пацієнтів, що потребували лікування.
При оцінці вторинного показника безпеки було встановлено, що клінічно значуща невелика кровотеча виникла у 2 пацієнтів, які отримували ривароксабан (одна носова та одна із сечостатевих органів), і 2 – у контрольній групі. Із сукупності подій великих, клінічно значущих невеликих та інших кровотеч на тлі ривароксабану кровотеча виникла у 4 осіб та у 3 осіб, що не приймали антикоагулянти.
Первинні та вторинні результати ефективності й безпеки наведені в таблиці.
Обговорення
У дослідженні за участю пацієнтів групи високого ризику, госпіталізованих із підтвердженим COVID‑19, призначення схеми лікування, що включала стандартну внутрішньолікарняну парентеральну тромбопрофілактику з розширенням ривароксабаном у дозі 10 мг/добу після виписки тривалістю 35 днів, дозволило досягти кращих результатів порівняно з відсутністю антикоагулянтної терапії. Клінічні наслідки включали зниження частоти серйозних і фатальних тромбоемболічних подій без зростання ризику великих кровотеч.
Як стверджують автори, MICHELLE є першим рандомізованим дослідженням у сфері розширеної тромбопрофілактики після виписки в осіб із COVID‑19, яке продемонструвало клінічну користь. Переваги терапії ривароксабаном загалом були відзначені за рахунок нижчої частоти ТЕЛА у пацієнтів порівняно з контрольною групою. Крім того, зниження ризику первинної кінцевої точки було послідовним, що свідчило про стійку гомогенність результатів випробування.
Слід зауважити, що у раніше проведених дослідженнях за участю пацієнтів, госпіталізованих із COVID‑19, було підтверджено, що як підвищений показник IMPROVE стосовно ВТЕ, так і збільшена концентрація D-димеру (відносно нового біомаркера для осіб, що потрапили до стаціонару із COVID‑19) є предикторами зростання ризику тромботичних подій у період після виписки (Giannis et al., 2021; Cohen et al., 2021).
Використання розширеної профілактики ВТЕ після госпіталізації у пацієнтів із соматичними захворюваннями лишається дискусійним. У дослідженні MARINER також вивчали застосування ривароксабану порівняно з плацебо для профілактики тромбозу протягом 45 днів (Spyropoulos et al., 2020). Незважаючи на те, що отримані результати не продемонстрували статистично значущої різниці між ривароксабаном та плацебо у зниженні пов’язаної з ВТЕ смертності після виписки, розширена стратегія тромбопрофілактики ривароксабаном знижувала частоту симптомної ВТЕ на 56% без підвищення кількості великих кровотеч. До того ж, враховуючи значну протромботичну природу COVID‑19, було доцільно оцінити роль тривалої профілактики ВТЕ ривароксабаном у зниженні частоти тромботичних подій та ризику кровотеч в осіб, госпіталізованих із приводу COVID‑19.
Дослідження MICHELLE є частиною комплексної програми антикоагулянтної терапії під час пандемії COVID‑19 у Бразилії, що включає ще три рандомізованих клінічних випробування (CARE, APOLLO, COALIZAO-ACTION), у яких вивчають роль антитромботичних стратегій, зокрема ривароксабаном, на тлі COVID‑19. Отримані докази високої якості слугуватимуть основою для рекомендацій із клінічної практики щодо ведення пацієнтів із COVID‑19 на догоспітальному, госпітальному етапах та після виписки, а також допоможуть лікарям у прийнятті рішень щодо призначення таким хворим антикоагулянтної терапії.
Окрім того, наразі тривають клінічні випробування, присвячені активному оцінюванню розширеної тромбопрофілактики у пацієнтів із COVID‑19. Наприклад, дослідження в Мексиці за участю 130 пацієнтів сфокусоване на внутрішньолікарняному застосуванні гепарину в профілактичних та повних дозах із подальшим призначенням 10 мг/добу ривароксабану або без нього (NCT04508439).
До випробування XACT залучено 150 пацієнтів, рандомізованих для отримання еноксапарину під час госпіталізації або ривароксабану перорально (10, 15 чи 20 мг/добу) після виписки протягом 28 днів (NCT04640181). Первинна кінцева точка включає смерть або 30-денну летальність від усіх причин, штучну вентиляцію легень, інтубацію або переведення у ВІТ.
Висновки
Як зазначили E. Ramacciotti et al. (2022), у пацієнтів із високим ризиком щодо тромботичних подій, виписаних після госпіталізації з приводу COVID‑19, тромбопрофілактика ривароксабаном у дозі 10 мг/добу протягом 35 днів покращувала клінічні результати, зменшуючи тромботичні події, порівняно з відсутністю антикоагулянтної терапії.
Отже, застосування ривароксабану в межах розширеної тромбопрофілактики після виписки зі стаціонару слід розглядати як ефективну стратегію для поліпшення якості життя таких хворих.
Підготувала Олена Коробка