22 квітня, 2023
Позалікарняні пневмонії у дітей
Стандарти медичної допомоги
Лікарі різних спеціальностей мають бути обізнані щодо основних клінічних проявів позалікарняної пневмонії (ПП) з метою її ранньої діагностики і призначення лікування пацієнтам із ПП для попередження розвитку ускладнень та запобігання смертності дітей.
Стандарт 1. Організація надання медичної допомоги при позалікарняній пневмонії у дітей
ПП є основною причиною скерування до педіатричного стаціонару (близько половини ПП лікуються амбулаторно) і госпіталізації в соматичне стаціонарне відділення, а також одним із найпоширеніших показань до призначення антибактеріальної терапії (АБТ). В епоху зростання резистентності до антибактеріальних лікарських засобів (ЛЗ) обґрунтоване доказове лікування ПП в дитячому віці особливо важливе і з економічної точки зору.
Рання діагностика та початок лікування пацієнтів із ПП сприяють запобіганню ускладнень і смертності дітей раннього віку.
Ефективні системи комунікації, що відповідають конкретним потребам окремих осіб, є найважливішими для забезпечення своєчасної діагностики, скерування і лікування. Пацієнтам із ПП має бути гарантовано, що в усіх фахівців охорони здоров’я, які беруть участь у наданні медичної допомоги, налагоджений контакт між собою і з пацієнтом, членами сім’ї/особами, які здійснюють догляд.
Критерії якості медичної допомоги
Обов’язкові
- Існують локально узгоджені письмові документи, що координують та інтегрують медичну допомогу для забезпечення своєчасного направлення, діагностики й лікування пацієнтів із ПП.
- Існує задокументований індивідуальний план допомоги, що містить дані щодо діагнозу, плану обстеження й лікування, узгоджений із законним представником пацієнта, якщо медичної допомоги потребують особи до 14 років або пацієнти, визнані недієздатними (далі – законний представник), чи пацієнтом.
- Законний представник або пацієнт забезпечуються у доступній формі інформацією щодо перебігу захворювання, плану обстеження та лікування і подальшого спостереження, навчання навичок, необхідних для поліпшення результатів лікування, контактів для отримання додаткової інформації та консультацій.
Бажані
- Заклади охорони здоров’я (ЗОЗ) розміщують інформаційні матеріали стосовно основних клінічних проявів ПП у доступних для пацієнтів місцях (Додаток 1).
- Усі діти повинні бути вакциновані проти пневмококів, H. influenzae типу b, кашлюку, кору та вітряної віспи для запобігання ПП; за наявності факторів ризику – також проти сезонного грипу та гострої респіраторної хвороби COVID-19, спричиненої коронавірусом SARS-CoV-2.
Стандарт 2. Діагностика позалікарняної пневмонії у дітей
Положення стандарту медичної допомоги
Діагноз ПП встановлюють на підставі даних анамнезу, клінічних проявів (панель 1), інструментальних і лабораторних методів дослідження. Наявність ПП може припустити лікар будь-якої спеціальності на підставі виявлення в пацієнта клінічних проявів ПП.
У більшості дітей діагноз ПП може бути встановлений на підставі анамнезу і клінічних даних (панель 1). Обсяг подальших діагностичних заходів, які можуть бути використані, залежить від індивідуальних особливостей перебігу хвороби з урахуванням анамнезу життя, анамнезу захворювання, вакцинального статусу й оцінки ризику.
Обґрунтування
Для диференційної діагностики і динамічного спостереження парапневмонічного випоту (ППВ) й емпієми плеври (ЕП) методом вибору є ультразвукове дослідження (УЗД). Дані комп’ютерної томографії (КТ) із контрастуванням дають змогу ідентифікувати і диференціювати внутрішньогрудні паренхіматозні патологічні процеси з високим рівнем роздільної здатності.
У ЗОЗ, що надають спеціалізовану медичну допомогу, в усіх випадках призначення емпіричної АБТ необхідно отримати зразок біологічного матеріалу для проведення бактеріологічного дослідження з метою ідентифікації збудника ПП до введення пацієнту антибактеріального ЛЗ. У ЗОЗ, що надають первинну медичну допомогу, необхідно отримати зразок біологічного матеріалу для проведення бактеріологічного дослідження з метою ідентифікації збудника ПП перед призначенням антибактеріального ЛЗ за умови, що пацієнт відповідає перерахованим нижче критеріям.
- Є фактори ризику щодо наявності бактерій продуцентів β-лактамаз розширеного спектра.
- В анамнезі звернення по медичну допомогу (денний стаціонар, гемодіаліз (тривалістю понад 30 днів), перебування в закладах довготривалого огляду) або госпіталізація тривалістю понад 48 год протягом останніх 3 міс.
- В анамнезі попередня АБТ протягом останніх 90 днів (з будь-якої причини).
- В анамнезі попереднє лікування інфекції, спричиненої бактерією з множинною резистентністю до антибактеріальних ЛЗ.
- Наявність у пацієнта тяжкої супутньої патології (хронічної ниркової недостатності, цирозу печінки, цукрового діабету, алкогольної вісцеропатії, наркоманії, імуносупресивного стану).
- В анамнезі перебування протягом останніх 90 днів у країнах із високим рівнем поширеності бактерій із множинною резистентністю до антибактеріальних ЛЗ.
- Обґрунтована підозра колонізації або інфікування пацієнта ентеробактеріями продуцентами β-лактамаз розширеного спектра.
Симптоми залежать від типу й локалізації ПП, а також від віку пацієнта і часто бувають неспецифічними. За підозри на ПП необхідно завжди проводити повне фізикальне обстеження, щоб визначити симптоми захворювання, виявити ураження позалегеневих органів, наявність напруження м’язів черевної стінки або зневоднення, оцінити тяжкість захворювання. У хворих дітей зазвичай спостерігають погіршення загального стану з лихоманкою, тахіпное, задишкою і кашлем. Біль у грудях, животі і блювання – часті супутні симптоми ПП.
Критерії якості медичної допомоги
Обов’язкові
- Для неінвазивної оцінки вмісту кисню в артеріальній крові застосовують пульсоксиметрію. Безперервний моніторинг SpO2 показаний пацієнтам із тяжкою формою ПП і гіпоксією при самостійному диханні атмосферним повітрям, пацієнтам із респіраторним виснаженням, пацієнтам зі зміною поведінки. Це слід враховувати в недоношених немовлят і дітей першого року життя через ризик апное/брадикардії.
- У пацієнтів із тяжкою формою ПП і відсутнім клінічним ефектом призначеної терапії або ускладненнями (панель 5) слід провести дослідження гемокультури і, в разі можливості отримання біологічного зразка, мокротиння і плеврального випоту (ПВ) з метою ідентифікації та визначення чутливості до антибактеріальних ЛЗ. У разі проведення пацієнту з лікувальною або діагностичною метою бронхоскопії необхідно провести посів аспірату з трахеї або бронхоальвеолярного лаважу.
- За допомогою полімеразної ланцюгової реакції (ПЛР) або серологічних методів дослідження проводять ідентифікацію бактеріальних агентів, таких як мікоплазма або Bordetella pertussis, у пацієнтів із тяжкою ПП чи відсутнім клінічним ефектом призначеної терапії ПП або з її ускладненим перебігом.
- Для ідентифікації респіраторних вірусів рекомендовано проводити експрес-тести і ПЛР.
- Рентгенологічне дослідження ПП проводиться в прямій проєкції. Не слід проводити рентгенологічне дослідження в бічній проєкції.
- Пацієнтів із ПП і локальним ослабленням дихання або постійними тахі-/диспное і гіпоксемією обстежують за допомогою УЗД або рентгенологічно. Якщо порушення вентиляції не зникає під час терапії або є підозра на аспірацію стороннього тіла, проводять бронхоскопічне дослідження.
- У пацієнтів із ПП однобічне вкорочення перкуторного звуку, ослаблене дихання, стійка лихоманка або повторне погіршення стану можуть бути ознаками плеврального ускладнення: парапневмонічного ПВ або ЕП. Плевральну пункцію проводять пацієнтам із ПП і ПВ/ЕП за діагностичними і/або терапевтичними показаннями. Пунктат досліджують цитологічно, біохімічно і мікробіологічно.
- У ЗОЗ, що надають спеціалізовану медичну допомогу, забезпечена цілодобова можливість для збору зразків біологічного матеріалу, тимчасового зберігання до надсилання до мікробіологічної лабораторії (за необхідності) та отримання результатів мікробіологічних досліджень.
Бажані
За підозри ускладнення рекомендовано провести візуалізацію плевральної порожнини за допомогою УЗД.
Стандарт 3. Лікування дітей із позалікарняною пневмонією
Положення стандарту медичної допомоги
Для лікування пацієнтів із ПП застосовують симптоматичну й етіотропну терапію. Симптоматична терапія ПП охоплює, перш за все, оксигентерапію, застосування жарознижувальних засобів, аналгетиків, а також регідратацію.
Пацієнти з нетяжкою формою ПП лікуються амбулаторно, якщо особи, які здійснюють догляд за ними, пройшли інструктаж із лікування та спостереження, а медична допомога гарантована. Пацієнти з тяжкою формою ПП мають бути госпіталізовані (панель 3).
Оцінка лікарем відсутності клінічного ефекту призначеної АБТ повинна базуватися на індивідуальній оцінці клінічних проявів (панель 1). Динаміка лабораторних показників, таких як кількість лейкоцитів у загальному аналізі крові, рівень С-реактивного білка (СРБ) або прокальцитоніну, доповнює оцінку клінічної відповіді.
Обґрунтування
ПП – це інфекційне захворювання, що спричинюється мікроорганізмами, з подальшим запаленням в альвеолах з ураженням бронхів і/або бронхіол чи без нього.
У дітей раннього віку з нетяжкою формою ПП без лихоманки або з ознаками бронхіальної обструкції високою є ймовірність вірусної етіології. За наявності ознак вірусної етіології ПП (або за відсутності ознак бактеріальної етіології ПП) можна відмовитися від призначення антибактеріального ЛЗ як препарату першої лінії терапії або відмінити вже розпочату АБТ. За умови виявлення вірусу грипу дітям із ПП негайно призначають специфічну противірусну терапію. ПП, спричинену бактеріями, необхідно лікувати з використанням антибактеріальних ЛЗ.
Клінічні скарги і симптоми, такі як лихоманка, прискорене дихання і зниження рівня кисню, мають покращитися протягом 48-72 год після початку АБТ.
Рішення щодо стартової АБТ у дітей із ПП приймають емпірично, на основі клінічної картини, передбачуваних причинно-значущих збудників і наявності факторів ризику, даних вакцинального статусу.
Діти з ПП при наданні адекватної медичної допомоги зазвичай одужують швидко й повністю. На тлі терапії, що проводиться, впродовж 48-72 год у дітей відзначається зниження температури тіла, покращується апетит і максимум через 1-2 тиж після початку АБТ відновлюється активність. Рубцеві зміни паренхіми легень і плеври або розвиток бронхоектазів трапляється рідко і, як правило, у випадках пізньої/неадекватної терапії або деструктивних форм ПП.
Критерії якості медичної допомоги
- Пацієнти з ПП і результатами пульсоксиметрії: SpO2 <92% при диханні атмосферним повітрям отримують оксигенотерапію до досягнення SpO2 >92%.
- У немовлят та дітей молодшого віку нетяжка форма ПП без лихоманки або з ознаками бронхіальної обструкції характеризується високою ймовірністю вірусного генезу захворювання, тому слід розглянути можливість терапевтичного ведення таких пацієнтів без антибактеріальних ЛЗ. Пацієнтам із ознаками вірусної етіології ПП (за відсутності ознак або симптомів приєднання вторинної бактеріальної коінфекції/суперінфекції, які вимагатимуть проведення АБТ; панель 2) можна відмовитися від призначення АБТ або скасувати вже розпочату АБТ.
- Усім пацієнтам з обґрунтованим клінічним діагнозом ПП призначаються антибіотики, зважаючи на тяжкість диференціювання ПП бактеріальної та вірусної природи.
- Амоксицилін (перорально) або ампіцилін (для внутрішньовенного введення) є препаратами вибору для лікування пацієнтів із ПП. У дітей із неповною вакцинацією проти Haemophilus influenzae типу b і Streptococcus pneumoniae, дітей, які застосовували АБТ упродовж останніх 3 міс, а також госпіталізованих у стаціонар препаратом першого вибору можуть бути цефалоспорини ІІ або ІІІ покоління.
- Пацієнтам із ПП за наявності алергії або непереносимості пеніцилінів призначають терапію цефалоспоринами (з урахуванням можливої перехресної реакції), макролідами або, пацієнтам віком від 12 років із масою тіла >45 кг, тетрациклінами.
- Пацієнтам із ускладненою формою ПП, персистуючою лихоманкою чи підозрою на грип або кір із бактеріальною коінфекцією призначають амінопеніциліни з інгібіторами бета-лактамаз або цефалоспорини ІІ покоління.
- При тяжкій формі ПП і за наявності ознак мікоплазмової або хламідійної інфекції призначають макроліди або тетрацикліни (у пацієнтів віком від 12 років із масою тіла >45 кг), або спочатку, чи як доповнення до амінопеніцилінів, або в разі неефективності терапії (панель 4).
- У випадку визначення етіологічного чинника ПП АБТ проводиться відповідно до його чутливості.
- У випадку неускладненого перебігу ПП і клінічного покращення при лікуванні, що розпочате з внутрішньовенного введення антибактеріального ЛЗ, продовжується його пероральний прийом.
- АБТ проводиться протягом 5 днів у пацієнтів із нетяжкою формою ПП і не менше 7 днів при тяжкій формі ПП. У пацієнтів із ускладненою формою ПП тривалість терапії визначається клінічною картиною та перебігом даного захворювання.
- АБТ у пацієнтів із ПП, ускладненою ПВ/ЕП, починають із внутрішньовенного введення цефалоспоринів ІІ покоління або комбінацією амінопеніциліну та інгібіторів бета-лактамаз.
- Пацієнти з ПВ/ЕП без респіраторних порушень одужують під час лікування антибактеріальними ЛЗ без додаткових терапевтичних заходів. Клінічно значуща ексудація в плевральній порожнині є показанням до проведення плевральної пункції або постановки дренажу. Рекомендовано внутрішньоплевральне введення фібринолітичних засобів.
- У пацієнтів із ПП та абсцесом легені першою лінією лікування є проведення хірургічного контролю та АБТ (панель 2); периферичні абсцеси легень без зв’язку з бронхіальною системою контролюються за допомогою візуалізації, пункції та дренажу.
- У пацієнтів із деструктивною формою ПП першою лінією терапії є лікування антибактеріальними ЛЗ. Інвазивні втручання слід застосовувати з обережністю.
- У випадках, коли після дводенної терапії бета-лактамним антибактеріальним ЛЗ відсутня терапевтична відповідь, припускається ймовірність інфікування атиповими патогенами, такими як M. pneumoniae, або резистентними до амінопеніциліну патогенами, такими як S. аureus (MRSA), особливо у дітей шкільного віку.
Індикатори якості медичної допомоги
Наявність у ЗОЗ, що надають медичну допомогу пацієнтам із пневмонією, клінічного маршруту пацієнта (КМП).
Паспорти індикаторів якості медичної допомоги
- Наявність у ЗОЗ, що надають медичну допомогу пацієнтам із пневмонією, клінічного маршруту пацієнта.
Зв’язок індикатора із затвердженими настановами, стандартами та протоколами медичної допомоги.
Індикатор ґрунтується на положеннях стандартів медичної допомоги (СМД) «Позалікарняні пневмонії у дітей».
Зауваження щодо інтерпретації та аналізу індикатора.
Даний індикатор характеризує організаційний аспект запровадження сучасного клінічного маршруту пацієнта (КМП) у регіоні. Якість медичної допомоги дітям, хворим на ПП, відповідність надання медичної допомоги вимогам КМП, відповідність КМП чинному СМД даним індикатором висвітлюватися не може, але для аналізу цих аспектів необхідне обов’язкове запровадження КМП у ЗОЗ.
Бажаний рівень значення індикатора:
2023 р. – 50%
2024 р. – 90%
2025 р. і надалі – 100%.
Інструкція з обчислення індикатора
Організація (ЗОЗ), яка має обчислювати індикатор: структурні підрозділи з питань охорони здоров’я місцевих державних адміністрацій.
Дані надаються ЗОЗ, розташованими на території обслуговування, до структурних підрозділів з питань охорони здоров’я місцевих державних адміністрацій.
Дані надаються поштою, в тому числі електронною.
Метод обчислення індикатора: підрахунок шляхом ручної або автоматизованої обробки.
Індикатор обчислюється структурними підрозділами з питань охорони здоров’я місцевих державних адміністрацій після надходження інформації від усіх ЗОЗ, зареєстрованих на території обслуговування. Значення індикатора обчислюється як відношення чисельника до знаменника.
Знаменник індикатора складає загальна кількість ЗОЗ, зареєстрованих у районі обслуговування. Джерелом інформації є звіт структурних підрозділів із питань охорони здоров’я місцевих державних адміністрацій, який містить інформацію про кількість лікарів, що надають медичну допомогу дітям із ПП, зареєстрованим на території обслуговування.
Чисельник індикатора складає загальна кількість ЗОЗ, зареєстрованих у районі обслуговування, для яких задокументований факт наявності КМП, хворого на ПП (наданий екземпляр КМП). Джерелом інформації є КМП, наданий лікарем, який надає медичну допомогу дітям із ПП.
Значення індикатора наводиться у відсотках.
Панель 1
Клінічні прояви та скарги в пацієнтів із позалікарняною пневмонією
Клінічні скарги пацієнтів із ПП можуть включати: респіраторні симптоми, такі як кашель, задишка, біль у грудній клітці; загальні симптоми, такі як лихоманка, відмова від їжі, біль у животі, зниження активності та зміна поведінки (апатія, збудження).
Клінічні прояви, що можуть вказувати на наявність ПП: тахіпное, лихоманка, задишка, ослаблення дихання, бронхіальне чи амфоричне дихання, крепітація, укорочення перкуторного звуку, тахікардія, зневоднення.
ПП також може бути у пацієнтів із лихоманкою без тахіпное та/або задишки.
І навпаки, пацієнти з ПП можуть не мати лихоманки.
Фізикальні дані: вкорочення перкуторного звуку над легенями, ослаблене, бронхіальне чи амфоричне дихання, крепітація.
Клінічно ПП зазвичай можна розділити на:
нетяжку ПП
частота дихання:
- 50/хв – для дітей віком 2-11 міс;
- 40/хв – для дітей віком 12-59 міс;
- 20/хв – для дітей старше 5 років із ретракцією (втяжінням) грудної клітки і без неї.
тяжку ПП: додаткові небезпечні симптоми, такі як різке погіршення загального стану, відмова від їжі, зневоднення, сонливість або непритомність, церебральні судоми.
Панель 2
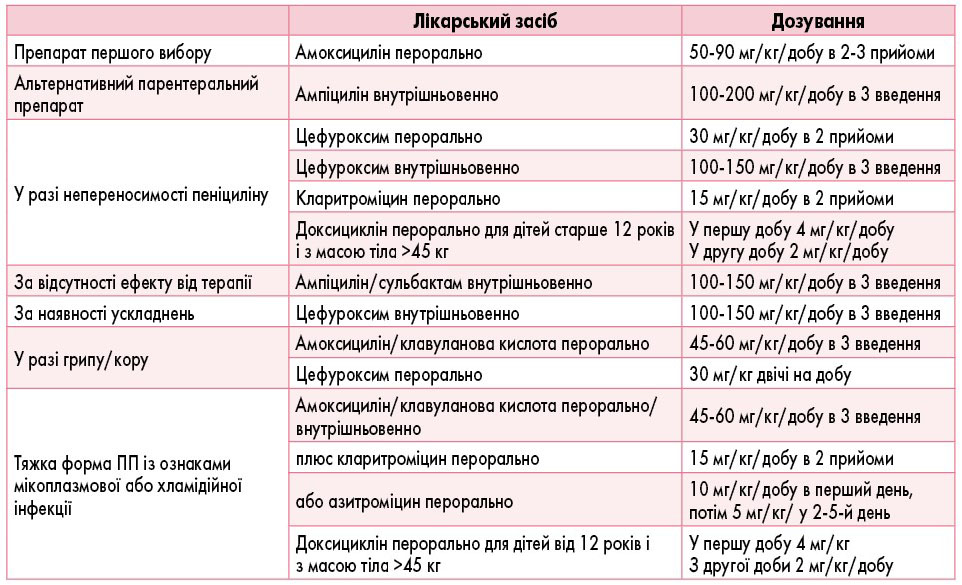
Емпірична антибактеріальна терапія в дітей, хворих на ПП
Вибір емпіричної терапії ПП залежить від наявності в дитини вакцинації пневмококовою вакциною, вакциною проти Haemophilus influenzae типу b і кашлюку, а також пасивної імунізації від респіраторно-синцитіальної вірусної інфекції.
Ампіцилін або пеніцилін G призначають повністю імунізованим дітям (у тому числі кон’югованою вакциною Haemophilus influenzae типу b і Streptococcus pneumoniaе) усіх вікових груп за умови відсутності високої частоти виявлення пеніцилінрезистентних штамів S. pneumoniaе (епідеміологічні дослідження в конкретному регіоні).
Емпіричну терапію цефалоспоринами ІІІ покоління (цефтріаксон/цефотаксим) призначають не повністю імунізованим або неімунізованим дітям у випадку високої частоти виявлення пеніцилінрезистентних штамів S. pneumoniaе (епідеміологічні дослідження в конкретному регіоні).
Комбіновану терапію макролідами (перорально/парентерально) і β‑лактамами призначають дітям із доведеною етіологією Mycoplasma pneumonia/Chlamydophila pneumonia.
Комбіновану терапію ванкоміцином/кліндаміцином і β‑лактамними антибактеріальними ЛЗ призначають дітям із доведеною етіологією S. aureus.
Амоксицилін (перорально) або ампіцилін (внутрішньовенно) є препаратом першого вибору для лікування раніше здорових, імунізованих за календарем профілактичних щеплень дітей дошкільного/шкільного віку з легкою і середньотяжкою ПП.
Панель 3
Амбулаторне і стаціонарне спостереження дітей
Пацієнти з ПП частіше лікуються амбулаторно та можуть бути переведені на амбулаторне лікування, якщо у них спостерігається стійке клінічне покращення, нормалізація частоти дихання, частоти серцевих скорочень, повсякденної активності та апетиту, відзначається нормалізація температури тіла, якщо в них SpO2 при диханні атмосферним повітрям перевищує 92%, якщо їм забезпечений подальший догляд та медична допомога в домашніх умовах. Зокрема, особи, які здійснюють догляд за ними, повинні вміти розпізнавати симптоми «небезпеки», повторного погіршення стану або симптоми ускладнення і повинні бути проінструктовані щодо необхідних дій у цих ситуаціях.
У разі амбулаторного лікування особи, які здійснюють догляд за хворим, повинні бути поінформовані про негайне звернення до лікаря, якщо у пацієнта погіршився стан або не знижується температура тіла і не покращився стан протягом 48 год від початку АБТ. У цьому випадку розглядається питання про госпіталізацію для подальшої діагностики та корекції терапії.
У разі стаціонарного лікування проводяться щоденні контрольні огляди з метою оцінки загального стану пацієнта, його температурного профілю, респіраторних симптомів. Якщо через 48 год АБТ поліпшення стану хворої дитини не спостерігається, проводять повторну оцінку стану пацієнта і корекцію лікування.
При госпіталізації пацієнтів із тяжкою формою ПП до стаціонару проводиться загальний аналіз периферичної крові, визначення рівня СРБ, електролітів сироватки крові та газів крові.
Усі пацієнти з ПП проходять повторне клінічне обстеження через 48-72 год після встановлення діагнозу та початку терапії.
Ведення пацієнтів, у яких не настає покращення протягом 48-72 год, охоплює:
- клініко-медико-лабораторну оцінку поточного ступеня тяжкості захворювання та його динаміки;
- візуалізацію для реєстрації ступеня і, за необхідності, прогресування легеневого чи парапневмонічного процесу;
- розширену ідентифікацію патогенів;
- розгляд питання про зміну терапії.
Показання до виписки зі стаціонару
Термін перебування пацієнта з ПП у стаціонарі залежить від перебігу захворювання й індивідуальних особливостей. Загальні емпіричні критерії ґрунтуються на зменшенні лихоманки і респіраторних симптомів, а також на стабільному насиченні крові киснем >92% при диханні атмосферним повітрям. Для цього достатньо багаторазових пульсоксиметричних вимірювань протягом 24 год. Пацієнти мають можливість вживати їжу і рідину та, за необхідності, антибактеріальні ЛЗ.
Пацієнтів із ПП виписують на амбулаторне лікування, якщо спостерігають у них стійке клінічне покращення: нормалізацію частоти дихання, частоти серцевих скорочень, підвищення фізичної активності й апетиту в поєднанні з нормалізацією температури тіла і SpО2 > 92% при диханні атмосферним повітрям.
Спостереження в динаміці
При виписці зі стаціонару пацієнти й особи, які здійснюють догляд за пацієнтом у домашніх умовах, повинні бути поінформовані про небезпечні симптоми, симптоми погіршення стану та відповідні заходи, які мають бути вжиті в разі їх виникнення.
Контрольне медичне обстеження має проводитися не лише через 48 год після початку лікування, а й після виписки зі стаціонару і/або після закінчення терапії.
Після одужання через 3-7 днів діти можуть знову відвідувати громадські установи і через 1-2 тиж можуть бути допущені до занять спортом, але вирішення питання про допуск до занять спортом має ґрунтуватися на індивідуальній оцінці стану здоров’я дитини.
Імунологічні, пульмонологічні дослідження та функціональна оцінка стану дихальних шляхів після лікування пневмонії показані лише в поодиноких випадках, наприклад, у разі тяжкого/ускладненого перебігу та при повторних епізодах пневмонії (особливо іпсилатеральній).
Панель 4
Неефективність терапії при позалікарняній пневмонії у дітей
Ведення пацієнтів у разі неефективного лікування
- Якщо клінічне покращення не настає протягом 48-72 год, під час повторної оцінки стану пацієнта слід відповісти на наступні питання.
- Чи проводилася адекватна, правильно дозована та регулярна терапія?
- Чи розвинулося ускладнення пневмонії (наприклад, ПВ, ЕП, абсцес легені)?
- Чи є імунодефіцитні стани або інші супутні захворювння?
При оцінці ефективності терапії через 48-72 год після початку АБТ враховують наступні аспекти.
Основні показники життєдіяльності та насичення киснем:
- лихоманка зберігається або посилюється;
- тахіпное, шумне дихання, задишка, ціаноз;
- стійка тахікардія;
- насичення крові киснем при диханні атмосферним повітрям, чи є потреба в кисневій терапії або штучній вентиляції легень.
Системні або вогнищеві симптоми та клінічні ознаки:
- чи сильно порушений загальний стан, знижена увага;
- біль у грудній клітці;
- неможливість пероральної регідратації;
- наявність патологічних змін при аускультації або вкорочення перкуторного звуку при перкусії.
Результати загальноклінічних, біохімічних і рентгенологічних досліджень
- Абсолютна кількість лейкоцитів і зсув формули крові вліво (рівень паличкоядерних гранулоцитів, інших молодих форм), ШОЕ;
- рівень прозапальних маркерів (наприклад, СРБ, прокальцитоніну);
- ідентифікація збудника під час проведення бактеріологічного дослідження або методом ПЛР; наявність антибіотикорезистентних патогенів, у тому числі резистентних до АБТ, що проводиться;
- збільшення обсягу ураження паренхіми (ПВ, абсцесу легені, наявність ознак мікробної деструкції) при візуалізації.
Пацієнти з ПП за відсутності ефекту від терапії повторно обстежуються клінічно і отримують лікування в умовах стаціонару, що спеціалізується на лікуванні пневмоній (дитячих інфекцій), і має відділення інтенсивної терапії.
У разі відсутності ефекту лікування в амбулаторних умовах при госпіталізації пацієнта потрібна модифікація терапії, оскільки неефективність терапії може бути зумовлена:
- неадекватним дозуванням антибактеріальних ЛЗ для досягнення відповідного тканинного рівня (концентрації), наприклад, у разі емпієми або абсцесу;
- неадекватним вибором АБТ і шляху введення антибактеріального ЛЗ;
- дією патогену, не чутливого до призначеного антибактеріального ЛЗ, або суперінфекції.
Дітям із тяжким перебігом ПП до отримання результатів мікробіологічного дослідження призначають захищені амінопеніциліни або цефалоспорини ІІ покоління і, можливо, у поєднанні з макролідом.
У випадках неефективності початкової АБТ у госпіталізованих пацієнтів припускається ймовірність інфікування MRSA, особливо в пацієнтів із раніше відомою колонізацією зазначеним патогеном.
У випадках неефективності терапії проводять дослідження щодо наявності в пацієнта імунодефіциту або інших захворювань. У пацієнтів із повторними епізодами пневмонії або пневмонією, резистентною до лікування, необхідно виключити інші захворювання (вроджену, спадкову патологію, недіагностоване стороннє тіло трахеобронхіального дерева та ін.).
Можливі причини повторних епізодів пневмонії у дітей:
- вплив тютюнового диму (пасивний, активний);
- бронхіальна астма, атопія;
- гастроезофагеальний рефлюкс, мікроаспірація;
- тяжкі інфекції нижніх дихальних шляхів (бронхіоліт, зумовлений респіраторно-синцитіальним вірусом);
- хронічний бактеріальний трахеобронхіт;
- бронхоектатична хвороба/хронічне гнійне захворювання легень.
Основні нервово-м’язові захворювання
- Аспірація стороннього тіла;
- вроджені вади розвитку (кровоносних судин/серця/легень/дихальних шляхів);
- муковісцидоз;
- туберкульоз легень;
- вроджені чи набуті імунодефіцити;
- хронічна хвороба легень у недоношених дітей;
- первинна циліарна дискінезія;
- новоутворення середостіння.
Паренхіматозні/інтерстиційні захворювання легень
Автоімунні/автозапальні захворювання.
Ведення пацієнтів, у яких не настає поліпшення протягом 48-72 год:
- клініко-лабораторна оцінка поточного ступеня тяжкості захворювання;
- візуалізація легень для визначення ступеня та, за необхідності, прогресування легеневого або парапневмонічного процесу;
- використання широкого спектра методів ідентифікації патогенів;
- перегляд АБТ.
Панель 5
Можливі типи ускладнень позалікарняної пневмонії в дітей
Легеневі ускладнення
Ателектаз
Рентгенологічне дослідження легень дає пояснення відсутності ефекту терапії, а порушення вентиляції можуть бути діагностовані за допомогою УЗД.
У дітей із пневмонією і порушенням вентиляції легень розглядається спроба лікування за допомогою фізіотерапії та інгаляцій гіпертонічним сольовим розчином (наприклад, тричі на день по 4 мл 3% або 6% розчину натрію хлориду). Бронхоскопію виконують пацієнтам зі стійким ателектазом із метою виключення іншого захворювання або лікування.
Пацієнтам із ПП і локальним ослабленням дихання або стійкими тахі-/диспное і гіпоксемією проводять УЗД або рентгенологічне дослідження для виявлення ателектазів. Якщо порушення вентиляції зберігається під час терапії або за підозри аспірації стороннього тіла, проводять бронхоскопію.
Парапневмонічний випіт та емпієма плеври
Парапневмонічний випіт (ППВ) часто виникає під час перебігу пневмонії, ЕП – після пневмонії (постпневмонічний процес).
Виділяють три стадії ЕП.
І стадія: ексудативна фаза з утворенням прозорого, переважно стерильного випоту та потовщенням плеври.
ІІ стадія: фібринозно-гнійна фаза з утворенням товстого фібринового нальоту, із каламутним або гнійним секретом.
III стадія: організаційна стадія з формуванням товстої плевральної оболонки і рубцюванням плевральної порожнини.
Стійка лихоманка і різке погіршення загального стану на тлі адекватно проведеної медикаментозної терапії ПП, а також наявність клінічних симптомів, таких як стійке зниження апетиту, кашель, біль у грудях і задишка, асиметрія грудної клітки, ослаблення дихання й укорочення перкуторного звуку, мають викликати підозру на наявність ППВ/ЕП. Початкова підозра ППВ/ЕП може бути підтверджена за допомогою УЗД або рентгенологічного дослідження органів грудної клітки. УЗД органів грудної клітки є методом вибору визначення обсягу випоту і стадії емпієми і характеризується високим рівнем роздільної здатності.
Однобічне вкорочення перкуторного звуку, ослаблене дихання, стійка лихоманка або повторне погіршення стану можуть бути ознаками плеврального ускладнення з ППВ або ЕП.
Для верифікації причинно-значущого збудника всім дітям із ППВ/ЕП рекомендують проводити посів крові на стерильність. Плевральна рідина (випіт), отримана при проведенні пункції плевральної порожнини, досліджується за допомогою мікроскопічного, біохімічного і мікробіологічного методу. ЕП ймовірна, якщо pH <7,0, рівень глюкози <40 мг/дл і лактатдегідрогенази (ЛДГ) >1000 МО/л. Проведення дослідження на бактеріальний геном із подальшим секвенуванням збільшує частоту виявлення в пацієнтів, що попередньо отримували лікування.
Подальше спостереження пацієнтів із підозрою на ППВ/ЕП охоплює регулярний контроль рівня натрію в сироватці крові (щоб виключити недостатню секрецію АДГ), загальний аналіз крові і рівень СРБ.
Якщо існує ризик розвитку туберкульозу легень, проводять шкірну туберкулінову пробу (у дітей до 5-річного віку) або аналіз вивільнення гамма-інтерферону (квантифероновий тест; з 5 років).
Плевральну пункцію слід проводити в пацієнтів із ПП і ППВ/ЕП із діагностичною і/або терапевтичною метою.
Пунктат досліджується цитологічно (підрахунок клітин і диференціація), біохімічно (значення pH, рівня глюкози, білка, ЛДГ, лактату) і мікробіологічно (забарвлення за Грамом, посів, еубактеріальна ПЛР).
Дітям із ПП і ППВ/ЕП спочатку проводять емпіричну АБТ (Додаток 2), за необхідності вона коригується відповідно до результатів бактеріологічних досліджень.
АБТ проводиться внутрішньовенним шляхом протягом не менш ніж 5 днів, після нормалізації температури можливе переведення на пероральну АБТ, яка в середньому триває протягом принаймні 2 тиж.
У більшості випадків для лікування ПП із ППВ/ЕП достатньо проведення лише АБТ. Проведення плевральної пункції можливе як з діагностичною, так і з терапевтичною метою, особливо в пацієнтів, які не отримували попереднього лікування, і технічно можлива з глибини близько 1 см, визначеної за допомогою УЗД, від 2 см має сенс для вільних, гіпоехогенних та не сильно організованих скупчень рідини.
Якщо вилив зберігається протягом 48 год після пункції, слід розглянути можливість повторної пункції і дренування. Місце пункції має бути визначене за допомогою УЗД. Пункція виконується досвідченим персоналом із відповідною аналгетичною седацією або анестезією. Зонд можна видалити, якщо немає внутрішньогрудного витоку повітря і протягом останніх 12 год було отримано менш ніж 0,5 мл/кг рідини. Пацієнти з плевральним дренажем повинні бути клінічно стабільними протягом щонайменше 24 год після його видалення перед випискою.
У пацієнтів із великими і складними ППВ/ЕП тривалість захворювання скорочується шляхом внутрішньоплеврального застосування фібринолітичних агентів. Урокіназа вводиться двічі (6 разових доз) через дренажну систему протягом 3 днів поспіль. Доза для дітей із масою тіла <10 кг становить 10 000 Од у 10 мл NaСІ 0,9%; для дітей із масою тіла від 10 кг – 40 000 Од у 40 мл NaСІ 0,9% з часом утримування 4 год перед зливом через дренажну систему.
Завжди слід виявляти обережність, щоб забезпечити адекватну аналгезію. За відсутності ефекту від проведеної консервативної терапії рекомендується консультація дитячого хірурга або торакального дитячого хірурга і вирішення питання про необхідність проведення відеоторакоскопії.
Вибір антибактеріальних ЛЗ, шляхів уведення і тривалості АБТ у пацієнтів із ПП і ППВ/ЕП слід проводити індивідуально. Зазвичай внутрішньовенно вводять або цефалоспорин ІІ покоління, або комбінацію амінопеніциліну та інгібіторів бета-лактамаз. Для більшості пацієнтів достатньо 2-4 тиж терапії.
У переважній більшості випадків для лікування пацієнтів із ППВ/ЕП без респіраторних порушень достатньо АБТ. Клінічно значущі ППВ/ЕП потребують проведення плевральної пункції або дренажу. Також можливе внутрішньоплевральне введення фібринолітиків.
Абсцес легені
Розвиток абсцесу легені запідозрюють у пацієнтів із постійною або інтермітуючою лихоманкою після перенесеної респіраторної інфекції і наявністю обмеженої ділянки ослабленого дихання та укорочення перкуторного звуку. Остаточний діагноз ставиться на підставі даних рентгенограми органів грудної клітки та інших методів візуалізації.
Контрастна КТ грудної клітки є кращим методом візуалізації при діагностиці абсцесу легені, оскільки це дослідження дає змогу диференціювати абсцес від ЕП, деструктивної пневмонії, секвестру або інших вроджених змін. При лікуванні абсцесів легені необхідне раннє залучення торакальних хірургів, особливо у разі вторинних абсцесів легені на тлі патології розвитку (наприклад, при секвестрації легені). Тривалість АБТ варіює від 3 до 8 тиж. Парентерально вводити ЛЗ рекомендується впродовж 1-3 тиж.
Враховуючи спектр причинно-значущих патогенів для первинної емпіричної терапії, рекомендовано комбінацію амінопеніциліну та інгібіторів бета‑лактамаз. Альтернативою є кліндаміцин у поєднанні з цефалоспоринами ІІ чи ІІІ покоління (цефуроксим, цефотаксим, цефтріаксон; панель 2).
При терапії вторинних абсцесів легень необхідно враховувати анаеробні мікроорганізми слизової оболонки ротоглотки. Більш інвазивний хірургічний підхід із частковою резекцією частки або лобектомії застосовують при таких ускладненнях, як масивна ЕП з необхідністю декортикації або в разі бронхоплевральної фістули. Пневматоцеле, яке часто спричинюється S. aureus, може різко погіршувати стан пацієнта у разі розвитку пневмотораксу, але при належному догляді захворювання виліковується без наслідків. Виняток становлять інфекції, спричинені Panton-Valentin-лейкоцидин-позитивними стафілококами, які можуть призводити до тяжкого некрозу легень із високою летальністю. Оскільки ПП, спричинена стафілококами, не притаманна імунологічно здоровим людям, проводять відповідне імунологічне дослідження.
Пацієнтам із ПП і абсцесами легень першочергово рекомендується призначення АБТ; периферичні абсцеси легень, не пов’язані з бронхіальною системою, можуть бути пунктовані і дреновані за допомогою методів візуалізації.
Деструктивна пневмонія (некротична пневмонія, легенева гангрена)
Деструктивна пневмонія – тяжке ускладнення ПП із деструкцією й утворенням порожнин у легеневій тканині в дітей із вродженими або набутими кістозними вадами розвитку органів грудної клітки, секвестрацією легені, бронхоектазами, супутніми захворюваннями й імунними дефектами.
За наявності клінічної картини і рентгенологічних даних, таких як ознаки розправлення легеневої тканини і/або кіст, частково заповнених рідиною, розглядається можливість проведення КТ для підтвердження діагнозу.
Рекомендується значно триваліша АБТ, ніж у пацієнтів із ПП без ускладнень. Середня тривалість лікування становить 28 днів. Якщо збудник не ідентифікований, то емпірично використовують піперацилін/тазобактам, цефалоспорини ІІ або ІІІ покоління і кліндаміцин. У разі резистентного перебігу захворювання після ретельного зважування ризиків і переваг рекомендується хірургічне втручання на грудній клітці (відеоторакоскопія, можливо, з декортикацією легені). Для лікування при більшості деструктивних пневмоній у дітей достатньо проведення консервативної АБТ. Рентгенологічне дослідження органів грудної клітки проводять протягом тривалого періоду для виявлення основної вади розвитку або інших патологій.
У пацієнтів із ПП і деструктивною формою пневмонії першою лінією лікування є АБТ. Інвазивні втручання слід застосовувати з великою обережністю.
Дихальна недостатність
Встановити прогностичну оцінку для дітей, до якої входять такі параметри, як ранній дитячий вік (<6 міс), коморбідність, гіпоксемія (SpO2<90%), артеріальна гіпотензія, доведена бактеріємія, тяжкість захворювання легень і позалегеневі порушення (наприклад, ниркова або печінкова дисфункція). Дітям з ізольованою дихальною недостатністю рекомендується неінвазивна вентиляція легень, щоб уникнути ендотрахеальної інтубації.
Системні ускладнення
Порушення водно-електролітного балансу
У дітей із ПП як саме захворювання, так і ятрогенні порушення можуть призводити до порушень балансу рідини, електролітів і метаболізму глюкози. Гіпонатріємія часто асоційована з тяжкою формою ПП і підвищенням температури тіла, рівнів лейкоцитів, нейтрофілів, СРБ, прокальцитоніну і зниженням осмолярності сироватки. Синдром неадекватної секреції АДГ (SIADH, Schwartz-Bartter-Syndrom) може виявлятися в пацієнтів із ПП у вигляді порушення свідомості і церебральних судом. Патофізіологічно як водно-електролітний дисбаланс, так і прямі ендокринні явища (підвищена секреція натрійуретичного пептиду у правому відділі серця через пневмонію). У пацієнтів із тяжкою формою ПП регулярно контролюють рівень електролітів у сироватці і рівень глюкози у крові.
Сепсис і дисеміновані інфекції
Пневмонія може виникнути не тільки внаслідок інфекції верхніх дихальних шляхів, але й гематогенно як легеневі прояви інвазивного пневмококового захворювання. Діти з пневмонією і сепсисом тяжко хворіють і потребують проведення інтенсивної терапії. Метастатичні осередки інфекції для різних патогенів (пневмококи, S. aureus) можуть проявлятися як остеомієліт, перикардит або септичний артрит.
Інші позалегеневі прояви
Гемолітико-уремічний синдром (ГУС) зустрічається в поодиноких випадках, особливо при ПП, спричиненій пневмококами. ГУС проявляється блідістю шкірних покривів, набряками, наявністю анемії та гострої ниркової недостатності. Факторами ризику розвитку ГУС при інвазивній пневмококовій пневмонії є деструктивна пневмонія, інфікування пневмококом серотипу 3 і виявлення гена нейрамінідази NanC.
У дітей із ПП, спричиненою M. pneumoniae, іноді спостерігають позалегеневі прояви, такі як висипання, кропив’янка або дискомфорт у суглобах. Рідко спостерігають такі ускладнення, як гемолітична анемія, панкреатит, гепатит, пери-/міокардит, різні форми мукозиту, багатоформна ексудативна екзантема, а також асептичний менінгіт, енцефаліт, поперечний мієліт і гострі психози. Тоді як легеневі прояви є наслідком прямого пошкодження патогену, у разі позалегеневих ускладнень обговорюється імунореактивний процес.
Затверджено Наказом МОЗ України № 1380 від 02.08.2022 р.
Друкується у скороченні. Текст адаптовано й уніфіковано до стандартів тематичного випуску медичної газети «Здоров’я України».
Повний текст за посиланням: https://moz.gov.ua/.
Тематичний номер «Педіатрія» № 1 (67) 2023 р.