3 травня, 2023
Керівництво Глобальної стратегії діагностики, лікування та профілактики ХОЗЛ
Global Initiative for Chronic Obstructive Lung Disease, GOLD, перегляд 2023 року
Наразі хронічне обструктивне захворювання легень (ХОЗЛ), як і прогнозували, уже є однією з трьох основних причин смерті в усьому світі, причому 90% цих смертей – у країнах із низьким і середнім рівнем доходу [1, 2]. 2012 року від ХОЗЛ померло понад 3 млн світової популяції, що становить 6% усіх смертей у світі. ХОЗЛ є значною проблемою для охорони здоров’я, однак ця хвороба піддається лікуванню та профілактиці. ХОЗЛ є основною причиною хронічної захворюваності та смертності в усьому світі; багато людей хворіють роками і передчасно помирають через ХОЗЛ або його ускладнення. Тягар, зумовлений ХОЗЛ, за прогнозами, упродовж наступних десятиліть збільшуватиметься внаслідок тривалого впливу факторів ризику розвитку ХОЗЛ і старіння населення [3]. Метою Глобальної стратегії діагностики, лікування та профілактики ХОЗЛ (редакція 2023 року) є надання неупередженого огляду поточних доказових даних щодо оцінки, діагностики та лікування пацієнтів із ХОЗЛ, що може допомогти клініцисту. Обговорення ХОЗЛ та його лікування, рівні доказів і конкретні цитати з наукової літератури наведені в оригіналі документа, що доступний на сайті www.goldcopd.org.
Визначення та загальні положення
У новій редакції GOLD 2023 було запропоновано нове визначення ХОЗЛ.
Хронічне обструктивне захворювання легень – гетерогенний стан легень, що характеризується хронічними респіраторними симптомами (задишка, кашель, виділення мокротиння, загострення) внаслідок патологічних змін дихальних шляхів (бронхіт, бронхіоліт) і/або альвеол (емфізема), що спричиняють персистувальну, часто прогресувальну обструкцію повітряного потоку [1].
Чинники та фактори ризику ХОЗЛ
- ХОЗЛ є результатом взаємодії генів (gene, G) із середовищем (environment, E), яка відбувається протягом життя (lifetime, T) людини (GETomics) і може призводити до ушкодження легень і/або порушення їх нормального розвитку / процесу старіння.
- Основним фактором довкілля, що призводить до ХОЗЛ, є куріння тютюну та вдихання токсичних часточок, побутових газів, забрудненого атмосферного повітря, зумовити захворювання також можуть інші екологічні та індивідуальні фактори з боку організму людини (у тому числі аномалії розвитку легень, прискорені процеси їх старіння).
- Найважливішим (хоча й досить рідкісним) генетичним фактором ризику розвитку ХОЗЛ, що його було виявлено на сьогодні, є мутації в гені SERPINA1, який призводить до дефіциту α‑1-антитрипсину. Є також низка інших генетичних факторів, асоційованих із порушенням функції легень і ризиком розвитку ХОЗЛ, але масштаб їх індивідуального впливу незначний.
Критерії діагнозу і клінічні симптоми ХОЗЛ
Діагностика
Діагноз ХОЗЛ потрібно припускати в будь-якого пацієнта із задишкою, хронічним кашлем або продукцією мокротиння і/або наявністю факторів ризику розвитку захворювання в анамнезі (табл. 1), але обов’язковою для встановлення діагнозу ХОЗЛ є спірометрія з форсованим видихом, що після застосування бронходилататора демонструє відношення об’єму форсованого видиху за 1-шу секунду до функціональної життєвої ємності легень (ОФВ1_/ФЖЄЛ) <0,70% [4].
Симптоми ХОЗЛ
Хронічна задишка є найхарактернішим симптомом ХОЗЛ. Кашель із виділенням мокротиння зазвичай спостерігають у 30% пацієнтів. Ці симптоми можуть варіювати щодня [5] і передувати розвитку бронхіальної обструкції за багато років. Особи з такими симптомами, зокрема за наявності факторів ризику ХОЗЛ, обов’язково мають бути обстежені щодо виявлення причин цих симптомів. Бронхіальна обструкція може розвиватися як без хронічної задишки і/або кашлю і виділення мокротиння, так і навпаки [6]. Хоча ХОЗЛ переважно визначається як бронхіальна обструкція, у лікарській практиці зазвичай саме вплив симптомів на функціональні можливості пацієнта спонукає його звернутися по медичну допомогу.
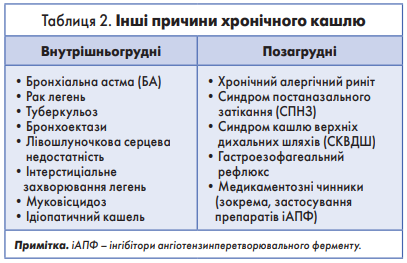
Хронічний кашель
Хронічний кашель часто є першим симптомом ХОЗЛ, але пацієнти зазвичай не вважають його очікуваним наслідком куріння і/або негативного впливу навколишнього середовища. Спочатку кашель може бути періодичним, але згодом починає турбувати щодня і часто протягом дня. Хронічний кашель у разі ХОЗЛ може бути як продуктивним, так і непродуктивним [7]. У деяких випадках значна бронхіальна обструкція може розвиватися без симптому кашлю. Інші причини хронічного кашлю наведені в таблиці 2. У пацієнтів із тяжким перебігом ХОЗЛ під час кашлю можуть виникати синкопальні стани через швидке підвищення внутрішньогрудого тиску у разі тривалих нападів кашлю. Останні навіть можуть спричиняти переломи ребер, які іноді є безсимптомними.
Продукція мокротиння
У пацієнтів із ХОЗЛ під час кашлю зазвичай виділяється невелика кількість в’язкого мокротиння. Класичним визначенням хронічного бронхіту є регулярна продукція мокротиння упродовж ≥3 місяців протягом 2 років поспіль (за відсутності будь-яких інших чинників, які б могли пояснити цей симптом) [8], хоче це визначення є дещо довільним і таким, яке не відображає всіх нюансів виділення мокротиння в разі ХОЗЛ (детальніше – в основному документі GOLD2023, Розділ 1). Продукцію мокротиння зазвичай важко оцінити об’єктивно, оскільки пацієнти можуть його радше ковтати, ніж відхаркувати, звичка, яка значуще залежить від культурних і статевих відмінностей.
Крім того, виділення мокротиння може бути інтермітуючим, з періодами загострення і ремісії [9]. Пацієнти, в яких виділяється велика кількість мокротиння, можуть страждати на бронхоектатичну хворобу [10, 11]. Наявність гнійного мокротиння є результатом збільшення вмісту медіаторів запалення [12, 13], це може вказувати на початок бактеріального загострення, хоча зв’язок є досить слабким [13, 14].
Хрипи та відчуття стиснення в грудях
Хрипи на вдиху і/або видиху, відчуття стиснення в грудях є симптомами, які можуть варіювати як щоденно, так і протягом дня. Крім того, під час аускультації на вдиху або видиху вислуховують розсіяні хрипи. Відчуття стиснення в грудній клітці, як правило, розвивається внаслідок фізичного навантаження, не має чіткої локалізації, має м’язовий характер і може виникати внаслідок ізометричного скорочення міжреберних м’язів. Відсутність хрипів або стиснення в грудній клітці не виключає діагнозу ХОЗЛ, як і наявність цих симптомів не є підтвердженням астми.
Слабість
Слабість – це суб’єктивне відчуття втоми або виснаження і є одним із найпоширеніших і тривожних симптомів, що їх відчувають пацієнти з ХОЗЛ [15]. Вони описують слабість як відчуття «загальної втоми» або «вичерпаної енергії» [16, 17]. Втома впливає на повсякденну активність пацієнта та якість його життя.
Додаткові клінічні ознаки на тлі тяжкого перебігу ХОЗЛ
Втрата ваги та м’язової маси, анорексія – поширені ознаки в пацієнтів із тяжким і дуже тяжким ХОЗЛ [18-20]. Зазначені симптоми мають прогностичне значення [21, 22], а також можуть бути ознакою інших захворювань, таких як туберкульоз або рак легень, тому в таких осіб треба завжди проводити дообстеження. Набряк щиколоток може вказувати на наявність у пацієнта легеневого серця. Такі симптоми, як депресія і/або тривога, потребують особливої уваги під час збору анамнезу хвороби, оскільки вони є доволі поширеними в пацієнтів із ХОЗЛ [23] і асоціюються з погіршенням стану здоров’я, підвищеним ризиком загострень і екстреною госпіталізацією та потребують лікування [24].
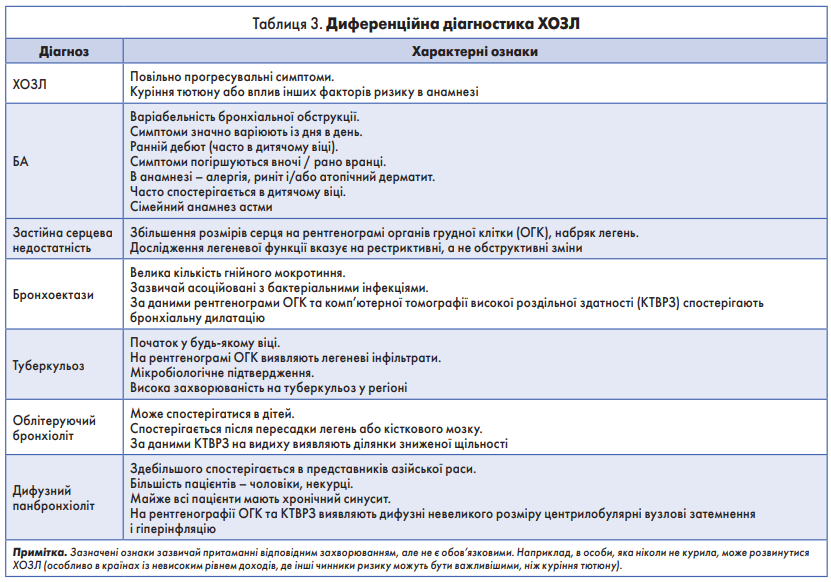
Диференційний діагноз ХОЗЛ
У деяких пацієнтів із ХОЗЛ дуже важко чітко відрізнити симптоми від таких у разі астми навіть за допомогою сучасних методів візуалізації та низки функціональних тестів, оскільки обидва захворювання мають спільні риси та клінічні прояви [25]. Більшість інших потенційних симптомів і діагнозів, з якими необхідно проводити диференційну діагностику ХОЗЛ, наведено в таблиці 3.
Оцінка тяжкості ХОЗЛ
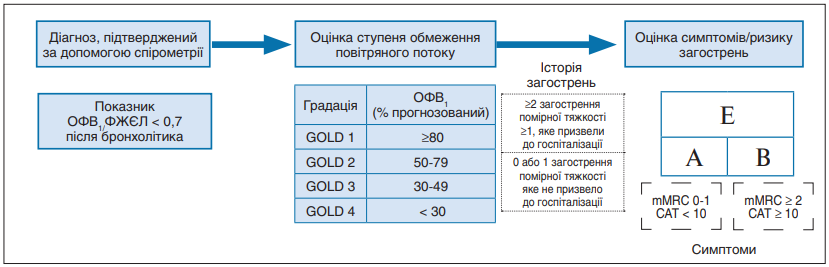
Коли діагноз ХОЗЛ підтверджено даними спірометрії, для того щоб рекомендувати відповідну терапію і досягти цілей лікування, необхідно оцінити такі чотири фундаментальні аспекти:
- тяжкість обмеження повітряного потоку;
- природа та вираженість поточних симптомів у пацієнта;
- попередній анамнез помірних і тяжких загострень;
- наявність і вид супутніх захворювань (мультиморбідність).
Оцінка тяжкості бронхіальної обструкції
За наявності співвідношення ОФВ1/ФЖЄЛ <0,7, оцінка тяжкості обмеження повітряного потоку в разі ХОЗЛ (зверніть увагу, що вона може відрізнятися від тяжкості самого захворювання) базується на значенні ОФВ1 після застосування бронхолітика, постбронхолітичного ОФВ1 (% прогнозованого значення). Для спрощення, в таблиці 4 наведено ступені тяжкості ХОЗЛ залежно від спірометричних даних.
Оцінка тяжкості симптомів
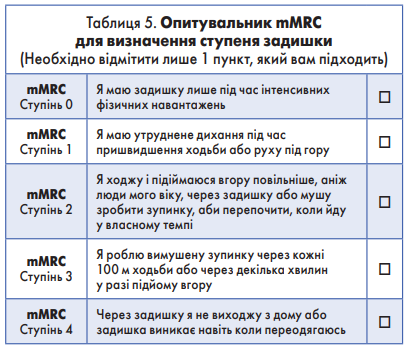
Оскільки кореляція між тяжкістю бронхіальної обструкції і симптомами, які демонструє пацієнт із ХОЗЛ, може бути доволі слабка [32, 33], формальну оцінку симптомів проводять згідно з даними Модифікованого опитувальника Ради медичних досліджень (modified Medical Research Council, mMRC) (табл. 5).
Для оцінки контролю симптомів застосовують також багатовимірні опитувальники. Оскільки наразі відомо, що окрім задишки ХОЗЛ також чинить багатовекторний вплив на стан пацієнтів [38], тож саме з цієї причини рекомендовані такі багатовимірні опитувальники. Нижче наведено один із таких – опитувальник з оцінки ХОЗЛ (COPD Assessment Test (CAT™), розроблений для використання в клінічній практиці. Це анкета з 8 пунктів, яка оцінює загальний стан здоров’я пацієнтів із ХОЗЛ (рис. 1).
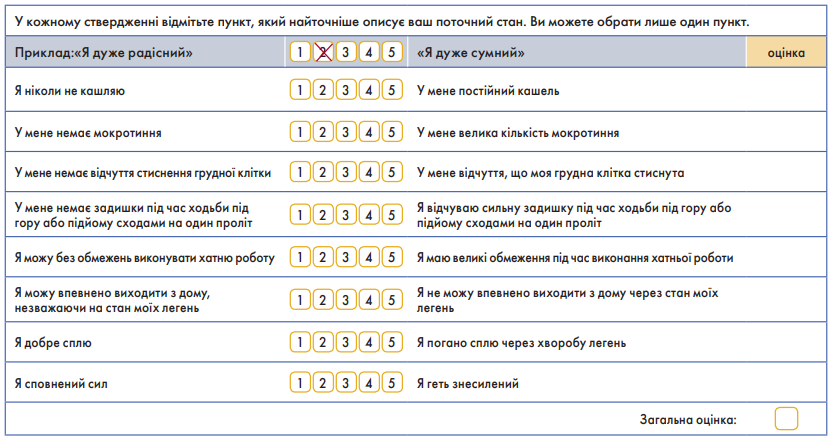 Рис. 1. Опитувальник з оцінки ХОЗЛ CAT™ (Jones et al., ERJ 2009)
Рис. 1. Опитувальник з оцінки ХОЗЛ CAT™ (Jones et al., ERJ 2009)
Комбінована початкова терапія ХОЗЛ
У 2011 р. GOLD запропонувала перейти від простої спірометричної системи класифікації тяжкості захворювання та, відповідно, лікування, до комбінованої стратегії, заснованої на оцінці тяжкості симптомів (за допомогою інструментів mMRC або CAT™), тяжкості обмеження повітряного потоку (1-4 класи GOLD) і частоти попередніх загострень. Така класифікація була запропонована як керівництво щодо початку фармакологічного лікування. Головним кроком уперед, зробленим завдяки цій комбінованій стратегії оцінки тяжкості ХОЗЛ, було враховувати інформацію про стан пацієнтів, яку повідомляють самі пацієнти, і наголошувати на важливості профілактики загострень у процесі лікуванні ХОЗЛ. Початкова версія комбінованої оцінки тяжкості перебігу ХОЗЛ залежала як від тяжкості бронхіальної обструкції (GOLD, класи 1-4), так і від частоти попередніх загострень для оцінки ризику майбутніх загострень.
Тяжкість бронхіальної обструкції згодом було виключено з цієї комбінованої схеми оцінки через її низьку точність на індивідуальному рівні (порівняно з такою в рамках популяції) щодо прогнозування наслідків і прийняття рішень із лікування, а також як таку, що ускладнює використання класифікації клініцистами [33, 48-50].
Нині, у новій редакції 2023 року, GOLD пропонує подальшу еволюцію комбінованого інструменту оцінки ХОЗЛ за ABCD, який визнає клінічну значимість загострень незалежно від рівня симптомів у пацієнта (рис. 2). Групи A і B залишилися без змін, але групи C і D тепер об’єднані в одну групу, позначену «E», щоб підкреслити клінічну значущість загострень. Ми визнаємо, що цю пропозицію доведеться прийняти і вона має бути підтверджена відповідними клінічними дослідженнями.
Рис. 2. Метод оцінки тяжкості ХОЗЛ за АВЕ GOLD 2023
Фармакологічна терапія стабільного ХОЗЛ
Ціллю фармакологічної терапії пацієнтів із ХОЗЛ є зменшення симптомів захворювання, зменшення ризику та тяжкості загострень, поліпшення загального стану здоров’я, підвищення толерантності до фізичних навантажень, а також виживаності.
Результати окремих клінічних випробувань щодо того, що фармакотерапія здатна сповільнювати швидкість зниження ОФВ1 у разі ХОЗЛ, не були достатньо переконливими [54-58]. Однак систематичний огляд, що поєднує дані 9 досліджень, продемонстрував, що, на відміну від плацебо, у групах активного лікування ХОЗЛ відбувалося зменшення швидкості зниження ОФВ1 на 5,0 мл/рік [59]. Різниця цього показника між групами лікування, що використовували бронходилататори тривалої дії, і групами плацебо, становила 4,9 мл/рік, а різниця між групами лікування, що застосовували інгаляційний кортикостероїд (ІКС), і групами плацебо становила 7,3 мл/рік.
Отже, звичайно, необхідно знати про потенційну користь фармакотерапії ХОЗЛ щодо зменшення зниження показників легеневої функції, але також необхідні подальші дослідження, щоб зрозуміти, в якій категорії пацієнтів вона буде найбільш ефективна.
Вибір класу препаратів для лікування ХОЗЛ залежить від деяких факторів – доступності і вартості ліків, балансу між ефективністю і побічними ефектами, до того ж будь-який режим лікування необхідно індивідуалізувати відповідно до тяжкості симптомів, рівня бронхіальної обструкції та тяжкості загострень.
Алгоритми оцінки симптомів, початкового та подальшого фармакологічного лікування
Пропозицію щодо початкового фармакологічного лікування ХОЗЛ відповідно до індивідуальної оцінки симптомів і ризику загострення показано в рамках алгоритму АВЕ на рисунку 3. Цей алгоритм є спробою надати клінічні рекомендації. Сьогодні немає доказів високої якості – таких як рандомізовані контрольовані дослідження (РКД) – на підтвердження стратегії початкового фармакологічного лікування в пацієнтів із вперше виявленим ХОЗЛ.
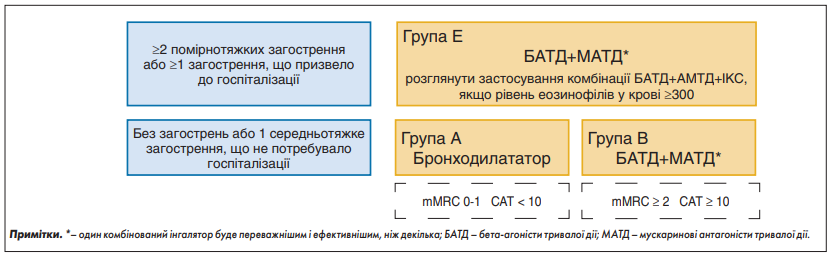 Рис. 3. Початкове фармакологічне лікування ХОЗЛ (GOLD 2023)
Рис. 3. Початкове фармакологічне лікування ХОЗЛ (GOLD 2023)
Після призначення терапії її ефективність щодо досягнення основних цілей лікування ХОЗЛ має бути оцінена під час повторного огляду пацієнта, також необхідно активно виявляти будь-які перешкоди для успішного лікування (рис. 4). Після оцінки відповіді пацієнта на початкове фармакологічне лікування може знадобитися його корекція.
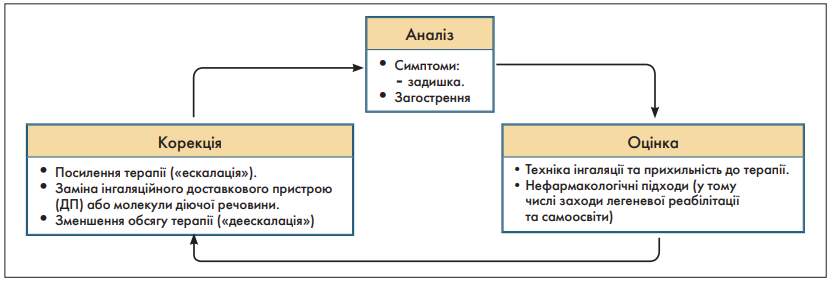 Рис. 4. Цикл ведення пацієнта з ХОЗЛ
Рис. 4. Цикл ведення пацієнта з ХОЗЛ
Окремий алгоритм надається для подальшого лікування ХОЗЛ, де менеджмент захворювання фокусується на двох ключових ознаках, які можна лікувати: стійкість задишки та поява загострень (рис. 5). Ці подальші рекомендації сформульовані для полегшення ведення пацієнтів, які вже приймають підтримувальну терапію, незалежно від того, як давно – невдовзі після призначення початкового лікування чи протягом років спостереження. Ці рекомендації засновані на даних клінічних випробувань і такого показника, як рівень еозинофілів у крові, як біомаркера доцільності використання ІКС для профілактики загострення ХОЗЛ.
Рис. 5. Схема подальшої фармакотерапії ХОЗЛ (GOLD 2023)
Початкове фармакологічне лікування
Швидкодопоміжні бронхолітики короткої дії мають бути призначені всім пацієнтам із ХОЗЛ для швидкого усунення симптомів.
Група А
- Усім пацієнтам групи А треба пропонувати бронхолітичну терапію, з огляду на її вплив на задишку. Це може бути бронхолітик короткої або тривалої дії. За наявності та доступності перевагу віддають бронходилататору тривалої дії, за винятком пацієнтів із дуже нерегулярною задишкою.
- Якщо було зафіксовано терапевтичний ефект, варто дотримуватися такого лікування і надалі.
Група В
- Терапію потрібно розпочинати з комбінації БАТД+МАТД. У рамках РКД було показано, що в пацієнтів із ≤1 помірним загостренням упродовж року перед дослідженням та CAT™ ≥10 комбінація БАТД+МАТД перевершує монотерапію МАТД за кількома кінцевими точками [126]. Таким чином, за умови відсутності проблем щодо доступності, вартості та побічних ефектів комбінація БАТД+МАТД є рекомендованим початковим вибором лікування.
- Якщо комбінацію БАТД+МАТД вважають неприйнятною, жодних доказів щодо переваг одного класу бронходилататорів тривалої дії над іншим (БАТД чи МАТД) для початкового усунення симптомів у пацієнтів групи В немає. Пацієнт може обрати бронхолітик, з огляду на власні вподобання і ефективність.
- Пацієнти групи B, імовірно, матимуть супутні захворювання, які можуть посилювати симптоми та впливати на подальший прогноз, отже, необхідно виявляти і вчасно лікувати коморбідність відповідно до певних національних та міжнародних настанов [254, 255].
Група Е
- Кокранівський систематичний огляд і мережевий метааналіз, у рамках якого порівнювали подвійну комбіновану терапію проти монотерапії бронходилататорами тривалої дії, продемонстрував, що застосування комбінації БАТД+МАТД сприяє зменшенню загострень ХОЗЛ [256]. Таким чином, за умови відсутності проблем щодо доступності, вартості та побічних ефектів комбінація БАТД+МАТД є переважною. Отже, БАТД+МАТД є кращим вибором для початкової терапії в пацієнтів групи E.
- Застосування комбінації БАТД+ІКС при ХОЗЛ не заохочується. Якщо є показання для призначення ІКС, то це має бути комбінація БАТД+МАТД+ІКС. Як показують дослідження, ефективність цієї комбінації перевершує таку в БАТД+ІКС і є кращим вибором [133, 204].
- Розгляньте можливість призначення комбінації БАТД+МАТД+ІКС у пацієнтів групи E, якщо рівень еозинофілів у крові ≥300 кл./мкл (практична рекомендація). Як зазначено, ефективність ІКС щодо профілактики загострень корелює з рівнем еозинофілів у крові. Оскільки в літературі немає прямих даних щодо початку потрійної терапії в пацієнтів із уперше діагностованим ХОЗЛ, ми вважаємо, що для пацієнтів із високим рівнем еозинофілів ≥300 кл./мкл потрійна терапія є обґрунтованою.
- Якщо пацієнти з ХОЗЛ мають супутню астму, їх треба лікувати, як пацієнтів з астмою. За таких обставин призначення ІКС є обов’язковим.
Подальше фармакологічне лікування
Алгоритм подальшого фармакологічного лікування (див. рис. 5) можна застосувати до будь-якого пацієнта, який вже отримує підтримувальну терапію незалежно від групи GOLD, що їх було виділено в рамках призначення початкової терапії. Необхідно орієнтуватися передусім на такі симптоми, як задишка / обмеження активності, які потрібно контролювати в кожного пацієнта, щоб запобігти подальшим загостренням. Якщо зміна лікування вважається необхідною, виберіть відповідний алгоритм для задишки (лівий стовпчик на рисунку) або загострень (правий стовпчик на рисунку); алгоритм загострення також необхідно обирати для пацієнтів, які потребують зміни в лікуванні як задишки, так і загострення.
Подальше фармакологічне лікування має керуватися вже відомими принципами – спочатку Аналіз та Оцінка, а потім Корекція:
- Аналіз: оцініти симптоми (задишка) та ризик загострення (анамнез, рівень еозинофілів у крові).
- Оцінка: оцінити техніку інгаляції та прихильність до терапії, а також можливу роль немедикаментозних підходів лікування.
- Корекція: відкоригувати – ескалація або деескалація фармакотерапії. Заміна інгаляційного ДП або молекули діючої речовини в межах одного класу препаратів (наприклад, використання іншого БАТД). Будь-яка зміна в складі терапії потребує подальшої оцінки клінічної відповіді, у тому числі моніторингу можливих побічних ефектів.
Задишка
- Для пацієнтів зі стійкою задишкою або обмеженням фізичної активності, які використовують монотерапію бронходилататорами [257], рекомендовано застосування комбінації двох бронхолітиків тривалої дії.
- Якщо додавання другого бронходилататора тривалої дії не покращує симптоми, пропонується розглянути заміну або інгаляційного ДП, або молекули діючої речовини.
- На всіх стадіях, якщо має місце задишка, спричинена іншими чинниками окрім ХОЗЛ, необхідно проведення діагностичних заходів щодо виявлення її причин та відповідне лікування. У разі неадекватної відповіді на належним чином призначене лікування серед причин потрібно розглядати неправильну техніку інгаляцій і недостатню прихильність до лікування.
Загострення
- Пацієнтам із персистуючими загостреннями ХОЗЛ, які отримують монотерапію бронходилататором, рекомендованo посилення терапії у вигляді комбінації БАТД+МАТД.
- Визначення рівня еозинофілів у крові може виявити пацієнтів, які з більшою ймовірністю дадуть позитивну терапевтичну відповідь на призначення ІКС. Для пацієнтів, в яких розвиваються загострення на тлі монотерапії БАТД, та кількістю еозинофілів у крові ≥300 кл/мкл, можна розглянути ескалацію терапії до потрійної комбінації – БАТД+МАТД+ІКС [133].
- Пацієнтам, в яких розвиваються подальші загострення під час терапії комбінацією БАТД+МАТД, пропонуються альтернативні шляхи. Рівень еозинофілів у крові <100 кл/мкл може бути маркером низької ймовірності сприятливої відповіді на застосування ІКС:
- вдавання до ескалації щодо потрійної комбінації БАТД+МАТД+ІКС. Позитивна терапевтична відповідь після додавання до комбінації ІКС може спостерігатися за рівніі еозинофілів у крові ≥100 кл/мкл, причому краща відповідь на ІКС корелює з вищим рівнем еозинофілів у крові.
- Якщо пацієнти, які отримували лікування комбінацією БАТД+МАТД+ІКС (або ті, у кого рівень еозинофілів у крові <100 кл./мкл), усе ще мають загострення, необхідно розглянути такі варіанти:
- додати рофлуміласт. Цю опцію можна розглянути в пацієнтів з ОФВ1 <50% від прогнозованого та з хронічним бронхітом [212], особливо якщо вони пережили принаймні одну госпіталізацію з приводу загострення ХОЗЛ упродовж останнього року [213, 258];
- додати макролід. Є найкраща доступна доказова база щодо ефективності застосування азитроміцину, особливо в пацієнтів, які нині не є курцями [214, 223]. Під час прийняття рішення щодо призначення азитроміцину необхідно враховувати проблему і наслідки розвитку антибіотикорезистентності;
- розглянути можливість відміни ІКС у разі розвитку пневмонії або інших значущих побічних ефектів. Якщо рівень еозинофілів у крові ≥300 кл/мкл, деескалація, швидше за все, буде асоційована з розвитком загострень [162, 163]. Ретельно оцініть дозу ІКС, що використовується, для зменшення потенційної побічні дії ІКС, яка розвивається радше за умови застосування вищих доз.
Пацієнти, що отримують комбінацію БАТД+ІКС
- Якщо пацієнт із ХОЗЛ і без ознак астми з будь-якої причини отримував лікування комбінацією БАТД+ІКС і захворювання добре контролювалося з огляду на симптоми і загострення, продовження такої терапії – БАТД+ІКС – буде засобом вибору. Проте, якщо пацієнт має:
а) подальші загострення, необхідна ескалація лікування, а саме – перехід на потрійну комбінацію БАТД+МАТД+ІКС;
б) виражені основні симптоми – потрібно розглянути перехід на комбінацію БАТД+МАТД.
Інше фармакологічне лікування
Інше фармакологічне лікування ХОЗЛ представлено в таблиці 6.
Нефармакологічне лікування стабільного ХОЗЛ
Немедикаментозне лікування доповнює фармакологічне та має бути частиною комплексної терапії ХОЗЛ.
Після встановлення діагнозу ХОЗЛ пацієнт має отримати всю подальшу інформацію про свій стан. Лікарі мають наголошувати на важливості середовища, вільного від тютюнового диму, прихильності до призначеної терапії, впевнитися правильності і контролювати техніку інгаляції під час застосування інгаляційних препаратів, усіляко сприяти фізичній активності, призначати щеплення та направляти пацієнтів на пульмонологічну реабілітацію.
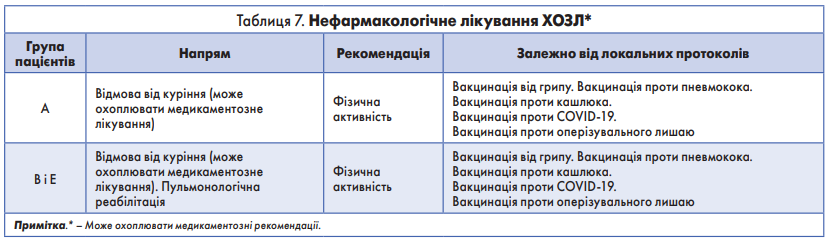
Деякі відповідні немедикаментозні заходи узагальнені в таблиці 7.
Лікування загострень ХОЗЛ – ключові положення
- Загострення ХОЗЛ визначається як подія, що характеризується задишкою і/або кашлем з виділенням мокротиння, які погіршуються протягом <14 днів. Загострення ХОЗЛ часто асоціюється з посиленням системного і локального запального процесу, що його спричиняє інфекція дихальних шляхів, полютанти або інші негативні впливи не легені.
- Оскільки симптоми загострення ХОЗЛ не є специфічними, необхідно проводити диференційну діагностику, у рамках якої необхідно розглядати, зокрема, такі стани, як пневмонія, застійна серцева недостатність, емболія легеневої артерії.
- Метою лікування загострень ХОЗЛ є мінімізація негативного впливу поточного загострення та запобігання подальшим таким подіям.
- Як початковий бронхолітик в лікуванні загострення ХОЗЛ рекомендовано застосування БАКД з/без антихолінергічних засобів короткої дії.
- Підтримувальна терапія БАТД має бути розпочата якнайшвидше. У пацієнтів із частими загостреннями і підвищеним рівнем еозинофілів у крові до комбінації двох бронходилататорів необхідно розглянути доцільність додавання ІКС.
- У пацієнтів із тяжким загостренням призначення системних кортикостероїдів може покращити функцію легень (ОФВ1), оксигенацію та скоротити час відновлення, у тому числі зменшити тривалість госпіталізації. Тривалість терапії зазвичай не має перевищувати 5 днів.
- Антибіотики, за наявності показань, можуть пришвидшити одужання, знизити ризик розвитку раннього рецидиву, неефективності лікування та скоротити строк госпіталізації. Тривалість терапії має становити 5 днів.
- Метилксантини не рекомендуються через часті побічні ефекти.
- Неінвазивна механічна вентиляція має бути першим методом вентиляції у хворих на ХОЗЛ із гострою дихальною недостатністю, які не мають абсолютних протипоказань, оскільки вона покращує газообмін, полегшує дихання і зменшує потребу в інтубації, скорочує тривалість госпіталізації та поліпшує виживаність пацієнтів.
- Тривалість реабілітації після загострення може бути різною, 4-6 тиж, при цьому деяким пацієнтам так і не вдається повернутися до функціонального стану, який передував загостренню. Після загострення необхідно вжити відповідних заходів для подальшої профілактики загострень.
ХОЗЛ і COVID‑19 – ключові положення
- Особам із ХОЗЛ, в яких з’являються або прогресують респіраторні симптоми, лихоманка і/або будь-які інші прояви, що можуть бути асоційовані з COVID‑19, навіть якщо вони мають легкий перебіг, необхідно провести тестування і виключити факт зараження SARS-CoV‑2.
- Пацієнти мають продовжувати приймати раніше призначені пероральні та інгаляційні респіраторні препарати для лікування ХОЗЛ.
- Під час періодів широкої поширеності COVID‑19 у спільноті спірометрію слід проводити обмежено і тільки в пацієнтів, які потребують термінових або вкрай необхідних досліджень щодо діагностики ХОЗЛ і/або для оцінки стану функції легень перед проведенням інтервенційних процедур або операції.
- Фізичне дистанціювання, захист або «укриття на місці» (sheltering-in-place), які стали поширеними під час пандемії, не мають призводити до соціальної ізоляції та відмови від активності. Пацієнтам потрібно підтримувати зв’язок зі своїми друзями та родиною телекомунікаційно і залишатися фізично активними. Пацієнти також мають подбати про те, щоб забезпечити себе необхідними ліками.
- Треба заохочувати пацієнтів використовувати авторитетні ресурси для отримання медичної інформації щодо COVID‑19 та його лікування.
- Пацієнту з ХОЗЛ необхідно надати відповідні рекомендації щодо дистанційного спостереження (телефоном/віртуального/онлайн) та роздрукований план дій.
Список літератури – у редакції.
Реферативний огляд Pocket guide to COPD diagnosis, management, and prevention (2023 REPORT).
Підготувала Анна Артюх
Повну версію дивіться: https://goldcopd.org/
Тематичний номер «Пульмонологія, Алергологія, Риноларингологія» № 1 (62) 2023 р.