24 травня, 2023
Щитоподібна залоза та йодна профілактика: як коректно діяти в умовах радіаційних ризиків?
 Радіаційна небезпека існувала від початку виникнення атомних електростанцій. В умовах війни рф проти України увага всього світу прикута до них, адже наслідки аварії чи ядерної атаки можуть бути масштабними та катастрофічними. У березні 2022 року росіяни захопили Чорнобильську АЕС, а пізніше з’явилася загроза в Енергодарі. Відтоді розпочалися запеклі дискусії стосовно йодної профілактики.
Радіаційна небезпека існувала від початку виникнення атомних електростанцій. В умовах війни рф проти України увага всього світу прикута до них, адже наслідки аварії чи ядерної атаки можуть бути масштабними та катастрофічними. У березні 2022 року росіяни захопили Чорнобильську АЕС, а пізніше з’явилася загроза в Енергодарі. Відтоді розпочалися запеклі дискусії стосовно йодної профілактики.
Лікарі завжди шукають баланс між користю лікарських засобів та небажаними ефектами, які можуть нашкодити здоров’ю людини, тому необхідно інформувати людей про адекватну йодну профілактику. Слід чітко розуміти, чого треба боятися при радіаційних ризиках та як правильно діяти. Приймати йод чи ні? Якщо ж приймати, то в якій дозі та наскільки тривало?
У рамках ІV Конгресу української академії педіатричних спеціальностей Prime Pediatrics 2022 Голова правління ГС «Українська академія педіатричних спеціальностей», декан педіатричного факультету НУОЗ України ім. П.Л. Шупика, доктор медичних наук, професор Марина Євгеніївна Маменко представила доповідь «Щитоподібна залоза та йодна профілактика: як коректно діяти в умовах радіаційних ризиків?» та розповіла про аспекти застосування йоду для профілактики і лікування різноманітних захворювань, побічні дії та протипоказання до використання препаратів йоду, а також чого не слід робити при йодному дефіциті, пояснила, що є фізіологічним для щитоподібної залози (ЩЗ).
Як побудована ЩЗ?
ЩЗ називають «першою скрипкою в оркестрі ендокринних залоз» завдяки її ролі в ендокринній системі. Тиреоїдні гормони регулюють усі без винятку види обміну речовин та енергії в нашому організмі, а тому, беззаперечно, впливають на функцію всіх органів та систем в організмі людини. Найбільш вагомий вплив здійснюється на етапі інтенсивного обміну енергії та речовин у період від народження дитини до досягнення двох років.
ЩЗ розташована у нижній третині шиї і в нормі забезпечує адекватну продукцію гормонів, що і є її основною функцією. Головними «будівельним матеріалом» для створення тиреоїдних гормонів є атоми йоду. Звичайно, окрім них, важливу роль відіграють амінокислоти та необхідні ферменти, але галоген йод складає більше половини молекулярної маси у трийодтироніні (59%) та тироксині (65%) [1].
ЩЗ має специфічну фолікулярну будову, завдяки чому вона якісно відчуває вплив тиреотропного гормону, а йод надходить у необхідній кількості. Синтез гормонів відбувається у фолікулах ЩЗ, які є своєрідними мішечками, наповненими колоїдною речовиною. У ній містяться запаси йоду, прекурсорів, тобто попередників майбутніх гормонів, та ферментів. Кожен такий мішечок має стінку, що складається з одного шару тиреоцитів. Один бік тиреоциту повернутий до колоїдної речовини, а інший – до судин, які приносять йод, тиреотропний гормон, різні амінокислоти, необхідні для створення тиреоїдних гормонів.
Роль йоду у функціонуванні організму
Йод називають есенціальним мікроелементом, адже без нього синтез тиреоїдних гормонів неможливий, а відтак, і функціонування різних органів і систем. У нормі в тілі дорослої людини повинно бути 15-20 мг йоду [1].
Міжнародні експерти вже давно прорахували, скільки саме йоду має надходити з продуктами харчування в організм щодня. Це мізерна кількість, що становить лише кілька мікрограмів. Якщо порахувати усю кількість йоду, який у нормі потрібен нашому організму протягом життя для побудови тиреоїдних гормонів, то вийде дуже невелика кількість атомів, які забезпечують гормоногенез. З огляду на перерахунок на кілограм маси тіла, у ранньому дитинстві людині потрібно 90 мкг йоду щодоби, дорослим – приблизно 150 мкг, тільки під час вагітності та періоду лактації людина потребує більше – 250 мкг на добу [1]. Кількість йоду має бути стабільною, адже в нашому організмі немає природного сховища, крім колоїдного простору, який би дозволяв нам тривалий час зберігати й у потрібну хвилину мобілізувати запас йоду.
Отже, ми отримуємо йод із продуктів харчування. Сьогодні родючі ґрунти є збіднілими на цей мікроелемент. Тому, вживаючи продукти рослинного і тваринного походження, ми фізіологічно опиняємося в межах йодного дефіциту. Лише людей, у раціоні яких щодня є морепродукти, можна вважати поза зоною ризику розвитку йододефіцитних захворювань [2].
У структурі йододефіцитних захворювань також наявні ризики і для певних вікових когорт населення: для новонароджених – неонатальний гіпотиреоз, для дітей і підлітків – порушення розумового та фізичного розвитку, для дорослих та осіб будь-якого віку – зоб, гіпотиреоз, порушення когнітивної функції, підвищення чутливості ЩЗ до радіації, яка виникає внаслідок активації інтратиреоїдного захоплення йоду в умовах недостатнього його надходження з продуктами харчування [2].
Якими можуть бути наслідки для ЩЗ від ядерного опромінення?
Зоб – найбільш поширений наслідок йодного дефіциту. На ранніх етапах його розвиток можна розглядати як компенсаторну реакцію, спрямовану на збільшення захоплення йоду для тиреоїдного гормоногенезу. При цьому відбуваються процеси гіперплазії та гіпертрофії, збільшується кровообіг, активізуються ферментативні системи, які відповідають за інтратиреоїдне захоплення йоду, формується колоїдний зоб. За умови збільшення надходження за рахунок додавання у раціон йодованої солі або проведення саплементації препаратами калію йодиду із фізіологічним вмістом йоду процес формування зоба є зворотнім, і об’єм ЩЗ може нормалізуватися. Якщо йодна профілактика не проводиться і йодний дефіцит не ліквідований, у разі виникнення техногенної катастрофи з викидом радіоактивних ізотопів йоду у людини, що проживає в умовах дефіциту йоду, «голодна» ЩЗ починає активно захоплювати ці ізотопи та використовувати для тиреоїдного синтезу. Звісно, серед населення за таких умов буде зростати частота тиреоїдної патології, адже радіація є однією з причин формування зоба та злоякісних новоутворень ЩЗ. Саме зростання кількості випадків тиреоїдного раку у віддаленій перспективі із піком через 7-10 років було головним соматичним наслідком ураження населення, у тому числі дітей, після катастрофи на Чорнобильській АЕС.
Саме на цих знаннях базуються рекомендації щодо використання препаратів калію йодиду для профілактики радіаційного ураження ЩЗ. Прийом йоду у такій формі дозволяє створити конкуренцію радіоактивним ізотопам і знизити вірогідність використання їх для побудови тиреоїдних гормонів.
Для використання під час техногенних катастроф зазвичай рекомендується прийом високих доз йоду (65-130-250 мг), які в сотні разів перевищують фізіологічні потреби. Звісно, це може створювати певні ризики для організму. Серед побічних ефектів на першому місці знаходиться ефект Джода – Базедова, або йод-індукований тиреотоксикоз, але також може виникати і гіпотиреоз. Після прийому високих доз йоду часто виникають порушення серцевого ритму, підйом тиску, токсичні ураження ШКТ, клінічні прояви отруєння йодом, алергічні реакції. Крім того, існують протипоказання до прийому високих доз йоду, до яких відносять достатньо поширені серед населення патологічні стани: вузловий та багатовузловий зоб, хворобу Грейвса, аутоімунний тиреоїдит, герпетиформний дерматит, гіпокомплементарний васкуліт, підвищену чутливість до йоду, артеріальну гіпертензію та захворювання серцево-судинної системи.
До того ж, є суттєві обмеження у використанні цих препаратів для профілактики радіаційного ураження. Прийом високих доз йоду дозволений лише одноразово відразу після радіоактивного викиду або, якщо ситуація була прогнозованою, максимум за 4 години до того, як відбудеться радіоактивний викид. Повторні прийоми не рекомендовані.
Якою має бути адекватна йодна профілактика?
Для профілактики йодного дефіциту необхідно забезпечити фізіологічне надходження йоду щодня. Оскільки за рахунок лише харчування в Україні забезпечити його неможливо (більшість українців не вживає морепродукти постійно), необхідно пропагувати постійне використання йодованої солі в домогосподарствах для приготування їжі та підтримувати на законодавчому рівні обов’язкове універсальне йодування солі в країні. Через втрату найбільшого в країні виробника цього фортифікованого продукту – комбінату «Артемсіль» – у нас в магазинах з’явилася імпортована сіль, переважно польського виробництва. Цікаво, що уся сіль, яка виробляється в Польщі, йодована, навіть якщо про це не вказано на упаковці. Після аварії на Чорнобильській АЕС у Польщі введені певні стандарти щодо обов’язкового йодування солі в країні для профілактики ураження ЩЗ. Отже, з доступом в Україні до цього профілактичного продукту все добре.
Чому для масової профілактики в багатьох країнах світу використовують саме йодовану сіль? Це універсальний продукт, який щодня вживає практично все населення планети. Технології йодування прості та достатньо дешеві. Йод із солі добре абсорбується та засвоюється. Сучасні технології йодування з використанням калію йодату, який наноситься на сіль паром, дозволяють забезпечити тривале зберігання і зручне використання для приготування будь-яких страв, у тому числі гарячих. Крім того, при вживанні йодованої солі майже відсутній ризик надмірного надходження йоду в організм.
Для профілактики також можна використовувати препарати з фізіологічним вмістом йоду, такі як Йодомарин. Вони є безпечними, а дозування слід підбирати відповідно до віку та функціональної активності організму. Так, Йодомарин 100 підходить для профілактики йододефіциту та лікування зоба у дітей дошкільного і шкільного віку, а Йодомарин 200 використовується ддля профілактики йододефіциту у вагітних та жінок у період лактації, також його можуть приймати підлітки.
Особливо важливо забезпечити адекватне надходження йоду на етапі розвитку та формування нервової тканини. Для цього вагітним та жінкам, які годують грудьми, рекомендовано щодня приймати препарати, які містять щонайменше 150 мкг йоду (наприклад, Йодомарин 200). Слід пам’ятати, що саме для цієї категорії населення, а також для дітей до 2 років забезпечити адекватне надходження йоду за рахунок використання збагаченої солі неможливо.
Оскільки ми живемо в зоні йодного дефіциту – від легкого на півдні та сході країни,середньотяжкого на заході та навіть до тяжкого в гірській місцевості Карпат, слід обрати зручний спосіб йодної профілактики. Краще і безпечніше підготувати власну ЩЗ до зустрічі з радіацією, ніж через чисельні загрози в медійному просторі приймати високі дози калію йодиду [3].
Чого не слід робити для профілактики, так це вживати дієтичні добавки з невизначеним вмістом йоду. Також не слід щодня їсти морські водорості (максимум – 1 раз на тиждень), а тим паче використовувати висушені морські водорості як дієтичні добавки. Не можна використовувати з профілактичною метою також спиртовий розчин йоду. Всі ці засоби можуть містити надмірну кількість йоду і створювати такі самі загрози, як і високодозові препарати калію йодиду. Слід дотримуватися рекомендацій та приймати йод у межах безпечних рівнів добового споживання (табл.).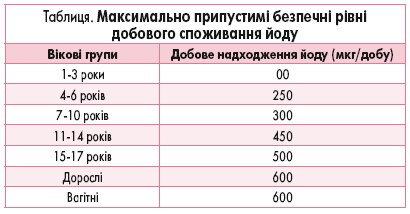
Чи можна використовувати для профілактики левотироксин?
L-тироксин – препарат вибору для терапії гіпотиреозу завдяки високому профілю безпечності, легкості використання, добрій абсорбції у ШКТ, тривалому періоду напіввиведення та низькій ціні.
Експерти АТА (2014) виступають проти призначення гормонів ЩЗ еутиреоїдним пацієнтам, а також проти використання біологічно активних та харчових добавок і високих доз йоду для профілактики й лікування гіпотиреозу [4]. Тому левотироксином не можна замінювати йодовмісні препарати для профілактики дефіциту йоду.
Отже, адекватне надходження йоду в організм людини є необхідною умовою як для профілактики широкого спектру тиреоїдної патології, так і попередження негативного впливу радіації. Для цього у раціоні повинна бути морська риба, морепродукти, йодована сіль. Люди, що входять у групу особливого ризику розвитку йододефіцитних захворювань, – діти, підлітки, вагітні та жінки, які годують грудьми, повинні приймати препарати з фізіологічним вмістом йоду.
Підготувала Єлизавета Лисицька
Список літератури знаходиться в редакції.
Тематичний номер «Педіатрія» № 2 (68) 2023 р.




