5 лютого, 2024
Лікування тривожних станів на первинній ланці медичної допомоги
Тривожні стани (ТС) являють собою біопсихосоціальні стани, асоційовані з генералізованими або ситуативними відповідями на чинники, котрі сприймаються як загрози. ТС можуть проявлятися у формі фобій або панічних розладів і провокувати психофізіологічну відповідь у формі запаморочення, підвищеної частоти серцевих скорочень і посиленого потовиділення. За відсутності лікування хронічна тривожність може спричиняти артеріальну гіпертензію (АГ), серцево-судинні захворювання (ССЗ), деменцію, гострі порушення мозкового кровообігу, цукровий діабет, новоутворення [1, 2]. За даними S.F. Javaid і співавт. (2023), загальносвітова поширеність ТС станом на 2019 р. становила 4,05%. Із 1990 по 2019 р. кількість осіб із ТС у світі зросла зі 194,9 до 301,4 млн, що приблизно відповідає показнику 3895 осіб на 100 тис. населення [1].
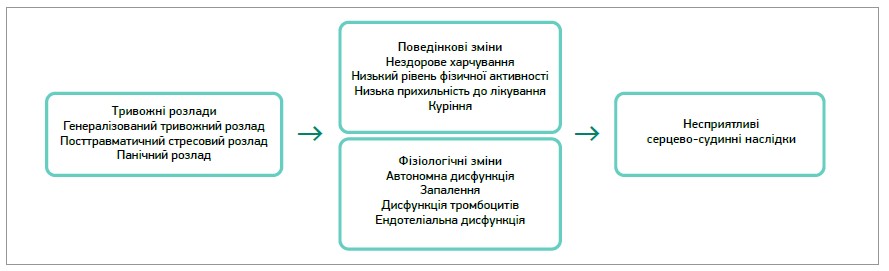
Окремим важливим завданням лікарів первинної ланки є лікування ТС в осіб із кардіо- та цереброваскулярними патологічними станами. Показано, що ССЗ підвищують імовірність психоемоційних розладів більш ніж удвічі, й навпаки: тривожність має несприятливий вплив на перебіг АГ, ішемічної хвороби серця (ІХС), серцевої недостатності (СН), аритмій тощо (рис. 1) [3, 4].
Рис. 1. Потенційні взаємозв’язки тривожності та ССЗ
ТС можна вважати модифікованими чинниками ризику розвитку й ускладненого перебігу ССЗ, які також істотно знижують прихильність пацієнтів до лікування, погіршують якість життя, збільшують імовірність інвалідизації та витрати на медичну допомогу. Скринінг щодо появи та прогресування ТС доцільно проводити не рідше 2-4 разів на рік, наприклад, за допомогою шкали Hospital Anxiety and Depression Scale (HADS) та опитувальника Generalized Anxiety Disorder‑7 (GAD‑7, табл.) [3, 5].
|
Таблиця. Опитувальник GAD-7 |
||||
|
Як часто Ви відзначали такі симптоми протягом останніх 2 тиж? |
Не відзначав (-ла) |
Кілька днів |
Більш |
Практично щодня |
|
Нервозність, тривожність, відчуття того, |
0 |
1 |
2 |
3 |
|
Неспроможність зупинити чи контролювати занепокоєність |
0 |
1 |
2 |
3 |
|
Надмірна занепокоєність із різних приводів |
0 |
1 |
2 |
3 |
|
Неспроможність розслабитися |
0 |
1 |
2 |
3 |
|
Метушливість, неспроможність перебувати |
0 |
1 |
2 |
3 |
|
Легка дратівливість |
0 |
1 |
2 |
3 |
|
Передчуття чогось жахливого |
0 |
1 |
2 |
3 |
|
Примітка: якщо сума балів становить 0-4, рівень тривожності є мінімальним, 5-9 – помірним, 10-14 – середнім, |
||||
Маркерами ТС для лікарів первинної ланки можуть виступати надмірна тривога чи занепокоєння, котрі не підлягають контролю та тривають не менш як 1 міс, а також наявність щонайменше 3 із наведених нижче симптомів:
- збудженість чи нервозність, стан «на межі нервових можливостей»;
- швидка втомлюваність;
- знижена концентрація уваги;
- дратівливість;
- м’язова напруга;
- порушення сну;
- посилена активність вегетативної нервової системи: посилене потовиділення, тахікардія, сухість у роті, дискомфорт в епігастральній ділянці, порушення випорожнення, запаморочення [3].
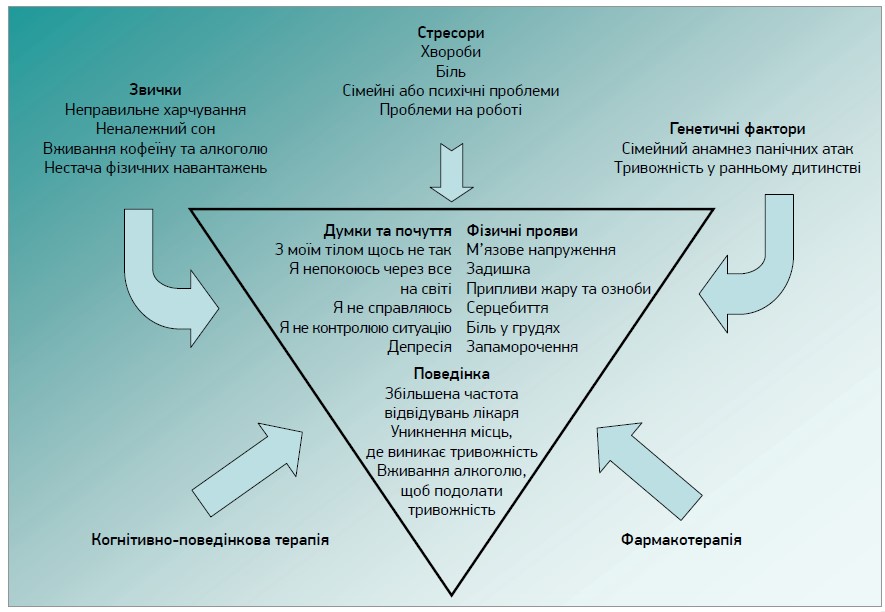
Якщо в пацієнта виражена тривога, пропонується передусім з’ясувати, чи не має він суїцидальних намірів, і за їх наявності призначити консультацію психіатра. Якщо ж суїцидальні наміри відсутні, варто провести скринінг тривожності за допомогою опитувальника GAD‑7. У разі перевищення 10 балів рекомендовано консультацію психіатра, натомість якщо оцінка становить <10, то доцільно призначити немедикаментозне лікування (релаксаційні техніки, психотерапію, тренінги навиків стресостійкості, фізичну активність, нормалізацію режиму сну та харчування тощо) й сучасну фармакотерапію [5]. Цикл тривожності та потенційні можливості впливу представлено на рисунку 2 [6].
Рис. 2. Цикл тривожності
Для усунення тривоги та вегетативних симптомів іноді призначають короткі курси бензодіазепінових транквілізаторів (гідазепаму), але перед цим потрібно ретельно зібрати наркологічний анамнез і не призначати ці засоби особам із залежністю чи ризиком формування залежності від психоактивних речовин. За різкого припинення терапії бензодіазепінові анксіолітики можуть спричинити синдром відміни, що проявляється погіршенням стану та посиленням тривоги. Крім того, застосування цих засобів асоціюється з потужними небажаними ефектами: вираженою седацією, запамороченням, розладами координації, зниженням концентрації уваги та пам’яті, порушеннями психомоторних функцій і симптомами так званої когнітивної токсичності. Тривалість застосування бензодіазепінів має обмежуватися 3-4 тиж [3, 7-9]. Загалом через велику кількість побічних ефектів бензодіазепіни (гідазепам) не рекомендовані для рутинного лікування пацієнтів із тривогою, а лише для усунення гострих нападів на кшталт панічних атак.
У зв’язку з переліченими недоліками на зміну бензодіазепіновим транквілізаторам дедалі частіше приходять анксіолітики небензодіазепінового ряду. Слід зауважити, що не всі такі препарати є однаково ефективними та безпечними. Наприклад, популярний препарат фенібут здатен пригнічувати моторні функції й больову відповідь, провокувати зміни на електроенцефалограмі. Довготривале застосування фенібуту асоціюється з розвитком толерантності, фізичної залежності, виникненням психозів, описано також випадки інтоксикації цим препаратом і синдрому відміни [10]. За даними звітів американських токсикологічних центрів, безконтрольний прийом фенібуту може спричинити надмірну седацію, пригнічення дихання, ажитацію, тахікардію, сплутаність свідомості, звикання, сонливість тощо. Автори узагальненого аналізу токсикологічних звітів зауважили, що доступність фенібуту та його потенційна здатність формувати залежність викликають особливе занепокоєння [11]. У зв’язку з переліченими небезпеками лікарю первинної ланки краще звернути увагу на інші небензодіазепінові анксіолітики, як-от фабомотизол.
Небензодіазепіновий анксіолітик фабомотизол є селективним агоністом σ1-рецепторів у нервових клітинах головного мозку, завдяки чому він відновлює фізіологічний перебіг асоційованого з γ-аміномасляною кислотою (ГАМК) гальмування в центральній нервовій системі. σ1-рецептори можна розглядати як універсальний інструмент для ремонту ГАМК-А-рецепторів. Він нормалізує конформаційні властивості ГАМК-А-рецепторів і забезпечує відновлення здатності цих рецепторів до фізіологічної відповіді на власну ендогенну ГАМК – усунення ГАМК-резистентності. У результаті розглянута стратегія впливу на патогенез тривоги принципово відрізняється від раніше відомих підходів, є максимально фізіологічною і може бути названа однією з найперспективніших у цьому плані. Фабомотизол не спричиняє м’язової слабкості, сонливості й не має несприятливого впливу на концентрацію уваги та пам’ять, тому є безпечним для пацієнтів похилого віку. При застосуванні фабомотизолу не формуються звикання та залежність і не розвивається синдром відміни. Ефективність і безпека фабомотизолу вивчені в багатьох дослідженнях за участю пацієнтів із ССЗ та широким спектром ТС, у тому числі при тривалому застосуванні препарату [12-22]. Зокрема, в рандомізованому дослідженні показано, що додавання фабомотизолу до основної терапії в жінок похилого віку з гіпертонічною хворобою II-III стадії дає змогу ефективніше досягати контролю артеріального тиску – АТ (за даними добового моніторування) [13]. В іншому дослідженні тривала курсова терапія фабомотизолом (17 тиж) сприяла достовірному зменшенню частоти розвитку пароксизмів фібриляції передсердь, скороченню тривалості епізодів аритмії, легшій переносимості пароксизмів, зниженню кількості випадків госпіталізації та звернень по медичну допомогу [12].
Вивчення експресії генів на моделі емоційного стресу на щурах показало, що анксіолітична дія фабомотизолу, в тому числі, є результатом регуляції трансляції білків, синаптичних функцій і клітинного метаболізму [23].
За даними багатоцентрового рандомізованого клінічного дослідження ІІІ фази (2016), фабомотизол виявився не гіршим за діазепам у лікуванні пацієнтів із генералізованим тривожним розладом (ГТР) і розладами адаптації. У цьому дослідженні учасників із ГТР було рандомізовано в групи фабомотизолу (30 мг/добу) та діазепаму (30 мг/добу) на 30 днів. Первинною кінцевою точкою була зміна оцінки за шкалою тривожності Гамільтона (Hamilton Anxiety Rating Scale, HAMA). Обидва препарати забезпечували зниження оцінки тривожності, але дія фабомотизолу виявилася достовірно потужнішою за ефект діазепаму (на 2,93 бала [95% довірчий інтервал 0,67-5,19]; p=0,01). Частка пацієнтів, у яких зменшилася тяжкість ГТР, становила 72% у групі фабомотизолу та лише 58% у групі діазепаму. Після повного завершення курсу лікування частка пацієнтів без ГТР або з легким ГТР у групі фабомотизолу також була достовірно вищою, ніж у групі діазепаму (69% проти 44% відповідно; p=0,014). Привернув увагу дослідників і відмінний профіль безпеки фабомотизолу: сумарна кількість побічних ефектів у групі цього препарату становила 15 випадків, а в групі діазепаму – 199. Синдром відміни на тлі фабомотизолу не спостерігався, а в пацієнтів, які приймали діазепам, відзначався в 68% випадків [24].
Багатоцентрове крос-секційне дослідження COMETA включало пацієнтів віком ≥55 років із верифікованими АГ, ІХС і коморбідною тривожністю (≥11 балів за шкалою Hospital Anxiety and Depression Scale – Anxiety [HADS-A]), яких було рандомізовано в групи основної терапії ССЗ та основної терапії в поєднанні з фабомотизолом (10 мг 3 р/добу). Через 6 тиж лікування в групі лікування фабомотизолом частка пацієнтів із повною відсутністю симптомів тривожності за HADS-A була достовірно вищою, ніж у групі стандартної терапії: 37,9% проти 19,2%, p=0,001. Аналогічна картина спостерігалася й через 12 тиж лікування: 66,9% та 32% відповідно. Середня оцінка хронічного психоемоційного стресу в групі фабомотизолу через 6 тиж знизилася на 25% (із 6,45±2,20 до 5,05±1,96 бала за візуальною аналоговою шкалою (ВАШ); р=0,001), а через 12 тиж – на 40% (до 3,98±1,99 бала; р=0,001). У контрольній групі також спостерігалося певне зниження оцінки стресу, але воно було вдвічі меншим (на 11 і 20% через 6 і 12 тиж відповідно). Автори дійшли висновку, що застосування фабомотизолу в пацієнтів з АГ й ІХС забезпечує покращення психологічного статусу (зменшення симптомів тривожності та зниження рівня хронічного психоемоційного стресу) [25].
Багатообіцяльним є й вивчення фабомотизолу в експериментальних дослідженнях, пов’язаних з ішемічними та геморагічними ураженнями головного мозку. З’ясовано, що фабомотизол збільшує вміст нейротрофіну BDNF (brain-derived neurotrophic factor) у культурі гіпокампальних нейронів [26] і протидіє зниженню рівня BDNF в умовах стресу [27].
Дослідження впливу фабомотизолу на структуру головного мозку при експериментальній перманентній ішемії, спричиненій перев’язкою середньої мозкової артерії показало, що введення цього препарату (5 мг/кг внутрішньоочеревинно 2 р/добу протягом 6 днів) забезпечує зменшення зони ішемії. За умови застосування фабомотизолу впродовж 12 днів після перев’язки артерії нейропротекторний ефект стає ще вираженішим. Особливу увагу привертає протекторна дія фабомотизолу в стріопалідарній системі, яка найбільше страждає при ішемії. Зона ішемічного некрозу при застосуванні цього препарату залишається чітко окресленою, ішемічна напівтінь (пенумбра) практично відсутня, а реперфузія відбувається рано [28]. Фабомотизол нормалізує мозковий кровоток у обох півкулях, запобігаючи дистонії, повнокров’ю та тромбозу судин мозку [29, 30]. Досліди також показали, що внутрішньовенне введення фабомотизолу при минущій ішемії посилює локальний мозковий кровоток на 40,0±9,3% і підвищує виживаність експериментальних тварин. Окрім того, фабомотизол підвищує стійкість мембранних структур нейронів кори та смугастого тіла до вільнорадикального окиснення після ішемії й посилює власний антиоксидантний захист завдяки підвищенню активності каталази [31].
Ще одним механізмом дії фабомотизолу, крім нейропротекторного й антиоксидантного, є нормалізація вмісту нейромедіаторів, передусім уже згадуваної ГАМК. За умов експериментальної ішемії в мозку щурів уміст ГАМК знижується, а глутамінової кислоти – зростає, але введення фабомотизолу забезпечує відновлення фізіологічного балансу цих медіаторів [32].
Фабомотизол ефективний і в умовах геморагічного ушкодження мозку, оскільки при внутрішньовенному введенні в дозі 10 мг/кг покращує кровопостачання уражених ділянок на 36,0±5,7%. Механізм цього ефекту вважається ГАМК‑ергічним [33]. В експериментах на щурах з інфарктом міокарда також було продемонстровано здатність фабомотизолу покращувати мозковий кровоток і знижувати АТ (на 16,3%) [28].
Отже, фабомотизол вибірково покращує кровопостачання ішемізованого мозку, обмежує зону ураження при ішемії, відновлює баланс нейромедіаторних амінокислот, підвищує стійкість структур мозку до вільнорадикальних процесів і збільшує вміст нейротрофічних факторів у нейронах, що дає можливість усувати психоневрологічні порушення та забезпечує нейропротекцію [28].
Фабомотизол має низку інших сприятливих плейотропних властивостей, зокрема ангіогенні, кардіопротекторні, антиішемічні [34-36]. Наприклад, на моделі гострої субендокардіальної ішемії фабомотизол достовірно зменшував індуковану ізопротеренолом депресію сегмента ST в експериментальних тварин [36], а в моделі алкогольної кардіоміопатії нормалізував експресію генів регуляторних білків у міокарді лівого шлуночка (ЛШ), водночас зменшуючи ступінь ремоделювання ЛШ і покращуючи його інотропну функцію [35]. Продемонстровано здатність фабомотизолу знижувати плазмовий рівень мозкового натрійуретичного пептиду – біохімічного маркера хронічної СН, а також пригнічувати надмірну експресію генів, які кодують ангіотензинові, вазопресинові та глюкокортикоїдні рецептори, протидіючи механізмам патологічного ремоделювання серця, що може виступати механізмом кардіопротекторної дії цього препарату [37].
Висновки
1. Тривожні стани (ТС) являють собою поширену групу патологічних станів, яка разом із серцево-судинними захворюваннями (ССЗ) формує хибне коло зі взаємним погіршенням перебігу.
2. Важливими завданнями сімейного лікаря є своєчасні діагностика та лікування ТС, у тому числі за допомогою фармакотерапії небензодіазепіновими анксіолітиками, як-от фабомотизол.
3. Застосування фабомотизолу є особливо доцільним у лікуванні ТС в осіб із кардіо- та цереброваскулярною патологією, які становлять більшість пацієнтів сімейного лікаря.
4. Крім безпосереднього усунення тривоги, фабомотизол чинить сприятливий вплив на перебіг основних ССЗ та ішемічних і геморагічних уражень мозку, що дає змогу за допомогою одного препарату досягати багатогранного покращення стану пацієнта, уникаючи поліпрагмазії.
На фармацевтичному ринку України активну речовину фабомотизол представлено, зокрема, препаратом Бафазол ІС. Проведена клінічна апробація Бафазолу ІС у пацієнтів із проявами тривоги продемонструвала високу ефективність і хорошу переносимість препарату, що ілюструють представлені далі клінічні випадки.
Клінічні ілюстрації використання препарату Бафазол ІС у лікуванні коморбідних пацієнтів із супутніми проявами хронічного стресу та тривоги надані лікарем-неврологом, кандидатом медичних наук Іванною Леонідівною Ревенько (ДУ «Національний науковий центр «Інститут кардіології, клінічної та регенеративної медицини ім. академіка М.Д. Стражеска НАМН України», м. Київ).
Клінічний випадок 1: пацієнтка В., 39 років, програмістка
Причина звернення: головний біль (ниючий, стискальний, помірної інтенсивності, не пов’язаний із рівнем АТ); коливання АТ від 120/80 до 180/95 мм рт. ст.; відчуття тривоги, яке посилюється ввечері; болі в серці, що виникають переважно після хвилювання.
Анамнез: гіпертонічна хвороба II стадії, ризик помірний із 2020 р. Протягом останніх 2 років приймає ліки (небіволол 2,5 мг, лізиноприл 20 мг, гідрохлоротіазид 12,5 мг), але нерегулярно. Веде малорухливий спосіб життя, має надлишкову масу тіла. Сімейний анамнез обтяжений: у матері АГ із 30 років. Не курить, алкоголем не зловживає, місячні регулярні.
Під час огляду: індекс маси тіла (ІМТ) – 28,3 кг/м2, окружність талії (ОТ) – 94 см, АТ – 141/76 мм рт. ст., пульс – 74 уд./хв.
- Електрокардіографія (ЕКГ): ритм синусовий, регулярний, частота серцевих скорочень (ЧСС) – 75 уд./хв.
- Ехокардіографія (ЕхоКГ): концентрична гіпертрофія ЛШ.
- Ультразвукове дослідження (УЗД) судин шиї: початкові атеросклеротичні зміни сонних артерій.
- Добове моніторування ЕКГ протягом 24 год: поодинокі шлуночкові та передсердні екстрасистоли.
- Добовий моніторинг АТ: середньодобовий АТ – 142/91 мм рт. ст., середньоденний АТ – 144/93 мм рт. ст., середньонічний АТ – 137/88 мм рт. ст.
- Лабораторні показники: калій – 4,5 ммоль/л, креатинін – 78 мкмоль/л, швидкість клубочкової фільтрації (ШКФ) – 80 мл/хв/1,73 м2, сечова кислота – 374 мкмоль/л, глюкоза крові – 5,5 ммоль/л, холестерин (ХС) загальний – 4,2 ммоль/л, ХС ліпопротеїнів низької щільності (ЛПНЩ) – 1,93 ммоль/л, ХС ліпопротеїнів високої щільності (ЛПВЩ) – 1,44 ммоль/л, тригліцериди – 1,81 ммоль/л.
- Загальний аналіз крові – норма.
- Монреальський когнітивний тест (MoCA) – 27 балів.
- Шкала депресії PHQ-9 – 4 бали; шкала тривоги GAD‑7 – 10 балів.
- Оцінка інтенсивності болю за ВАШ – 6 балів.
- Шкала якості життя SF‑36: фізичне функціонування – 90 балів; рольове функціонування, зумовлене фізичним станом, – 50 балів; рольове функціонування, зумовлене емоційним станом, – 33 бали; життєва активність – 45 балів; інтенсивність болю – 45 балів; психічне здоров’я – 52 бали; соціальне функціонування – 88 балів; загальний стан здоров’я – 60 балів.
Попередній діагноз: гіпертонічна хвороба II стадії, 2 ступеня, ризик помірний. Тривожний синдром (GAD – 7-10 балів). Головний біль напруги.
Призначена терапія: амлодипін/індапамід 5/1,5 мг; бісопролол/периндоприл 5/10 мг; Бафазол ІС 10 мг 3 р/день 2 міс, потім – 10 мг 2 р/день 1 міс; регулярні фізичні навантаження (заняття в спортклубі 3 р/тиж).
Повторний огляд через 3 міс: самопочуття покращилося; головний біль турбував 1 раз на 3 тиж, безпричинна тривога відсутня, АТ <130/80 мм рт. ст.
- Об’єктивно: АТ – 128/82 мм рт. ст.; середньоденний систолічний АТ – 126 мм рт. ст.; середньоденний діастолічний АТ – 80 мм рт. ст.; середньонічний систолічний АТ – 116 мм рт. ст.; середньонічний діастолічний АТ – 72 мм рт. ст.
- MoCA – 29 балів.
- PHQ‑9 – 3 бали; шкала тривоги GAD‑7 – 3 бали.
- Оцінка інтенсивності болю за ВАШ – 0 балів.
- Шкала SF‑36: фізичне функціонування – 95 балів; рольове функціонування, зумовлене фізичним станом, – 75 балів; рольове функціонування, зумовлене емоційним станом, – 95 балів; життєва активність – 65 балів; інтенсивність болю – 78 балів; психічне здоров’я – 60 балів; соціальне функціонування – 88 балів; загальний стан здоров’я – 70 балів.
Висновки: включення Бафазолу ІС у схему терапії коморбідного пацієнта з АГ і тривожним синдромом дало змогу:
- зменшити вираженість тривоги за шкалою GAD‑7 більш ніж у 3 рази;
- зменшити вираженість болю за ВАШ;
- нормалізувати середньодобові показники АТ;
- на 30% покращити якість життя за шкалою SF‑36.
Клінічний випадок 2: пацієнтка В., 33 роки, офісна працівниця
Причина звернення: постійний головний біль помірної інтенсивності, стискального характеру, який турбує постійно протягом останніх 3 міс; болі в м’язах рук, спини; постійне відчуття тривоги, періодичне відчуття страху, не пов’язане зі стресорними чинниками; зниження концентрації уваги, розсіяність; запаморочення не системне; порушення ритму сну.
Анамнез: 2 роки тому лікувалася з приводу панічного розладу, протягом року приймала селективні інгібітори зворотного захоплення серотоніну. Стан покращився, але набрала 10 кг ваги. Протягом року вважала себе здоровою, але останні декілька місяців з’явилися вищезазначені симптоми. Не курить, менструації регулярні. Спадковість: мати – АГ; батько – ІХС, СН.
Під час огляду: ІМТ – 28,9 кг/м2, ОТ – 87 см, АТ – 133/87 мм рт. ст., пульс – 76 уд./хв. Із боку внутрішніх органів і систем – без клінічно значущих змін. У неврологічному статусі не виявлено вогнищевої неврологічної патології.
- ЕКГ: ритм синусовий, регулярний, ЧСС – 70 уд./хв.
- ЕхоКГ: розміри серця в межах нормальних значень, без ознак гіпертрофії ЛШ, фракція викиду збережена (62%).
- УЗД судин голови та шиї: звивистість сонних артерій.
- Лабораторні показники: калій – 3,8 ммоль/л, креатинін – 79 мкмоль/л, ШКФ – 87 мл/хв/1,73 м2, сечова кислота – 264 мкмоль/л, АЛТ – 10 Од/л, АСТ – 18 Од/л, глюкоза крові – 5,2 ммоль/л, ХС загальний – 6,2 ммоль/л, ХС ЛПНЩ – 3,91 ммоль/л, ХС ЛПВЩ – 1,15 ммоль/л, тригліцериди – 1,34 ммоль/л.
- MoCA – 24 бали.
- PHQ‑9 – 12 балів; шкала тривоги GAD‑7 – 12 балів.
- Оцінка інтенсивності болю за ВАШ – 4 бали.
- Шкала SF‑36: фізичне функціонування – 45 балів; рольове функціонування, зумовлене фізичним станом, – 75 балів; рольове функціонування, зумовлене емоційним станом, – 70 балів; життєва активність – 25 балів; тілесний біль – 35 балів; емоційний добробут – 32 бали; соціальне функціонування – 75 балів; загальний стан здоров’я – 15 балів.
Попередній діагноз: хронічний головний біль напруги. Соматоформний вегетативний розлад нервової системи. Тривожно-депресивний синдром. Фіброміалгія (?).
Призначена терапія: Бафазол ІС 10 мг 3 р/день 2 міс, регулярні аеробні фізичні навантаження (хода зі швидкістю 5 км/год протягом 60 хв щоденна; заняття в спортклубі 2 р/тиж, консультація психотерапевта).
Повторний огляд через 2 міс: самопочуття значно покращилося. Головний біль не турбує, періодичні болі в м’язах легкої інтенсивності. Збільшилася фізична активність. Зберігається емоційна лабільність.
- MoCA – 28 балів.
- PHQ‑9 – 7 балів; шкала тривоги GAD‑7 – 5 балів.
- Оцінка інтенсивності болю за ВАШ – 2 бали.
- Шкала SF‑36: фізичне функціонування – 85 балів; рольове функціонування, зумовлене фізичним станом,– 75 балів; рольове функціонування, зумовлене емоційним станом, – 100 балів; життєва активність – 40 балів; тілесний біль – 45 балів; емоційний добробут – 56 балів; соціальне функціонування – 75 балів; загальний стан здоров’я – 50 балів.
Висновки: включення Бафазолу ІС у схему терапії коморбідного пацієнта з хронічним головним болем напруги, соматоформним вегетативним розладом нервової системи та тривожно-депресивним синдромом дало змогу:
- зменшити вираженість тривоги за шкалою GAD‑7 у 2,4 раза;
- зменшити вираженість депресії за шкалою PHQ‑9 на 71%;
- зменшити вираженість болю за ВАШ у 2 рази;
- на 41% покращити якість життя за шкалою SF‑36.
Клінічний випадок 3: пацієнт К., 58 років, економіст
Причина звернення: коливання АТ від 120/70 до 150/90 мм рт. ст., АТ підвищується переважно у вечірні години. Кризи характеризуються серцебиттям, відчуттям тривоги, болем у ділянці серця, котрий супроводжується відчуттям нестачі повітря.
Анамнез: діагноз АГ встановлено 3 роки тому; антигіпертензивні препарати приймав нерегулярно, статини самостійно скасував. Стан погіршився протягом останніх тижнів на тлі хронічного стресу.
Під час огляду: ІМТ – 28,9 кг/м2, ОТ – 87 см, АТ – 156/92 мм рт. ст., пульс – 76 уд./хв. Із боку внутрішніх органів і систем – без клінічно значущих змін. У неврологічному статусі не виявлено вогнищевої неврологічної патології.
- ЕКГ: ритм синусовий, ЧСС – 80 уд./хв, гіпертрофія ЛШ.
- ЕхоКГ: помірна дилатація лівого передсердя. Потовщення стінок ЛШ. Скоротлива функція ЛШ збережена.
- Добовий моніторинг АТ: середньодобовий АТ – 143/72 мм рт. ст., середньоденний АТ – 149/77 мм рт. ст., середньонічний АТ – 132/65 мм рт. ст.
- УЗД судин голови та шиї: в біфуркації загальної сонної артерії (ЗСА) справа напівконцентрична гетерогенна атеросклеротична (АС) бляшка товщиною 2,8 мм, стеноз 30-35% (ECST). У біфуркації ЗСА справа з розповсюдженням у гирло внутрішньої сонної артерії АС‑бляшка 2,5 мм, стеноз 25% (ECST). У біфуркації ЗСА зліва напівконцентрична гомогенна ізоехогенна АС‑бляшка 1,7 мм, стеноз 20% (ECST). Хребтові артерії: входження в канал типове. Кровоплин у межах нормативних значень.
- Лабораторні показники: калій – 4,12 ммоль/л; натрій – 134 ммоль/л; креатинін – 95 мкмоль/л; ШКФ – 87 мл/хв/1,73 м2, сечова кислота – 232 мкмоль/л, АЛТ – 16 Од/л, АСТ – 18 Од/л, глюкоза крові – 4,3 ммоль/л; ХС загальний – 5,5 ммоль/л; ХС ЛПНЩ – 3,57 ммоль/л; ХС ЛПВЩ – 1,2 ммоль/л. Загальний аналіз крові – норма.
- MoCA – 22 бали.
- PHQ‑9 – 12 балів; шкала тривоги GAD‑7 – 14 балів.
- Оцінка інтенсивності болю за ВАШ – 6 балів.
- Шкала SF‑36: фізичне функціонування – 20 балів; рольове функціонування, зумовлене фізичним станом, – 10 балів; рольове функціонування, зумовлене емоційним станом, – 10 балів; життєва активність – 30 балів; тілесний біль – 45 балів; емоційний добробут – 44 бали; соціальне функціонування – 25 балів; загальний стан здоров’я – 45 балів.
Попередній діагноз: гіпертонічна хвороба II стадії, 2 ступеня, ризик високий. Церебральний атеросклероз. Синдром помірних когнітивних порушень (MoCA – 22 бали). Тривожно-депресивний синдром (GAD‑7 – 14 балів, PHQ‑9 – 12 балів).
Призначена терапія: телмісартан/амлодипін 40/5 мг; аторвастатин 40 мг; Бафазол ІС 10 мг 3 р/день 2 міс.
Повторний огляд через 2 міс: самопочуття покращилося. Нормалізувався АТ. Збільшилася фізична активність.
- Добовий моніторинг АТ: середньоденний систолічний АТ – 125 мм рт. ст.; середньоденний діастолічний АТ – 73 мм рт. ст.; середньонічний систолічний АТ – 115 мм рт. ст.; середньонічний діастолічний АТ – 66 мм рт. ст.
- MoCA – 26 балів.
- PHQ‑9 – 7 балів; шкала тривоги GAD‑7 – 7 балів.
- Оцінка інтенсивності болю за ВАШ – 2 бали.
- Шкала SF‑36: фізичне функціонування – 90 балів; рольове функціонування, зумовлене фізичним станом, – 85 балів; рольове функціонування, зумовлене емоційним станом, – 67 балів; життєва активність – 60 балів; тілесний біль – 100 балів; емоційний добробут – 80 балів; соціальне функціонування – 88 балів; загальний стан здоров’я – 75 балів.
Висновки: включення Бафазолу ІС у схему терапії коморбідного пацієнта з АГ і тривожно-депресивним синдромом дало змогу:
- зменшити вираженість тривоги за шкалою GAD‑7 у 2 рази;
- зменшити вираженість депресії за шкалою PHQ‑9 на 71%;
- зменшити вираженість болю за ВАШ у 3 рази;
- нормалізувати середньодобові показники АТ;
- у 2,8 раза покращити якість життя за шкалою SF‑36.
Клінічний випадок 4: пацієнтка Щ., 43 роки, домогосподарка
Причина звернення: в останні 2 тиж щоденні підйоми АТ до 200/100 мм рт. ст.; запаморочення та порушення координації; відчуття тривоги, порушення сну.
Анамнез: близько 5 років фіксує підйоми рівня АТ до 170/100 мм рт. ст., регулярно не лікувалася, знижувала АТ каптопресом. Не курить. Місячні регулярні. У 2017 р. видалено жовчний міхур із приводу жовчнокам’яної хвороби.
Під час огляду: ІМТ – 29,7 кг/м2, ОТ – 91 см, АТ – 154/87 мм рт. ст., пульс – 78 уд./хв. Із боку внутрішніх органів і систем – без клінічно значущих змін.
- ЕКГ: ритм синусовий, ЧСС – 64 уд./хв, гіпертрофія ЛШ.
- ЕхоКГ: перикард без особливостей; легка дилатація лівого передсердя. Концентрична гіпертрофія ЛШ. Скоротливість ЛШ збережена.
- Добовий моніторинг АТ: середньодобовий АТ – 134/81 мм рт. ст., середньоденний АТ – 137/83 мм рт. ст., середньонічний АТ – 129/75 мм рт. ст.
- УЗД судин голови та шиї: без патології.
- Лабораторні показники: калій – 4,5 ммоль/л; натрій – 139 ммоль/л, креатинін – 66 мкмоль/л, сечова кислота – 266 мкмоль/л, АЛТ – 20 Од/л, АСТ – 20 Од/л, глюкоза – 4,6 ммоль/л; ХС загальний – 6,6 ммоль/л; ХС ЛПНЩ – 4,44 ммоль/л; ХС ЛПВЩ – 1,74 ммоль/л. Загальний аналіз крові – норма.
- MoCA – 25 балів.
- PHQ‑9 – 8 балів; шкала тривоги GAD‑7 – 16 балів.
- Оцінка інтенсивності болю за ВАШ – 4 бали.
- Шкала SF‑36: фізичне функціонування – 75 балів; рольове функціонування, зумовлене фізичним станом, – 50 балів; рольове функціонування, зумовлене емоційним станом, – 33 бали; життєва активність – 55 балів; тілесний біль – 45 балів; емоційний добробут – 48 балів; соціальне функціонування – 31 бал; загальний стан здоров’я – 40 балів.
Попередній діагноз: гіпертонічна хвороба II стадії, 2 ступеня, ризик високий. Гіперхолестеринемія. Синдром легких когнітивних порушень (MoCA – 25 балів). Тривожний синдром (GAD‑7 – 16, PHQ‑9 – 8).
Призначена терапія: периндоприл/індапамід/амлодипін 5/1,25/5 мг; бісопролол 5 мг, Бафазол ІС 10 мг 3 р/день 2 міс, щоденна хода зі швидкістю 5 км/год протягом 40 хв.
Повторний огляд через 2 міс. Добовий моніторинг АТ: середньоденний систолічний АТ – 117 мм рт. ст.; середньоденний діастолічний АТ – 63 мм рт. ст.; середньонічний систолічний АТ – 102 мм рт. ст.; середньонічний діастолічний АТ – 56 мм рт. ст.
- MoCA – 29 балів.
- PHQ‑9 – 4 бали; шкала тривоги GAD‑7 – 5 балів.
- Оцінка інтенсивності болю за ВАШ – 0 балів.
- Шкала SF-36: фізичне функціонування – 90 балів; рольове функціонування, зумовлене фізичним станом, – 75 балів; рольове функціонування, зумовлене емоційним станом, – 80 балів; життєва активність – 55 балів; тілесний біль – 90 балів; емоційний добробут – 64 бали; соціальне функціонування – 75 балів; загальний стан здоров’я – 65 балів.
Висновки: включення Бафазолу ІС у схему терапії коморбідного пацієнта з АГ і тривожним синдромом дало змогу:
- зменшити вираженість тривоги за шкалою GAD‑7 більш ніж у 3 рази;
- повністю усунути біль;
- нормалізувати середньодобові показники АТ;
- на 53% покращити якість життя за шкалою SF‑36.
Список літератури знаходиться в редакції.
Підготувала Лариса Стрільчук