15 березня, 2024
Нутритивна підтримка при онкологічних захворюваннях у дорослих
Стандарт медичної допомоги
Харчування має вирішальне значення у комбінованій протипухлинній терапії. Переконливі докази вказують на те, що проблеми харчування слід враховувати в межах алгоритму лікування та діагностики ще з моменту виявлення раку та контролювати паралельно з провадженням протипухлинної терапії. Цей стандарт медичної допомоги не стосується певної специфічної нозологічної форми, а охоплює сучасні рекомендації щодо лікувального харчування пацієнтів дорослого віку з онкологічними захворюваннями.
Загальна частина
Назва діагнозу: злоякісні новоутворення.
Коди стану або захворювання. НК 025:2021 «Класифікатор хвороб та споріднених проблем охорони здоров’я»: злоякісні новоутворення (С00-С96).
Розділ І. Організація надання медичної допомоги пацієнтам зі злоякісними новоутвореннями
Положення стандарту медичної допомоги. Цей стандарт призначений для лікарів-онкологів, хірургів-онкологів, анестезіологів, хіміотерапевтів, радіологів, лікарів з променевої терапії, онкогематологів, дієтологів, середнього медичного персоналу для організації надання медичної допомоги та покращення результатів лікування онкологічних хворих шляхом оптимізації їх лікувального харчування.
Обґрунтування. У світі і в нашій країні мальнутриція, пов’язана з онкологічним захворюванням, досі недостатньо виявляється, недооцінюється у комплексному веденні пацієнтів та неоптимально лікується. Мальнутриція є спільною ознакою у хворих на рак і виникає внаслідок як самої пухлини, так і медикаментозної та хірургічної протипухлинної терапії. Недостатність харчування негативно впливає на якість життя та переносимість лікування. Було підраховано, що близько 10-20% онкологічних пацієнтів помирають через наслідки мальнутриції, а не через саму пухлину.
Критерії якості медичної допомоги
Обов'язкові
- Наявні локально узгоджені письмові документи, що координують та інтегрують медичну допомогу пацієнтам з мальнутрицією при онкологічних захворюваннях.
- Існує задокументований індивідуальний план обстеження, лікування та спостереження, узгоджений з пацієнтом, членами сім’ї/особами, які здійснюють догляд за ним.
- Пацієнти і, за згодою, члени сім’ї/особи, які здійснюють догляд, забезпечуються у доступній формі інформацією щодо стану пацієнта з мальнутрицією при онкологічних захворюваннях.
Бажані
У закладах охорони здоров’я (ЗОЗ), де надають медичну допомогу пацієнтам з мальнутрицією при онкологічних захворюваннях, розміщуються інформаційні матеріали щодо проявів, профілактики та факторів ризику.
Розділ ІІ. Діагностика
Положення стандарту медичної допомоги. Діагноз встановлюється виключно у ЗОЗ, що надають спеціалізовану медичну допомогу.
Обґрунтування. Неповноцінна дієта зумовлює хронічну недостатність харчування. Для підтримання стабільного нутритивного статусу харчування має відповідати потребам пацієнта в калоріях, що є сумою енергетичних витрат у стані спокою, фізичної активності і в незначній кількості – аліментарно-індукованого термогенезу. В онкологічних пацієнтів енергетичні витрати у стані спокою при визначенні за допомогою непрямої калориметрії (золотого стандарту) можуть бути не зміненими, підвищеними або зниженими щодо цього показника в осіб з контрольної групи без пухлин
В онкологічних пацієнтів не пригнічується синтез м’язових білків, цей процес не порушується та зберігається відповідь на надходження амінокислот із їжею, хоча і з вищою потребою в амінокислотах (білках), ніж у здорових осіб молодого віку.
Критерії якості медичної допомоги
Обов'язкові
- Для виявлення мальнутриції або ризику мальнутриції у всіх пацієнтів, які надходять на лікування до ЗОЗ, проводиться оцінка нутритивного ризику за шкалами, що наведені у таблиці 1 та рисунках 1, 2.
- З метою виявлення ранніх стадій нутритивних порушень регулярно оцінюють надходження поживних речовин, зміни маси тіла та індексу маси тіла (ІМТ) починаючи від встановлення діагнозу онкологічного захворювання та при повторних обстеженнях залежно від стабільності клінічної ситуації відповідно до алгоритму, представленого на рисунку 3.
- Проводиться скринінг на наявність дисфагії та її лікування, а також пацієнтів заохочують та навчають підтриманню функції ковтання під час ентерального харчування (ЕХ).
- Здійснюють рутинний скринінг онкологічних пацієнтів на пізніх стадіях захворювання щодо споживання кількості поживних речовин, втрати маси тіла та виявлення низького ІМТ.
|
Таблиця 1. Протокол нутритивного ризику в онкології (PRONTO) |
||||
|
Що? |
Чому? |
Як? |
Відповіді та дії |
|
|
1. Маса тіла |
|
Запитайте пацієнта
Досліджувальні запитання
|
Так |
Втручатися Пацієнт може потребувати медичного втручання в харчуванні згідно з цим протоколом |
|
Ні |
Спостерігати
|
|||
|
2. Апетит і споживання їжі |
|
Запитайте пацієнта
Досліджувальні запитання
|
Так |
Втручатися Пацієнт може потребувати медичного втручання в харчуванні згідно з цим протоколом |
|
Ні |
Спостерігати
|
|||
|
3. Міцність і рухливість |
|
Запитайте пацієнта
Досліджувальні запитання
|
Так |
Втручатися Пацієнт може потребувати медичного втручання в харчуванні згідно з цим протоколом |
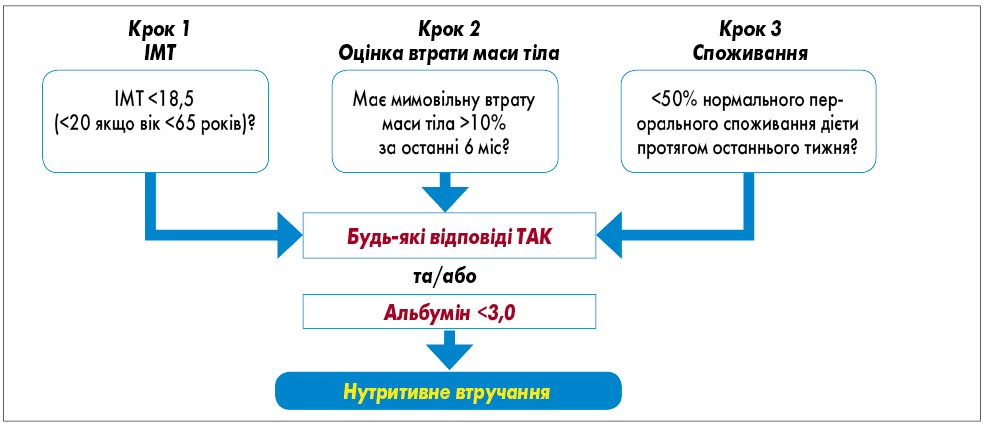 Рис. 1. Оцінка нутритивного ризику
Рис. 1. Оцінка нутритивного ризику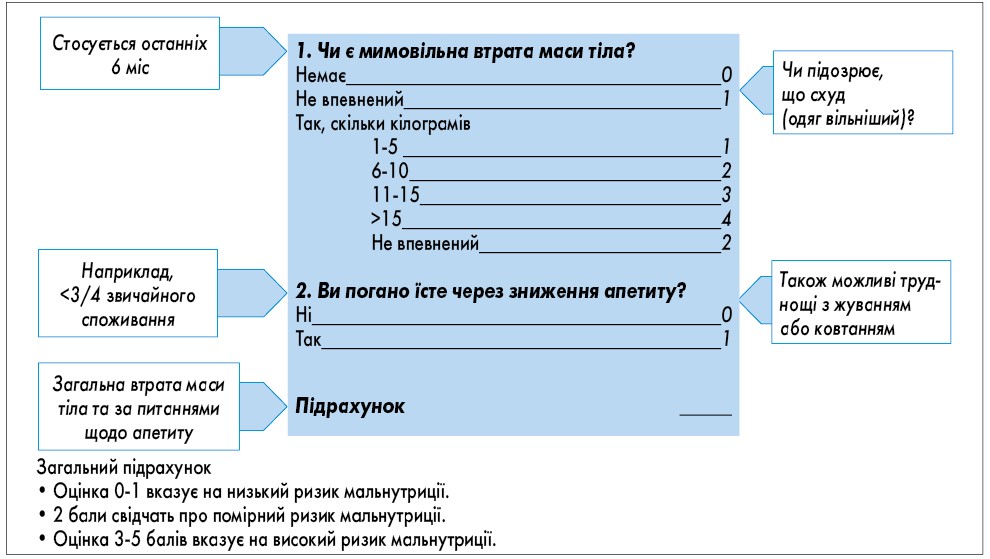 Рис. 2. Скринінг нутритивних порушень
Рис. 2. Скринінг нутритивних порушень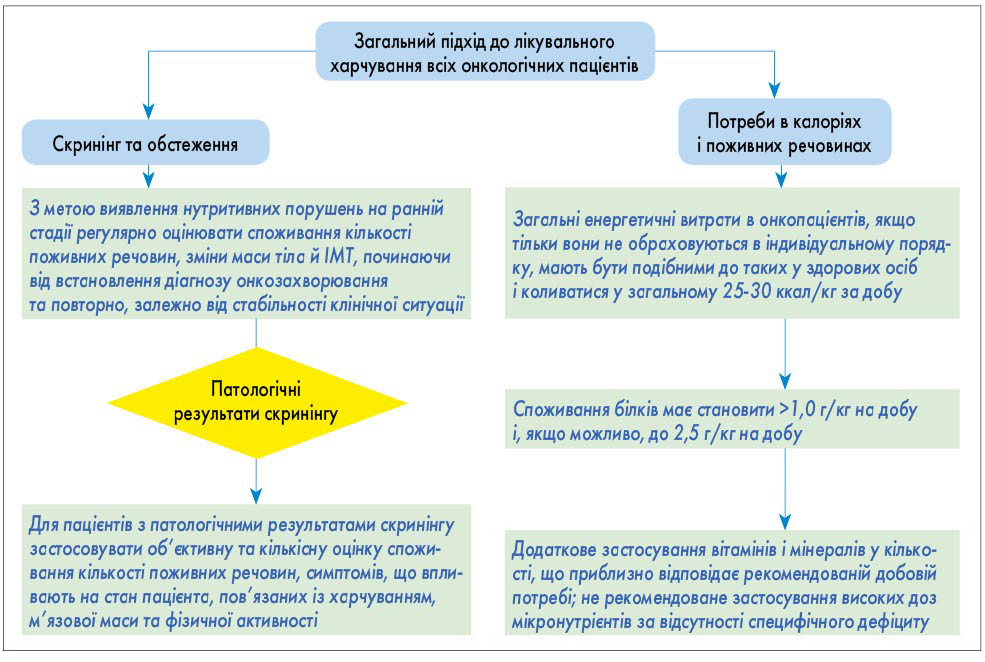 Рис. 3. Загальний підхід до лікувального харчування всіх онкологічних пацієнтів
Рис. 3. Загальний підхід до лікувального харчування всіх онкологічних пацієнтів
Бажані
- Для пацієнтів з патологічними результатами скринінгу застосовується об’єктивна та кількісна оцінка надходження поживних речовин, симптомів, що впливають на стан пацієнта, пов’язаних із харчуванням, м’язової маси, фізичної працездатності та ступеня системного запалення.
- Онкологічні пацієнти, яким проводять радикальні чи паліативні хірургічні втручання, ведуться в межах програми «Прискорена реабілітація після операції» (ERAS). Згідно з цією програмою, кожен пацієнт проходить скринінг на мальнутрицію та, якщо пацієнт перебуває в групі ризику, забезпечується додаткова нутритивна підтримка.
Розділ ІІІ. Лікування
Положення стандарту медичної допомоги. Дієтотерапію бажано розпочати тоді, коли пацієнти ще не перейшли в стан тяжкої мальнутриції. Першою формою нутритивної підтримки має бути консультування з приводу харчування, щоб полегшити контроль симптомів, і заохочення до споживання збагаченої білками та висококалорійної їжі й рідини, які добре засвоюються. Перевагу слід віддавати висококалорійній і високобілковій дієті як методу підтримки та покращення нутритивного статусу.
Обґрунтування. В онкологічних пацієнтів з порушенням процесів травлення або всмоктування їжі, які не здатні споживати їжу, можна стабілізувати нутритивний статус за допомогою лікувального харчування. У пацієнтів з пухлинами, які перешкоджають пероральному споживанню або пасажу їжі вздовж верхніх відділів шлунково-кишкового тракту (ШКТ), нутритивний статус можна стабілізувати за допомогою ЕХ. У разі тяжкої кишкової недостатності внаслідок радіаційного ентериту, хронічної кишкової непрохідності, синдрому короткої петлі, канцероматозу очеревини або хілотораксу нутритивний статус можна підтримати шляхом парентерального харчування (ПХ).
У пацієнтів із резистентністю до інсуліну спостерігається порушення засвоєння й окиснення глюкози міоцитами, проте утилізація жирів залишається нормальною або підвищується, що також свідчить на користь вищого співвідношення жирів до вуглеводів. Відбувається ефективна мобілізація жирів і використання їх як джерела енергії. Порівняно зі здоровими суб’єктами, метаболічний кліренс різних ліпідних емульсій в онкологічних пацієнтів зі стабільною масою тіла підвищений, а у пацієнтів, які втрачали масу тіла, – ще вищий. Крім того, наявні додаткові переваги використання ліпідів замість глюкози при різних схемах ПХ.
Критерії якості медичної допомоги
Обов'язкові
- Загальний підхід до лікувального харчування (ЛХ) всіх онкологічних пацієнтів: скринінг та обстеження; визначення потреби в калоріях і поживних речовинах проводять відповідно до алгоритму (рис. 3).
- Клінічне харчування при онкологічних захворюваннях необхідно забезпечувати з урахуванням факторів, представлених на рисунку 4.
- Загальний підхід до лікування всіх онкологічних пацієнтів: типи ЛХ; фізичні вправи проводять відповідно до алгоритму, поданого на рисунку 5.
- Лікувальні втручання для окремих категорій пацієнтів при хірургічній операції проводять відповідно до алгоритму, представленого на рисунку 6.
- Під час променевої терапії, особливо променевої терапії голови й шиї, грудної клітки та ШКТ, потрібно забезпечити в першу чергу споживання достатньої кількості поживних речовин, застосовуючи індивідуальне консультування з приводу харчування та/або за допомогою перорального додаткового харчування (ПДХ) з метою уникнення погіршення нутритивного статусу, підтримання засвоєння їжі й уникнення переривання променевої терапії відповідно до рекомендацій, згрупованих на рисунку 7.
- Лікувальні втручання для окремих категорій пацієнтів, що проходять радикальну або паліативну протипухлинну медикаментозну терапію та/або високодозову хіміотерапію та трансплантацію гемопоетичних стовбурових клітин (ТГСК), проводять за алгоритмом, представленим на рисунку 8.
- Загальні енергетичні витрати в онкологічних пацієнтів, якщо тільки вони не обраховуються в індивідуальному порядку, мають бути подібними до аналогічних у здорових осіб та становити від 25 до 30 ккал/кг на добу.
- Споживання білків має становити понад 1 г/кг на добу та, якщо можливо, до 1,5 г/кг на добу.
- ЕХ за допомогою назогастрального або черезшкірного зонда (наприклад, черезшкірні ендоскопічні гастростоми) проводиться при тяжкому мукозиті, індукованому променевою терапією, або при обструктивних пухлинах голови та шиї чи грудної клітки.
- Надання нутритивної підтримки онкологічному хворому проводять відповідно до таблиці 2.
- ЛХ в онкологічних пацієнтів здійснюють за схемою, поданою на рисунку 9.
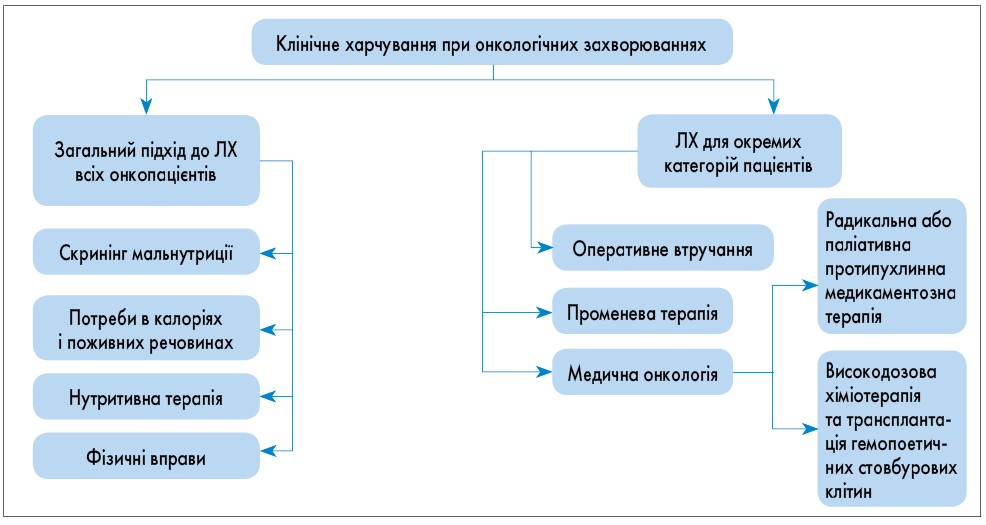 Рис. 4. Клінічне харчування при онкологічних захворюваннях
Рис. 4. Клінічне харчування при онкологічних захворюваннях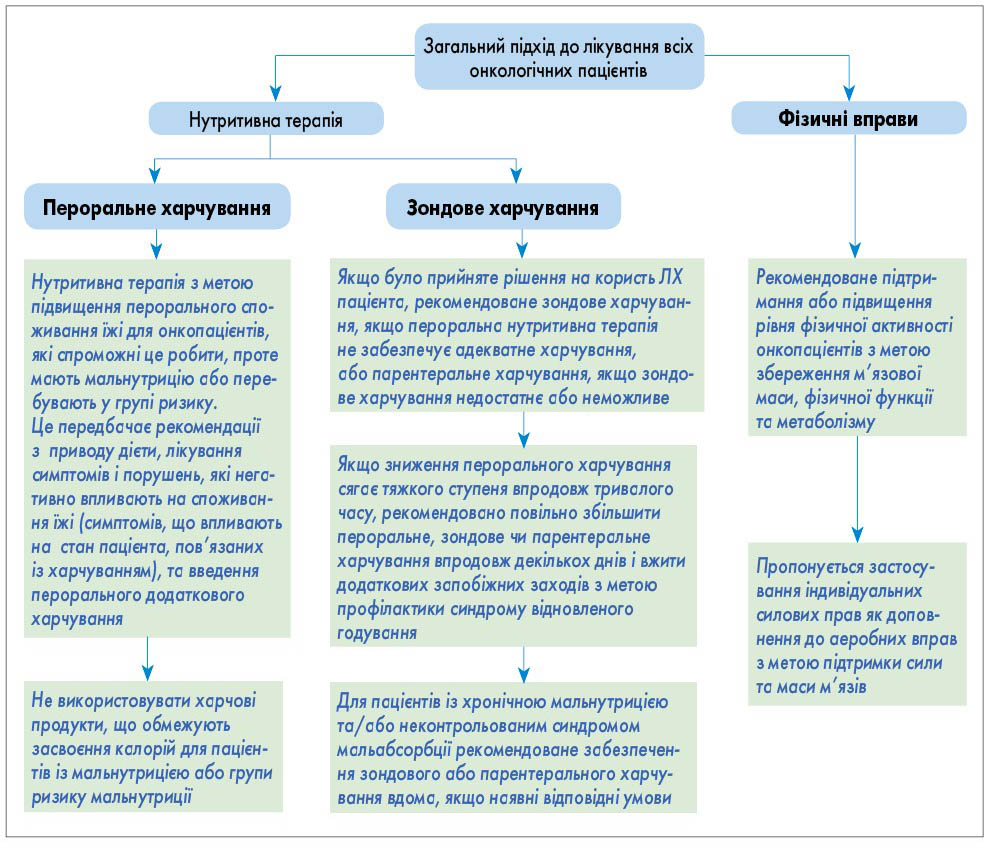 Рис. 5. Загальний підхід до лікування всіх онкологічних пацієнтів: типи ЛХ; фізичні вправи
Рис. 5. Загальний підхід до лікування всіх онкологічних пацієнтів: типи ЛХ; фізичні вправи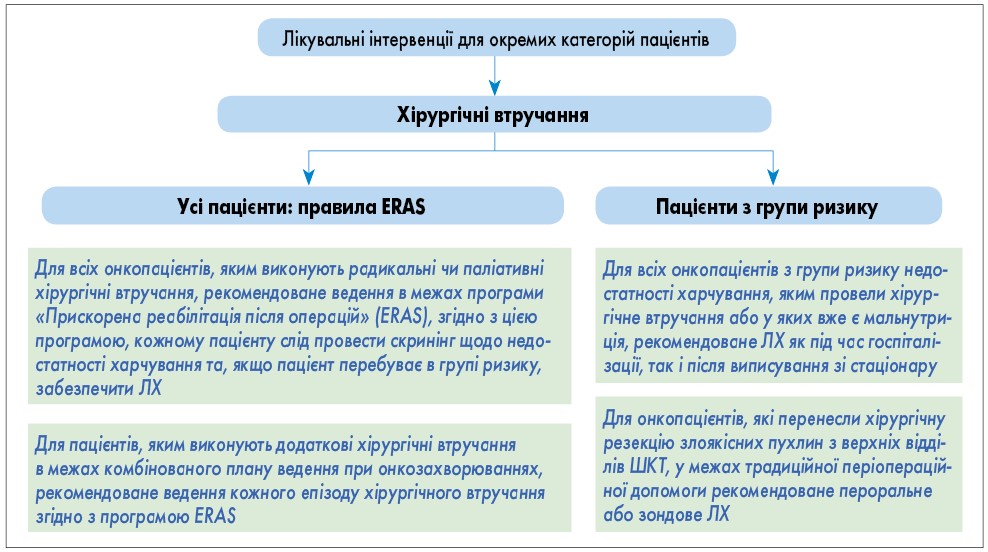 Рис. 6. Хірургічні втручання для окремих категорій пацієнтів
Рис. 6. Хірургічні втручання для окремих категорій пацієнтів 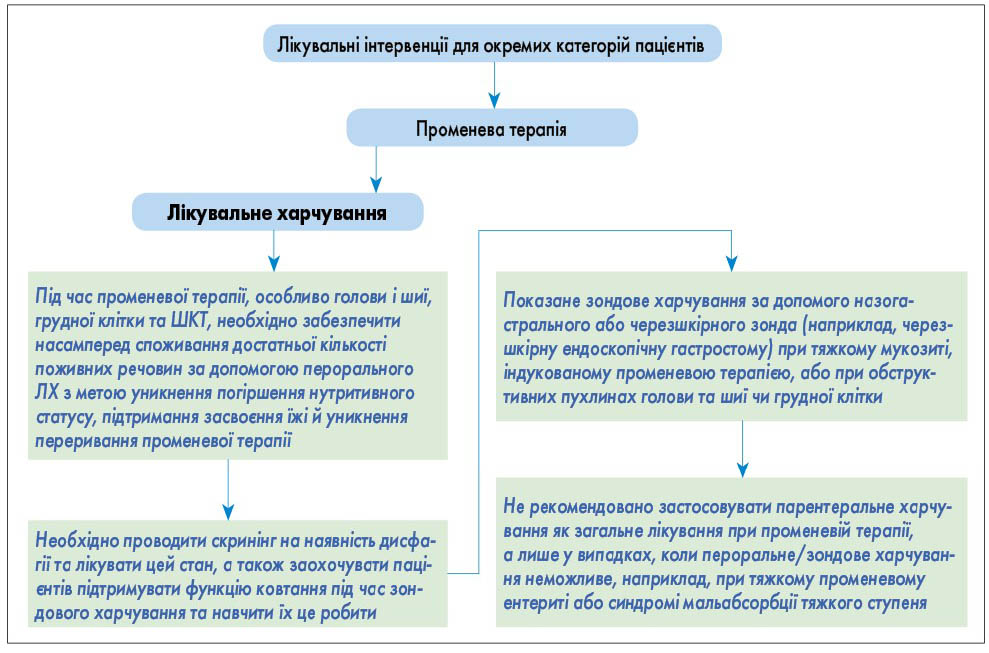 Рис. 7. Лікувальні інтервенції для пацієнтів при променевій терапії
Рис. 7. Лікувальні інтервенції для пацієнтів при променевій терапії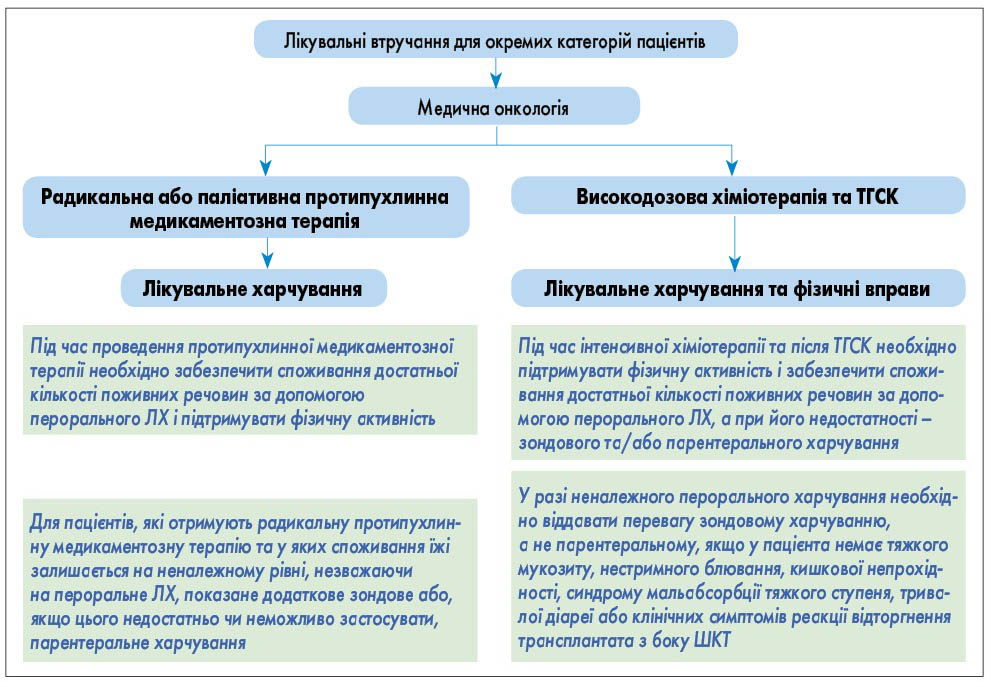 Рис. 8. Лікувальне харчування та фізичні вправи при радикальній або паліативній протипухлинній медикаментозній терапії, високодозовій хіміотерапії та ТГСК
Рис. 8. Лікувальне харчування та фізичні вправи при радикальній або паліативній протипухлинній медикаментозній терапії, високодозовій хіміотерапії та ТГСК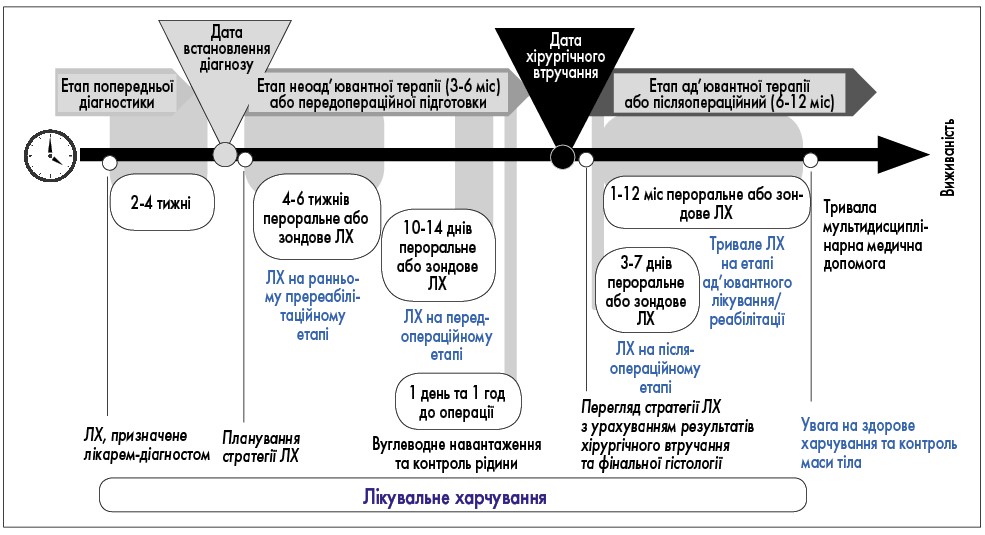 Рис. 9. Лікувальне харчування онкологічного хворого
Рис. 9. Лікувальне харчування онкологічного хворого
|
Таблиця 2. Етапи надання нутритивної підтримки онкологічному хворому |
|||
|
Назва етапу |
Тривалість етапу |
Завдання ЛХ |
Тип ЛХ |
|
Етап попередньої діагностики (до дати встановлення діагнозу) |
24 тижні |
ЛХ, призначене лікаремдіагностом |
Пероральне |
|
Етап неоад’ювантної терапії або Етап передопераційної підготовки |
36 міс
1014 днів |
Раннє пререабілітаційне ЛХ
Передопераційне ЛХ |
Пероральне або зондове
Пероральне або зондове |
|
Етап ад’ювантної терапії або Етап післяопераційний |
612 міс
112 міс |
Тривале ЛХ на етапі ад’ювантної терапії Тривале ЛХ на етапі реабілітації |
Пероральне або зондове
Пероральне або зондове |
Бажані
- Рекомендоване додаткове застосування ПДХ в тих випадках, коли висококалорійна дієта неефективна при досягненні цілей, пов’язаних із харчуванням. ЛХ показане, якщо пацієнти не можуть харчуватися належним чином (наприклад, менше 50% від потреби протягом більше одного тижня або лише 50-75% від потреби протягом більше двох тижнів). Якщо було прийняте рішення на користь додаткового харчування пацієнта, рекомендуємо застосовувати ЕХ, якщо дієтотерапія (консультування, ПДХ) не забезпечує належне пероральне харчування, або ПХ, якщо ЕХ недостатньо або воно неможливе.
- Проводиться додаткове застосування вітамінів і мінералів у кількостях, що приблизно відповідають рекомендованій добовій фізіологічній потребі, не рекомендується введення високих доз мікронутрієнтів за відсутності підтвердженого специфічного дефіциту.
- Для онкологічних пацієнтів, які втрачають масу тіла та мають резистентність до інсуліну, рекомендується збільшити співвідношення калорій, отриманих із жирів, до калорій, отриманих із вуглеводів. Це необхідно для підвищення енергетичної цінності харчування й обмеження глікемічного навантаження.
- Призначаються нутритивні інтервенції з метою підвищення перорального споживання їжі для онкологічних пацієнтів, які здатні споживати їжу, проте мають ознаки мальнутриції або перебувають у групі ризику.
- Підтримання або підвищення рівня фізичної активності в онкологічних пацієнтів з метою збереження м’язової маси, фізичної функції та метаболізму. Застосування індивідуальних силових вправ як доповнення до аеробних вправ з метою підтримання сили та маси м’язів.
- Застосування кортикостероїдів упродовж обмеженого часу (1-3 тижні) для підвищення апетиту в онкологічних пацієнтів зі втратою апетиту на пізніх стадіях захворювання, проте потрібно зважати на побічні ефекти (атрофія м’язів, резистентність до інсуліну, інфекції).
- Застосування прогестинів з метою підвищення апетиту в онкологічних пацієнтів із втратою апетиту на пізніх стадіях захворювання, однак необхідно пам’ятати про потенційні серйозні побічні ефекти (тромбоемболія).
- Додаткове застосування довголанцюгових омега-3 жирних кислот або риб’ячого жиру у пацієнтів на пізніх стадіях онкологічного захворювання, які отримують хіміотерапію та перебувають у групі ризику втрати маси тіла чи страждають від недостатності харчування, з метою стабілізації або покращення апетиту, засвоєння їжі, безжирової маси тіла та загальної маси тіла.
- У пацієнтів зі скаргами на відчуття швидкого насичення після діагностики й лікування запорів слід розглянути необхідність застосування прокінетиків, при цьому потрібно пам’ятати про потенційні побічні ефекти метоклопраміду на центральну нервову систему, а домперидону – на серцевий ритм.
- Якщо пероральне харчування впродовж тривалого періоду було зниженим, проводиться повільне збільшення (пероральне, ентеральне чи парентеральне) харчування впродовж декількох днів і вживаються додаткові запобіжні заходи з метою профілактики синдрому відновленого годування.
Розділ ІV. Подальше спостереження за пацієнтами
Положення стандарту медичної допомоги. Для пацієнтів з групи помірного чи тяжкого нутритивного ризику (особливо ті, хто перенесли оперативне втручання з приводу злоякісних пухлин верхніх відділів ШКТ) слід розглянути можливість рутинної післяопераційної нутритивної підтримки (де можливо – пероральним або ентеральним шляхом). Потрібно зважити щодо подовження такої підтримки, коли пацієнт виписується за місцем проживання. Надати рекомендації пацієнтам щодо фізичної активності. Фізична активність – це ефективна стратегія покращення аеробної здатності, фізичної форми та функціонального статусу.
Обґрунтування. Деякі онкологічні пацієнти продовжують жити виключно на ПХ впродовж багатьох місяців і років, тобто такий часовий проміжок, протягом якого будь-яка особа без їжі за інших умов загинула б від голодного виснаження. Перш ніж розпочати програму тренінгів з домашнього ПХ, важливо оцінити когнітивні та фізичні можливості пацієнта.
Критерії якості медичної допомоги
Обов'язкові
- Для пацієнтів із хронічною недостатністю надходження поживних речовин та/або неконтрольованим синдромом мальабсорбції проводиться забезпечення ЕХ або ПХ вдома за наявності відповідних умов.
- Для онкологічних пацієнтів з групи ризику мальнутриції, яким провели хірургічне втручання або в яких вже є мальнутриція, рекомендуємо належну нутритивну підтримку як під час госпіталізації, так і після виписування зі стаціонару.
- Для онкологічних пацієнтів, які перенесли хірургічну резекцію верхніх відділів ШКТ з приводу злоякісних пухлин, в межах традиційної періоперційної допомоги рекомендуємо пероральне/ентеральне імунне харчування (аргінін, омега-3 жирні кислоти, нуклеотиди).
- Необхідно підтримувати нормальну масу тіла (ІМТ 18,5-25 кг/м2) та дотримуватися здорового способу життя, що передбачає фізичну активність і дієту на основі овочів, фруктів та цільнозернових продуктів із низьким умістом насичених жирів, червоного м’яса й алкоголю.
Індикатори якості медичної допомоги
Наявність у лікаря загальної практики – сімейного лікаря клінічного маршруту пацієнта з мальнутрицією при онкологічних захворюваннях.
Індикатор ґрунтується на положеннях Стандарту медичної допомоги «Нутритивна підтримка при онкологічних захворюваннях».
Дані подаються лікарями, які надають первинну медичну допомогу, лікарями-онкологами, що надають спеціалізовану медичну допомогу пацієнтам на території обслуговування, до структурних підрозділів з питань охорони здоров’я місцевих державних адміністрацій.
Затверджено наказом Міністерства охорони здоров’я України № 142 від 26.01.2024 р.
Дата оновлення стандартів – 2029 рік.
Текст адаптовано та уніфіковано відповідно до стандартів Тематичного випуску «Медичної газети «Здоров’я України».
Повний текст за посиланням: https://www.dec.gov.ua/wp-content/uploads/2024/01/smd_142_26012024.pdf.
Тематичний номер «Онкологія. Гематологія. Хіміотерапія» № 1 (87) 2024 р.



