29 жовтня, 2024
Метформін: від лікування діабету до профілактики раку та подовження життя
Молекула метформіну відома вже понад століття, а її клінічне застосування розпочалося ще в 1950-х роках. Відтоді використання метформіну постійно зростало, і сьогодні його приймають понад 150 млн осіб із цукровим діабетом (ЦД). Із кращим розумінням нових механізмів розширився й терапевтичний профіль препарату. Пропонуємо до уваги читачів огляд статті R. Sirtori та співавт. Metformin: from diabetes to cancer to prolongation of life, опублікованої у журналі Pharmacological Research у серпні, в якій детально висвітлюються відомі на сьогодні ефекти метформіну.
Метформін – цукрознижувальний препарат, представник класу бігуанідів, молекула якого синтезована ще в 1922 році (Werner et al., 1922). Перша публікація, яка свідчить про явний гіпоглікемічний ефект метформіну, з’явилася ще в 1957 році, де зазначено про помірні суб’єктивні побічні ефекти та відсутність очевидного ризику гіпоглікемії – побічного ефекту, який на той час був поширеним при застосуванні препаратів сульфонілсечовини (Sterne, 1957). Пізніші дослідження інсулінорезистентності та виявлення нового механізму активації аденозинмонофосфат-активованої кінази зробили метформін протидіабетичним препаратом з унікальним потенціалом, що виправдовує його дуже широке використання (Zhou et al., 2001).
Всмоктування/розподіл метформіну та побічні ефекти з боку шлунково‑кишкового тракту
Метформін є одним із найширше призначуваних препаратів щодо кількості виписаних рецептів, а добові дози часто можуть перевищувати 2000 мг/день. Високі добові дози часто пов’язані з несприятливими побічними ефектами з боку шлунково-кишкового тракту (ШКТ): від дискомфорту в животі до нудоти, діареї, метеоризму та блювання (як у діабетиків, так і в недіабетиків). Такі побічні ефекти виникають у 25% усіх пацієнтів, що зумовлює припинення лікування в 5% з них (McCreight et al., 2016). Експериментальні дослідження свідчать про те, що такі прояви виникають за рахунок інгібування травних протеаз.
Багаторазове введення та приймання препарату під час їди може допомогти зменшити побічні ефекти. Крім того, поява та доступність таблеток із пролонгованим вивільненням препарату для приймання 1 р/день перед вечерею або 2 р/день перед сніданком і вечерею також сприяє покращенню переносимості й підвищенню прихильності до терапії (Bailey, 2024).
Метформін і кишкова мікробіота
Метформін, який концентрується переважно в дистальному відділі ШКТ, привертає увагу як можливий модулятор кишкової мікробіоти, що зумовило передчасні висновки доклінічних досліджень про його можливу користь для метаболічного й імунного здоров’я (Pollak, 2017). Загальним висновком клінічних досліджень метформіну було збагачення таксономічних одиниць з Bacteroides і скорочення таксономічних одиниць з Faecalibacterium (Elbere et al., 2018). Повідомляється про підвищений рівень Escherichia spp. і знижений Intestinebacter spp. як у людей з нормоглікемією, так і в пацієнтів із ЦД 2 типу (Bryrup et al., 2019).
Більшість даних щодо зміни мікробіоти після прийому метформіну переважно стосуються товстого кишечнику; оскільки метформін може досягати високих концентрацій і в тонкому кишечнику (Bailey et al., 2008), зміни мікробіоти здатні спричинити модифікацію генів, що впливає на поглинання глюкози та жирних кислот, сприяючи іншим метаболічним ефектам метформіну (Sun et al., 2018). Цікаво, що трансплантація мікробіоти, обробленої метформіном, у верхній відділ тонкої кишки супроводжувалася відновленням механізмів сприйняття глюкози (Bauer et al., 2018).
Основний механізм захисної дії метформіну на кишковий бар’єр слизової оболонки – збільшення відносної чисельності Akkermansia muciniphila, що сьогодні зумовлює значний інтерес через потенційну роль у зниженні маси тіла (Abuqwider et al., 2021). Зростання Akkermansia та келихоподібних клітин спричиняє захисне потовщення слизового шару (Ke et al., 2021).
Метформін та інсулінорезистентність
Гіпоглікемічна дія метформіну була детально вивчена із практичного та клінічного погляду. Безсумнівно, припинення приймання метформіну спричинить швидке підвищення рівня глікемії та глюкозурію (Siitonen et al., 1980). Застосування його при лікуванні пацієнтів із ЦД 1 типу зумовлювало зниження постпрандіальної потреби в інсуліні (Gin et al., 1982).
Метформін зазвичай знижує рівень глюкози та інсуліну, зменшуючи в такий спосіб інсулінорезистентність. Цей стан лежить в основі порушення гомеостазу глюкози, що зумовлює типові форми ЦД 2 типу й ожиріння (Reaven, 1988): резистентність до інсуліну спочатку спричиняє компенсаторне підвищення секреції інсуліну, а гіперінсулінемія, своєю чергою, – дисліпідемію, артеріальну гіпертензію, атеросклероз, гіперурикемію, прокоагулянтний стан (Thomas et al., 2019). Еволюція концепції інсулінорезистентності зумовила запровадження терміна «метаболічний синдром» (поєднання щонайменше 3 із 5 станів: гіпертригліцеридемія, гіпертонія, низький рівень холестерину ліпопротеїнів високої щільності, збільшення окружності живота та помірна гіперглікемія), пов’язаного з резистентністю до інсуліну (Jamali et al., 2024).
Відомо, що в покращенні чутливості до інсуліну активно діють агоністи GLP‑1, які використовуються переважно за надмірної маси тіла (Drucker, 2018). Метформін самостійно може підвищувати рівень GLP‑1 (Bahne et al., 2018) і в такий спосіб здатен посилювати відчуття насичення, а відтак, попереджувати переїдання (Kim et al., 2024). Комбіноване застосування з агоністами GLP‑1 (Ke et al., 2017) демонструє ефективне зниження маси тіла, а також чинить позитивний вплив на ендотеліальну функцію.
Позитивний вплив на масу тіла
Ожиріння часто супроводжує ЦД 2 типу (Zimmet et al., 2001), тому в лікуванні варто віддавати перевагу протидіабетичним препаратам, які не лише знижують рівень глюкози в крові, а й чинять значний вплив на масу тіла. E. Lazzaroni та співавт. (2021) засвідчили, що протидіабетичні препарати можуть сприяти значному зниженню маси тіла в пацієнтів із ЦД, покращуючи в такий спосіб контроль глікемії та знижуючи ризик пов’язаних ускладнень. Виявлено, що метформін може зумовити помірну втрату маси тіла чи запобігти її збільшенню, що пов’язано з лікуванням інсуліном (Stumvoll et al., 1995; Kahn et al., 2006). Механізми цього явища включають зниження апетиту через підвищення рівня GLP‑1 (Kim et al., 2024). Крім того, показано, що використання метформіну зумовлює покращення складу тіла шляхом зменшення вісцерального й абдомінального жиру в пацієнтів із ЦД 2 типу. В разі звичайного застосування пацієнти можуть втрачати масу тіла на початку лікування через супутні побічні ефекти з боку ШКТ.
Метформін і гіполіпідемічні ефекти
Ще в ранніх клінічних дослідженнях повідомлялося про зниження рівня холестерину ліпопротеїнів низької щільності (ХС ЛПНЩ) на 12% на тлі прийому метформіну порівняно з глібенкламідом (Rains et al., 1988). В експериментальному дослідженні D. Hu та співавт. (2021) виявили зв’язок між зниженням загального холестерину та ХС ЛПНЩ і зниженням циркулювальної пропротеїнконвертази субтилізин/кексинового типу 9 (PCSK9) на тлі метформіну. Альтернативним запропонованим механізмом є інгібування ангіопоетин-подібного білка‑3, який діє як антагоніст ліпопротеїнліпази й ендотеліальної ліпази (Shimizugawa et al., 2002). Пригнічення експресії цього білка може слугувати підставою для призначення метформіну за тяжких гіперліпідемій (Lin et al., 2019).
Ендотеліальна дисфункція
Атеросклеротичні серцево-судинні захворювання (ССЗ), зокрема захворювання периферичних артерій, є основними причинами захворюваності та смертності в осіб із ЦД 2 типу (Wong and Sattar, 2023). Субклінічна ендотеліальна дисфункція – один із найперших факторів, що сприяють розвитку атеросклерозу; визначається в пацієнтів із ЦД у молодому віці. Останні результати клінічних та експериментальних досліджень свідчать про те, що гіперглікемія зумовлює порушення фізіологічних механізмів вазодилатації, що є передвісником ССЗ (Verma and Anderson, 2002). Явна ендотеліальна дисфункція спостерігалася в дітей/підлітків із діабетом (Pastore et al., 2020), а в дорослих часто пов’язана з гіперактивністю тромбоцитів (Kaur et al., 2018).
Ендотеліальна дисфункція є добре описаною мішенню метформіну. Низка клінічних спостережень свідчить про сприятливу дію метформіну. Рандомізоване плацебо-контрольоване дослідження за участю пацієнтів із ЦД 2 типу продемонструвало суттєве зниження маркерів ендотеліальної дисфункції на тлі терапії метформіном (de Jager et al., 2014).
Накопичення ліпідів в ендотелії, що відбувається після споживання значної кількості жиру, пригнічує активність ендотеліальної синтази оксиду азоту, що спричиняє підвищення артеріального тиску (Kim et al., 2023). Антагонізуючи накопичення ліпідів, метформін може асоціюватися зі зниженням артеріального тиску (Duan et al., 2017).
Метформін і рак
Неочікувана протиракова активність метформіну була результатом раннього епідеміологічного дослідження J.M. Evans і співавт. (2005), яке продемонструвало, що пацієнти, котрі отримували метформін, мали значно нижчий тягар раку порівняно з діабетиками, що застосовували інші препарати. Це спостереження підтверджено даними інших досліджень (McFarland and Cripps, 2010; Decensi et al., 2010). Два незалежні метааналізи, які порівнювали метформін з іншими методами лікування ЦД 2 типу, засвідчили зниження захворюваності на рак на 30-40% у разі застосування метформіну (Gandini et al., 2014; Noto et al., 2012).
Діабет має чіткий зв’язок із підвищеним ризиком раку, особливо в осіб, які отримують інсулін (Colhoun and Group, 2009). Показано, що застосування метформіну знижує частоту специфічних видів раку, зокрема раку молочної залози (Cejuela et al., 2022), і є ефективним радіосенсибілізатором при лікуванні цієї пухлини (Song et al., 2012). Метформін демонструє ефективність під час лікування раку, зокрема тих його варіантів, котрі лікують цисплатином (Rocha et al., 2011). Крім того, застосування метформіну пов’язано з явним зниженням ризику розвитку раку порівняно з іншими протидіабетичними засобами (Libby et al., 2009). Існують свідчення того, що пухлини, яким властива неповноцінна регуляція окисного фосфорилювання (імовірно, за рахунок мутацій у MRC1), виявляються найчутливішими до бігуанідів (Birsoy et al., 2014).
Метаболічні стани, пов’язані із застосуванням метформіну і, ймовірно, з позбавленням клітин глюкози, були виявлені на клітинній моделі потрійного негативного підтипу раку грудної залози (TNBC), тобто зі зниженою експресією рецептора HER2, а також рецепторів естрогену та прогестерону (Foulkes et al., 2010). Метформін у поєднанні з депривацією глюкози, ймовірно, пригнічує клітини тричі негативного підтипу раку молочної залози шляхом зменшення проліферації та посилення апоптозу, а також шляхом стимулювання розгорнутих білкових відповідей ендоплазматичного ретикулуму (Li et al., 2023). Наразі >400 клінічних досліджень, що вивчають протиракову активність метформіну, перераховані в ClinicalTrials.gov. Нещодавно проведений огляд O’Connor і співавт. (2024) також чудово ілюструє ефективність метформіну в боротьбі проти раку.
Ймовірно, вражаючі метаболічні властивості метформіну допомагають у лікуванні внутрішньої дифузної понтинної гліоми, що здебільшого уражає дітей та не має ефективного лікування. Націлюючись на шлях PI3K/mTOR, препарат паксалісиб забезпечує стабілізацію захворювання в деяких пацієнтів, але водночас спостерігаються значна гіперінсулінемія та гіпоглікемія (Hopkins et al., 2018).
Потенційні протиракові механізми метформіну представлено на рисунку 1.
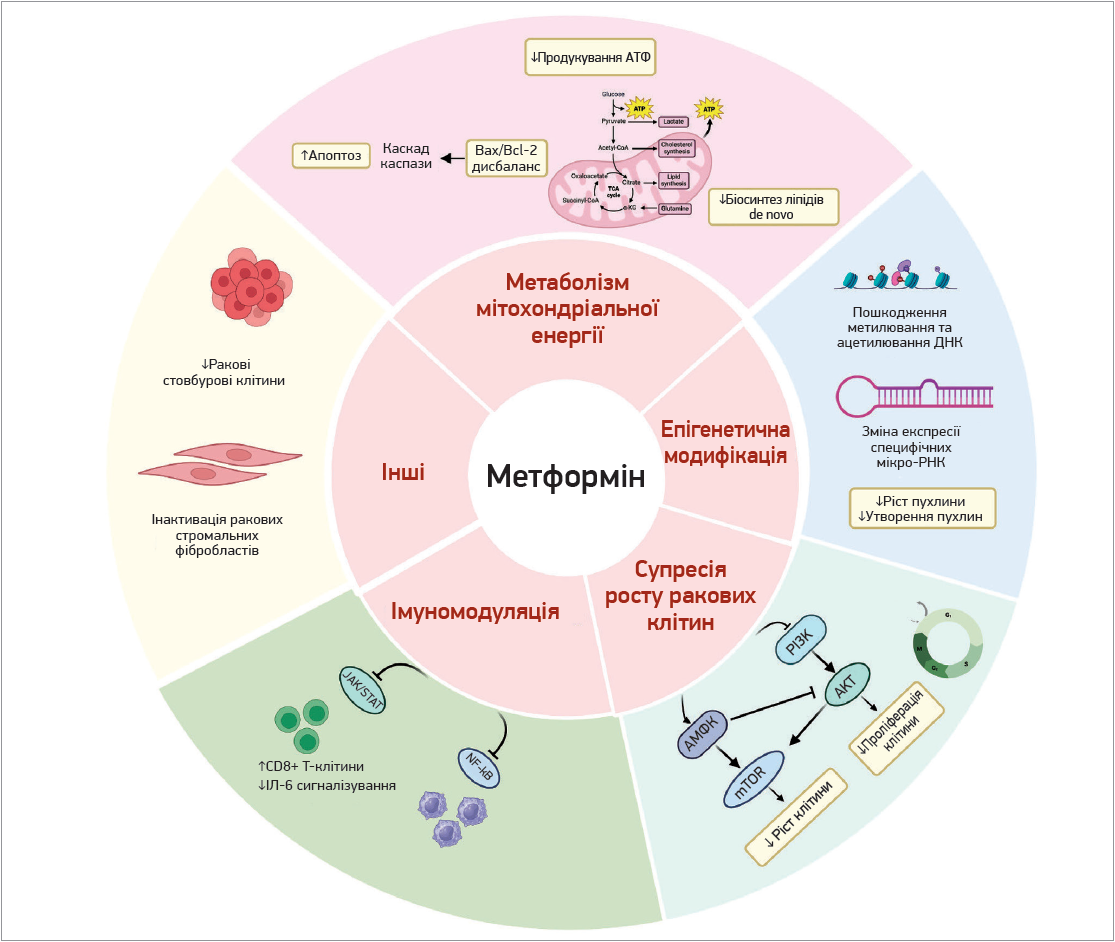 Рис. 1. Потенційні протиракові механізми метформіну
Рис. 1. Потенційні протиракові механізми метформіну
Примітки: PI3K – фосфатидилінозитол кіназа‑3; AKT – протеїнкіназа В.
Метформін і старіння
Прогресувальна втрата фізіологічних функцій, у т. ч. на тлі хронічних захворювань і станів, які супроводжуються слабкістю й обмеженою рухливістю, спричиняє старіння. Виявилося, що метформін може перешкоджати цьому процесу (Guarente et al., 2024; Kulkarni et al., 2020).
С. Lopez-Oti та співавт. (2013) визначили 9 основних ознак старіння: геномна нестабільність, епігенетичні зміни, втрата протеостазу, стирання теломер, дерегуляція сприйняття поживних речовин, мітохондріальна дисфункція, клітинне старіння, виснаження стовбурових клітин і змінений міжклітинний зв’язок, до яких нещодавно вони додали відключену макроавтофагію, хронічне запалення і віковий дисбактеріоз (Lopez-Otin et al., 2023).
Роль метформіну в пригніченні біологічного старіння здебільшого є наслідком його активності як інгібітора MRC‑1, що зумовлює численні ефекти на метаболічні та неметаболічні шляхи в процесі старіння (Barzilai et al., 2016), включаючи лізосомальні шляхи (Chen et al., 2017).
Запалення є основною мішенню метформіну. Пригнічення прозапальних цитокінів шляху NF-kB пов’язано зі зниженням смертності в осіб літнього віку із ЦД, які отримували метформін (Tizazu et al., 2019). Дія метформіну на дисфункціональні мітохондрії зі старінням досить передбачувана з огляду на механізм дії препарату на окислювальний стрес (Murphy and Hartley, 2018), імовірно, затримуючи мітохондріальний біогенез і старіння за допомогою AMPK-опосередкованого метилювання H3K79, що діє через вісь SIRT1-DOT1L (Karnewar et al., 2018).
Цікавою дією метформіну є антагонізм до виснаження стовбурових клітин, що зазвичай пов’язано зі зниженням відновлення тканин у стабільному стані разом із порушенням відновлення тканин після травми. Препарат може затримувати клітинне виснаження та запобігати передчасному старінню, збільшуючи в такий спосіб тривалість життя мезенхімальних стовбурових клітин (Fang et al., 2018).
Механізми, що сприяють довголіттю та зниженню розвитку непроліферативних захворювань, включаючи захворювання нирок, стеатоз печінки 1 і 2 типу, хворобу Паркінсона, згруповані в асоційованому зі старінням секреторному фенотипі (АССФ).
Постійне приймання метформіну в низьких дозах може сповільнювати старіння клітин і пригнічувати АССФ шляхом регуляції GPx7 через Nrf2 (Fang et al., 2018). Метформін також може діяти в рамках DICER1-залежного механізму, знижуючи білки p16 і p21, рівні РНК АССФ-асоційованих IL‑6, IL‑8 у фібробластах людини (Noren and Hooten et al., 2016).
Завдяки зменшенню регуляції АССФ, навантаження на старіючі клітини знижуватиметься під дією метформіну, що захищає від окисного стресу та сприяє автофагії в умовах хронічного запалення (Kuang et al., 2020).
У випадку раку та старіння підвищена автофагія може потенційно зменшити проліферацію клітин-попередників через секрецію факторів росту та змін у системі «автофагія – лізосома» (Young et al., 2021) з виявленням пов’язаної зі старінням β-галактозидази. Залежно від індивідуальних особливостей процес автофагії може мати різні результати (як при раку, так і при старінні); яскравим прикладом є тривалість голодування в стратегії втрати маси тіла з періодичним голодуванням (Shabkhizan et al., 2023). Для метформіну анти-АССФ і проавтофагічна активність може виникати практично за всіх умов, що є ефективним інструментом для придушення клітинного старіння з віком (рис. 2).
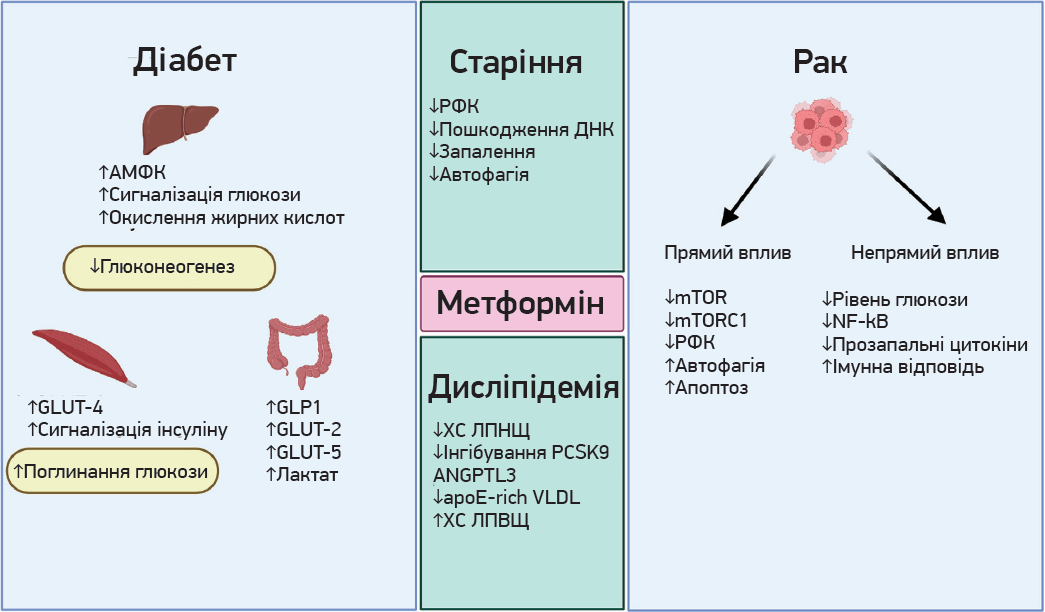 Рис. 2. Схема основних механізмів дії метформіну за різних захворювань
Рис. 2. Схема основних механізмів дії метформіну за різних захворювань
Примітки: AMPK – аденозинмонофосфаткіназа; GLUT‑4 – транспортер глюкози 4 типу; GLP1 – глюкагоноподібний пептид 1 типу; GLUT‑2 – транспортер глюкози 2 типу; GLUT‑5 – транспортер глюкози 5 типу; ХС ЛПНЩ – холестерин ліпопротеїнів низької щільності; ХС ЛПВЩ – холестерин ліпопротеїнів високої щільності; РФК – реактивні форми кисню.
Інші потенційні ефекти метформіну
Широке застосування метформіну в пацієнтів із ЦД дозволило виявити інші потенційні сфери терапевтичного інтересу. Серед них найбільшу увагу привернули хвороба Альцгеймера, судинна деменція та хвороба Паркінсона. Існують свідчення, що метформін може забезпечити простий і недорогий підхід до лікування лобно-скроневої деменції та бічного аміотрофічного склерозу (Rosbash, 2020).
Синдром полікістозних яєчників (СПКЯ) характеризується резистентністю до інсуліну (Bozdag et al., 2016). Для СПКЯ характерні ановуляція, олігоменорея та морфологія полікістозних яєчників, що пов’язано зі зниженням рівня GLUT4 в ендометрії, котрий підвищується під час лікування метформіном (Carvajal et al., 2013). Під час нещодавнього метааналізу оцінювали ефекти метформіну при СПКЯ порівняно з оральними контрацептивами (ОК) (Melin et al., 2024). Виявилося, що комбіноване лікування надає певну користь щодо рівня інсуліну, гіперандрогенії та резистентності до інсуліну порівняно з лікуванням лише ОК.
Висновки
Отже, метформін – ефективний і безпечний препарат для лікування ЦД, котрий характеризується низкою переваг, як-от: доступність, хороша переносимість (у разі прийому під час їди), мінімальний ризик гіпоглікемії, втрата маси тіла, легке поєднання з будь-якими іншими протидіабетичними засобами. Нещодавнє впровадження в практику пролонгованих форм метформіну забезпечило покращення переносимості препарату, а також можливість застосування його при гестаційному діабеті. Метформін входить до переліку основних лікарських засобів, рекомендованих Всесвітньою організацією охорони здоров’я, що робить використання цієї простої молекули обов’язковим. Використання метформіну стало особливо цінуватися після виявлення додаткових властивостей молекули, декотрі з яких безпосередньо пов’язані з діабетом, а саме зниження маси тіла та рівня ліпідів, натомість інші забезпечують неочікувану користь для здоров’я.
Метформін демонструє терапевтичну ефективність за різних форм раку: найефективнішим він є у разі колоректального раку з мутаціями KRAS. Нещодавні спостереження демонструють його ефективність у дітей із практично невиліковною дифузною внутрішньою гліомою моста, а також у комбінації з інгібіторами PD‑1/PD-L1 при гепатоцелюлярній карциномі. Очевидна потенційна дія метформіну на подовження життя пов’язана з мітохондріальною активністю препарату, а також із протизапальними властивостями, пов’язаними з лізисом клітин за допомогою АССФ, що, ймовірно, зумовлює автофагію, збільшення довжини теломер. Нещодавно виявлено, що вплив метформіну на тривалість життя потенційно пов’язаний з антагонізмом RANs, контролюючи розширення багатьох повторів класичної ініціації AUG у центральній нервовій системі (ЦНС). Цей тяжкий стан, який не піддається лікуванню, може виникати при розладах ЦНС, як-от бічний аміотрофічний склероз і фронтотемпоральна деменція, які є потенційними мішенями метформіну.
Sirtori C.R., Castiglione S., Pavanello С. Metformin: from diabetes to cancer to prolongation of life. Pharmacological Research, Vol. 208, 2024. doi.org/10.1016/j.phrs.2024.107367.
Реферативний огляд підготувала Людмила Суржко
Довідка «ЗУ»
На фармацевтичному ринку України метформін представлений, зокрема, препаратом європейського виробництва Сіофор® (компанія «Берлін-Хемі АГ»). Таблетки Сіофор® доступні в дозуванні по 500, 850 або 1000 мг метформіну гідрохлориду. Препарат показаний для лікування ЦД 2 типу в дорослих і дітей віком >10 років, особливо за наявності надлишкової маси тіла, неефективності дієтотерапії та фізичного навантаження. Сіофор® можна застосовувати як монотерапію з іншими пероральними гіпоглікемічними засобами або в комбінації з інсуліном. Пролонговані форми: Сіофор® XR 500 та Сіофор® XR 1000 сприяють підвищенню прихильності пацієнтів до терапії через зменшення кратності прийому, а також мають переваги в переносимості з боку ШКТ.
Варто зазначити, що пролонговані форми препарату Сіофор® є в переліку препаратів для реімбурсації, що робить Сіофор® доступним широкому колу пацієнтів.
Медична газета «Здоров’я України 21 сторіччя» № 18 (579), 2024 р




