3 липня, 2021
Контроль над симпатичним овердрайвом: патогенетичний підхід до попередження ускладнень артеріальної гіпертензії
21-23 травня відбулася науково-практична конференція з міжнародною участю «Міжнародний досвід у діагностиці та лікуванні артеріальної гіпертензії (АГ)». На конференції пролунали виступи провідних українських та іноземних фахівців щодо АГ, а також проведено низку майстер-класів і цикл круглих столів. Учасники заходу мали можливість підвищити свій рівень знань щодо сучасної діагностики АГ і новітніх поглядів на лікування цієї хвороби.
Велику увагу аудиторії привернула бінарна лекція «Контроль над симпатичним овердрайвом: патогенетичний підхід до попередження ускладнень АГ» завідувача відділення симптоматичних гіпертензій ДУ «ННЦ «Інститут кардіології ім. академіка М. Д. Стражеска» НАМН України» (м. Київ), доктора медичних наук, професора Юрія Миколайовича Сіренка та завідувачки кафедри загальної практики (сімейної медицини) Національного медичного університету ім. О. О. Богомольця (м. Київ), доктора медичних наук, професора Ольги Миколаївни Барни.
Показник серцево-судинної смертності чоловіків в Україні за період 1976-2013 рр. є найвищим серед європейських країн. У середньому в світі на серцево-судинні захворювання (ССЗ) припадає 45-50% усієї смертності, а в Україні – понад 65%. Юрій Миколайович продемонстрував слухачам типовий портрет пацієнта, в якого з високою імовірністю відбудеться серцево-судинна катастрофа. Зазвичай це чоловік середнього віку, котрий не дотримується здорового харчування і вживає багато м’яса, хворіє на АГ та дисліпідемію, однак не знає про це, має надмірну масу тіла, курить, веде малорухливий спосіб життя. В таких пацієнтів надзвичайно важливою є підтримка нормальних значень артеріального тиску (АТ).
У контролі АТ важливу роль відіграє симпатична нервова система. Симпатичні імпульси спричиняють розширення зіниць, пригнічення слиновиділення, розслаблення мускулатури бронхів, прискорення серцебиття, гальмування перистальтики та секреції органів травної системи; стимулюють утворення і вивільнення глюкози, секрецію адреналіну та норадреналіну; інгібують активність сечового міхура; стимулюють розвиток оргазму, тобто виконують низку необхідних фізіологічних функцій. Однак постійна активація симпатичної нервової системи (чи симпатичний овердрайв) є одним із чинників розвитку метаболічного синдрому й інших факторів ризику ССЗ. Ця симпатична гіперактивація запускається рефлекторними механізмами (порушення функції артеріальних барорецепторів), метаболічними (інсулінорезистентність) та гуморальними факторами (ангіотензин ІІ, лептин).
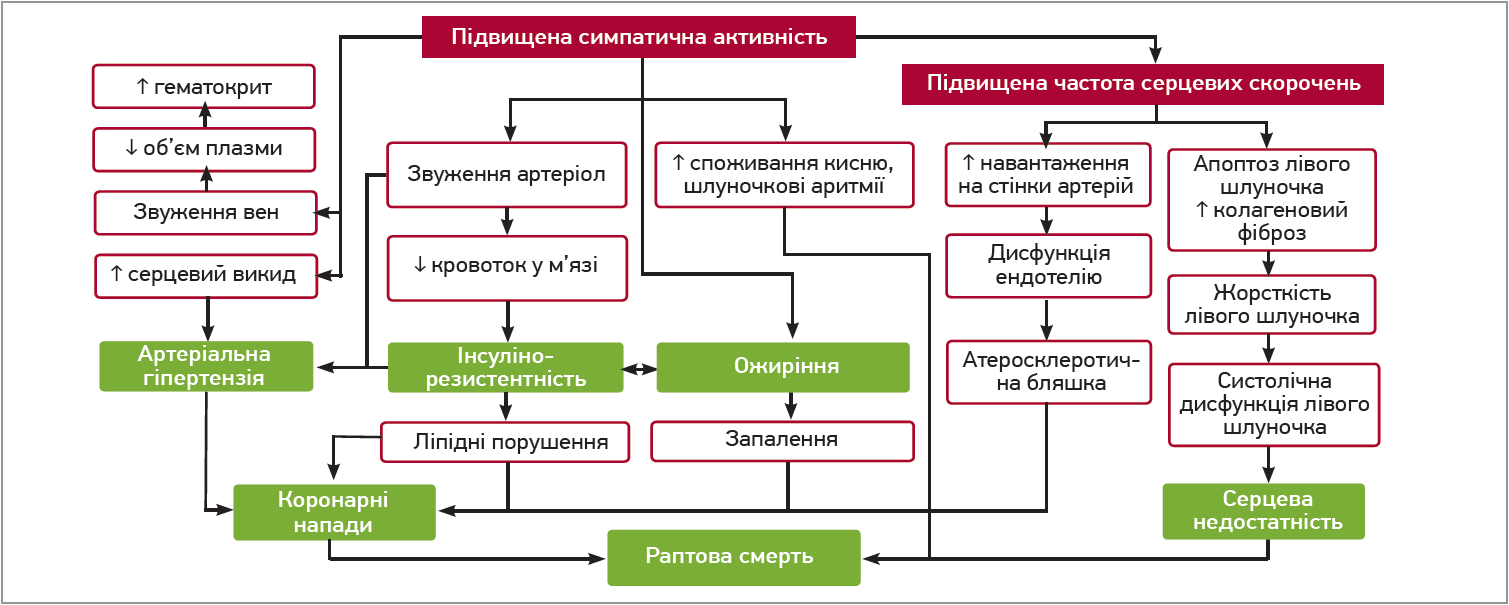
За визначенням, симпатичний овердрайв являє собою постійну надмірну активність симпатичної нервової системи. Небезпека симпатичного оведрайву полягає у тому, що внаслідок тривалої гіперсимпатикотонії в організмі людини запускається низка змін, наприклад, постійно підвищений апетит сприяє накопиченню жирової тканини, а тривале збільшення АТ спричиняє перебудову серця. Симпатичний овердрайв пов’язана зі збільшенням частоти серцевих скорочень (ЧСС) та іншими факторами кардіоваскулярного ризику: ендотеліальною дисфункцією, дисліпідемією, звуженням артеріол, підвищенням жорсткості стінки лівого шлуночка (рис. 1). Ці та інші метаболічні, а також судинні зміни зрештою зумовлюють напади стенокардії, раптової серцевої смерті чи розвиток серцевої недостатності (СН).
Рис. 1. Несприятливий вплив підвищеної симпатичної активності
Підвищення симпатичного тонусу можуть провокувати такі стани, як цукровий діабет (ЦД) 2 типу, ожиріння (здебільшого центрального характеру), куріння та хронічні психологічні стреси. При ЦД з’являється своєрідне хибне коло: підвищення вмісту адреналіну спричиняє інсулінорезистентність, а зростання вмісту інсуліну, своєю чергою, зумовлює викид адреналіну. За схожим механізмом розвивається і гіперсимпатикотонія при центральному ожирінні. Адипоцити продукують лептин, який сприяє вивільненню норадреналіну, а також вазотоксичні адипокіни, що посилюють запальну відповідь ендотелію з розвитком інсулінорезистентності. Механізм гіперсимпатикотонії на тлі куріння полягає у тому, що нікотин стимулює ганглії симпатичної нервової системи з вивільненням норадреналіну. Останній спричиняє вазоконстрикцію з підвищенням периферичного судинного опору, отже, і зростанням АТ та ЧСС. Що стосується хронічного психологічного стресу, то він зумовлює активацію симпатичної нервової системи за рахунок вивільнення кортизолу та прозапальних цитокінів. На тлі стресу з’являється ендотеліальна дисфункція, що спричиняє зниження здатності судин розширюватися у відповідь на механічні та хімічні стимули, отже, й зменшення перфузії та зростання ризику розвитку ішемічної хвороби серця (ІХС).
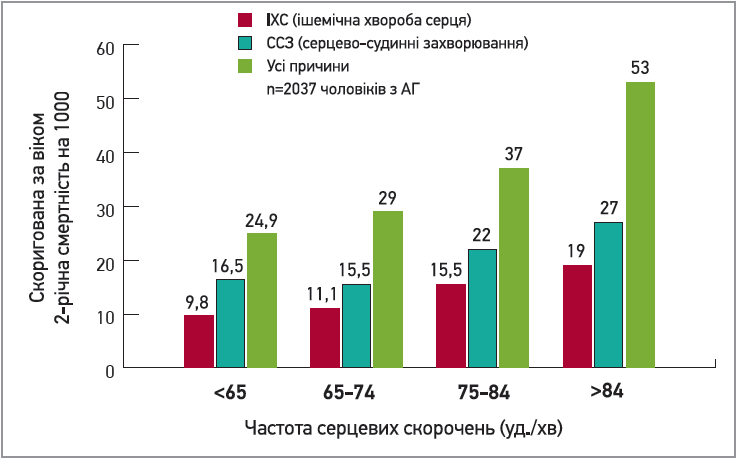
Підвищення ЧСС як безпосередній наслідок гіперсимпатикотонії – важливий чинник ризику на всіх етапах серцево-судинного континууму. За даними Фрамінгемського дослідження, симпатичний овердрайв є ключовим фактором зростання ЧСС і зумовлює зростання смертності від ССЗ незалежно від вікової категорії (рис. 2).
Рис. 2. Вплив ЧСС на смертність
Доведено, що підвищена ЧСС – довготривалий прогностичний фактор серцево-судинних подій у пацієнтів з АГ. Навіть на тлі контрольованого АТ у пацієнтів з високою ЧСС частіше з’являються кардіоваскулярні катастрофи. Неконтрольований АТ і низька ЧСС супроводжуються меншою кумулятивною частотою первинних подій, ніж контрольований АТ та висока ЧСС (Julius S. еt al., 2012).
У дослідженні MESA з’ясувалося, що для найвищого квартиля ЧСС скоригований відносний ризик розвитку СН був утричі вищим, ніж для найнижчого. Кожне збільшення середньої ЧСС на 1 уд./хв підвищувало відносний ризик СН на 4% (Opdahl A. et al., 2014). Ці дані зумовлюють потребу в суворому контролі не лише АТ, а й ЧСС.
Зниження ЧСС за рахунок пригнічення симпатичного овердрайву можна фармакологічно досягти лише за допомогою β-адреноблокаторів (БАБ) без внутрішньої симпатоміметичної активності. ЧСС також знижується на тлі вживання недигідропіридинових блокаторів кальцієвих каналів (верапаміл, дилтіазем), але брадикардитична дія цих препаратів пов’язана не з впливом на симпатичні ганглії, а з уповільненням проведення збудження та подовженням ефективного рефрактерного періоду всередині АV-вузла та збільшенням періоду реполяризації. Ще одним препаратом, який виражено зменшує ЧСС, є івабрадин – засіб, котрий специфічно впливає на If-потік, що контролює водій ритму в синоатріальному вузлі. Івабрадин рекомендовано застосовувати при ІХС як препарат другої лінії тільки в разі непереносимості БАБ або за потреби додаткового зниження ЧСС після призначення максимальної дози БАБ. За даними досліджень, івабрадин ефективний лише в пацієнтів зі схильністю до тахікардії (ЧСС >70 уд./хв).
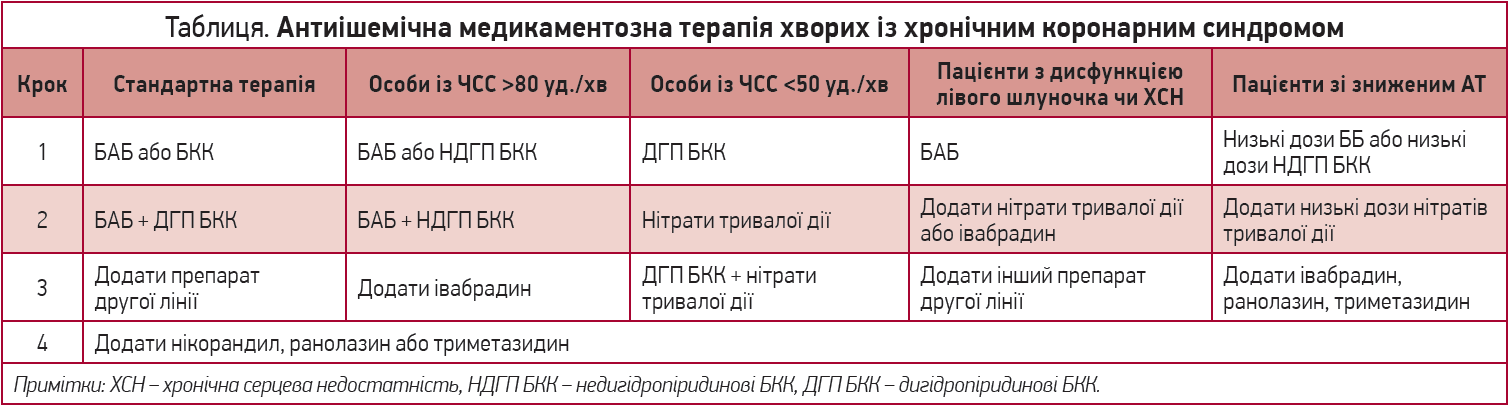
Сучасні БАБ чинять сприятливий вплив не лише на ЧСС, а й на низку інших точок серцево-судинного континууму. Відповідно до рекомендацій Європейського товариства кардіологів (2019), БАБ є першою лінією антиішемічної медикаментозної терапії у всіх груп хворих, крім осіб із ЧСС <50 уд./хв (табл.).
Важливо, що БАБ також здатні модифікувати прогноз у хворих на ІХС. За даними проспективного багатоцентрового дослідження CORONOR (n=4149), застосування БАБ на 57% знижує серцево-судинну смертність у пацієнтів зі стабільною стенокардією з інфарктом міокарда чи реваскуляризацією в анамнезі. Доведено, що БАБ достовірно покращують виживаність хворих з інфарктом міокарда після перкутанного коронарного втручання. Найбільші переваги застосування БАБ були в осіб з низькою фракцією викиду лівого шлуночка та багатосудинним ураженням.
Деякі лікарі помилково вважають, що в сучасному лікуванні АГ немає місця БАБ, оскільки провідні позиції посідають різні комбінації препаратів інших класів. Однак у рекомендаціях Європейського товариства кардіологів та Європейського товариства гіпертензії (2018) чітко зазначено, що БАБ можуть бути призначені на будь-якому етапі лікування АГ за наявності відповідних показань: ІХС, ХСН, стан після інфаркту міокарда, фібриляція передсердь. Застосування БАБ також є доцільним у молодих жінок з АГ, які планують вагітність.
Одним з найчастіших побоювань пацієнтів щодо БАБ є еректильна дисфункція (ЕД), однак ЕД більшою мірою є психологічною проблемою, ніж побічним явищем БАБ. У дослідженні A. Silvestri та співавт. (2003) ЕД удвічі частіше спостерігалася в тих пацієнтів, які знали, що ЕД може бути побічним явищем на тлі прийому БАБ, ніж у тих, хто не був обізнаний щодо можливості розвитку цього ефекту. Тобто знання про ЕД як побічний ефект супроводжувалося більшою імовірністю розвитку цього явища. Крім того, автори дослідження виявили, що 95-100% випадків ЕД на тлі БАБ ефективно коригувалися плацебо (на рівні із силденафілом), що може підтверджувати психологічний характер проблеми.
У США бісопрололу фумарат застосовується вже понад 20 років. За даними американської електронної системи охорони здоров’я, ЕД становила лише 0,21% побічних явищ серед пацієнтів, які приймали цей препарат. Слід зауважити, що найчастіше ЕД спостерігалася в осіб віком ≥65 років, у яких статева функція може бути порушена і внаслідок низки інших причин.
Продовжуючи лекцію, О.М. Барна нагадала слухачам, що вимірювання АТ завжди має супроводжуватися вимірюванням ЧСС, оскільки ЧСС є незалежним прогностичним фактором ССЗ і фатальних подій при АГ. При високій ЧСС, яка є ознакою симпатичного овердрайву, рекомендовано призначати БАБ як першу лінію антигіпертензивної терапії у вигляді монотерапії або в поєднанні з іншими препаратами для зниження АТ. Рекомендації Європейського товариства кардіологів / Європейського товариства гіпертензії (2018) вказують, що БАБ можуть застосовуватися для початкової та підтримувальної антигіпертензивної терапії як препарат першої лінії.
БАБ представлено і в інших європейських рекомендаціях. Так, рекомендації Національного інституту вдосконалення медичної допомоги Великої Британії (NICE) наголошують, що БАБ показані для початкової терапії особам молодого віку з АГ та ознаками підвищеної симпатичної активності, а також жінкам дітородного віку і пацієнтам з протипоказаннями до прийому інших класів антигіпертензивних препаратів (АГП).
Блокада β1-адренорецепторів може виявитися особливо ефективною в пацієнтів з АГ та ожирінням за центральним типом або ЦД чи інсулінорезистентністю. Перевагами такої блокади є зменшення ймовірності розвитку шлуночкових аритмій, запобігання підвищенню АТ, у тому числі в нічний час, профілактика підвищення внутрішньоклубочкового тиску та розвитку нефропатії. 20-річне проспективне спостереження під час британського дослідження UKPDS виявило, що БАБ на 23% знижують смертність у пацієнтів із надлишковою вагою / ожирінням, ЦД 2 типу та високим ризиком розвитку АГ порівняно з інгібіторами ангіотензинперетворювального ферменту.
Говорячи про переваги БАБ, маються на увазі селективні препарати, передусім бісопролол. Селективність бісопрололу перевищує показники атенололу та бетаксололу більше ніж удвічі, а показник метопрололу – майже вчетверо. Така висока селективність забезпечує бісопрололу відмінний профіль безпеки.
Бісопролол ефективний не лише в молодих пацієнтів. За даними рандомізованого подвійного сліпого дослідження ADLIB, бісопролол виявився найефективнішим АГП у чоловіків віком 28-55 років із діастолічною АГ порівняно з амлодипіном, доксазозином, лізиноприлом і бендрофлюазидом. Перевагу бісопрололу над іншими засобами (лосартан, амлодипін, гідрохлортіазид) було підтверджено й у дослідженні GENRES, у якому оцінювали 24-годинний контроль АТ у чоловіків віком 35-60 років. Порівняння різних БАБ та АГП інших класів виявило, що бісопролол (Конкор® виробництва Мерк КГаА, Німеччина) забезпечував кращу 15-річну виживаність порівняно з небівололом та іншими БАБ, а також порівняно з іншими АГП (Sabido M. et al., 2018).
Окрім збільшення ризику смерті від кардіоваскулярних причин симпатичний овердрайв також підтримує хибне коло між коронавірусною хворобою (COVID-19) та супутніми захворюваннями, сприяючи ушкодженню серця, судин, легень й імунної системи. Це стосується як гострого періоду COVID-19, так і постковідного синдрому. За даними М.В. Шестакової та співавт. (2020), терапія БАБ знижувала ймовірність смерті від COVID-19 на 74%, тому в жодному разі не слід відміняти БАБ у пацієнтів з коронавірусною хворобою.
Від симпатичного овердрайву страждають не лише пацієнти з АГ, а й хворі на ІХС, у яких на фоні гіперактивації симпатичної нервової системи зростає ймовірність серцево-судинних подій. Ретроспективний аналіз даних дослідження TNT, у якому брали участь 9580 пацієнтів зі стабільною ІХС, продемонстрував, що симпатичний овердрайв підвищує ймовірність значних серцево-судинних подій у цього контингенту хворих. Зростання ЧСС на кожні 10 ударів вище за показник 70 уд./хв супроводжувалося збільшенням ризику значних серцево-судинних подій на 8% (Ho J.E. et al., 2010). Застосування бісопрололу в пацієнтів зі стабільною стенокардією зменшувало кількість епізодів ішемії, загальний тягар ішемії та кількість стенокардитичних нападів, що свідчить про потужний протиішемічний вплив цього препарату. На відміну від ніфедипіну, бісопролол дозволяє нівелювати ранкові та вечірні піки ішемічних епізодів, стабілізуючи стан пацієнтів з ІХС протягом усієї доби. Дослідження TIBBS довело, що бісопролол (Конкор®) покращує довгостроковий прогноз у пацієнтів з ІХС, сприяючи подовженню тривалості життя: через 400 днів спостереження частка кардіоваскулярних подій у групі бісопрололу становила 22,1%, натомість у групі ніфедипіну – 33,1% (р=0,03).
Таким чином, призначення бісопрололу є доцільним і при АГ, і при ІХС. У всіх цих пацієнтів необхідно виявляти симпатичний овердрайв і коригувати його за допомогою БАБ. Перевагу варто віддавати бісопрололу як препарату з високою селективністю та найкращим впливом на виживаність.
Наприкінці лекції професор Ю.М. Сіренко зауважив, що хворим високого ризику та пацієнтам, які прагнуть ефективного лікування, доцільно призначати брендові препарати, а не генерики. Нерідко за підозри на резистентну АГ або при стійкій тахікардії варто замінити генеричний препарат бісопрололу на брендовий Конкор®, й одразу спостерігається відмінний результат.
Підготувала Лариса Стрільчук
UA-CONC-PUB-062021-053
UA-CONCO-00007
Медична газета «Здоров’я України 21 сторіччя» № 10 (503), 2021 р.