25 вересня, 2021
Ключові аспекти самодопомоги при лікуванні пацієнтів із серцевою недостатністю
Самодопомога має важливе значення при довгостроковому лікуванні пацієнтів із хронічною серцевою недостатністю (СН). Асоціація серцевої недостатності (HFA) Європейського товариства кардіологів (ESC) цьогоріч розробила оновлені практичні рекомендації на допомогу клініцистам при веденні хворих на СН, в яких підкреслено невід’ємну роль інформування пацієнтів щодо дотримання режиму лікування, здорового способу життя, моніторингу симптомів тощо. Самодопомога сприяє покращенню якості життя пацієнтів, зниженню частоти повторних госпіталізацій та рівня смертності. Пропонуємо до вашої уваги основні положення цього документа, розміщеного у European Journal of Heart Failure (2021; 23: 157‑174).
Впровадження міждисциплінарних програм лікування, спрямованих на поліпшення самодопомоги осіб із СН, значно зменшило кількість випадків СН та госпіталізації від усіх причин. Це підтверджено метааналізом даних 5624 хворих на СН із 20 досліджень, в якому було виявлено сприятливий ефект самодопомоги під час поступлення до лікарні з приводу СН та підвищення якості життя пацієнтів, а також зниження частоти госпіталізацій і летальних випадків за будь-яких причин (McAlister et al., 2004).
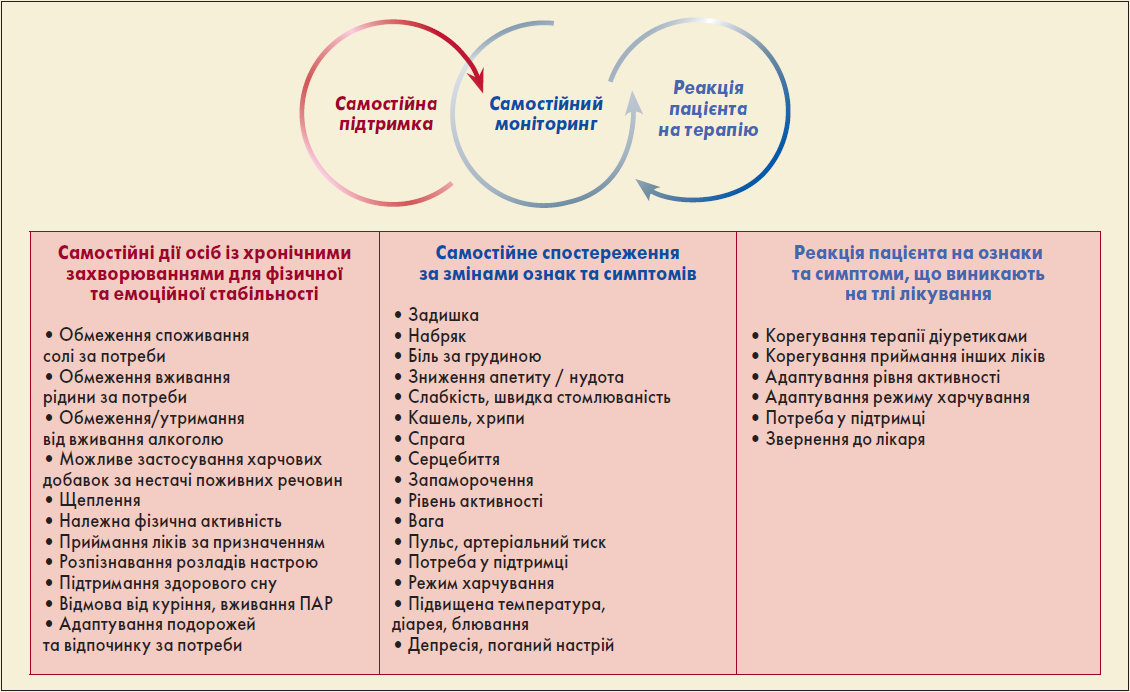
Через недостатнє розуміння проблеми, хибні уявлення та брак знань самодопомога в осіб із СН є недостатньою, тож їхнє інформування та навчання життєво важливі (Riegel et al., 2019). Самодопомога – це всеосяжна концепція, що складається із трьох ключових аспектів, як-то:
- самостійна підтримка (наприклад, приймання або корегування призначених ліків, фізична активність, дотримання здорового харчування);
- самостійний моніторинг стану (регулярне зважування тощо);
- реакція хворого на терапію (наприклад, зміна дози діуретика при виникненні симптомів) (рисунок).
Рисунок. Основні аспекти самодопомоги
Примітка: ПАР – психоактивні речовини.
Пацієнтам із СН можуть знадобитися регулювання та адаптація самодопомоги залежно від перебігу захворювання, наприклад, у періоди погіршення стану, при розвитку супутніх патологій або якщо потрібна оптимізація терапії. Слід зауважити, що наразі у всьому світі триває боротьба з інфекцією SARS-CoV‑2, що призвело до соціальної ізоляції та суспільного дистанціювання, а також значною мірою вплинуло на осіб із СН. За цих обставин самодопомога, моніторинг та лікування мають ще важливіше значення, ніж зазвичай, для підтримання стабільності та уникнення погіршення СН.
Самодопомога для підтримання стабільної СН
Оптимізація харчування
Контроль маси тіла. Зайва вага пов’язана з погіршенням ознак та симптомів будь-якого типу СН, збільшенням маси лівого шлуночка та його деформацією. У пацієнтів, які страждають на ожиріння, може бути доцільною баріатрична операція для досягнення щонайменше 10% втрати ваги та позитивного ремоделювання лівого шлуночка (Mahajan et al., 2020; Vest et al., 2019). Існують обмежені дані щодо прогнозу осіб із СН та ожирінням, що мають індекс маси тіла (ІМТ) ≥40 кг/м2. Однак ця категорія пацієнтів, ймовірно, має гірші клінічні результати. Тож для даної підгрупи хворих значна втрата ваги важлива і пов’язана зі зниженням основних ризиків для здоров’я (Nagarajan et al., 2013).
Кахексія асоційована з поганим прогнозом і розвитком термінальної стадії СН. Вона пов’язана із застійними явищами, запаленнями, мальабсорбцією, нейрогормональною гіперактивацією та, як наслідок, зростанням рівня смертності в осіб із СН (Valentova et al., 2016). Кахексія визначається як ненавмисна втрата ваги без набряків на >7,5% за 6‑12 місяців, або ІМТ <20 кг/м2 за наявності ознак саркопенії, виснаження та аномальних біохімічних параметрів (Evans et al., 2008). Такі пацієнти повинні бути уважно обстежені фахівцями із СН, отримувати оптимізоване лікування, рекомендації щодо фізичних вправ та дієтичну підтримку.
Вживання рідини й солі. Відповідно до рекомендацій, пацієнти мають обмежити споживання рідини до 1,5‑2 л при тяжкій СН для полегшення симптомів і збільшити (та/або зменшити приймання діуретиків) – у спекотну й вологу погоду або при втраті рідини (Ponikowski et al., 2016; Yancy et al., 2018). Вагомі докази переваг обмеження споживання солі при СН відсутні. Однак, згідно з критеріями Нью-Йоркської асоціації серця (NYHA), при СН III‑IV функціонального класу (ФК) вживання >3 г солі на день корелює з підвищеним ризиком госпіталізацій та смерті (Song et al., 2016; Lennie et al., 2011). В інших же джерелах зазначено, що обмеження натрію пов’язане зі збільшенням імовірності госпіталізації з приводу СН (Doukky et al., 2016). За рекомендаціями Всесвітньої організації охорони здоров’я, строге обмеження споживання солі недоцільне; адекватне споживання солі в популяції становить <5 г/добу.
Споживання алкоголю. Взаємозв’язок між прийманням алкоголю та серцево-судинними захворюваннями (ССЗ) досі є суперечливим незважаючи на те, що база доказів загальної шкоди зростає (Piepoli et al., 2020). Як відомо, вживання алкоголю, особливо надмірне, асоційоване з надшлуночковими аритміями, переважно пароксизмальною фібриляцією передсердь, що може прискорити або погіршити ознаки/симптоми СН. Утримання від його споживання може зменшити тягар аритмії в осіб із СН (Cardiol, 2015). Вживання алкоголю в дозах, що перевищують рекомендовані (2 Од./добу для чоловіків і 1 Од./добу для жінок) призводить до розвитку СН. При СН, що пов’язана з алкоголем, необхідно повністю від нього утримуватися; якщо цього вдається досягти, спостерігається значне клінічне поліпшення стану хворих на СН (Yancy et al., 2013).
Поживні речовини, харчові та вітамінні добавки. У настановах запропоновано перевіряти рівень заліза (феритину і сатурації трансферину) для визначення етіології СН (перевантаження залізом) та доцільності приймання добавок заліза. Було виявлено, що внутрішньовенне введення заліза покращує якість життя пацієнтів, пікове споживання кисню та здатність до фізичних навантажень, а також знижує частоту повторних госпіталізацій із приводу СН (Seferovic et al., 2019; Zhang et al., 2019). Наразі тривають рандомізовані контрольовані дослідження впливу застосування заліза внутрішньовенно на госпіталізацію та смертність (Mordi et al., 2018).
Гіперкаліємія зустрічається приблизно у 40% пацієнтів із хронічною СН. Вона зумовлює гірші клінічні результати, підвищення частоти госпіталізацій та летальних випадків серед хворих на СН. Гіперкаліємія може бути ятрогенною, спричиненою одночасним прийманням ліків та харчових/трав’яних добавок (Rosano et al., 2018). Дефіцит певних поживних речовин (наприклад, селену, коензиму Q10, цинку, заліза, білка, тіаміну) пов’язаний із розвитком СН (Cvetinovic et al., 2013). Хоча недостатнє споживання та низький рівень мікроелементів у плазмі крові пов’язані з несприятливими клінічними наслідками, доказів безпечного використання добавок при СН бракує (Vest et al., 2019).
Рекомендації. Пацієнтам та особам, які за ними доглядають, необхідно надати індивідуальні рекомендації залежно від споживання їжі та рідини, симптомів та поточного лікування. Тяжкохворих на СН із низькою якістю життя та зменшенням його тривалості не слід навантажувати радикальними змінами способу життя, які можуть мати обмежену користь.
В осіб із СН, що мають надмірну вагу, необхідний адаптований до особливостей хворого контроль маси тіла. Для пацієнтів із СН та кахексією важливо дотримуватися належних рекомендацій із харчування. Також хворим на СН слід оптимізувати споживання рідини та солі, а також розглянути доцільність використання додаткових мікроелементів.
Оптимізація фізичної активності
Фізичні вправи здатні покращити функціональні можливості, якість життя пацієнтів та зменшити кількість госпіталізацій (Piepoli et al., 2004). Відповідно до рекомендацій, пацієнтам із СН слід дотримуватися регулярних фізичних навантажень залежно від їхніх індивідуальних характеристик (Ponikowski et al., 2016; Yancy et al., 2013). Екстремальний атлетизм асоційований із певними несприятливими фенотипами СН, хоча прямий причинно-наслідковий зв’язок не встановлений (Dhutia, Sharma, 2015). Статеву активність можна відновлювати пацієнтам із СН I або II ФК за NYHA та тим, хто страждає на СН III чи IV ФК, якщо вони мають стабільний стан та отримують оптимальне лікування (Levine et al., 2012).
Рекомендації. Поради щодо фізичної активності мають враховувати уподобання, потреби та цінності пацієнтів, вік, супутні захворювання, звички та аспекти роботи, матеріальне положення тощо (Piepoli et al., 2011). Протоколи тренувань необхідно адаптувати до кожного пацієнта стосовно інтенсивності (аеробної та анаеробної), типу (витривалості, опору, сили), методу (безперервного й інтервального), застосування (системні, регіональні, дихальні м’язи), контролю (з/без нагляду) та місця виконання (лікарні / медичні центри, вдома) (Hansen et al., 2018). Зокрема, програми фізичних вправ мають бути індивідуальними для особливих груп пацієнтів із СН, таких як хворі на СН зі збереженою фракцією викиду (СНзбФВ), особи старечого віку, кахектичні чи слабкі. Роль телереабілітації щодо поліпшення фізичних можливостей у пацієнтів із СН зростає.
Пацієнтів із СН та проблемами з сексуальною активністю, стосунками слід переконати визнати їх та запропонувати фармакотерапію еректильної дисфункції або направити до спеціаліста за потреби. Варто інформувати хворих про особливості витрати енергії / толерантність до фізичних навантажень та зв’язок між сексуальними проблемами і СН.
Оптимізація прихильності до лікування
Причини недотримання режиму терапії є багатофакторними. Ефективні втручання включають покращення розуміння пацієнтами із СН переваг приймання ліків і самодопомоги, а також доступу та довіри до постачальника медичних послуг та системи охорони здоров’я загалом (Gast, Mathes, 2019). Хворі з поганим комплаєнсом мають значно вищі показники госпіталізації та декомпенсації СН (Fitzgerald et al., 2011). У рекомендаціях вказано на доцільність проведення навчання пацієнтів з особливим акцентом на важливість прихильності до лікування та самодопомоги (Ponikowski et al., 2016).
Депресія, слабкість та зниження когнітивних функцій – клінічні фактори, які можуть впливати на комплаєнс пацієнта (Vitale et al., 2019; Leslie et al., 2019). Члени сім’ї та особи, що здійснюють догляд, відіграють важливу роль у поліпшенні самодопомоги (Buck et al., 2018; Hooker et al., 2018).
Рекомендації. Необхідно ретельно оцінити можливість поліпрагмазії та обговорити пріоритети (виживання, якість життя, симптоми, побічні ефекти) із хворими та їх доглядальниками. У пацієнтів із супутніми захворюваннями слід оптимізувати лікування. При застосуванні препаратів із подібними фармакодинамічними властивостями перевагу варто віддавати лікам із цільовим дозуванням та доказовою базою, а не комбінованій терапії.
Лікарі мають надавати хворим інформацію про показання, дозування, користь, побічні ефекти препаратів та обговорити практичні питання, як-то оптимальний графік терапії, що робити у разі пропуску дози тощо. Фахівці з СН повинні розуміти, що на прихильність до лікування впливає кілька різних факторів, зокрема поліпрагмазія, пов’язана з коморбідними захворюваннями, використання декількох доз ліків на день, розуміння пацієнтом необхідності їх приймати, вік, когнітивні проблеми, залежність та погана соціальна підтримка (Leslie et al., 2019; Wu et al., 2013). За потреби можна залучити мультидисциплінарну команду до обговорення плану ведення осіб зі складними супутніми патологіями, наприклад психолога, лікаря загальної практики тощо.
Для поліпшення моніторингу та прихильності до лікування доцільно застосовувати сучасні підходи, як-то електронна охорона здоров’я.
Оптимізація психологічного статусу
Багато пацієнтів із симптомами СН (II‑IV ФК за NYHA) страждають на тривогу та депресію (Pattenden et al., 2007). Частка осіб із СН та депресивними симптомами під час госпіталізації зростає майже до 70% (Hare et al., 2014). Прояви депресії та тривоги можуть негативно впливати на інші види самодопомоги (наприклад, фізичну активність, прихильність до терапії), участь у прийнятті рішень та сімейну ситуацію (Müller-Tasch et al., 2018).
Депресія корелює з потенційними тяжкими симптомами, що призводять до підвищення частоти госпіталізацій і летальних випадків (Chioncel et al., 2017). Окрім того, вона пов’язана з підвищеною ризикованою поведінкою, поганим комплаєнсом хворих та соціальними проблемами (Biddle et al., 2020). Хороша психологічна підтримка важлива як для пацієнтів, так і їхніх сімей (Ponikowski et al., 2016). Систематичний огляд та метааналіз 19 рандомізованих контрольованих досліджень (n=3447) продемонстрували користь фізичних вправ для добробуту в таких хворих (Tu et al., 2014).
Антидепресанти безпечні для пацієнтів із СН та не пов’язані зі збільшенням смертності. Проте достатніх доказів того, що їх застосування сприяє значному зменшенню проявів депресії або кардіальних подій в осіб із СН, бракує (Rajeswaran et al., 2018; Sbolli et al., 2020). Втручання, такі як тай-чи, йога, медитація, релаксація та управління стресом, можуть покращити якість життя і психологічний статус хворих. Встановлено, що когнітивно-поведінкова терапія зменшує симптоми депресії у пацієнтів із СН (Peng et al., 2019; Freedland et al., 2015).
Рекомендації. У пацієнтів із СН може бути доцільним скринінг на наявність депресії та тривоги. Для точної оцінки психічного здоров’я та виявлення проблем слід розглянути використання опитувальників із самооцінкою. За згодою пацієнта можна залучити родину (Buck et al., 2015). Хворим необхідно регулярно надавати інформацію про захворювання, варіанти лікування та самодопомоги, мотивувати їх брати участь у нефармакологічних втручаннях тощо. У разі потреби слід направити пацієнта для отримання психологічної/психіатричної допомоги.
Оптимізація сну
Пацієнти із СН часто погано сплять через періоди перевантаження легеневою рідиною. Це призводить до розвитку ортопное, пароксизмальної нічної задишки та ніктурії (Pearse, Cowie, 2016). В осіб із СН психологічні проблеми (тривога, депресивний настрій) та ожиріння зазвичай асоційовані з безсонням. За даними досліджень, майже 75% таких хворих відзначають порушення та погану якість сну, 44% – неспокійний сон і 41% – труднощі із засипанням. Окрім того, 39% пацієнтів дуже рано прокидаються, а 32% не можуть знову заснути після раннього або короткого нічного пробудження (Jeon, Redeker, 2016; Al-Rawashdeh et al., 2017). Погана якість сну може впливати на здатність осіб із СН до адекватної самодопомоги (Spedale et al., 2020; Ryou et al., 2020).
Порушення дихання під час сну мають понад 50% пацієнтів із СН зі зниженою ФВ (СНзнФВ) (Pearse, Cowie, 2016). У міру збільшення виразності СН зростає поширеність дихання Чейна – Стокса з центральним апное уві сні (Cowie et al., 2015). Іншим основним типом розладу сну в осіб із СН є обструктивне апное уві сні (ОАС), яке частіше спостерігається у хворих, що страждають на надмірну вагу, цукровий діабет або мають велику окружність шиї, ретро- чи прогнатизм (Cowie et al., 2018). Також ОАС розглядають як одне з супутніх захворювань при СНзбФВ.
При СН та ОАС можна розглянути терапію методом створення постійного позитивного тиску (CPAP) із застосуванням маски. Існують певні докази того, що таке лікування ОАС у пацієнтів із СН може зменшити симптоми, поліпшити серцеву функцію, біомаркери ССЗ та якість життя, але дані щодо зниження рівня смертності не є переконливими (Pearse, Cowie, 2016). Хворі на СНзнФВ та переважно із центральним апное уві сні не повинні отримувати адаптивну сервовентиляцію, оскільки це може призвести до зростання частоти летальних випадків (Cowie et al., 2018).
Рекомендації. Проблеми зі сном у пацієнтів із СН слід оцінювати в межах комплексного клінічного обстеження. Зокрема, необхідно діагностувати основні причини їх розвитку, такі як перевантаження рідиною, ОАС або психологічні порушення (тривога, депресія), та призначити відповідні втручання. Варто мати на увазі, що безсоння може спричинити виникнення значних психічних та соматичних проблем зі здоров’ям в осіб із СН. Тому слід регулярно запитувати в них про характер і якість сну, а якщо порушення сну є, перевірити, чи наявна еуволемія. При виявленні депресії та тривоги за потреби доцільно направити пацієнта на консультацію до психолога/психіатра.
Якщо є підозра щодо наявності у пацієнта із СН порушення дихання під час сну, варто провести обстеження хворого під час сну, щоб підтвердити діагноз та тип апное. За наявності ОАС пацієнтові необхідно надати рекомендації щодо зниження/контролю ваги (за потреби) та наголосити на необхідності регулярного використання CPAP протягом щонайменше 6 год/добу.
Також доцільно розглянути й обговорити користь і шкідливу дію ліків для регулювання сну. Бензодіазепіни зазвичай не рекомендовані через можливість розвитку резистентності до лікування та залежності. У літніх осіб вони можуть погіршити когнітивні, моторні функції, навички водіння та підвищити ризик падінь. Антигістамінні препарати безпечні, але здатні викликати денну сонливість. Докази використання мелатоніну при СН відсутні. Зопіклон призначають частіше, адже він вважається безпечнішим, ніж бензодіазепіни (Sato et al., 2020; Manolis et al., 2021).
У пацієнтів із СН ефекти та віддалені клінічні наслідки застосування ліків для сну мають бути додатково вивчені. Також більшу увагу в таких хворих слід приділяти детермінантам якості сну та асоціаціям із супутніми патологіями. Взаємодія якості сну в осіб із СН та здатності до самодопомоги потребує прискіпливішого розгляду.
Імунізація та профілактика інфекцій
Грипозна інфекція є важливим тригером серцево-судинних подій (Clar et al., 2015). Пацієнти із СН є вразливими до розвитку вірусних інфекцій (наприклад, COVID‑19). Вакцинація проти вірусних інфекцій пов’язана зі значним зниженням ризику смерті від усіх причин у хворих на СН, що було нещодавно показано згідно з даними метааналізу за участю 179 158 пацієнтів, який включав осіб із СН (Rodrigues et al., 2020). Відповідно до рекомендацій, доцільно проводити щорічну імунізацію проти грипу та одноразову вакцинацію проти пневмококової інфекції (Ponikowski et al., 2016).
Рекомендації. Слід обговорити із хворими на СН переваги та можливі ризики, пов’язані з вакцинацією. Окрім того, варто розглянути застосування оптимальних втручань для захисту пацієнтів із СН від інфекцій та їх ускладнень.
Утримання від куріння та вживання психоактивних речовин
У настановах йдеться про необхідність отримання пацієнтами із СН консультації щодо відмови від куріння та вживання психоактивних речовин (ПАР) (Yancy et al., 2017). Використання електронних сигарет не рекомендоване, оскільки існує значно вищий ризик розвитку ССЗ серед користувачів електронних та звичайних сигарет порівняно з лише тютюнокурінням (Bhatnagar et al., 2019). При застосуванні кальяну курці піддаються значно вищому рівню важких і токсичних поліциклічних ароматичних вуглеводнів, ніж при курінні цигарок, а також токсичних речовин для кардіореспіраторної системи, як-то леткі органічні сполуки й важкі метали (кадмій, свинець), що можуть пошкодити кровоносні судини та мозок (Bhatnagar et al., 2019). Вживання ПАР, як-то кокаїн, амфетамін, екстазі, канабіс, псилоцибін, летючі речовини тощо, може викликати серйозні гострі зміни в роботі серцево-судинної системи, а також завдати незворотної шкоди серцю (Ghuran, Nolan, 2000).
Рекомендації. Незважаючи на те, що шкода куріння є очевидною, багато осіб із СН є активними курцями (13‑54%) (Reyes et al., 2016). До того ж на тлі зловживання ПАР часто виникають пов’язані з цим психосоціальні проблеми. Тож пацієнт-орієнтована консультація з наданням чітких та обґрунтованих рекомендацій щодо відмови від куріння і вживання ПАР є важливою (Pipe et al., 2011). Доцільно розглянути направлення хворого для отримання психологічної підтримки або когнітивно-поведінкової терапії, якщо він хоче кинути курити або приймати ПАР.
При розгляді практики відмови від куріння доцільним може бути призначення затверджених методів фармакотерапії, як-то нікотинозамінна терапія (бупропіон, вареніклін), з моніторингом серцево-судинних побічних ефектів та медикаментозної взаємодії з препаратами для лікування ССЗ. Пацієнта із СН необхідно поінформувати, що вживання ПАР та куріння виключають можливість трансплантації серця.
Моніторинг змін у межах самодопомоги
Погіршення СН або поява нових симптомів може суттєво впливати на якість життя пацієнтів та мати руйнівні негативні наслідки. Ефект самодопомоги вивчали у багатьох дослідженнях, але конкретно самомоніторинг – у жодному (Jonkman et al., 2016; Jonkman et al., 2016). Моніторинг має включати відстеження ознак та симптомів СН, супутніх захворювань та побічних ефектів ліків (Mentz et al., 2014).
Моніторинг симптомів
Відповідно до рекомендацій, моніторинг ознак та симптомів СН є невід’ємною частиною самодопомоги. Раннє виявлення погіршення симптомів СН важливе для запобігання госпіталізації та зниження смертності серед хворих. Моніторинг можуть здійснювати клініцисти або пацієнти шляхом дистанційного контролю (з/без імплантованих пристроїв), включно зі структурованою підтримкою за допомогою телефону (Ponikowski et al., 2016).
Оцінку самодопомоги у пацієнтів із СН можна проводити шляхом застосування європейської шкали поведінки на тлі самодопомоги при серцевій недостатності (EHFScBS) або переглянутого індексу самодопомоги при серцевій недостатності (SCHFI) (Sedlar et al., 2017; Riegel et al., 2019). Ці надійні та доступні інструменти використовують як у наукових дослідженнях, так і у клінічній практиці для навчання хворих.
Клінічні переваги дистанційного моніторингу підтверджено за даними кількох метааналізів (Eurlings et al., 2019). У дослідженні TIM-HF2 було продемонстроване поліпшення прогнозу в осіб із СН у контексті цілодобової системи підтримки (Eurlings et al., 2019). Моніторинг за допомогою імплантованих пристроїв може покращити результати (Koehler et al., 2018).
Рекомендації. Пацієнти мають пройти навчання з моніторингу симптомів СН та обговорити з лікарем план лікування. Самоконтроль пацієнтами симптомів протягом життя може здійснюватися різними способами залежно від уподобань хворого та наявності ресурсів. Поточна пандемія COVID‑19 змусила зосередитися на дистанційному моніторингу. Телемоніторинг можна розглядати як актуальний варіант підтримки пацієнтів у здійсненні самоконтролю.
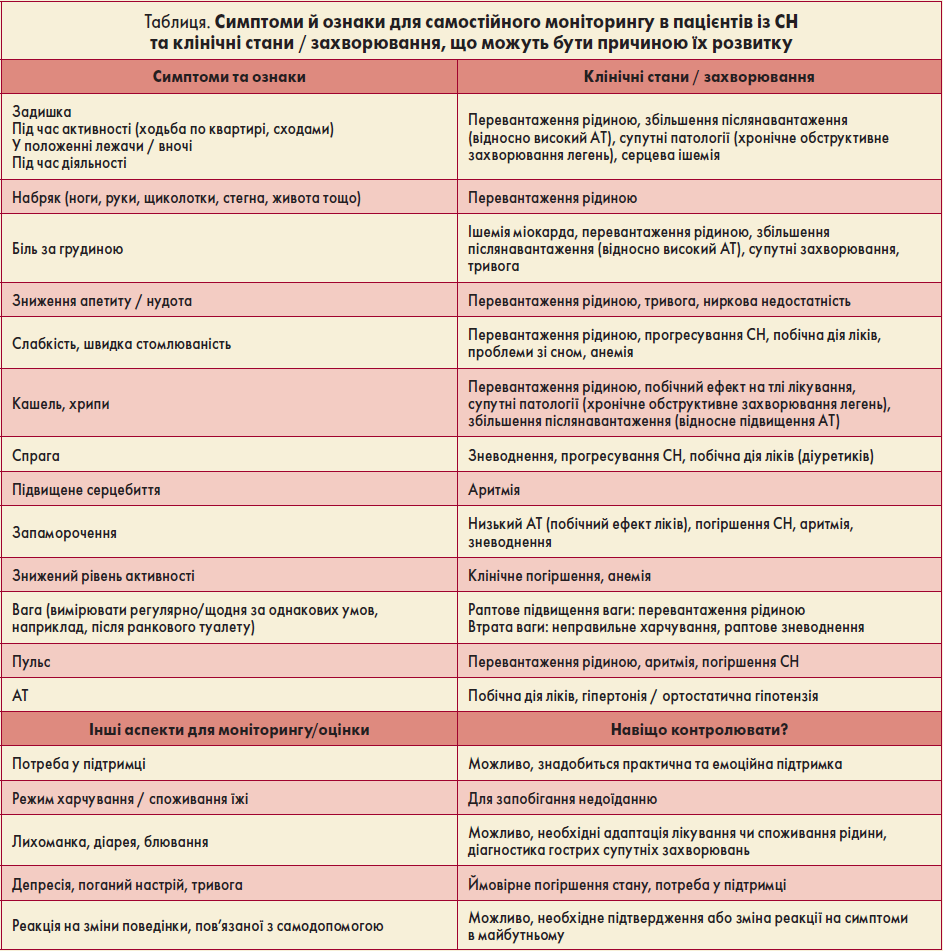
Частота моніторингу залежить від клінічного стану пацієнтів та стабільності хвороби. Моніторинг симптомів слід виконувати щонайменше кожні шість місяців для осіб зі стабільною СН (NICE, 2020). Симптоми й ознаки для самостійного моніторингу в пацієнтів із СН та клінічні стани / захворювання, що можуть бути причиною їх розвитку, наведені в таблиці.
Контроль побічних ефектів та ускладнень
Побічні ефекти ліків при СН зафіксовані у 10% у клінічних випробувань та 17‑22% – обсерваційних (Wirta et al., 2018). Несприятливі явища зазвичай призводять до недотримання режиму терапії СН, але близько третини пацієнтів, які їх мають, не повідомляють про це лікарям (De Smedt et al., 2009). Як хворим, так і клініцистам нерідко буває важко відокремити симптоми захворювання від побічних ефектів лікарських засобів (Rogers et al., 2002).
У рекомендаціях із СН зазначено важливість надання пацієнтам вичерпної інформації про поширені побічні явища препаратів для лікування СН (Ponikowski et al., 2016; Yancy et al., 2018). Також слід повідомити хворим про необхідність вчасного інформування лікаря про симптоми, пов’язані з препаратами.
Занепокоєння щодо гіпотензії, спричиненої терапією, часто є безпричинно надмірною як серед пацієнтів із СН, так і лікарів. Важливо, що асимптоматична АГ не є підставою для зменшення приймання ліків або уникнення титрування дози вгору в осіб із СНзнФВ. Є дані, що інтенсивний контроль АТ у літніх осіб порівняно зі стандартним лікуванням не посилює ортостатичну АГ і не підвищує ризик травматичних падінь (Williamson et al., 2016).
Початкові дані щодо використання інструментів електронної охорони здоров’я для самоконтролю пацієнтів свідчать про значне збільшення позитивних змін у прийманні ліків. Однак доказів на підтвердження їх ефективності для виявлення побічних ефектів або підвищення задоволеності хворих досі бракує (Lancaster et al., 2018).
Зниження функції нирок часто вважають побічною реакцією при застосуванні інгібіторів ренін-ангіотензин-альдостеронової системи у хворих на СНзнФВ. Проте сучасні дані свідчать, що, незважаючи на погіршення функції нирок, зниження рівня смертності на тлі лікування зберігається (Mullens et al., 2020).
Рекомендації. Майже половина пацієнтів із СН вважають побічні дії ліків серйозною проблемою, спричиненою захворюванням. Чіткі рекомендації лікаря з обґрунтуванням необхідності терапії, можливості внесення в неї змін та спільного прийняття рішень допоможуть запобігти розвитку несприятливих явищ. Лікування СН слід починати препаратами у низьких дозах та збільшувати поступово.
У разі виникнення побічних ефектів слід відкорегувати режим лікування, пояснити пацієнтові причини їх розвитку та надати рекомендації щодо усунення цих проблем. При набряку губ або горла хворому потрібно наголосити негайно звернутися по медичну допомогу. Також для пацієнтів із СН доцільно провести консультацію щодо того, як знизити ризик падінь.
Необхідно виключити застій у легенях та печію як причину кашлю, перш ніж припиняти приймання інгібіторів ангіотензинперетворювального ферменту. Крім того, хворим слід рекомендувати не пропускати терапію діуретиками, навіть коли вони знаходяться далеко від дому, але заохочувати вибирати оптимальний час приймання.
Доцільно порадити пацієнтам письмово фіксувати історію побічних ефектів. Важливо розробити стратегії запобігання та/або зниження частоти побічних ефектів, пов’язаних із застосуванням ліків, для довгострокової перспективи.
Рекомендації з лікування залежно від поведінки й стану хворих
Відповідно до рекомендацій, у пацієнтів із СН з ознаками та/або симптомами застійних явищ доцільно застосовувати діуретики для зменшення симптомів, збільшення фізичних навантажень і зниження ризику госпіталізації (Ponikowski et al., 2016). Гнучкий та індивідуалізований режим дозування діуретиків може покращити якість життя хворих та зменшити кількість госпіталізацій в осіб із СНзнФВ (Piano et al., 2011). Незважаючи на те, що рекомендовано використовувати діуретики у найменшій дозі та, за можливості, відмінити приймання петльових діуретиків, сучасних даних щодо припинення такої терапії у пацієнтів із СН небагато (Martens et al., 2018; Sica et al., 2018). Як відомо, корегування лікування діуретиками (частіше збільшення дози) може покращити клінічні результати (Abraham et al., 2016).
Через зміни стану пацієнтів (на тлі СН чи пов’язані з іншими причинами), може знадобитися корегування схеми лікування, зниження фізичної активності або зміна (тимчасова) споживання солі чи рідини.
Метою терапії діуретиками є досягнення та підтримання еуволемії за допомогою найменшої ефективної дози. Дозування цих препаратів необхідно з часом корегувати залежно від індивідуальних особливостей хворих. Гнучкий графік дозування діуретиків, що ґрунтується на конкретних ознаках та симптомах пацієнта із хронічною СН, є безпечним. В окремих осіб з еуволемією/гіповолемією застосування діуретиків може бути (тимчасово) припинене.
У пацієнтів із виразною генералізованою гіперемією, особливо за наявності набряку слизової кишечника, вплив фуросеміду при пероральному застосуванні може змінюватися через недостатню абсорбцію у шлунково-кишковому тракті. Рекомендовано перейти на інший діуретик або внутрішньовенне введення фуросеміду з метою збільшення діурезу, зменшення загальної непрохідності та набряку слизової кишечника й відновлення абсорбції пероральних діуретиків у шлунково-кишковому тракті.
Інгібітори ренін-ангіотензин-альдостеронової системи та діуретики в осіб із виразною гіповолемією значно підвищують ризик гострого ураження нирок та/або гіперкаліємії. Можливо, слід тимчасово припинити лікування або зменшити дозування до нормалізації стану хворих.
Висновки
Самодопомога є дуже важливою для покращення результатів лікування осіб із СН, зокрема якості життя, зниження частоти госпіталізацій та смертності. Однак багатьом пацієнтам важко дотримуватися рекомендацій щодо самодопомоги, ймовірно, через брак мотивації, здібностей чи підтримки. Медичні працівники відіграють важливу роль в інформуванні хворих, навчанні навичкам, адаптації даних та взаємодії з пацієнтами для прийняття спільних рішень. Самодопомога не означає, що пацієнт має робити все сам. Члени родини, друзі чи доглядальники можуть бути залучені залежно від бажання та можливостей хворого до всіх аспектів самодопомоги (підтримка, моніторинг та лікування).
Підготувала Олена Коробка