2 травня, 2022
Пероральне і місцеве лікування больової форми діабетичної полінейропатії
Резюме оновлених практичних рекомендацій Американської академії неврології
Цукровий діабет (ЦД) – найпоширеніша причина периферичної нейропатії (ПН), відповідальна за 32-53% випадків захворювання [1-4]. Больова форма діабетичної нейропатії (БДН) спостерігається в більш як 16% пацієнтів із ЦД. Треба зазначити, що цей симптом для лікарів не завжди є приводом для обговорення з пацієнтами, тому біль часто залишається нелікованим [5]. БДН, навіть у порівнянні з безбольовою формою нейропатії, негативно впливає на фізичний і психічний аспекти якості життя хворих [6].
Велике національне репрезентативне дослідження показників надання медичної допомоги показало, що для лікування болю, пов’язаного з ПН, найчастіше призначають опіоїди, за якими слідують габапентин, прегабалін, дулоксетин, амітриптилін і венлафаксин [7].
Лікарі продовжують широко використовувати опіоїди в пацієнтів із БДН, незважаючи на позицію Американської академії неврології (AAN) та настанови Центрів з контролю та профілактики захворювань (Centers for Disease Control and Prevention, CDC), що рекомендують з обережністю застосовувати опіоїди особам із хронічним нераковим болем [8, 9]. За даними CDC, смертність від передозування опіоїдами зросла під час пандемії, що підкреслює важливість належного призначення цих засобів [10]. Для оцінки результатів великої кількості нових рандомізованих контрольованих досліджень (РКД), які вивчали різні підходи до лікування болю в пацієнтів із БДН, і висвітлення альтернатив опіоїдів у цій популяції був проведений метааналіз РКД, де оцінювали ефективність окремих ліків, а також класів препаратів, які зазвичай використовують із цією метою. На основі результатів метааналізу були оновлені рекомендації AAN 2011 року щодо лікування БДН [11]. Крім того, дослідники мали на меті оцінити вплив на БДН різних класів ліків, тоді як більшість попередніх рекомендацій і систематичних оглядів були зосереджені виключно на окремих препаратах [11-14]. Розуміння того, чи однаково препарати одного класу зменшують больовий синдром, впливає на вибір оптимального лікування цього поширеного стану; крім того, такий фактор, як вартість, доводиться часто враховувати під час вибору між знеболювальними препаратами одного класу та вирішення, на які засоби перейти після невдалого лікування.
Ця настанова має на меті відповісти на запитання щодо ефективності застосування пероральних або місцевих фармакологічних засобів для зменшення болю, проти плацебо або активного препарату порівняння, в осіб із БДН.
Опис аналітичного процесу
У листопаді 2017 року Підкомітет із настанов (GS) AAN скликав групу клініцистів, які спеціалізуються на лікуванні БДН. У групу увійшли спеціалісти з інформаційного наповнення, методології, члени AAN GS і захисники інтересів / представники пацієнтів. Тих осіб, чия участь могла супроводжуватися фінансовим конфліктом або чия професійна та інтелектуальна упередженість знизила б довіру до результатів огляду, було виключено.
Для оцінки ми заздалегідь визначили 5 класів пероральних препаратів:
- габапентиноїди (габапентин і прегабалін);
- інгібітори зворотного захоплення серотоніну-норадреналіну (ІЗЗСН; дулоксетин, венлафаксин і десвенлафаксин);
- трициклічні антидепресанти (ТЦА; амітриптилін, нортриптилін, іміпрамін);
- блокатори натрієвих каналів (БНК; карбамазепін, окскарбазепін, ламотриджин, вальпроєва кислота, лакосамід);
- засоби з подвійним механізмом дії (ІЗЗСН/опіоїди; трамадол і тапентадол).
На основі систематичного аналізу даних комісія обґрунтувала рекомендації та сформулювала принципи надання медичної допомоги.
Аналіз доказів
Нижче наведено резюме проведеного аналізу. Повний текст оновлених рекомендацій, у тому числі більш детальний опис аналітичного процесу, можна переглянути за посиланням aan.com/Guidelines/home/GuidelineDetail/1038.
Пероральні засоби
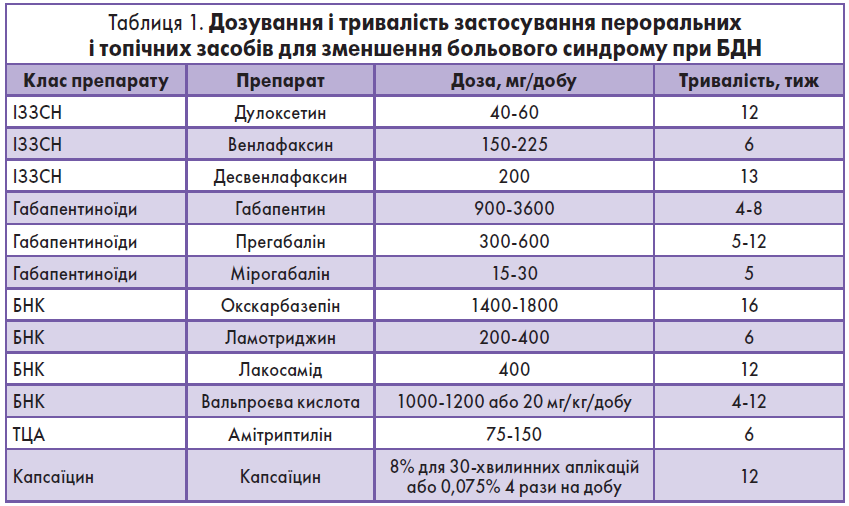
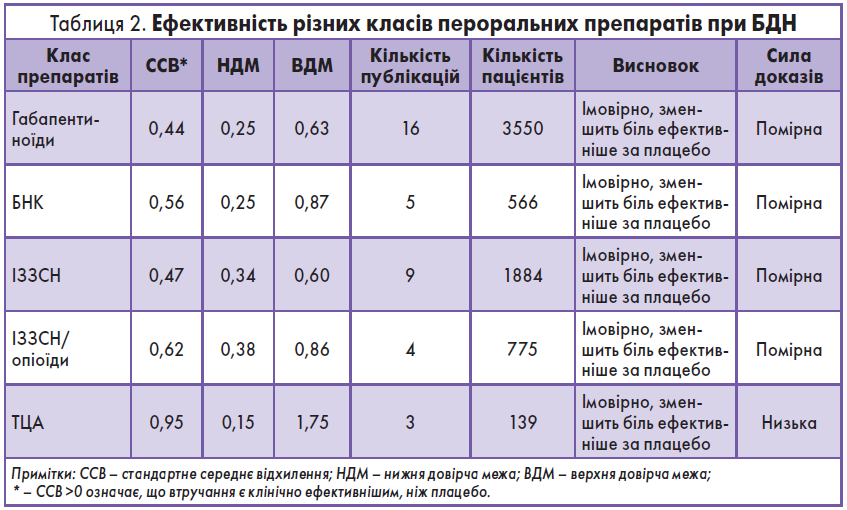
Інформація про дози, тривалість застосування і ефективність окремих класів препаратів щодо зменшення болю при ДПН проти плацебо або активного препарату порівняння відображена в таблицях 1 і 2.
Топічні препарати
Капсаїцин, імовірно, зменшує біль ефективніше за плацебо (ССВ 0,30; 95% ДІ 0,14-0,47; незначний ефект, низька сила доказів; 1 дослідження класу I із 8% і 1 дослідження класу II з 0,075% капсаїцином).
Пластир Nitrosense, імовірно, зменшує біль ефективніше за плацебо (ССВ 0,59; 95% ДІ 0,14-0,47; середній ефект, низька сила доказів; 1 дослідження класу II).
Citrullus colocynthis, імовірно, зменшує біль ефективніше за плацебо (ССВ 0,91; 95% ДІ 0,36-1,45; значний ефект, низька сила доказів; 1 дослідження класу II).
Спрей гліцерилтринітрату, імовірно, зменшує біль ефективніше за плацебо (ССВ 1,19; 95% ДІ 0,55-1,83; значний ефект, низька сила доказів; 1 дослідження класу II).
Топічний клонідин, імовірно, зменшує біль не більше, ніж плацебо (ССВ 0,29; 95% ДІ від -0,01 до 0,58); низька сила доказів; 1 дослідження класу II).
Трансдермальні пластирі з бупренорфіном, імовірно, зменшують біль не більше, ніж плацебо (ССВ 0,23; 95% ДІ від -0,09 до 0,55); низька сила доказів; 1 дослідження класу II).
Практичні рекомендації
Обґрунтування рекомендації 1. БДН є поширеним ускладненням ЦД і частіше спостерігається в пацієнтів із більшою тривалістю діабету і поганим глікемічним контролем [34-36]. Хворих на ЦД потрібно періодично обстежувати на наявність ПН та нейропатичного болю, хоча оптимальна частота такої оцінки не встановлена. Більшість досліджень, які вивчали ефективність лікування БДН, оцінювали вираженість болю за допомогою візуальних аналогових шкал (ВАШ), числових рейтингових шкал або подібних засобів. Такі шкали зазвичай використовують у клінічній практиці, але вони не дають уявлення про вплив болю на функціонування і самопочуття пацієнтів. Інші шкали, які оцінюють вплив болю на функціонування (Короткий опитувальник оцінки вираженості болю при БДН) [37] або якість життя (Норфолкський опитувальник для оцінки якості життя при ДПН) [38], можуть надати вагомішу інформацію для оцінки необхідності лікування та його успішності.
Рекомендація 1
Лікарі мають оцінювати пацієнтів із ЦД на предмет периферичного нейропатичного болю та його впливу на функції та якість життя цих пацієнтів (рівень B).
Обґрунтування рекомендації 2. Продемонстровано, що кілька класів фармакологічних препаратів зменшують біль у пацієнтів із БДН. Однак досягти повного усунення симптомів часто не вдається. Пацієнти очікують вираженого полегшення болю, а багато хто – його повного усунення [39]. Для збільшення задоволеності пацієнтів варто узгодити їх очікування з реальною ефективністю втручань (у клінічних дослідженнях вважається успіхом зменшення болю приблизно на 30%).
Рекомендація 2
Розпочинаючи фармакологічні втручання при БДН, клініцисти мають пояснити пацієнтам, що метою лікування є зменшення, а не повне усунення болю (рівень B).
Обґрунтування рекомендації 3. При лікуванні пацієнтів із БДН важливо оцінити інші фактори, які можуть впливати на сприйняття болю та якість життя. Пацієнти з ЦД частіше, ніж представники загальної популяції, мають розлади настрою (найчастіше великий депресивний розлад) і порушення сну (особливо обструктивне апное уві сні) [40, 41]. Настрій і сон можуть впливати на сприйняття болю [42, 43]. Тому одночасне лікування розладів настрою і сну може допомогти зменшити біль і покращити якість життя незалежно від безпосереднього лікування БДН. Деякі методи лікування БДН також можуть сприятливо впливати на настрій і сон (наприклад, TЦА і ІЗЗСН) і, відповідно, мати переваги завдяки цим механізмам.
Рекомендація 3
Клініцисти мають проводити скринінг із метою виявлення в пацієнтів із БДН супутніх розладів настрою та сну і лікувати їх належним чином (рівень B).
Обґрунтування рекомендації 4. БДН є дуже поширеним захворюванням, яке значуще впливає на якість життя [6]. Результати метааналізів продемонстрували докази ефективності щодо зменшення болю чотирьох класів пероральних препаратів: TЦА, ІЗЗСН, габапентиноїдів і БНК. Точніша оцінка сили ефекту та відповідних довірчих інтервалів виявила їх зіставність для всіх цих класів препаратів, що не дає можливості рекомендувати якийсь один засіб з огляду на його переваги над іншими.
Рекомендація 4
Для зменшення болю пацієнтам із БДН клініцисти мають призначати ТЦА, ІЗЗСН, габапентиноїди і/або БНК (рівень B).
Обґрунтування рекомендації 5. Деякі пацієнти віддають перевагу місцевим, нетрадиційним або нефармакологічним втручанням, тому важливо мати можливість запропонувати заходи, які відповідають цим уподобанням. Крім того, з огляду на негативні наслідки опіоїдної терапії [8, 9], необхідні варіанти ефективних неопіоїдних засобів для зменшення болю в пацієнтів, в яких початкове лікування виявилося неефективним. Було показано, що TЦA, ІЗЗСН, габапентиноїди і БНК зменшують вираженість болю в пацієнтів із БДН. Хоча інші заходи менш добре вивчені, принаймні 1 РКД підтримує використання інших втручань, таких як місцеві (капсаїцин, спрей гліцерилтринітрату, Citrullus colocynthis), нетрадиційні (гінкго білоба) і нефармакологічні засоби (фізичні вправи, когнітивно-поведінкова терапія – КПТ) [44]. Крім того, є послідовні помірні докази ефективності використання КПТ для лікування багатьох типів хронічного болю [45, 46]. І хоча досі немає переконливих прямих доказів ефективності КПТ при БДН, є багатообіцяючий успішний досвід використання КПТ в терапії деяких видів нейропатичного болю [47, 48].
Рекомендація 5a
Під час вибору одного з ефективних пероральних, місцевих, нетрадиційних і нефармакологічних втручань для лікування БДН клініцисти можуть ураховувати побажання пацієнтів (рівень C).
Рекомендація 5b
Пацієнтам, які віддають перевагу місцевим, нетрадиційним або нефармакологічним втручанням, можна запропонувати місцеві (капсаїцин, спрей гліцерилтринітрату, Citrullus colocynthis), нетрадиційні (гінкго білоба) або нефармакологічні втручання (КПТ, фізичні вправи, тайцзи) (рівень C).
Обґрунтування рекомендації 6. Окремі фармакологічні засоби з класів TЦA, ІЗЗСН, габапентиноїдів і БНК мають порівнянну ефективність щодо кінцевої точки вираженості нейропатичного болю. Проте є специфічні для класу і препарату відмінності в потенціалі виникнення та характері побічних реакцій. Наприклад, потенційні антихолінергічні побічні ефекти ТЦА можуть гірше переносити пацієнти із закрепами, затримкою сечі або ортостатичною гіпотензією. Аналогічно, такі потенційні побічні ефекти ІЗЗСН і БНК, як нудота, втома і запаморочення, можуть погано переносити пацієнти з уже наявними аналогічними симптомами. Узявши до уваги, що габапентиноїди здатні спричинювати периферичні набряки, ці ліки необхідно з обережністю застосовувати пацієнтам із периферичними набряками через наявність таких супутніх патологій, як захворювання серця, нирок або печінки. Потенційними побічними ефектами вальпроєвої кислоти є тератогенний вплив (дефекти нервової трубки), а також гепатотоксичність, панкреатит, гіпонатріємія і панцитопенія [49]. У разі використання багатьох із цих препаратів потрібне корегування дози відповідно до функції нирок, тому її необхідно дослідити перед призначенням лікування. Також потрібно обговорити вартість препарату і побажання пацієнта. Крім того, такі супутні захворювання, як депресія/тривога (ТЦА та ІЗЗСН) і судоми (габапентиноїди і БНК), можуть зробити призначення певних терапевтичних класів доцільнішим унаслідок наявності подвійних показань.
Рекомендація 6a
З огляду на порівнянну ефективність, під час вибору засобу для лікування БДН клініцисти мають ураховувати інші фактори, зокрема потенційні побічні ефекти, супутні захворювання пацієнта, вартість ліків та уподобання пацієнта (рівень B).
Рекомендація 6b
Лікарі не мають призначати вальпроєву кислоту пацієнтам репродуктивного віку з БДН (рівень B).
Рекомендація 6c
Зважуючи на потенційний ризик виникнення серйозних побічних ефектів, лікарі не мають призначати вальпроєву кислоту пацієнтам із БДН, якщо тільки всі інші ефективні препарати не принесли бажаного ефекту (рівень B).
Обґрунтування рекомендації 7. Можливо, для визначення лікування, найефективнішого для конкретного пацієнта з БДН, доведеться спробувати серію препаратів. Лікування варто вважати неефективним, якщо препарат достовірно не зменшив біль при використанні в тій самій дозі та з тією самою тривалістю терапії, яка продемонструвала ефективність у клінічних дослідженнях (табл. 1). Зазвичай тривалість лікування, що забезпечує ефективність, становить приблизно 12 тиж із діапазоном від 4 до 16 тиж. Якщо препарат спричиняє побічні ефекти, які переважають користь від зменшення нейропатичного болю, потрібно вважати, що пацієнт не переносить призначене лікування. Хоча кожен окремий препарат має специфічний профіль побічних ефектів, запаморочення, сонливість і втома можуть виникати на тлі використання будь-якого класу пероральних засобів, а реакції в місці застосування – будь-якого топічного препарату. Необхідно вважати, що метод лікування нейропатичного болю не працює в конкретного пацієнта, якщо цей метод виявився неефективним або погано переноситься через 12 тиж використання. Неефективність одного препарату не виключає хорошу відповідь без побічних ефектів при використанні альтернативного методу лікування того самого або іншого класу. Очікується, що вибір засобу з іншим механізмом дії (класу ліків) підвищить імовірність полегшення болю або дасть можливість уникнути побічних ефектів, які виникають під час первинного втручання. Якщо досягнуто лише часткової ефективності, додавання другого препарату іншого класу може забезпечити комбіновану ефективність, вищу за ту, що забезпечує кожен препарат окремо.
Рекомендація 7a
Лікарі мають пояснити пацієнтам із БДН, що, імовірно, потрібно буде спробувати декілька препаратів, щоб визначити найкорисніше для хворого лікування (рівень B).
Рекомендація 7b
Має вважатися невдалим індивідуальне втручання для зменшення нейропатичного болю, якщо застосування протягом приблизно 12 тиж ліків, дозу яких було титровано до тієї, що продемонструвала ефективність у дослідженнях, не призвело до клінічно значущого зменшення болю або коли побічні ефекти від ліків переважають будь-яку користь від зменшення вираженості нейропатичного болю (рівень B).
Рекомендація 7c
Якщо застосування початкового методу лікування не допомогло досягнути значного покращення або якщо виникають виражені побічні ефекти, клініцисти мають запропонувати пацієнтам ліки з іншого ефективного класу (рівень B).
Рекомендація 7d
Пацієнтам, які досягли часткового покращення при використанні початкового методу лікування, клініцисти мають запропонувати препарат з іншого ефективного класу або комбіновану терапію, додавши ліки з іншого ефективного класу (рівень B).
Обґрунтування рекомендації 8. Використання опіоїдів для лікування хронічного неракового болю категорично не рекомендується в позиційному документі, опублікованому AAN в 2014 році, і в систематичному огляді CDC, головним чином через слабкість або відсутність доказів довгострокової ефективності та ймовірність виникнення серйозних довгострокових несприятливих наслідків [8, 9]. Відсутність довгострокової ефективності в поєднанні з незадовільним профілем ризику була згодом описана в систематичному огляді NIH. У цьому дослідженні було зроблено висновок, що «доказів для підтвердження ефективності тривалої опіоїдної терапії для зменшення хронічного болю та поліпшення функції недостатньо. Докази підтверджують дозозалежний ризик серйозної шкоди» [50]. В однорічному дослідженні ефективності опіоїдів для лікування помірного або сильного болю при остеоартрозі поперекового відділу хребта, кульшового або колінного суглобів повідомлялось, що ефективність опіоїдів не перевершує таку неопіоїдних ліків [51]. Найважливішими довгостроковими несприятливими наслідками є залежність, розлади, пов’язані з вживанням опіоїдів, передозування і підвищення смертності [8, 9, 46, 52]. Дані CDC свідчать про те, що, імовірно, залежність може виникнути протягом кількох днів або тижнів використання [53]. У рандомізованих дослідженнях частота серйозних подій занижена через їх відносну рідкість, розширені методи залучення пацієнтів і коротку тривалість більшості цих досліджень. Хоча найсерйозніші побічні ефекти залежать від дози, випадки передозування можуть виникати і в разі періодичного та нехронічного застосування, особливо коли опіоїди поєднують із седативними снодійними засобами, що є поширеним явищем [54]. Хоча було показане короткочасне зниження болю на тлі використання опіоїдів пацієнтами з БДН, жодне довгострокове рандомізоване дослідження опіоїдів не продемонструвало клінічно значущого зменшення болю та поліпшення функції при БДН [50].
Рекомендація 8a
Лікарі не мають використовувати опіоїди для лікування БДН (рівень В).
Рекомендація 8b
Якщо пацієнти вже приймають опіоїди для лікування БДН, лікарі можуть запропонувати варіант безпечного зменшення дози цих ліків і обговорити альтернативні стратегії неопіоїдного лікування (рівень C).
Обґрунтування рекомендації 9. Спочатку трамадол був схвалений до застосування і позиціонувався як менш опіоїдний, а отже, безпечніший. Управління з боротьби з наркотиками (DEA) віднесло його до списку IV, і донедавна трамадол не входив у більшість державних програм моніторингу обігу ліків, що відпускаються за рецептом. Проте профіль ризику трамадолу також незадовільний: пригнічення дихання, звикання і передозування відображені в особливому застереженні в чорній рамці Управління із санітарного контролю якості харчових продуктів і медикаментів США (FDA) [55]. Нещодавнє дослідження виявило збільшення смертності від усіх причин у пацієнтів, які приймають трамадол для лікування остеоартриту [56]. Хоча точна поширеність невідома, серотоніновий синдром також пов’язують із застосуванням трамадолу [57] Потенціал зловживання, визначений за частотою зареєстрованих випадків зловживання в популяції, є значним і вищим, ніж у морфіну [58].
Застосування тапентадолу також пов’язане із серйозними побічними явищами, як зазначено в попередженні FDA у чорній рамці, у тому числі загрозливе для життя пригнічення дихання, залежність, передозування і смерть [59]. Тапентадол є опіоїдом Списку II (класифікація DEA). Потенціал зловживання ним вищий за такий у гідрокодону [58]. Про ефективність трамадолу і тапентадолу при больовій нейропатії повідомляється лише в короткотривалих дослідженнях, тому є потреба в проведенні довгострокових досліджень безпеки й ефективності [60].
Рекомендація 9a
Лікарі не мають використовувати трамадол і тапентадол (засоби з подвійним механізмом дії опіоїди/ІЗЗСН) для лікування БДН (рівень C).
Рекомендація 9b
Якщо пацієнти вже приймають трамадол і тапентадол (засоби з подвійним механізмом дії, опіоїди/ІЗЗСН) для лікування БДН, лікарі можуть запропонувати варіант безпечного зменшення дози цих ліків і обговорити альтернативні стратегії неопіоїдного лікування (рівень C).
Пропозиції для майбутніх досліджень
В огляді висвітлено ключові прогалини в нинішніх знаннях, які потрібно усунути в майбутніх дослідженнях. Зокрема, лише кілька досліджень оцінювали вплив втручань на якість життя, функціонування пацієнта, настрій або сон. Крім того, було проведено кілька порівняльних досліджень ефективності. Ці дослідження з активним препаратом порівняння рідко включали більш як одне інше втручання; саме тому дані, які підтверджують перевагу одного терапевтичного втручання над іншим, обмежені. Єдиним винятком є дослідження PAIN-CONTRoLS, в якому порівнювали 4 активні препарати в пацієнтів із криптогенною нейропатією [61]. Дослідження показало, що дулоксетин і нортриптилін за ефективністю перевершують прегабалін і мексилетин. Також необхідні порівняльні дослідження засобів, ефективних при БДН. Обмеженими є дані щодо порівняння комбінованої терапії з монотерапією та щодо найкращої схеми титрування. Іншим обмеженням для наявних доказів є відсутність даних про ефективність будь-якого втручання після 16 тиж терапії. З огляду на хронічність болю в пацієнтів із БДН і можливість розвитку побічних ефектів, необхідні довгострокові дослідження для кращої поінформованості про довгострокове лікування болю в цій популяції пацієнтів. Зокрема, майбутні дослідження мають бути зосереджені на довгострокових ефектах (позитивних і негативних) опіоїдів, щоб визначити їхню роль у лікуванні таких пацієнтів. Крім того, є всього кілька досліджень, в яких порівнюють різні методи лікування, як-от пероральні ліки, місцеве лікування, нетрадиційні методи лікування і нефармакологічні втручання. Нарешті, немає інформації, яка б допомогла передбачити, які пацієнти найкраще реагуватимуть на конкретні втручання. Ми також об’єднали ліки в межах одного класу, але цілком можливо, що деякі ліки в межах класу кращі за інші. Таким чином, доступно кілька ефективних заходів для лікування пацієнтів із БДН, але необхідні нові дослідження, які б допомогли усунути наявні прогалини і забезпечити краще лікування в майбутньому.
Реферативний огляд Price R. et al. Oral and Topical Treatment of Painful Diabetic Polyneuropathy: Practice Guideline Update Summary Report of the AAN Guideline Subcommittee, Neurology, 2022;98:31-43.
Повну версію дивіться: https://n.neurology.org/content/98/1/31.long
Підготувала Ганна Кирпач
Тематичний номер «Діабетологія, Тиреоїдологія, Метаболічні розлади» № 1-2 (57-58) 2022 р.