24 квітня, 2026
Консенсус експертної ради щодо лікування екзокринної недостатності підшлункової залози в пацієнтів із цукровим діабетом
28 листопада 2025 року відбулося засідання Міжнародної експертно-консультативної ради (далі – Експертна рада) для обговорення теми «Екзокринна недостатність підшлункової залози в пацієнтів із цукровим діабетом». Провідні фахівці в галузі гастроентерології та ендокринології обмінялися думками стосовно цієї актуальної теми в онлайн-форматі. Модератор засідання – професор Ігор Скрипник (Полтавський державний медичний університет), президент Української гастроентерологічної асоціації. До складу Експертної ради увійшла міжнародна та міждисциплінарна команда спеціалістів: провідний ізраїльський гастроентеролог, доктор Юлія Рон (Тель-Авівський медичний центр Сураскі – Іхілов), професор Любов Соколова (ДУ «Інститут ендокринології та обміну речовин ім. В.П. Комісаренка НАМН України»), професор Ольга Бондаренко (ДНТ «Львівський національний медичний університет ім. Данила Галицького»), професор Ганна Маслова (Полтавський державний медичний університет) і професор Олександра Філіппова (Дніпровський державний медичний університет). На зустрічі розглянуто клінічні аспекти ведення пацієнтів із цукровим діабетом (ЦД) і підтвердженою або підозрюваною екзокринною недостатністю підшлункової залози (ЕНПЗ) з акцентом на практичних питаннях діагностики та лікування.
Мета: надати стислі рекомендації від експертів щодо раннього виявлення та лікування ЕНПЗ у пацієнтів із ЦД.
ЦД продовжує становити серйозну медичну та соціальну проблему в усьому світі. Міжнародна федерація діабету (IDF) повідомила, що у 2024 році 589 млн дорослих у світі жили із ЦД, що дорівнює 1 з 9 осіб [4]. Прогнози показують, що до 2050 року це число зросте до 853 млн, причому >40% уражених осіб потенційно залишатимуться недіагностованими [4]. В Україні тягар хвороби є аналогічно значним. Станом на листопад 2025 року Національна служба охорони здоров’я України зареєструвала >1,3 млн осіб із ЦД в електронній системі охорони здоров’я [6], тоді як епідеміологічні оцінки IDF свідчать про ще вищу поширеність серед дорослих [4]. Більшість випадків (майже 90%) пов’язані з ЦД 2 типу [5], який зазвичай асоціюється з ожирінням [7], артеріальною гіпертензією [7], дисліпідемією [7], метаболічно-асоційованим стеатозом печінки [8] та стеатозом підшлункової залози [11]. Ці супутні захворювання сприяють високому кумулятивному ризику ускладнень [7-10] та перешкоджають досягненню стабільного глікемічного контролю [12, 13]. У цьому контексті ЕНПЗ усе частіше визнається недооціненим, але клінічно значущим фактором. ЕНПЗ може впливати на харчовий статус, шлунково-кишкові симптоми та якість життя [1-3], вона пов’язана з варіабельністю глікемії та терапевтичними труднощами в деяких пацієнтів із ЦД [13, 14], а також може погіршувати серцево-судинні наслідки [1-3].
В європейських рекомендаціях щодо діагностики та лікування ЕНПЗ, розроблених під егідою Європейського панкреатичного клубу (EPC, 2024), де розглядають лікування ЕНПЗ у пацієнтів із ЦД 1 та 2 типу, підкреслено актуальність проблеми [1]. Це обґрунтовує необхідність упровадження систематичних підходів до своєчасного виявлення та лікування ЕНПЗ у пацієнтів із ЦД, адаптованих до українського клінічного контексту.
Патогенез
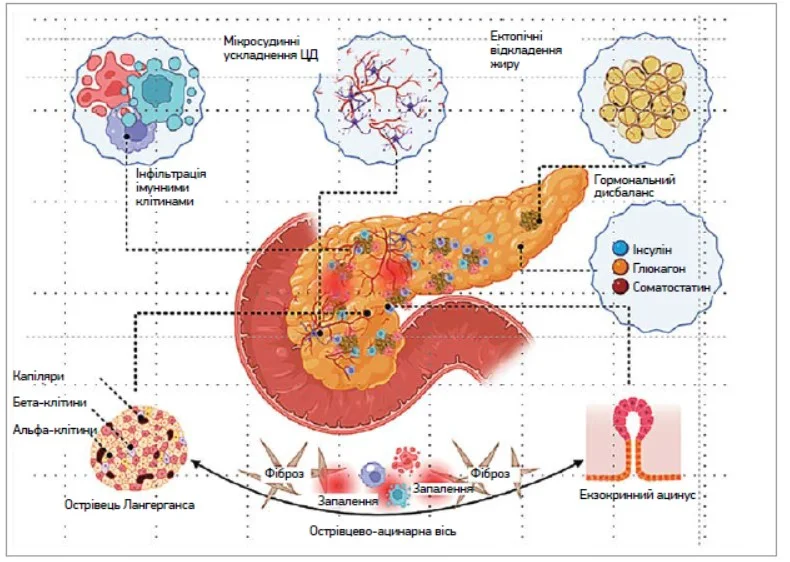
Ключові патогенетичні механізми ЕНПЗ у контексті ЦД визнані багатофакторними, як зазначено в рекомендаціях EPC (2024) [1] (рис. 1). ЕНПЗ виникає унаслідок перекриття гормональних, метаболічних, нейрогуморальних та структурних змін у підшлунковій залозі, які можуть взаємно посилювати одна одну [16-19]. Центральним у цих процесах є ендокринно-екзокринна взаємодія: порушення функції острівцевих клітин змінює трофічну підтримку та регуляцію життєздатності й секреції ацинарних клітин, тоді як екзокринна дисфункція може ще більше ускладнити метаболічний контроль [15, 18, 19].
Рис. 1. Патогенез ЕНПЗ, пов’язаної з ЦД: багатофакторний процес [16]
Основні патогенетичні механізми, що сприяють розвитку ЕНПЗ у пацієнтів із ЦД [1, 16]:
- втрата трофічного та стимулюючого впливу інсуліну на ацинарні клітини й екзокринну секрецію підшлункової залози;
- атрофія та фіброз підшлункової залози, що часто виникають унаслідок мікроангіопатії та хронічного ушкодження тканин;
- гіперглікемія, яка сприяє фіброгенезу та посилює дисфункцію залози;
- діабетична вегетативна нейропатія та порушення ентеропанкреатичних рефлексів, що спричиняє змінену регуляцію секреції;
- стеатоз як прояв метаболічного ураження підшлункової залози;
- порушення регуляції інших гормонів-острівців, зокрема глюкагону та соматостатину, які впливають на екзокринну функцію підшлункової залози;
- одночасне залучення ендокринної та екзокринної тканини при автоімунних, інфекційних або генетичних захворюваннях.
Клінічне значення ЕНПЗ при ЦД
ЕНПЗ у пацієнтів із ЦД має не лише гастроентерологічний, а й системний клінічний вимір, що проявляється феноменом «взаємного обтяження»: ЦД сприяє розвитку та прогресуванню екзокринної дисфункції підшлункової залози, тоді як ЕНПЗ, своєю чергою, погіршує перебіг ЦД [15, 17, 19, 20]. Прогностично найбільш значущими, хоча й не єдиними, несприятливими наслідками цього є двоспрямований вплив на підвищений ризик остеопорозу [21, 22], серцево-судинних захворювань [23, 24] та глікемічної варіабельності [15, 17, 19, 20]. Ключовим механізмом, що лежить в основі глікемічної варіабельності, є непередбачуване перетравлення та всмоктування поживних речовин зі зміненою доступністю вуглеводів через порушення інкретинової відповіді, що може клінічно проявлятися як підвищена глікемічна варіабельність (епізоди гіпер- та/або гіпоглікемії), а це ускладнює досягнення цільового рівня глікованого гемоглобіну (HbA1c) і стабільного метаболічного контролю [15, 17, 19, 20].
Ключовим клінічним наслідком ЕНПЗ у пацієнтів із ЦД є прогресуючий дефіцит поживних речовин. Порушення травлення та мальабсорбції зумовлюють втрату маси тіла, саркопенію, білково-калорійний дефіцит і дефіцит мікронутрієнтів, насамперед жиророзчинних вітамінів (A, D, E, K), що має прямі клінічні наслідки [1, 3]. Дефіцит вітаміну D і порушення кальцієво-фосфорного гомеостазу при ЕНПЗ пов’язані зі зниженням мінеральної щільності кісток, остеопорозом та підвищеним ризиком переломів. У клінічних рекомендаціях надано пораду моніторувати метаболічні захворювання кісток і проводити корекцію дефіциту в межах комплексної нутритивної підтримки та замісної ферментної терапії (ЗФТ) [1, 33].
Дефіцит вітаміну А може проявлятися як «куряча сліпота» та порушення трофіки слизових оболонок, що має додаткове клінічне значення при ЦД. Дефіцит вітаміну Е здебільшого пов’язаний з неврологічними та м’язовими симптомами (периферична нейропатія, слабкість, швидка стомлюваність), які ще більше погіршують функціональний стан пацієнтів із ЦД [1, 3].
Дефіцит вітаміну К може зумовити коагулопатію зі схильністю до кровотеч (подовжені показники коагуляції, легке утворення синців), що особливо важливо в пацієнтів, які отримують антитромбоцитарну або антикоагулянтну терапію [1, 3].
Дефіцит вітаміну B12 потребує особливої уваги: при ЕНПЗ він може проявлятися макроцитарною анемією, втомою та неврологічними симптомами (парестезії, порушення ходи, когнітивні скарги), що виправдовує скринінг і корекцію як складові комплексного лікування пацієнтів із ЦД [3].
Порушення гідролізу і всмоктування ліпідів при ЕНПЗ, особливо незамінних жирних кислот, пов’язані з дерматологічними проявами (сухість шкіри, дерматит) й уповільненим відновленням тканин, що в пацієнтів із ЦД може корелювати з підвищеним ризиком інфекції та порушенням загоєння ран [1, 2].
Водночас наявний дефіцит поживних речовин та недостатнє засвоєння вітамінів і мікроелементів при ЕНПЗ можуть знизити імунну відповідь, підвищити сприйнятливість до інфекцій, а також погіршити перебіг діабетичних ускладнень через порушення репаративних процесів та загального метаболічного стану. У клінічних рекомендаціях наголошено на необхідності систематичної оцінки стану харчування, корекції дефіциту та адекватної ЗФТ у цих пацієнтів [1, 3].
Шлунково-кишкові прояви ЕНПЗ (діарея, стеаторея, здуття живота, біль у животі, метеоризм, постпрандіальний дискомфорт, відчуття важкості після їди) є частими та клінічно значущими, оскільки вони знижують якість життя, впливають на харчову поведінку і дотримання терапії, а також можуть супроводжуватися психологічним дистресом [1, 3].
У пацієнтів із ЦД ці неспецифічні симптоми часто помилково пояснюються побічними ефектами антигіперглікемічних засобів (зокрема, метформіну, агоністів рецепторів глюкагоноподібного пептиду-1 (ГПП-1) та/або інгібіторів дипептидилпептидази-4). Це неправильне пояснення чітко виокремлено в розділі 10 європейських рекомендацій (2024) щодо ЕНПЗ при ЦД і вважається однією з причин недооцінки ЕНПЗ та затримки діагностики [1].
У результаті цієї діагностичної пастки клінічний фокус часто зміщується до непереносимості лікування: пацієнти самостійно припиняють прийом ліків, зменшують дозування або наполягають на необґрунтованих змінах у терапії. Згідно з рекомендаціями [1], такі дії можуть погіршити глікемічний контроль, але не усувають першопричину – порушення травлення та мальабсорбції, спричинені ЕНПЗ [1, 3]. Це може зумовити прогресування дефіциту поживних речовин і подальше зниження якості життя [1, 3].
Для належної інтерпретації симптомів у пацієнтів із ЦД рекомендується:
- підозрювати ЕНПЗ, коли симптоми мальабсорбції (стеаторея, здуття живота, метеоризм, діарея, біль у животі, тяжкість) наявні в поєднанні з ознаками дефіциту поживних речовин (втрата маси тіла, дефіцит жиророзчинних вітамінів та/або мікроелементів) [1, 3];
- проводити неінвазивне тестування, насамперед визначення фекальної еластази‑1 (ФЕ‑1), у поєднанні з оцінкою стану харчування (вітаміни A, D, E, K, B12; альбумін/преальбумін; антропометрія) [1, 3];
- якщо підтверджено ЕНПЗ, ініціювати ЗФТ з адекватними дозами панкреатичних ферментів і корекцію дефіциту поживних речовин, що не тільки зменшує тяжкість симптомів, а й сприяє стабілізації глікемічного контролю, уникаючи необґрунтованого припинення антигіперглікемічної терапії [1, 3]. Згідно з когортними дослідженнями, ЕНПЗ пов’язана зі збільшенням захворюваності, смертності та гіршим серцево-судинним прогнозом [1]. ЕНПЗ вважається маркером несприятливішого перебігу хронічних захворювань підшлункової залози, що слід ураховувати під час стратифікації ризику, профілактики та лікування ускладнень [1, 3].
З огляду на високу ймовірність недостатньої діагностики ЕНПЗ у пацієнтів із ЦД і неспецифічний характер симптомів (біль у животі, тяжкість, метеоризм, здуття живота, діарея, стеаторея) експерти визначили клінічні ситуації, за яких ризик ЕНПЗ зростає (табл. 1). Це обґрунтовує проактивний підхід – цілеспрямовану оцінку ЕНПЗ у групах ризику ще до появи виражених шлунково-кишкових симптомів або дефіциту поживних речовин. Додатковим маркером ризику розвитку ЕНПЗ, як рекомендують експерти, є виражена глікемічна варіабельність, котру неможливо пояснити винятково режимом антигіперглікемічної терапії [20].
Важливими модифікаторами ризику та/або наслідків ЕНПЗ є стани т. зв. метаболічного континууму: стеатоз підшлункової залози (в англомовній літературі його називають жировою хворобою підшлункової залози) [1], саркопенія та саркопенічне ожиріння [34], а також вікові структурні й функціональні зміни підшлункової залози (т. зв. старіюча підшлункова залоза) [1, 36].
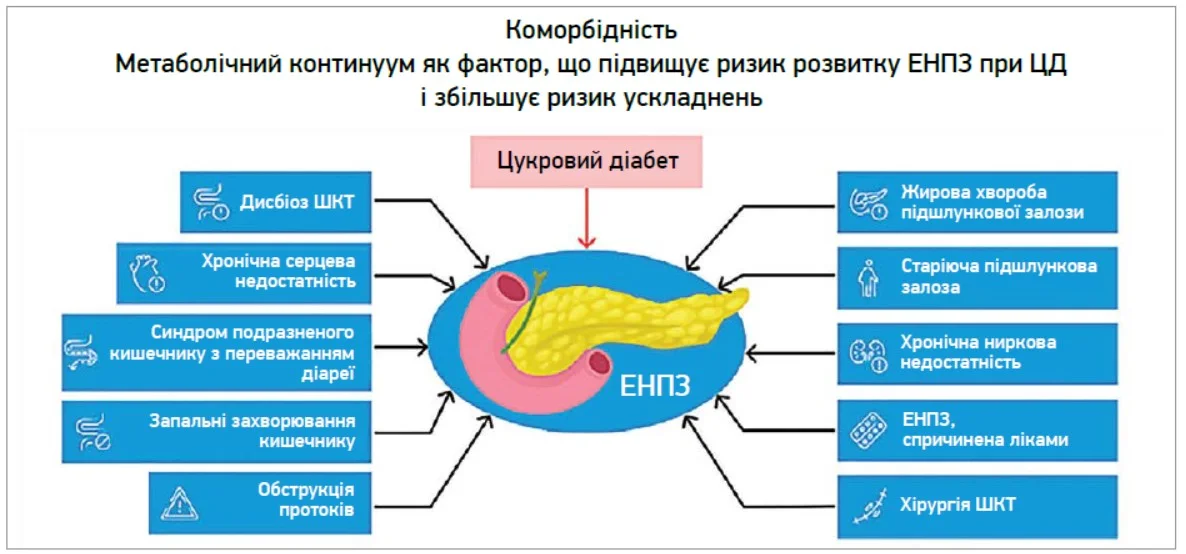
Також необхідно враховувати супутні патологічні стани, пов’язані з підвищеним ризиком ЕНПЗ і розладів травлення: порушення кишкового мікробіому [37], хронічна серцева [35] та ниркова недостатність [1], запальні захворювання кишечнику, обструкція панкреатичної протоки, попередні операції на підшлунковій залозі та/або шлунково-кишковому тракті, а також медикаментозні ураження підшлункової залози [1] (рис. 2).
Рис. 2. Метаболічний континуум: захворювання, що підвищують ризик ЕНПЗ при ЦД [1-3, 33-37]
Примітка: ШКТ – шлунково-кишковий тракт.
Діагностика
Експерти запропонували активний підхід до ведення пацієнтів із ЦД, який передбачає перехід від стратегії оцінки ЕНПЗ лише у випадках вираженої стеатореї та значної втрати маси тіла до систематичної стратегії раннього виявлення. Практичною метою цього підходу є зменшення частки нерозпізнаних випадків ЕНПЗ і запобігання наслідкам мальабсорбції, яка, крім загальних наслідків ЕНПЗ, може впливати на глікемічну варіабельність, кістковий метаболізм, серцево-судинну систему та загальний прогноз. Впровадження активної стратегії базується на виявленні пацієнтів із підвищеним ризиком (табл. 1, рис. 2), активному виявленні легких шлунково-кишкових симптомів за допомогою валідованих опитувальників, ранньому використанні доступних методів оцінки екзокринної функції підшлункової залози та паралельній оцінці харчового статусу. Систематичний скринінг у групах ризику розглядається як інструмент, здатний покращити раннє виявлення ЕНПЗ та оптимізувати результати лікування.
|
Таблиця 1. Фактори ризику розвитку ЕНПЗ у пацієнтів із ЦД |
|
|
Фактор ризику |
Клінічне значення |
|
ЦД 1 типу |
Ймовірність ЕНПЗ є вищою порівняно із ЦД 2 типу [1, 25] |
|
Інсулінозалежність, низький рівень С-пептиду |
Маркери інсулінової недостатності, пов’язані з вираженішим зниженням екзокринної функції підшлункової залози [26, 27] |
|
ЦД 3с типу (панкреатогенний ЦД) |
Часто поєднується з ЕНПЗ [1, 28] |
|
Поганий глікемічний контроль (високий рівень HbA1c) |
Пов’язано з вищою частотою ЕНПЗ [20, 29, 30, 32] |
|
Великий стаж ЦД |
Ризик ЕНПЗ зростає із тривалістю захворювання; підвищена пильність необхідна пацієнтам із тривалим анамнезом ЦД [1, 31, 32] |
|
Мимовільне зниження маси тіла |
Маркер можливого порушення травлення / мальабсорбції; основа для проактивної оцінки ЕНПЗ |
Експерти зазначили, що діагностика ЕНПЗ у пацієнтів із ЦД має базуватися на загальних принципах, поєднуючи клінічну оцінку симптомів, аналіз харчового статусу та доступні тести для оцінки екзокринної функції підшлункової залози [1-3]. Водночас фахівці наголошували на високому ризику діагностичних помилок через неспецифічність шлунково-кишкових проявів: здуття живота, дискомфорт у животі, діарея та стеаторея можуть бути помилково інтерпретовані як функціональні розлади кишечнику або гастропарез, побічні ефекти гіпоглікемічних препаратів (зокрема, метформіну, агоністів рецептора ГПП‑1) або прояви діабетичної вегетативної нейропатії [1, 38-40]. Такі неправильні інтерпретації можуть затримати своєчасну діагностику ЕНПЗ, що може супроводжуватися прогресуванням дефіциту поживних речовин і потенційним погіршенням глікемічного контролю.
Згідно з рекомендаціями EPC (2025), визначення ФЕ-1 рекомендується як метод первинної оцінки ЕНПЗ. Він не є золотим стандартом і має певні обмеження, однак залишається найдоступнішим тестом у рутинній клінічній практиці [1].
Для покращення діагностики ЕНПЗ доцільно використовувати стандартизований PEI-Q (опитувальник ЕНПЗ), який дозволяє структурувати скарги, кількісно оцінити їхню тяжкість та подальше використання для моніторингу відповіді на ЗФТ. Анкета містить 18 запитань, доступна українською мовою та може бути заповнена онлайн. Із практичного погляду оптимальною тактикою є заповнення PEI-Q перед консультацією, що підвищує структурованість візиту та полегшує виявлення пацієнтів із вищою імовірністю ЕНПЗ [41]. Використання PEI-Q рекомендовано в Національній клінічній настанові «Хронічний панкреатит» (2023) [42], що базується на принципах доказової медицини.
Якщо після комплексної оцінки симптомів, анамнезу, стану харчування та екзокринної функції підшлункової залози діагноз ЕНПЗ не може бути встановлений однозначно, можна використати додатковий інструмент – пробна ЗФТ у терапевтичних дозах протягом 4-6 тиж. Експерти наголосили, що позитивна відповідь на таку терапію може свідчити про ймовірну ЕНПЗ та є як діагностичним, так і терапевтичним підходом. Навіть часткове клінічне покращення за допомогою ЗФТ слід вважати позитивним результатом та підставою для продовження терапії [1, 2].
Лікування
Під час розгляду сучасних підходів до лікування ЕНПЗ Експертна рада ґрунтувалася на положеннях рекомендацій EPC (2024), де надано пораду віддавати перевагу серед засобів для ЗФТ ферментним препаратам (ФП) у вигляді гранул малого розміру з кислотостійким (кишковорозчинним) покриттям. На сьогодні клінічну ефективність продемонстрували лише препарати панкреатину свинячого походження [1].
Ключовими вимогами до вибору ФП, що визначають ефективність ЗФТ, є добре змішування з хімусом, захист від інактивації шлунковим соком, евакуація зі шлунка синхронно із харчовим болюсом та швидка активація ферментів у проксимальному відділі дванадцятипалої кишки. Особливо наголошується, що сучасні ФП мають містити дрібні частинки (<2 мм, оптимально – <1,8 мм), які краще змішуються з їжею та синхронно із хімусом переносяться зі шлунка до дванадцятипалої кишки. Ці характеристики ФП сприяють ефективнішому травленню, а також вищій терапевтичній ефективності [1-3, 43]. Члени Експертної ради наголосили, що для корекції ЕНПЗ доцільно використовувати лікарські засоби з доведеною ефективністю, а не харчові добавки [3]. Початкові (мінімально ефективні) дози ФП залежать від віку, тяжкості ЕНПЗ і вмісту жиру в раціоні. Для дорослих базовий початковий режим має ураховувати 40 000-50 000 одиниць ліпази на основний прийом їжі та 20 000-25 000 одиниць ліпази на перекус [1-3, 42]. Ці дози спрямовані на зменшення шлунково-кишкових симптомів, покращення та підтримку харчового статусу; при нижчих дозах, навіть якщо спостерігається симптоматичне покращення, в 70% пацієнтів продовжуються патологічно знижені показники нутритивного статусу [43].
ФП слід приймати так, щоб вони надходили в кишечник одночасно з їжею; оптимальний час для прийому – під час їди, а не до чи після. Прийом ФП із перекусами обов’язковий, якщо їжа містить жир або білок [1-3, 42].
Згодом початкові дози слід титрувати на підставі клінічної відповіді, змін маси тіла та параметрів харчового статусу. Приблизну контрольну оцінку варто провести через 4-6 тиж, враховуючи симптоми, масу тіла та динамічні зміни балів за шкалою PEI-Q. У разі недостатнього ефекту необхідно перевірити дотримання терапії, правильність прийому ФП (із кожним прийомом їжі, без пропуску перекусів та уникнення прийому після їди), виключення супутньої патології, яка може погіршити травлення, або відповідність призначеного препарату сучасним вимогам ЗФТ. Можливе подальше збільшення дози та індивідуалізований розгляд питання про додавання інгібітора протонної помпи до схеми лікування [1-3, 42, 43].
Недостатня відповідь на ЗФТ визначається стійкою діареєю та/або стеатореєю, здуттям живота, метеоризмом, дискомфортом у животі, відсутністю збільшення чи стабілізації маси тіла, а також стійким дефіцитом поживних речовин. Якщо очікуваний ефект не досягається після корекції тривалості та дози ФП, необхідно одночасно виключити інші причини мальабсорбції або діареї [1-3, 42, 43].
Перший крок в оцінці ефективності ЗФТ слід провести через 4-6 тиж, оцінюючи шлунково-кишкові симптоми (бажано за допомогою стандартизованої валідованої анкети). Згодом, згідно з європейськими рекомендаціями (2024), для довгострокового спостереження за пацієнтами з ЕНПЗ у контексті ЦД рекомендується моніторинг параметрів, зазначених у таблиці 2 [1].
|
Таблиця 2. Параметри, рекомендовані для довгострокового спостереження в пацієнтів з ЕНПЗ, пов’язаною із ЦД |
|||
|
Нутритивні/функціональні |
|||
|
Маса тіла Індекс маси тіла Втрата маси тіла Сила стискання |
Антропометрія: окружність м’язів середньої ділянки плеча; кількісний аналіз м’язової маси (вимірювання біоелектричного імпедансу та/або комп’ютерна томографія) |
Оцінка складу тіла та кісткової тканини за допомогою двофотонної рентгенівської абсорбціометрії (кожні 2 роки) |
Тест 6-хвилинної ходьби |
|
Біохімічні |
|||
|
Загальний аналіз крові та запаси заліза |
Білки плазми: альбумін, ретинолозв’язуючий білок і трансферин |
Мікронутрієнтний статус: магній, жиророзчинні вітаміни, цинк, селен, вітамін B12 та фолат |
С-реактивний білок Глюкоза та HbA1c Паратгормон |
|
Клінічні |
|||
|
Оцінка симптомів ураження кишечнику: частота та колір випорожнень; здуття живота / метеоризм; біль у животі після їди |
Фактори, що впливають на якість життя: зміна ліків (особливо опіоїдів та протидіарейних препаратів) |
Дотримання способу життя (відмова від куріння, фізична активність та достатнє перебування на сонці) |
|
|
Харчові |
|||
|
Оцінка відрази до їжі через абдомінальні симптоми |
Аналіз добового раціону (харчовий анамнез / харчова карта) порівняно з відповідною дозою ЗФТ для оцінки дотримання режиму терапії та відповідності ЗФТ харчуванню |
Оцінка уникнення жирної їжі |
Оцінка адекватності дієти |
Ефективність ЗФТ оцінюється комплексно – з урахуванням зменшення шлунково-кишкових проявів у поєднанні з корекцією дефіциту поживних речовин, покращенням або підтримкою адекватного харчового статусу та якості життя. Дані довгострокових спостережень свідчать про те, що клінічно значуще покращення параметрів трофологічного статусу, включаючи стабілізацію або збільшення маси тіла разом зі зменшенням симптомів, можливе протягом 6-12 міс після початку терапії [43]. У цьому контексті частковий ефект слід розглядати як підставу для продовження терапії: навіть неповне, але клінічно помітне зменшення деяких симптомів або дефіцитів свідчить про те, що обрана стратегія працює та потребує подальшої оптимізації (насамперед дозування і дотримання режиму), а не припинення лікування [1].
З огляду на патогенез ЕНПЗ у контексті ЦД та його прогностичні наслідки лікування має бути довгостроковим і насамперед спрямованим на відновлення харчового статусу та корекцію дефіцитів, а не лише на полегшення шлунково-кишкових симптомів [1, 3, 43].
Для досягнення максимальної ефективності ЗФТ лікування слід поєднувати з нутритивною підтримкою та корекцією дефіциту мікроелементів; за показаннями доцільно залучити клінічного дієтолога [1, 3]. Експерти рекомендують включити консультацію дієтолога як складову стандарту лікування пацієнтів із підозрою на ЕНПЗ або підтвердженою ЕНПЗ у контексті ЦД. Доцільно розробити дієту без суворих обмежень жирів, із достатнім вмістом білка та дробовим режимом харчування 5-6 р/день, індивідуалізованим відповідно до глікемічних цілей. Корекцію дефіциту жиророзчинних вітамінів слід проводити з подальшим лабораторним контролем; частоту контролю варто визначати індивідуально, приблизно кожні 6-12 міс. Рекомендовані дози: вітамін D – 2000-4000 МО/день, вітамін A – 10 000-25 000 МО/день, вітамін E – 400-800 МО/день, вітамін K – 5-10 мг/день за потреби [1].
Висновки
Після обговорень Експертної ради було ухвалено такі резолюції:
- ЕНПЗ у контексті ЦД слід визнавати клінічно значущим і недостатньо діагностованим станом, який негативно впливає на харчовий статус, якість життя, глікемічний контроль та довгостроковий прогноз пацієнта.
- Неспецифічна картина шлунково-кишкових симптомів та їх часте неправильне тлумачення часто зумовлюють затримку діагностики та прогресування дефіциту поживних речовин.
- Рекомендується активний підхід, що включає систематичну оцінку ЕНПЗ у групах високого ризику з використанням установлених діагностичних критеріїв, включаючи ФЕ‑1, опитувальник PEI-Q та комплексну оцінку харчового статусу.
- Вважається доцільним розпочинати ЗФТ у рекомендованих початкових дозах із подальшим титруванням, керуючись як клінічними симптомами, так і харчовими маркерами. Часткова клінічна відповідь на ЗФТ має слугувати основою для продовження та оптимізації терапії.
- Консультація із клінічним дієтологом має бути включена до стандарту догляду за пацієнтами з підозрюваною або підтвердженою ЕНПЗ у контексті ЦД. Також рекомендуються систематична корекція дефіциту мікронутрієнтів і постійний моніторинг результатів лікування.
- Для підвищення якості діагностики та ведення пацієнтів слід започаткувати серію наукових та освітніх ініціатив для ендокринологів, гастроентерологів і лікарів загальної практики або сімейних лікарів. Рекомендується поширення інформації серед професійної спільноти шляхом публікації цієї резолюції та розробки консенсусного документа.
- Враховуючи, що ЕНПЗ у контексті ЦД є поширеним, але постійно недостатньо діагностованим і недооціненим станом зі значними прогностичними наслідками, необхідно та доцільно розробити національні клінічні рекомендації щодо лікування ЕНПЗ у пацієнтів із діабетом, які б забезпечили структуровану, засновану на доказах систему підтримки рішень для лікарів різних спеціальностей, що беруть участь у лікуванні цих складних випадків.
Skrypnyk I., Ron, Y., Sokolova L., Bondarenko O., Maslova G., Filippova O. Експертний консенсус щодо ведення екзокринної недостатності підшлункової залози у пацієнтів із цукровим діабетом.
Сімейна медицина. Європейські практики. 2026. № 1 (115). С. 9-16. https://doi.org/10.30841/2786-720X.1.2026.353747.
Переклав з англ. Ігор Петренко
Медична газета «Здоров’я України 21 сторіччя» № 6 (617), 2026 р