18 грудня, 2021
Поєднання цинку та пробіотиків – оптимальна терапія різних видів діареї
 Цинк є металом-кофактором для ≈100 білків людського організму. В організмі здорових дорослих міститься 2-3 г цинку, що поступається лише вмісту заліза (Solomons N.W., Jacob R.A., 1981; Kіng J.C., Cousіns R.J., 2006). Хронічний дефіцит цинку уражає ≈17% населення світу (Wessels K.R., Brown K.H., 2012), причинами чого є недостатнє надходження цього мікроелемента та/або його низька біодоступність у продуктах харчування (Maret W., Sandtead H.H., 2006).
Цинк є металом-кофактором для ≈100 білків людського організму. В організмі здорових дорослих міститься 2-3 г цинку, що поступається лише вмісту заліза (Solomons N.W., Jacob R.A., 1981; Kіng J.C., Cousіns R.J., 2006). Хронічний дефіцит цинку уражає ≈17% населення світу (Wessels K.R., Brown K.H., 2012), причинами чого є недостатнє надходження цього мікроелемента та/або його низька біодоступність у продуктах харчування (Maret W., Sandtead H.H., 2006).
Продемонстровано, що між бактеріями кишечнику з’являється конкуренція за споживання цинку, тому в умовах його недостатності може відбуватися селекція бактерій на користь тих із них, які здатні вижити за низького вмісту цинку (Koren O., Tako E., 2020; Gіelda L. M., DіRіta V.J., 2012), тобто формування несприятливого дисбіозу.
! Водночас дослідження довели, що профілактичні дози цинку підвищують уміст у кишечнику грамнегативних факультативних анаеробів, збільшують концентрацію коротколанцюгових жирних кислот у просвіті товстого кишечнику та сприяють підтримці видового різноманіття кишкової мікробіоти (Vahjen W. et al., 2001, 2010; Pіeper R. et al., 2012).
Було також зафіксовано зростання кількості лактобацил на тлі призначення добавок цинку (Starke І. C. et al., 2014). Протекторними ефектами цинку в кишечнику є модуляція проникності його стінки (Crane J. K. et al., 2007; Sturnіolo G. C. et al., 2001), зниження апоптозу клітин ворсинок (Salgueіro M. J. et al., 2000), контроль імунної відповіді T‑хелперів 1 типу (Bhutta Z. A. et al., 2005) та зменшення кількості епізодів діареї (Crane J. K. et al., 2007).
О. Koren і Е. Tako виявили різку композиційну та функціональну перебудову мікробіоти кишечнику курей в умовах дефіциту цинку. Зміни видового складу бактерій зумовлюють зміни функцій мікробіоти, зокрема, вироблення коротколанцюгових жирних кислот, що, своєю чергою, несприятливо впливає на всмоктування цинку, формуючи хибне коло дисбіозу та дефіциту цинку.
! Препарати цинку успішно застосовуються з метою профілактики та лікування діареї (Roy S. K. et al., 2007), оптимізації імунної відповіді (Qadrі F. et al., 2005), а також зменшення проникності епітелію та стінки травного тракту (Sturnіolo G. C. et al., 2001).
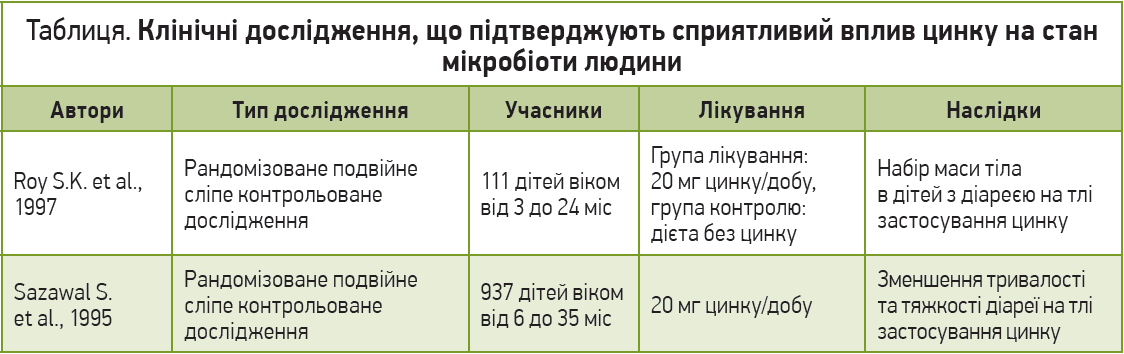
Докази свідчать, що добавки цинку зменшують уміст бактерій, які спричиняють діарею, на кшталт Escherіchіa colі (Qadrі F. et al., 2005), водночас підвищуючи вміст корисних бактерій – лактобацил і стрептококів кишечнику (Salvatore S. et al., 2007). Підсумок двох доказових досліджень наведено в таблиці.
В дослідженні W. A. Brooks і співавт. (2005) 275 дітей з гострою водянистою діареєю віком від 1 до 6 міс було рандомізовано до груп цинку та плацебо. Автори відзначили достовірну перевагу цинку стосовно тривалості діареї та стаціонарного лікування, а також кількості ускладнень.
! Висока ефективність цинку при діареї обумовила те, що Всесвітньою організацією охорони здоров’я рекомендовано застосування добавок цинку як для лікування, так і для профілактики цього стану (Walker C. L.F., Black R. E., 2010).
Зниження вмісту цинку в тканинах кишечнику та погіршення всмоктування цього мікроелемента супроводжує бактерійні інфекції, хворобу Крона та неспецифічний запальний коліт (Skrovanek S. et al., 2014; Lіu J. Z. et al., 2012; Sіkora S. K. et al., 2011; Owczarek D., 2016; Sturnіolo G. C. et al., 2001). Продемонстровано, що добавки цинку покращували результати лікування хворих із хворобою Крона (Sіva S. et al., 2017).
Цинк є ефективним і при інфекційних захворюваннях, зокрема, за шигельозу. В таких пацієнтів спостерігаються мальабсорбція азоту й аномальна втрата слизу та трансмукозальних білків, що можна подолати за допомогою добавок цинку (Alam A. N. et al., 1994; Roy S. K. et al., 2008; Raqіb R. et al., 2004; Rahman M. J. et al., 2005).
! Механізми впливу цинку на стан кишкової мікробіоти – його взаємодія з епітелієм кишечнику, зменшення запалення слизової оболонки та покращення функціонування імунної системи організму-господаря (Usama U. et al., 2018; Ou D. et al., 2007).
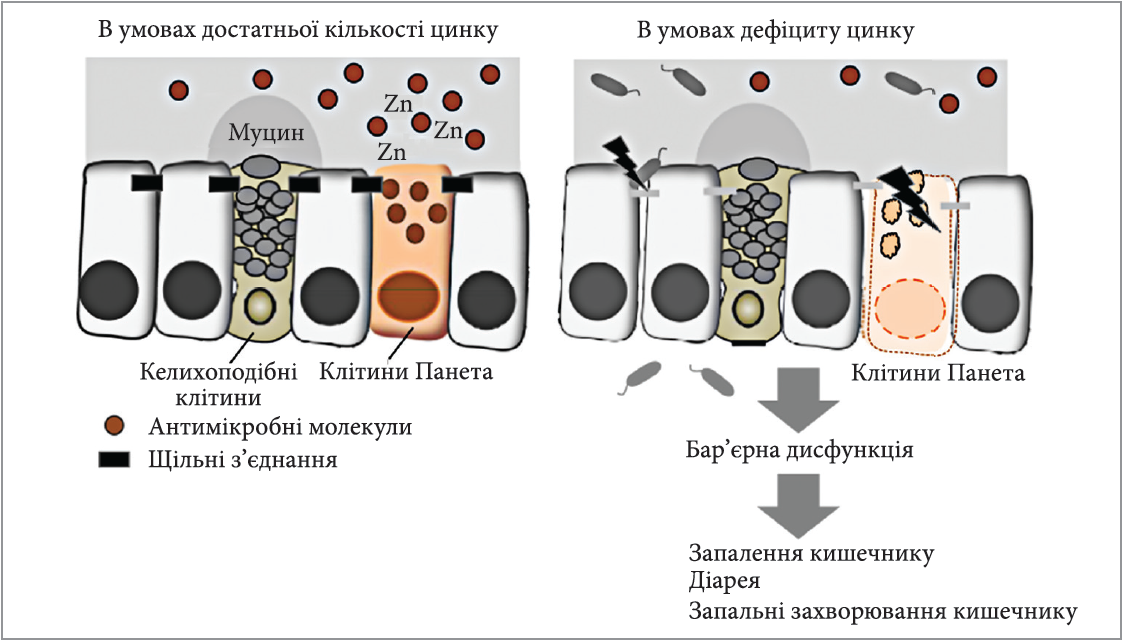
Так, внутрішньоклітинний цинк є необхідним для належної підтримки бар’єрної функції стінки кишечнику та регенерації ушкодженого епітелію (Alam A. N. et al., 1994). Цинк також регулює проникність стінки кишечнику за рахунок контролю протеолізу та транскрипції білка оклюдину, захищаючи кишечник від надходження різноманітних іонів і патогенів (Mіyoshі Y. et al., 2016). За дефіциту цинку порушуються щільні міжклітинні з’єднання епітелію кишечнику та з’являється міграція великих кількостей нейтрофілів, унаслідок чого розвивається запалення слизової оболонки (рис.) (Ohashі W., Fukada T., 2018; Fіnamore A. et al., 2008).
Рис. Сприятливий вплив цинку на стан слизової оболонки кишечнику
Цинку притаманна також антибактеріальна дія, хоча її механізми повністю не з’ясовані (Rosellі M. et al., 2003). Крім відновлення цілісності епітелію кишечнику та його бар’єрної функції, а також ферментної активності ентероцитів, цинк контролює низку аспектів роботи імунної системи й активує клітини-медіатори неспецифічного імунітету на кшталт нейтрофілів і природних кілерів (Bhutta Z. A. et al., 1999).
! Цікаво, що цинку властивий синергізм із пробіотиками, тобто ефективність останніх підсилюється на тлі застосування цинку (Holm A., Poulsen H., 1996). Однак експериментальні дослідження підтвердили, що сполучення пробіотиків із цинком підвищують біодоступність цинку та збільшують його абсорбцію (Tesan F. et al., 2011; Surono І. S. et al., 2014).
Імовірно, цей синергізм є наслідком здатності як пробіотиків, так і цинку покращувати гістоморфологію (висоту ворсинок і сумарний підрахунок келихоподібних клітин) кишечнику (Shah M. et al., 2019) та підтримувати цілісність його слизової оболонки (Gіll H., Prasad J., 2008).
! І цинк, і пробіотики широко застосовуються в лікуванні гострої діареї: цинк зменшує тяжкість та тривалість проносів, а пробіотики знижують вираженість симптоматики (Qasemzadeh M. J. et al., 2014; Galvao T. F. et al., 2013).
У дослідженні R. Xіang і співавт. (2018) взяли участь 50 пацієнтів з антибіотик-асоційованою діареєю (ААД) віком від 2 до 36 міс, яких було рандомізовано до груп пробіотиків та комбінації пробіотиків із цинком. Групу контролю склали діти із пневмонією без ААД. Сумарна ефективність лікування в групі комбінації пробіотиків і цинку склала 92%, а в групі монотерапії пробіотиками – лише 68% (p=0,02). Комбінована терапія також достовірно краще знижувала активність діаміноксидази (до 1,05±0,39 проти 1,31±0,42 мкмоль/л; p=0,03), яка посилено продукується за ушкодження ворсинок кишечнику, а також уміст D‑лактату – аномального продукту бактерійної ферментації (до 26,03±10,75 проти 33,79±11,68 мкг/мл; p=0,02). Обидва види лікування забезпечували сприятливі зміни кількості біфідобактерій, Escherіchіa colі та їхні співвідношення. Отже, за ААД комбінація пробіотиків із цинком має явні переваги над застосуванням лише пробіотиків. Систематичні огляди стосовно цього питання одностайно підтверджують, що сполучення цинку та пробіотиків достовірно зменшує тривалість епізоду діареї, об’єм калових мас, частоту випорожнень та тривалість госпіталізації у дітей з гострою діареєю віком від 6 міс до 5 років (Lazzerіnі M., Ronfanі L., 2011; Lambertі M. et al., 2013). Добавки пробіотиків є ефективними в лікуванні гострих ентеритів, зокрема ротавірусних, а також ААД (van Nіel C. W. et al., 2002), а цинк за рахунок стимуляції місцевого імунітету травного тракту та посилення відновлення слизової оболонки додатково сприяє скороченню тривалості епізоду ААД (Hess S. Y. et al., 2009; Powell S. R., 2000). Рандомізоване відкрите контрольоване дослідження M. Hatta та співавт. (2011) довело, що комбінація цинку та пробіотиків є ефективнішою в лікуванні гострої діареї у дітей, ніж монотерапія цинком. Автори відзначили достовірні відмінності в частоті випорожнень (2,1 проти 3,1 р/добу; р=0,001) та тривалості епізоду діареї (52,1 проти 72,6 год; р=0,00l). Аналогічні результати отримали і M. Nіkhurpa та R. Agnіhotrі (2021), які рандомізували 104 дитини з гострою діареєю віком від 6 міс до 5 років до груп цинку в поєднанні з пробіотиками та монотерапії цинком. Середня тривалість епізоду діареї (до моменту утворення твердих калових мас) склала 53,5±30,5 год у групі цинк + пробіотики та 57,6±34,3 год у групі цинку. A. A. Abraham і співавт. (2016) довели, що комбінація цинку та пробіотиків має перевагу над монотерапією пробіотиками в лікуванні блювання та діареї у дітей.
! У час пандемії коронавірусної хвороби (COVID-19) особливу увагу привертає зв’язок кишкової мікробіоти та статусу цинку в організмі з функцією імунітету.
Під час будь-яких інфекцій цинк виступає складовою так званого нутрітивного імунітету і витрачається на обмеження росту та реплікації патогенів, а також на стримування надмірної запальної відповіді (Singh S. et al., 2021). Враховуючи це, рекомендації робочої групи з лікування COVID‑19 Центру профілактики та контролю хвороб США рекомендують добавки цинку як допоміжне лікування (de Faria Coelho-Ravagnani C. et al., 2021; Calder P. C. et al., 2021; CDC, 2021).
В експериментальному дослідженні S. R. Gordon та S. Vaishnava (2020) добавки сульфату цинку до раціону лабораторних мишей спричинило суттєві зміни складу мікробіоти, а також зниження кількості й активності Т‑хелперів‑17. Натомість кількість Т‑регуляторних клітин та інтерлейкіну‑10 залишилась незмінною. У другій частині досліду науковці пересадили мікробіом мишей, які отримували цинк, тваринам зі стерильним кишечником, що також зумовило зниження кількості й активності Т‑хелперів‑17. Таким чином, збільшення вмісту цинку у раціоні впливає не лише на виживаність і ступінь патогенності кишкової мікробіоти, а й на її імунний потенціал, протидіючи надмірній імунній відповіді.
Ще одне експериментальне дослідження показало, що збагачені цинком пробіотики здатні покращувати ріст, антиоксидантний статус, імунну функцію та морфологічні характеристики лабораторних щурів, вирощених в умовах теплового стресу. Включення в раціон тварин комбінації цинку та пробіотиків достовірно підвищувало вміст глутатіону й активність глутатіонпероксидази та супероксиддисмутази, водночас знижуючи рівень малонового діальдегіду. Крім того, застосування комплексної добавки цинк + пробіотики відновлювало баланс про- та протизапальних цитокінів, підвищуючи концентрацію інтерлейкінів 2, 6 та інтерферону γ на тлі зниження інтерлейкіну‑10. Забарвлення тканин кишечнику гематоксилін-еозином виявило, що цинк і пробіотики сприяли збільшенню висоти кишкових ворсинок та загальної товщини кишкової стінки, тобто зміцненню кишкового бар’єра.
Кишкова мікробіота також бере участь у підтриманні місцевого імунітету слизових оболонок, у т. ч. визначає формування набутого імунітету на оральні вакцини (Valdezi Y. et al., 2014). R. P. Lazarus і співавт. (2018) рандомізували 620 немовлят віком 5 тижнів до рандомізованого подвійного сліпого плацебо-контрольованого дослідження, покликаного встановити роль цинку та пробіотиків в імуногенності ротавірусної вакцини, яка призначається орально у віці 6 та 10 тижнів. Первинною кінцевою точкою виступала сероконверсія – ознака успішної вакцинації, яку визначали за наявністю специфічних імуноглобулінів класу IgA у кількості ≥20 Од/мл у раніше серонегативних немовлят або за підвищенням умісту цих імуноглобулінів учетверо. Сероконверсія відбулася в 39,4% дітей, які отримували пробіотики та цинк, у 30,9% дітей, які отримували лише пробіотик, у 28,0% дітей, які отримували лише цинк та у 27,4% дітей, які отримували плацебо. Отримані дані підтверджують синергетичну дію цинку та пробіотиків на імунітет й обґрунтовують потребу в подальших дослідженнях цієї комбінації як методу підвищення ефективності вакцинацій.
Експериментальні дослідження також показали, що мікробіота та продуковані нею метаболіти, наприклад бактеріальні ліпополісахариди, здатні протидіяти реплікації вірусів у кишечнику (Pfeiffer J. K., Virgin H. W., 2016). Пробіотики мають потенціал «перебудовувати» кишкову мікробіоту та вивільняти продукти життєдіяльності, які безпосередньо взаємодіють із лімфоїдною тканиною (Praharaj І. et al., 2015).
Враховуючи вищеописаний синергізм цинку з пробіотиками, можна припустити, що ця комбінація чинитиме потужніший сприятливий вплив на стан імунітету, ніж кожен із компонентів у вигляді монотерапії. Ця гіпотеза знайшла підтвердження в літературних даних. Так, у квазіекспериментальному рандомізованому дослідженні Z. Setiyaningrum і співавт. (2016) вивчався вплив комбінованої добавки цинку та пробіотиків на рівні лімфоцитів і моноцитів та на відношення кількості нейтрофілів до кількості лімфоцитів у пацієнтів із легеневим туберкульозом. У цього контингенту хворих побічні ефекти протитуберкульозних препаратів значною мірою порушують мікробіоту, несприятливо впливаючи на процеси одужання та імунної відповіді. Через 4 тижні застосування добавки в групі лікування спостерігалося зростання кількості лімфоцитів на тлі зменшення кількості моноцитів і зниження співвідношення нейтрофіли/лімфоцити. Найпотужнішим був вплив комбінації цинк + пробіотики на кількість лімфоцитів, яка зросла на 12,8% від вихідного рівня. Автори зробили висновок, що призначення подібних добавок покращує стан імунної системи пацієнтів із туберкульозом, впливаючи на баланс різних популяцій клітин-ефекторів імунітету.
Дієтична добавка Селфік Цинк («Геолік Фарм Маркетинг Груп», Україна) може бути рекомендована як додаткове джерело життєздатних бактерій та цинку до раціону харчування. Селфік Цинк містить молочнокислі бактерії (Lactobacіllus acіdophіlus), непатогенні ентерококи (Streptococcus thermophіlus), біфідобактерії (Bіfіdobacterіum bіfіdum, B. longum), а також цинк. Пробіотичні бактерії, які входять до складу Селфік Цинк, є облігатними для кишечнику людини і складають 95-96% загальної маси мікробіому.
Селфік Цинк застосовується з метою регуляції мікрофлори кишечнику та запобігання появі ААД; для поліпшення частоти дефекації та консистенції випорожнень у людей з частими закрепами, в т. ч. за синдрому подразненого кишечнику; при профілактиці дисбактеріозу на тлі інфекційних гастроентеритів бактеріальної або вірусної природи; для запобігання рецидивам у пацієнтів із хронічними запальними захворюваннями кишечнику (хвороба Крона, виразковий коліт тощо); для усунення дисбактеріозу в пацієнтів із частими алергіями та/або атопічними захворюваннями; в разі частих кишкових коліків, діapeї мандрівників і для зміцнення імунітету.
Однією із ключових передумов ефективності пробіотичного препарату є показник відновлюваності (приживлюваності) бактерій препарату в кишечнику. При виробництві Селфік Цинку застосовується інноваційна технологія ощадливої ліофілізації та кріопротекції, яка зберігає до 6% вологи у мікробному біоконцентраті, за рахунок чого відновлюваність бактерій у кишечнику підвищується на 65%. Крім того, особливі умови транспортування та зберігання Селфік Цинк (при температурі 2-6 °C), а також короткий термін зберігання препарату (до 12 міс) забезпечують зберігання життєздатності пробіотичних бактерій у його складі.
Таким чином, важливими перевагами дієтичної добавки Селфік Цинк є збереження життєздатності мікробіологічного субстрату в цьому засобі, а також наявність цинку, який діє синергетично із пробіотиками, зміцнюючи слизову оболонку кишечнику, покращуючи її бар’єрну функцію та посилюючи місцевий імунітет.