25 лютого, 2021
Раннє призначення бромгексину зменшує смертність при COVID‑19
Захворювання, спричинене коронавірусом SARS-CoV‑2, характеризується різноманітністю варіантів перебігу – від асимптомного носійства чи помірно виражених проявів інфекції дихальних шляхів до критичного стану, що зумовлений респіраторним дистрес-синдромом і гіперактивацією імунної відповіді. Надмірне виділення маси прозапальних цитокінів (т. зв. цитокіновий шторм) – один з основних механізмів, який спричиняє погіршення перебігу COVID‑19 [1, 2]. Для лікування COVID‑19 вивчалися численні засоби: протималярійні, противірусні, зокрема анти-ВІЛ-препарати, стероїдні гормони, проте результати досліджень були здебільшого нейтральними чи виявляли неприйнятні побічні ефекти. До сьогодні не було жодного засобу з доведеною здатністю знижувати смертність пацієнтів із COVID‑19.
Вірус SARS-CoV‑2 прикріплюється до рецептора ангіотензинперетворювального ферменту на поверхні клітин організму хазяїна, після чого є два шляхи проникнення всередину клітини – ендоцитоз і без ендоцитозу. Сучасні коронавіруси використовують переважно шлях без ендоцитозу, що контролюється трансмембранною сериновою протеазою TMPRSS2 [3]. Інгібітори цього шляху можуть бути перспективними засобами для лікування COVID‑19 [4]. Серед відомих молекул зі здатністю пригнічувати TMPRSS2 можна виокремити бромгексин (рис.), що має достатньо високий об’єм розподілу в легеневій тканині [5]. Бромгексину гідрохлорид – добре відомий безрецептурний препарат, який застосовується як муколітичний засіб. Нещодавно іранські автори K. Ansarin і співавт. [6] опублікували перше клінічне дослідження ефективності та безпеки бромгексину при лікуванні пацієнтів із пневмонією COVID‑19, в якому отримали вражаючі результати зменшення смертності, потреби в інтенсивній терапії та механічній вентиляції легень.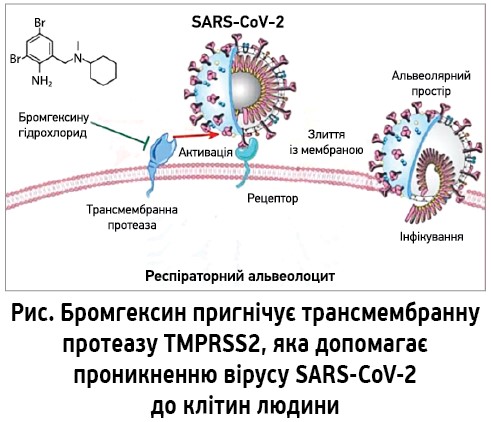
Матеріали та методи
Відкрите рандомізоване клінічне дослідження проводилося на базі університетської клініки. Набір пацієнтів здійснювався з 18 квітня по 19 травня 2020 року. Діагноз коронавірусної пневмонії установлював сертифікований пульмонолог, базуючись на клінічних симптомах та ознаках, а також на картині комп’ютерної томографії легень, якщо вона відповідала типовим ознакам COVID‑19. Хоча тестування методом полімеразної ланцюгової реакції було доступним на той час, результат тесту не був обов’язковим для залучення до випробування, оскільки через затримку очікувалася висока частка хибнонегативних результатів.
Відповідно до критеріїв включення пацієнтів рандомізували у співвідношенні 1:1 на дві групи – дослідну та контрольну. Хворі контрольної групи отримували лікування згідно з Іранським національним протоколом COVID‑19 й актуальними на той час настановами з найкращої практики. Зокрема, їм призначали гідроксихлорохін дозою 200 мг/день упродовж 2 тиж на додачу до підтримувальної та симптоматичної терапії. У дослідній групі додатково до стандартної терапії пацієнти приймали бромгексин по 8 мг 3 р/день упродовж 2 тиж після рандомізації.
Первинними кінцевими точками ефективності були частота переведень до відділення інтенсивної терапії (ВІТ), потреба в механічній вентиляції легень і 28-денна смертність. Вторинні клінічні наслідки, що оцінювалися в цьому дослідженні, – клінічне покращення (за такими симптомами, як лихоманка, задишка, слабкість), покращення лабораторних показників, зокрема С-реактивного білка (СРБ), лактатдегідрогенази (ЛДГ), співвідношення нейтрофіли/лімфоцити та тривалість перебування в стаціонарі. Клінічне покращення визначали як полегшення симптомів до такого рівня, що давав змогу виписати пацієнта та продовжувати лікування амбулаторно. Клінічні симптоми оцінювалися лікарем, якому не було відомо, до котрої групи належить пацієнт.
Щодня всім хворим вимірювали сатурацію крові киснем, а за потреби призначали рентгенографію грудної клітки. Критеріями виписки додому на самоізоляцію були клінічна стабільність і сатурація ≥90% при диханні кімнатним повітрям. Загальна тривалість спостереження становила 28 днів. Критерії переведення до ВІТ – погіршення респіраторного дистресу за оцінкою лікаря, нестабільна гемодинаміка, що потребувала призначення вазопресорних засобів, сатурація крові киснем <85%, що не покращувалася при диханні киснем із низькою швидкістю потоку.
Результати
Популяція дослідження налічувала 78 пацієнтів із діагнозом пневмонії COVID‑19, яких порівну розподілили в дослідну та контрольну групи. Усі хворі отримували призначене лікування й без передчасного вибування завершили участь у випробуванні. За демографічними та клінічними характеристиками дослідна й контрольна групи не мали суттєвих відмінностей. Середній вік у дослідній групі становив 58,4±13,7 року, в контрольній – 61,1±16,1 року. Чоловіки становили 54,4% популяції. Групи не відрізнялися за поширеністю коморбідних станів, як-от цукровий діабет і гіпертензія, а також за затримкою від появи симптомів до госпіталізації, що становила 7,7±4,1 дня в дослідній групі та 8,3±5,8 дня в контрольній групі (p=0,632). Індекс маси тіла й оцінки за шкалою APACHE в обох групах були майже однаковими.
Первинні клінічні наслідки
Значиму різницю було отримано в показниках 28-денної смертності: в дослідній групі вижили всі, тоді як у контрольній 5 пацієнтів (12,8%) померли (p=0,027). У дослідній групі двох хворих (5,1%) перевели до ВІТ, у контрольній групі таку потребу мали 11 пацієнтів (28,2%). Ця різниця також була статистично значимою (p=0,006). У дослідній групі механічну вентиляцію легень проводили 1 пацієнту (2,6%), а в контрольній – 9 хворим (23,1%) зі статистично значимою різницею (p=0,007).
Вторинні клінічні наслідки
За більшістю вторинних критеріїв ефективності було отримано значимі відмінності між групами. Покращення основних респіраторних симптомів, як-от кашель і задишка, впродовж 2 тиж відзначалося в обох групах, але в дослідній групі після лікування задишка залишалася в 3,4% пацієнтів, а в контрольній – у 48,3% (p≤0,001); кашель – відповідно в 6,9 та 40,0% випадків (p=0,003). Про залишкову слабкість повідомили 6,9% хворих дослідної групи та 34,5% пацієнтів контрольної (p=0,010). На початку випробування не було значимої різниці між групами за такими симптомами, як лихоманка, головний біль, а також за симптомами з боку шлунково-кишкового тракту. У пацієнтів, які отримували бромгексин, порівняно з контрольною групою, відзначалося покращення лабораторних показників: ЛДГ (363,2±83,6 vs 445,3±115,2; p=0,056), співвідношення нейтрофіли/лімфоцити (1,7 (1,0) vs 3,0 (6,3); p=0,052) та СРБ (0 vs 81,8%; p<0,001). Не відзначалося суттєвої різниці за тривалістю перебування в стаціонарі (від рандомізації до виписки), що становила 7,6±3,5 дня в дослідній групі та 8,1±5,5 дня в контрольній (p=0,587). Під час дослідження не зафіксовано серйозних побічних ефектів терапії.
Обговорення та висновки
Результати випробування K. Ansarin і співавт. підтвердили, що раннє призначення бромгексину по 8 мг 3 р/день істотно зменшує переведення до ВІТ, потребу в інтубації, механічній вентиляції легень і знижує смертність серед госпіталізованих пацієнтів із COVID‑19. Це дуже важливі результати, що мають пряму кореляцію з наслідками захворювання. Як показали клінічні спостереження, зазвичай стан пацієнтів із COVID‑19 швидко погіршується в перші 24 год після інтубації та початку механічної вентиляції легень, що корелює з несприятливими наслідками [7, 8]. Це може спонукати лікарів-реаніматологів ретельніше визначати показання до інтубації. Переведення до ВІТ, інтубацію та механічну вентиляцію слід розцінювати радше як перехід пацієнта в небезпечну зону, ніж як міст до одужання. Отже, будь-яке лікувальне втручання, що запобігає переведенню пацієнтів до ВІТ, може чинити значний вплив на смертність. Різниця в кількості померлих між групами бромгексину (0) та контрольною (5 хворих, що становило 12,8% групи) є красномовним індикатором ефективності цього лікарського засобу.
Що стосується впливу на симптоми захворювання (кашель, слабкість, задишка), то застосування бромгексину також виявилося ефективнішим порівняно зі стандартною терапією. Ця різниця може відображати обмежене ураження легеневої тканини в групі пацієнтів, які приймали бромгексин. Вірус SARS-CoV‑2 активує каскад вивільнення прозапальних цитокінів в організмі. СРБ є маркером запалення, що пропонується визначати для скринінгу за підозри на COVID‑19. У дослідженні K. Ansarin і співавт. до початку будь-якого лікування СРБ був позитивним у 87,9 та 91,7% пацієнтів у дослідній і контрольній групах відповідно. Повторний аналіз через 2 тиж після лікування виявив повну нормалізацію СРБ у 100% пацієнтів, які приймали бромгексин, тоді як у 83,3% хворих контрольної групи СРБ залишався позитивним. Цей результат яскраво демонструє ефективність впливу бромгексину на запалення при COVID‑19.
Отже, дослідження K. Ansarin і співавт. демонструє ефективність ранньої пероральної терапії бромгексином пацієнтів із COVID‑19, що проявлялося насамперед у покращенні виживаності. Крім того, терапія бромгексином пом’якшувала перебіг захворювання й у такий спосіб зменшувала потребу в інтенсивній терапії, інтубації та механічній вентиляції легень. Повна нормалізація СРБ після лікування відображає потужний протизапальний ефект препарату. Бромгексин – дешевий, доступний і безпечний безрецептурний лікарський засіб, який може бути застосований у більшості країн світу, зокрема в регіонах, віддалених від центрів спеціалізованої медичної допомоги. Незважаючи на малий розмір вибірки дослідження та досвід одного клінічного центру, результати випробування K. Ansarin і співавт. є дуже обнадійливими та можуть стати початком прориву в лікуванні COVID‑19. Звичайно, вони потребують підтвердження в більшому клінічному дослідженні. Утім, з огляду на темпи поширення пандемії та брак часу на пошук нових методів лікування, терапія бромгексином у найближчому майбутньому може змінити правила гри та стати дієвим чинником покращення прогнозу пацієнтів з інфекцією COVID‑19.
Список літератури знаходиться в редакції.
За матеріалами: Ansarin K. et al. Effect of bromhexine on clinical outcomes and mortality in COVID‑19 patients: a randomized clinical trial. Bioimpacts. 2020; 10 (4): 209-215.
Переклав з англ. Ігор Петренко
Медична газета «Здоров’я України 21 сторіччя» № 2 (495), 2021 р.



