29 березня, 2023
Холіну альфосцерат і нейроваскулярний юніт: нові обґрунтування клінічного застосування
Холіну альфосцерат (α-гліцерил-фосфорилхолін, α-GPC) – фізіологічний попередник ацетилхоліну, виявлений у складі головного мозку, вже кілька десятиліть успішно застосовують для лікування уражень мозку різної етіології. Основними клінічними показаннями для призначення α-GPC є лікування первинних і вторинних когнітивних порушень (наприклад, деменції, постінсультні порушення), а також черепно-мозкових травм у гострому періоді. Важливу роль у патогенезі та відновленні за цих патологій відіграє нейроваскулярний юніт (НВЮ) – анатомо-функціональна одиниця головного мозку, що складається з ендотелію, гліальних клітин і нейронів. В останніх дослідженнях продемонстровано, що позитивні ефекти на НВЮ є одним із механізмів дії α-GPC.
Що таке НВЮ?
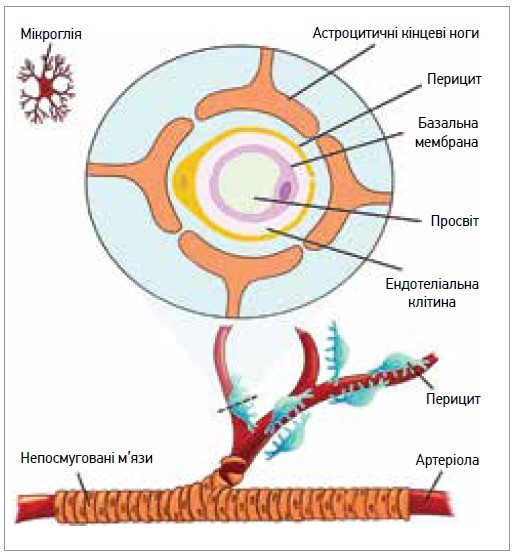
НВЮ (рис.) – це комплекс, що складається з нейронів, гліальних і судинних клітин, відповідає за інтеграцію змін у кровопостачанні з підвищенням або зниженням активності нейронів (Kim, Filosa, 2012). Судинні компоненти НВЮ включають ендотеліальні клітини, перицити і гладком’язові клітини судин, тоді як гліальні клітини містять астроцити, мікроглію та олігодендроглію. Кожен елемент тісно й взаємопов’язаний, що створює комплексну анатомічну та функціональну систему контролю церебрального кровотоку (Abbott, Friedman, 2012). Ацетилхолін і його попередник α-GPC відіграють активну роль у регуляції НВЮ. Ці молекули чинять захисну дію і запобігають загибелі нейронів, активації мікроглії, порушенню гематоенцефалічного бар’єра (ГЕБ), подальшому неврологічному ушкодженню (Inazu, 2019).
Рис. Елементи НВЮ
НВЮ підтримує оптимальне функціонування мікросередовища мозку, сприяючи виживанню нейронів та обробці інформації шляхом регулювання проникності ГЕБ і церебрального кровотоку. Ушкодження НВЮ спричиняє збій у роботі ГЕБ та порушення церебрального кровообігу, що може відповідати патофізіології нейродегенеративних захворювань. За такого стану надходження до мозку кисню та поживних речовин зменшується, як і елімінація нейротоксичних речовин (Sweeney et al., 2018). Щільні та міцні міжклітинні з’єднання мають вирішальне значення для контролю проникності ендотелію і допомагають підтримувати нормальну фізіологічну функцію мозку, обмежуючи надходження макромолекул, токсинів, небезпечних патогенів (Daneman, Prat, 2015).
Значення порушень НВЮ при поширених захворюваннях головного мозку
НВЮ відіграє провідну роль у патофізіології ішемічного інсульту завдяки впливу на ГЕБ, запальну імунну відповідь, виживанню нейронів та нейроваскулярному відновленню. Фармакотерапія, спрямована на НВЮ, сприяє реканалізації та покращує прогноз після інсульту (Wang et al., 2021).
Черепно-мозкова травма (ЧМТ) викликає тривалі структурні й функціональні зміни НВЮ, які спричиняють посттравматичну нейродегенерацію (Zhou et al., 2020). Для попередження цих змін одного впливу на нейрони (т. зв. чиста нейропротекція) недостатньо, адже необхідна захисна дія на всі клітини НВЮ (Lok et al., 2015).
При нейродегенеративних захворюваннях, як-от хвороба Паркінсона, хвороба Альцгеймера, судинна деменція та когнітивні дисфункції іншого ґенезу, відбувається порушення цілісності ГЕБ, мозкового кровотоку, виведення нейротоксинів – процесів, за які відповідає НВЮ (Yu et al., 2020; Nelson, 2022). Через це НВЮ розглядають як перспективну терапевтичну мішень для препаратів, які мають здатність впливати на всі його складові.
Позитивні ефекти α-GPC на НВЮ
Вплив на нейрони
В низці експериментальних досліджень вивчали здатність α-GPC попереджувати зміни нейронів при цереброваскулярних захворюваннях (Tomassoni et al., 2006, 2012; Tayebati et al., 2009, 2015). α-GPC забезпечував підвищення рівня вільного холіну і фосфоліпідів для синтезу ацетилхоліну та відновлював компоненти мембрани нервових клітин. Крім того, α-GPC підвищував рівень ацетилхоліну і його вивільнення в гіпокампі – частині головного мозку, що бере участь у формуванні емоцій та консолідації пам’яті (Sigala et al., 1992; Amenta et al., 2006).
Ці доклінічні дані пояснюють позитивні результати клінічних досліджень, у яких α-GPC застосовували при деменції у дорослих (Amenta et al., 2020).
У дослідженні Jeong Yu і співавт. (2022) призначення α-GPC протидіяло підвищенню рівня гормонів стресу, зменшувало втрату слуху та запобігало ушкодженню нейронів. Автори вважають, що цей ефект пов’язаний зі збільшенням холінацетилтрансферази та зменшенням нейрозапалення.
Вплив на астроцити
У НВЮ астроцити (астроглія) відіграють важливу роль у трофіці, підтримці та захисті нейронів, збереженні цілісності ГЕБ (Han et al., 2022). Астроцити огортають кровоносні судини кінцевими ніжками й опосередковують передання і рух молекул між нейронами та кровоносними судинами. В культурах астроцитів додавання α-GPC у різних концентраціях забезпечувало підвищення активності трансглутамінази – ферменту, необхідного для нормального функціонування цих клітин (Bramanti et al., 2008). У дослідженнях in vivo α-GPC зменшував астрогліоз і запобігав втраті нейронів (Tomassoni et al., 2006).
Вплив на мікроглію
Мікроглія – головні імунні клітини центральної нервової системи (ЦНС), схожі на периферичні макрофаги. α-GPC чинить протизапальні ефекти, запобігає надмірній активації мікроглії й відкладанню трансферину – амілоїдогенного білка, що бере участь у вікових когнітивних порушеннях (Kim J.H. et al., 2018; Matsubara, et al., 2018).
Вплив на ендотеліальні клітини та перицити
Важливою функцією ендотеліоцитів є виведення з ЦНС метаболітів і нейротоксичних субстанцій. Своєю чергою, перицити, котрі «огортають» ендотеліальні клітини, є ключовою ланкою ГЕБ, регулюють кровоток на капілярному рівні. В експериментальних дослідженнях було доведено, що холінвмісні фосфоліпіди підтримують тісні контакти між ендотеліоцитами і перицитами, підвищують рівні стовбурових клітин – попередників ендотеліоцитів, чинять нейропротекторний ефект у разі мозкової ішемії (Gutiérrez-Fernández et al., 2012).
Результати застосування α-GPC: приклади клінічних досліджень
L. Parnetti та співавт. (2001) проаналізували результати 13 клінічних досліджень за участю пацієнтів із гострим інсультом або із транзиторною ішемічною атакою. Призначення α-GPC покращувало функціональний стан і когнітивні функції, зменшувало неврологічний дефіцит і добре переносилося.
В італійському багатоцентровому дослідженні пацієнтам, які перенесли інсульт (n=2044), призначали α-GPC спочатку внутрішньом’язово в дозі 1000 мг/добу протягом 28 днів, потім перорально по 400 мг 3 р/добу протягом 5 міс. Тривале спостереження показало позитивний вплив на когнітивні функції та інші показники неврологічного статусу. Значне зменшення когнітивних порушень було виявлено в 71% пацієнтів. Відзначено хорошу переносимість препарату та низьку частоту побічних ефектів – лише в 2,14% випадків (Barbagallo Sangiorgi G. et al., 1994).
Ефективність α-GPC при легких або помірних когнітивних порушеннях було продемонстровано в рандомізованому плацебоконтрольованому дослідженні De Jesus Moreno Moreno (2003). Застосування α-GPC (1200 мг/добу протягом 180 днів) значно сповільнювало погіршення когнітивних функцій. α-GPC достовірно покращував усі оцінювані параметри – бали за шкалою оцінки психічного статусу (MMSE), шкалою оцінки геріатричної депресії (GDS), шкалою для аналізу поведінки (ADAS-Behav), шкалою загального клінічного враження (CGI) та кінцеві значення за шкалою ADAS-Total, тоді як у групі плацебо вони залишалися незмінними або погіршувалися.
У пацієнтів із ЧМТ різного ступеня тяжкості використання α-GPC у комплексній терапії дозволило досягти помітного поліпшення в когнітивній та психоемоційній сферах, що виражалося в підвищенні продуктивності, концентрації й стійкості уваги, зниженні рівня тривоги (Куцемелова І.Б. і співавт., 2016).
Гліатилін від компанії Italfarmaco – оригінальний італійський препарат α-GPC, що випускається у формі капсул і розчину для ін’єкцій. Основними показаннями для призначення Гліатиліну є гострий період тяжкої ЧМТ, вікові мозкові зміни та вторинні наслідки цереброваскулярної недостатності, тобто первинні й вторинні порушення розумової діяльності в людей літнього віку, котрі характеризуються порушенням пам’яті, сплутаністю свідомості, дезорієнтацією, зниженням мотивації та ініціативності, зниженням здатності до концентрації, а також змінами в емоційній сфері й сфері поведінки (емоційна нестабільність, дратівливість, байдужість до навколишнього середовища, псевдомеланхолія в людей літнього віку).
Останні дослідження доводять, що Гліатилін позитивно діє на всі компоненти НВЮ, отже, є патогенетичним засобом із комплексною нейропротекторною дією.
Підготував В’ячеслав Килимчук
Медична газета «Здоров’я України 21 сторіччя» № 4-5 (540-541), 2023 р.