24 серпня, 2023
Ускладнений перебіг вертеброгенної радикулопатії
Проблема вертеброгенної патології є актуальною як на території України, так і в глобальному масштабі. Вертеброгенна радикулопатія не лише суттєво впливає на якість життя пацієнтів, а й може зумовити серйозні соціально-економічні наслідки. Отже, систематичне дослідження клінічних випадків, пов’язаних із цією патологією, – цікава та важлива задача для медичних спеціалістів як в аспекті діагностики, так і в аспекті терапії.
Проблема вертеброгенної радикулопатії є актуальним і загальновизнаним явищем як в Україні, так і в світі. Згідно з даними Всесвітньої організації охорони здоров’я, хронічний біль у спині – один із найчастіших симптомів, характерних для вертеброгенної патології; спостерігається в >80% населення планети протягом їхнього життя, причому >540 млн осіб у всьому світі переживають цю патологічну симптоматику щороку [1]. Національне дослідження здоров’я населення України демонструє такі дані: понад половина українського населення має ті чи інші симптоми вертеброгенної патології, при цьому жінки зазнають таких проявів із більшою частотою, ніж чоловіки [2].
Вертеброгенна радикулопатія не лише чинить негативний вплив на якість життя людей, а й накладає серйозний тягар на соціально-економічний розвиток. Наприклад, зазначений стан суттєво погіршує продуктивність праці, спричиняє збільшення кількості втрачених робочих днів, підвищує потребу в медичних послугах [3]. Отже, вивчення клінічних випадків вертеброгенної радикулопатії завжди залишається актуальною і важливою задачею для клініцистів, що потребує глибокого розуміння в аспекті діагностики та лікування.
Клінічний випадок
Пацієнт Л., 68 років, звернувся до невролога для консультації через скарги на сильний дорсальний біль, що з’явився ≈3 міс тому та поступово прогресував. Біль, хоча і мав локалізацію в спинному відділі, демонстрував неоднозначну характеристику та часто іррадіював уздовж ділянки нижніх ребер по ходу міжреберних нервів, причому спостерігалося посилення больових відчуттів під час фізичної активності, а також під час кашлю або глибокого дихання.
Хворий працює в офісі, має незначні фізичні навантаження; додатково спостерігав відчуття «бігання мурашок» у нижньогрудному та поперековому відділах спини по обидва боки, що супроводжувалося посиленням болю. Ці симптоми зумовили значне зниження рухової активності та загальної якості життя. Крім того, пацієнт мав знижений апетит, що, за його словами, пов’язано з постійним больовим синдромом.
Після проведення ретельного збору анамнезу встановлено, що хворий має супутні патології, зокрема артеріальну гіпертензію, яка вже триває протягом 5 років і контролюється фармакологічно, а також страждає на ревматизм, через що регулярно отримує лікування. Крім того, за останні 4 роки двічі переніс перелом кісток.
Діагностика
Діагностичний алгоритм передбачав оцінку клінічної картини на основі даних неврологічного статусу. Під час паравертебральної пальпації у ділянці нижньо-грудного відділу спостерігалися виражені больові відчуття та м’язово-тонічне напруження (значення болю за ВАШ – 70 балів), а також позитивний симптом триніжка й виражені позитивні симптоми Нері, Вассермана, Мацкевича. Водночас пацієнт відчував парестезії у дерматомах Th12-L2 з обох боків. Рефлекси з рук не зазнали змін, з ніг були незначно підвищеними, зліва – дещо більшими. М’язова сила згідно з Оксфордською шкалою складає 3 бали на лівій нозі (рух проти сили гравітації за повної наявної амплітуди рухів) та становить 4 бали на правій нозі (рух проти сили гравітації за незначного опору). Спостерігався виражений позитивний характер симптому Штрюмпеля з обох боків. Абдомінальні та підошовні рефлекси з обох боків не викликаються. Наявна помірно виражена гіпестезія поверхневої чутливості по шкірі внутрішнього та переднього відділів стегна. Пацієнт також відзначав періодичні імперативні позиви до сечовипускання. Рівень інвалідизації згідно з індексом Бартел відображено в таблиці.
|
Таблиця. Оцінка інвалідизації пацієнта К. за індексом Бартел до початку лікування та реабілітації |
||
|
|
Вид діяльності |
Оцінка до початку лікування та реабілітації (індекс Бартел, бали) |
|
|
Прийом їжі |
10 |
|
|
Прийом ванни |
0 |
|
|
Персональна гігієна |
5 |
|
|
Одягання |
5 |
|
|
Контроль дефекації |
10 |
|
|
Контроль сечовипускання |
5 |
|
|
Користування туалетом |
5 |
|
|
Переміщення (з ліжка на крісло та назад) |
5 |
|
|
Здатність до пересування рівною площиною |
10 |
|
|
Подолання сходів |
5 |
|
Усього |
60 (помірна |
|
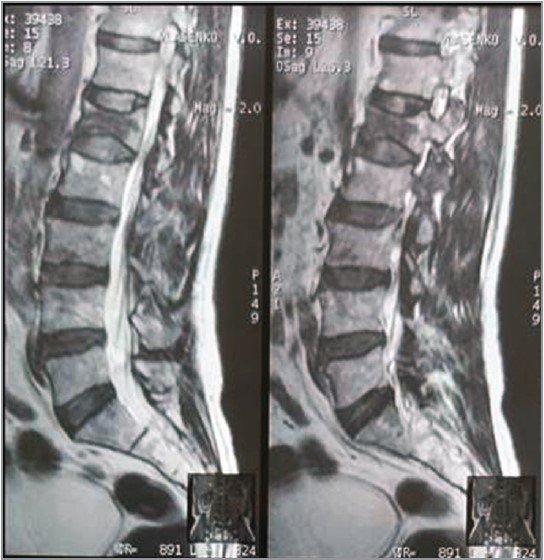
Необхідно підкреслити, що такий рівень інвалідизації переважно був обумовлений вираженим больовим синдромом і порушенням рухової функції, які виявили під час оцінки неврологічного статусу. Отже, саме соматичний дискомфорт і рухова дисфункція обмежували активність пацієнта Л., а також значною мірою спричиняли деградацію якості життя хворого. З метою уточнення клінічного діагнозу пацієнта спрямували для виконання магнітно-резонансної томографії (МРТ) хребта (рис. 1):
Рис. 1. Перелом хребця L1 із вираженою двобічною полірадикуломієлопатією
На МРТ візуалізується гіпоінтенсивне вогнище неправильної форми в ураженому та деформованому тілі хребця L1 без виражених ознак мієлопатії, проте зі значною двобічною компресією спинномозкових корінців на зазначених рівнях. Наявні ознаки остеопорозу різного ступеня у вигляді зменшення кісткової щільності в тілах хребців.
Після проведення детальної диференційної діагностики та виключення соматичної патології або онкологічних ускладнень, а також з урахуванням наявності в анамнезі червоних прапорців щодо ризику хронічних переломів (системне вживання стероїдних гормонів, системний остеопороз, часті переломи кісток) пацієнту встановлено клінічний діагноз патологічного перелому хребця L1 із вираженою двобічною вертеброгенною полірадикуломієлопатією.
Лікування
З урахуванням співвідношення супутніх патологічних станів, як-от остеопороз, імплементація хірургічного підходу на теперішньому етапі була виключена після консультації з командою нейрохірургів. Отже, ухвалено рішення акцентувати увагу на патогенетичному та симптоматичному лікуванні зі спрямуванням на корекцію хронічного больового синдрому та рухових розладів.
Механізми формування болю за дегенеративно-дистрофічних ушкоджень хребта (як-от остеохондроз із килами міжхребцевих дисків, спондилоз, спондилоартроз) можуть розрізнятися відповідно до локалізації причин гострого чи загострення хронічного больового синдрому. За радикулопатії у процесі беруть участь як нейропатичні, так і ноцицептивні механізми. Нейропатичний біль, який виникає унаслідок патологічного збудження нейронів у нервовій системі, має відмінності від звичайного болю, що походить від фізичного ушкодження організму. Зазвичай нейропатичний біль проявляється як алодинія або гіпералгезія, що з’являється внаслідок ураження чи хвороби соматосенсорної системи. Ця форма болю може мати центральний (пов’язаний з ураженням головного та спинного мозку) чи периферичний характер (пов’язаний з ураженням периферичних відділів нервової системи) [4].
Інтенсивність болю певною мірою залежить від початкового психоемоційного стану пацієнта. У випадках хворих із підвищеним рівнем тривожності, які страждають на вертеброгенний больовий синдром, за наявності часто повторюваних, але менш інтенсивних психогенних впливів і субклінічного типу дисфункції нервової системи не виникає відповідних умов для активації специфічних саногенетичних механізмів реагування й адаптації. У цій групі пацієнтів також може спостерігатися формування поведінки болісної відповіді зі суттєвим звуженням сфери життєвих інтересів та соціальної дезадаптації з проявами депресії [5].
Вплив механічної компресії на нервові стовбури зумовлює розвиток каскаду патологічних процесів в уражених нервах, який включає:
- порушення кровообігу та гіпоксію нерва, що виникає при порушенні постачання крові до нерва;
- збільшення проникності мієлінових оболонок, яке може спричинити їхню втрату та зниження ефективності передачі нервових імпульсів;
- розвиток дистрофічних змін у нервовій тканині, що може відбуватися внаслідок зниження постачання кисню та поживних речовин до нерва;
- збільшення фіброзу та зменшення розміру нерва, яке зазвичай відбувається при тривалій компресії або ушкодженні нерва;
- розвиток вторинних змін, що може включати збільшення кількості фібробластів, зміну складу екстрацелюлярної матриці та збільшення активності фагоцитів;
- розвиток рубцевої тканини, який виникає на місці ушкодження та може зумовити постійне ушкодження нерва.
В результаті ушкодження нервового стовбура порушується передача нервового імпульсу між нейронами й органами, які іннервуються ураженими нервами. Це спричиняє виникнення неврологічного дефіциту у вигляді порушення чутливої та рухової функцій і вегетативної іннервації у зазначених дерматомах, що потребує окремого підходу до ведення таких пацієнтів.
З огляду на те що больовий синдром у хворого мав переважно нейропатичний характер, а сам пацієнт наполягав на необхідності саме амбулаторного лікування, медичними засобами вибору щодо включення до терапевтичної схеми були таблетовані форми ліків – нестероїдні протизапальні препарати (мелоксикам 15 мг 1 р/добу 7 діб), парацетамол (500 мг 2 р/день упродовж 3 днів), антиконвульсанти (прегабалін 75 мг 2 р/день), антидепресанти (флуоксетин 20 мг 1 р/день). Додатково з метою активізації репаративних процесів в уражених корінцях та для позитивного впливу на відновлення рухової функції пацієнту Л. було призначено іпідакрину гідрохлорид (Нейромідин®) за такою схемою: в перші 10 днів в/м 1 мл 1,5% розчину 1-2 р/день, згодом – перорально у вигляді таблеток у дозі 20 мг (1 таблетка) 3 р/день протягом 30 днів.
Іпідакрину гідрохлорид (Нейромідин®) – препарат, що має біологічно вигідну комбінацію двох молекулярних ефектів – блокада калієвої проникності мембрани й інгібування холінестерази. Блокада калієвої проникності мембрани відіграє вирішальну роль [6] та зумовлює насамперед продовження реполяризаційної фази потенціалу дії збудженої мембрани, підвищення активності пресинаптичного аксона, що спричиняє збільшення входу іонів кальцію до пресинаптичної терміналі, а це, своєю чергою, зумовлює збільшення викиду медіатора до пресинаптичної щілини в усіх синапсах. Підвищення концентрації медіатора в синаптичній щілині сприяє сильнішій стимуляції постсинаптичної клітини внаслідок медіатор-рецепторної взаємодії. У холінергічних синапсах інгібування холінестерази стає причиною ще більшого накопичення нейромедіатора в синаптичній щілині, а також посилення функціональної активності постсинаптичної клітини (скорочення, проведення збудження) [6]. Нейромідин® посилює вплив ацетилхоліну, адреналіну, серотоніну, гістаміну, окситоцину на гладкі м’язи.
Загалом Нейромідин® має такі фармакологічні ефекти:
- стимуляція і відновлення нервово‑м’язової передачі;
- відновлення проведення імпульсу в периферичній нервовій системі після блокади різними агентами (травма, запалення, дія місцевих анестетиків, деяких антибіотиків, калію хлориду, токсинів тощо);
- посилення скоротливості гладком’язових органів;
- специфічно помірно стимулює центральну нервову систему з окремими проявами седативного ефекту;
- поліпшення пам’яті та здатності до навчання;
- аналгетична дія.
Аналгетичний ефект підтверджено під час проведення рандомізованого контрольованого дослідження ІІ фази. Контрольне дослідження, опубліковане в 2019 році, показало, що додавання іпідакрину до традиційної терапії тунельного синдрому зумовило регрес нейропатичного больового синдрому. Кількісно регрес оцінювали за допомогою шкал VAS, DN4, шкали виявлення болю, показники яких достовірно знизилися (p<0,01) [7].
Особливістю Нейромідину є те, що він не чинить тератогенної, ембріотоксичної, мутагенної, канцерогенної, алергізувальної, імунотоксичної дії, а також не впливає на ендокринну систему. Саме завдяки зазначеним позитивним ефектам вирішено імплементувати до схеми лікування препарат Нейромідин®, що надало змогу отримати позитивну динаміку в перебігу захворювання нашого пацієнта.
Результати лікування
Пацієнт проходив лікування за цією схемою в стаціонарі протягом 21 дня. Вже на 14-й день спостерігався виражений позитивний ефект у вигляді зменшення вираженості больового синдрому на 35 балів за шкалою ВАШ. Після завершення 21-денного періоду біль у пацієнта Л. зменшився до 20 балів за шкалою ВАШ і продовжував утримуватися на цьому рівні. Крім того, в неврологічному статусі, незважаючи на неможливість корекції органічної патології, спостерігалася позитивна динаміка у вигляді зменшення вираженості парестезій, гіпестезії, регресу частоти імперативних позивів до сечовипускання та наростання обсягу рухів і м’язової сили в обох нижніх кінцівках до 5 балів за Оксфордською шкалою (нормальна сила м’язів).
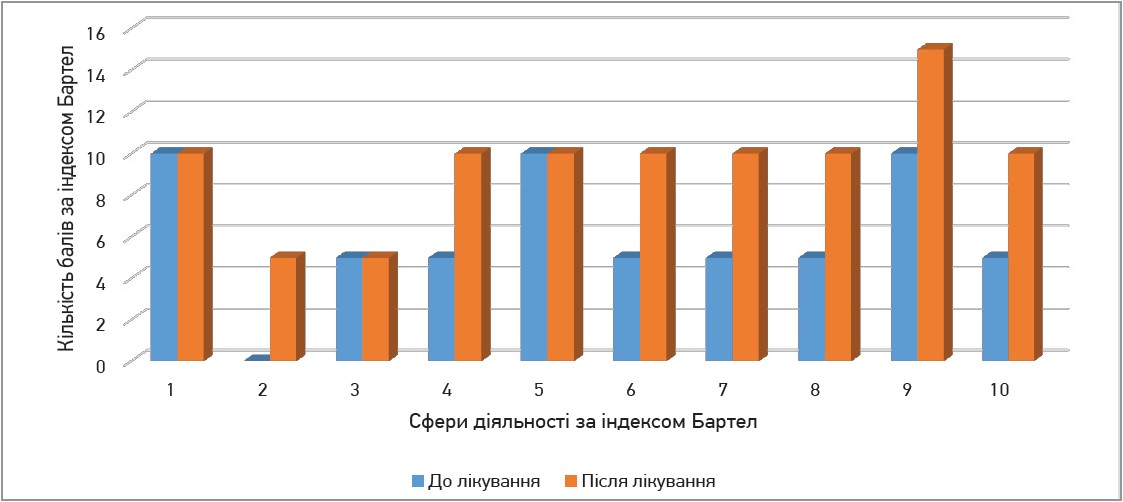
Через зменшення вираженості больового синдрому та регрес рухових розладів також на момент огляду спостерігалося значне зниження рівня інвалідизації пацієнта із 60 до 95 балів за індексом Бартел (рис. 2).
Рис. 2. Рівень інвалідизації пацієнта Л. до та після лікування
Очевидно, що регрес рівня інвалідизації та наростання балів за індексом Бартел спостерігалися майже в усіх сферах життєдіяльності, що підкреслює значний вплив вертеброгенної радикулопатії на здатність до самообслуговування і на загальні показники якості життя.
Обговорення
Зазвичай у таких хворих, як пацієнт Л., у котрого тривалість больового синдрому перевищувала 30 днів, зменшення болю навіть на 10 балів за ВАШ становить значуще досягнення, яке відчутно покращує якість життя хворого. Проте в нашому випадку досягнення такого результату було можливим лише після проведення комплексної патогенетичної терапії тривалістю 21 день, включаючи застосування антиконвульсантів, антидепресантів, антихолінестеразних препаратів. З високою імовірністю можна припустити, що це обумовлено не лише стійкими органічними факторами, які спричинили больовий синдром, а й хронізацією самого болю на тлі сформованого патогенетичного механізму, що включає розвиток т. зв. больової поведінки в пацієнта [4, 5].
Виражений клінічний ефект від використання Нейромідину, на нашу думку, пов’язаний з його впливом на всі складові механізми формування порушення іннервації тканин унаслідок вертеброгенної патології. Використання іпідакрину (Нейромідин®) завдяки блокаді калієвої проникності мембрани зумовлює насамперед продовження реполяризаційної фази потенціалу дії збудженої мембрани та підвищення активності пресинаптичного аксона, що фактично забезпечує посилення імпульсації ураженими корінцями, а також їхнє відновлення [6]. Крім того, підвищення концентрації ацетилхоліну в синаптичній щілині сприяє вираженішій стимуляції постсинаптичної клітини, в т. ч. не лише нейрона, а й м’язової тканини, що покращує тонус м’язів, зменшує ризик атрофії і сприяє відновленню порушеної рухової функції [6].
Висновки
Використання препарату Нейромідин® у контексті коригування патологічних симптомів, що супроводжують ускладнений перебіг вертеброгенної радикулопатії, асоціювалося з вираженою позитивною динамікою, внаслідок чого вдалося знизити рівень інвалідизації, а також значно покращити якість життя пацієнтів навіть з таким тяжким органічним ураженням, як, наприклад, хронічний перелом хребця. Отримані результати цього клінічного випадку потребують подальшого глибокого аналізу та проведення подальших досліджень з науковою метою, спрямованою на імплементацію новаторських підходів до корекції наслідків тяжкої вертеброгенної радикулопатії у пацієнтів.
Список літератури знаходиться в редакції.