30 жовтня, 2021
Майстер-клас до Всесвітнього дня боротьби з лімфомами: можливості підвищення ефективності терапії при ДВКЛ
 Світова онкологічна спільнота сьогодні активно вивчає нові молекулярні підтипи дифузної В-клітинної лімфоми (ДВКЛ) та розробляє перспективні лікарські засоби, які дозволили б підвищити ефективність терапії ДВКЛ як у 1-й лінії, так і при наявності рецидиву чи рефрактерності. З метою ознайомлення українських онкологів з останніми даними клінічних досліджень 23 вересня в онлайн-режимі було проведено науковий непромоційний майстер-клас «До Міжнародного дня обізнаності про лімфоми: новини та надії для наших пацієнтів».
Світова онкологічна спільнота сьогодні активно вивчає нові молекулярні підтипи дифузної В-клітинної лімфоми (ДВКЛ) та розробляє перспективні лікарські засоби, які дозволили б підвищити ефективність терапії ДВКЛ як у 1-й лінії, так і при наявності рецидиву чи рефрактерності. З метою ознайомлення українських онкологів з останніми даними клінічних досліджень 23 вересня в онлайн-режимі було проведено науковий непромоційний майстер-клас «До Міжнародного дня обізнаності про лімфоми: новини та надії для наших пацієнтів».
.jpg) Із вступним словом та доповіддю «15 вересня – Міжнародний день обізнаності про лімфоми» виступила завідувачка науково-дослідного відділення хіміотерапії гемобластозів та ад’ювантних методів лікування Національного інституту раку (м. Київ), доктор медичних наук, професор Ірина Анатоліївна Крячок.
Із вступним словом та доповіддю «15 вересня – Міжнародний день обізнаності про лімфоми» виступила завідувачка науково-дослідного відділення хіміотерапії гемобластозів та ад’ювантних методів лікування Національного інституту раку (м. Київ), доктор медичних наук, професор Ірина Анатоліївна Крячок.
– За даними Національного канцер-реєстру за 2019-2020 рр., в Україні перебувають на обліку близько 60 тис. пацієнтів з лімфопроліферативними захворюваннями, з них 30 тис. хворі на лімфому Ходжкіна та неходжкінські лімфоми. При порівнянні даних Національного канцер-реєстру за 2009-2018 рр. та світових показників реєстру SEER (Surveillance, Epidemiology, and End Results) за 2018 р. можна відзначити, що в Україні захворюваність на неходжкінські лімфоми (НХЛ) та лімфому Ходжкіна залишається на стабільному рівні, однак рівень виживаності є нижчим, а смертності – вищим, ніж у світі. Проте в нашій країні відмічалося зростання 5-річної виживаності пацієнтів з лімфомою станом на 2017 р. при порівнянні з 2011 р., що свідчить у тому числі про покращення доступу українських хворих до сучасних ліків.
У більшості країн світу використовують механізм договорів керованого доступу, що є одним зі способів купити лікарські засоби для тяжкохворих через домовленість із виробником про спеціальні умови закупівлі. Нещодавно було прийнято Закон України № 4662 «Про внесення змін до Закону України «Про публічні закупівлі» та інших законів України щодо закупівель лікарських засобів за договорами керованого доступу», що запроваджує застосування договорів керованого доступу для розширення можливості забезпечення пацієнтів необхідними препаратами. Такі договори дозволять запровадити систему спеціальних цін при закупівлях та оплати за результат, що надасть можливість пацієнтам отримати найсучаснішу ефективну терапію. Крім того, було розроблено та внесено на розгляд Верховної Ради проєкт Закону України № 5736 «Про ліки зі співчуття». Прийняття цих документів дає змогу спростити механізм взаємодії з провідними світовими виробниками медичних препаратів, які готові надавати українським пацієнтам інноваційні ліки, що перебувають на етапі клінічних досліджень.
Отже, в епоху стрімкого розвитку фармацевтичного ринку варто шукати нові шляхи забезпечення українських пацієнтів інноваційними ліками для покращення їх виживаності та якості життя.
 Нові дані щодо прогностичних факторів при ДВКЛ і їх нових підтипів повідомив директор кафедри гематології, онкології та пульмонології Університетської лікарні в Мюнстері (Німеччина), професор Георг Ленц.
Нові дані щодо прогностичних факторів при ДВКЛ і їх нових підтипів повідомив директор кафедри гематології, онкології та пульмонології Університетської лікарні в Мюнстері (Німеччина), професор Георг Ленц.
– ДВКЛ характеризується не тільки гетерогенністю клінічних проявів, а й різним профілем генної експресії, що дозволило виділити два молекулярні підтипи хвороби – ABC та GCB. Однак відомі й більш рідкісні підтипи, наприклад, первинна медіастинальна ДВКЛ. Існує близько 10-15% ДВКЛ, які не можна віднести до ABC чи GCB підтипів. При ABC-підтипі виживаність є гіршою, що змушує науковців шукати нові агенти, які чинили б сильніший вплив на більш агресивні варіанти. Однією зі спроб підвищити ефективність терапії пацієнтів з ABC-підтипом ДВКЛ було додавання схеми R-CHOP до леналідоміду, що не виявилося ефективним (U. Vitolo et al., 2019). Інші спроби також виявилися невдалими, тому сьогодні наявність підтипів ABC чи GCB не впливає на тактику терапії, а R-CHOP залишається стандартом лікування ДВКЛ.
Однак вивчення нових підтипів продовжується. Так, було ідентифіковано нові молекулярні підтипи (MCD, N-1(NOTCH1), BN2, EZB) усередині підтипів ABC та GCB (R. Schmitz et al., 2018).
Гірша виживаність при застосуванні схеми R-CHOP сьогодні також характерна для пацієнтів з double-hit лімфомами, в яких відмічається перебудова гена MYC, високий ступінь проліферації та наявність високого ризику рецидиву з метастазуванням у центральну нервову систему. Крім того, у 3 з 12 таких випадків виявляли інші транслокації, а саме BCL2 чи t[14;18] (K.J. Savage et al., 2017). У дослідженні D. Ennishi та співавт. (2019) було показано, що у пацієнтів з лімфомами зі спеціальною міткою (double-hit signature) спостерігався гірший результат лікування порівняно з хворими на лімфоми, в яких не було цієї мітки.
Останніми роками зростає інтерес до вимірювання циркулюючої пухлинної ДНК у плазмі крові як прогностичного фактора. На основі такого вимірювання D.M. Kurtz та співавт. (2018) виділили групи пацієнтів із ранньою та вираженою молекулярною відповідями. Виживаність без подій у групі хворих із вираженою молекулярною відповіддю значно відрізнялася від такої у групі пацієнтів з ранньою відповіддю, що можна використовувати під час моніторингу лікування. Вимірювання циркулюючої пухлинної ДНК також можна застосовувати як початковий орієнтир при плануванні терапії, оскільки у пацієнтів з вищим циркулючим рівнем відмічалася гірша виживаність (A. Herrera et al., 2020).
Таким чином, різні молекулярні особливості лімфоми визначають прогноз при ДВКЛ, що слід враховувати при плануванні терапії.
 Про нове у стандартах лікування ДВКЛ розповіли доктор медичних наук, професор Ірина Анатоліївна Крячок і завідувачка Центру гематології, хіміотерапії гемобластозів та трансплантації кісткового мозку Клінічної лікарні «Феофанія» Державного управління справами Лариса Василівна Михальська.
Про нове у стандартах лікування ДВКЛ розповіли доктор медичних наук, професор Ірина Анатоліївна Крячок і завідувачка Центру гематології, хіміотерапії гемобластозів та трансплантації кісткового мозку Клінічної лікарні «Феофанія» Державного управління справами Лариса Василівна Михальська.
Л.В. Михальська зосередила увагу учасників заходу на останніх результатах наукових досліджень щодо підвищення ефективності 1-ї лінії терапії ДВКЛ.
– Золотим стандартом лікування ДВКЛ є режим R-CHOP (циклофосфамід + доксорубіцин + вінкристин + преднізолон + ритуксимаб), при застосуванні якого 3-річна виживаність без прогресування (ВБП) складає 66,9% (P. Feugier et al., 2005). Проте у клінічній практиці зустрічаються й хворі з дуже агресивним перебігом ДВКЛ та наявністю факторів ризику, що свідчить про потребу у вдосконаленні теперішніх стандартів (U. Vitolo et al., 2017).
В одному з досліджень порівнювали ефективність схем R-CHOP та DA-EPOCH-R (етопозид + преднізолон + вінкристин + циклофосфамід + доксорубіцин + ритуксимаб) у 1-й лінії терапії ДВКЛ. За показниками 3- та 5-річної загальної виживаності (ЗВ) не виявлено переваг схеми DA-EPOCH-R, крім того, в учасників дослідження, яких лікували за цією схемою, кількість небажаних побічних ефектів була більшою (W.H. Wilson et al., 2016; N.L. Bartlett et al., 2019). Інтенсифікація режимів хіміотерапії у 1-й лінії при ДВКЛ також не супроводжувалася покращенням ЗВ порівняно зі стандартною терапією (D. Cunningham et al., 2013; C. Recher et al., 2011). Загалом протягом тривалого часу спроби підвищити ефективність схеми R-CHOP у 1-й лінії порівняно зі стандартною терапією шляхом інтенсифікації хіміотерапії, оптимізації анти-CD20 терапії, використання підтримуючої терапії та застосування нових молекул у поєднанні з R-CHOP не дали бажаного результату у пацієнтів з ДВКЛ (A. Goy, 2017).
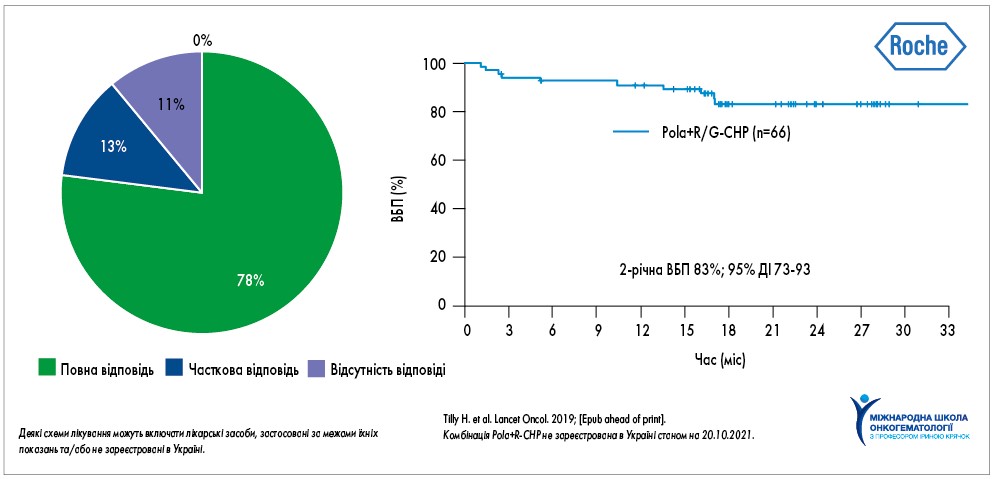
Однак у клінічному дослідженні II фази GO29044, в якому порівнювали схеми Pola (полатузумабу ведотин) +R-CHP (ритуксимаб + циклофосфамід + доксорубіцин + преднізолон) і Pola+G-CHP (обінутузумаб + циклофосфамід + доксорубіцин + преднізолон) у пацієнтів групи високого ризику, було встановлено, що при застосуванні схеми Pola+R/G-CHP 12-місячна ВБП та ЗВ складали 91 та 94% відповідно (рис. 1). Крім того, у разі призначення режиму Pola+R-CHP 2-річна ВБП становила 83% (95% довірчий інтервал – ДІ – 73-93; рис. 2), а частота повної та часткової відповіді, підтвердженої позитронно-емісійною комп’ютерною томографією (ПЕТ-КТ), – 78 та 13% відповідно; тільки в 11% хворих не досягнута відповідь на терапію. У цьому дослідженні також відмічали переваги застосування Pola+R-CHP у хворих групи високого ризику з double-expressor лімфомами (з експресією MYC та BCL2) та у пацієнтів з лімфомами ABC-підтипу. Побічні реакції, що розвивалися при застосуванні Pola+R/G-CHP, переважно були представлені гематологічними порушеннями та периферичною нейропатією, які були керованими, необхідність у відміні чи зниженні дози полатузумабу ведотину не виникала (H. Tilly et al., 2019).
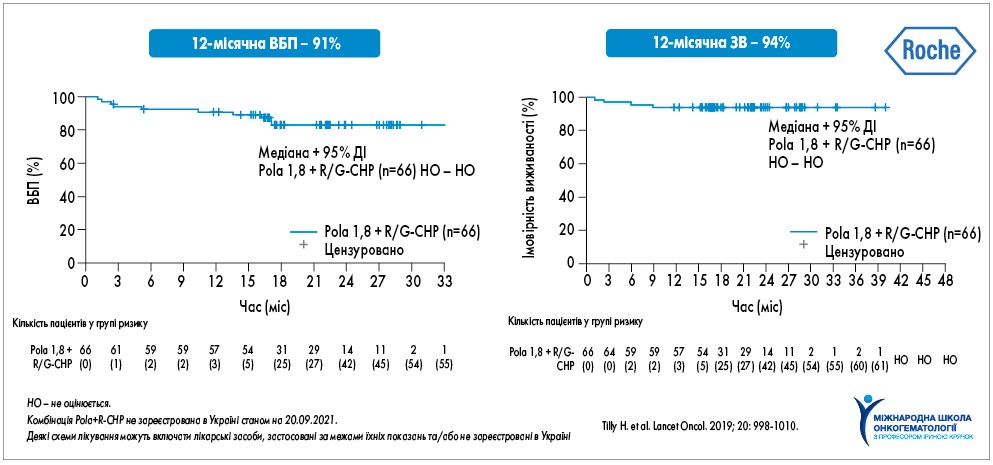 Рис. 1. Клінічна ефективність схеми Pola+R/G-CHP у 1-й лінії терапії ДВКЛ
Рис. 1. Клінічна ефективність схеми Pola+R/G-CHP у 1-й лінії терапії ДВКЛ
Рис. 2. Результати застосування Pola+R-CHP у дослідженні Ib/II фази у 1-й лінії терапії ДВКЛ
Тобто у дослідженні II фази було показано, що застосування полатузумабу ведотину – першого у своєму класі кон’югату антитіло-лікарський засіб до CD79b, який експресується на пухлинних клітинах у пацієнтів з ДВКЛ, – у поєднанні з R-CHP у 1-й лінії терапії характеризується високою клінічною активністю та керованим профілем безпеки порівняно з R-CHOP.
У грудні 2021 р. будуть опубліковані результати дослідження III фази POLARIX, в якому порівнюють ефективність схем Pola+R-CHP + вінкристин (плацебо) та R-CHOP+Pola (плацебо), які, можливо, змінять теперішні стандарти 1-ї лінії терапії ДВКЛ. У цьому дослідженні брали участь і українські клініки. За попередніми даними, у дослідженні POLARIX у раніше не лікованих пацієнтів з ДВКЛ вперше відмічалося покращення ВБП у 1-й лінії терапії порівняно зі стандартним лікуванням (R-CHOP). Це надзвичайно важливе досягнення, оскільки майже у 40% таких хворих сьогодні спостерігається рецидив.
І.А. Крячок детальніше зупинилася на останніх світових даних щодо лікування пацієнтів з рецидивуючою чи рефрактерною (р/р) ДВКЛ.
– Останніми роками у клінічних дослідженнях з метою оцінювання відповіді на терапію використовують ПЕТ-КТ. У дослідженні K. Kitajima та співавт. (2019) зазначалося про прогностичне значення цього методу дослідження після 3 курсів терапії. Було показано, що у хворого, в якого за даними проміжної ПЕТ-КТ зафіксовано повну відповідь, що зберігалася після 6 циклів терапії, рецидивів не відмічалося близько 3,82 року. Однак якщо на проміжній ПЕТ-КТ візуалізувалася наявність резидуальної маси, то у таких пацієнтів спостерігався несприятливий перебіг захворювання, а саме – прогресування протягом 1 року. Таким чином, за допомогою проведення проміжної ПЕТ-КТ у хворих на ДВКЛ можна визначити імовірність подальшого прогресування захворювання.
Згідно з рекомендаціями Національної онкологічної мережі США (National Comprehensive Cancer Network, NCCN) пацієнтів з р/рДВКЛ слід розглядати як кандидатів на аутологічну трансплантацію гемопоетичних стовбурових клітин (аутоТГСК). Однак не всі хворі є кандидатами на аутоТГСК через наявність коморбідної патології, похилий вік і відповідь на сальвадж-терапію. У рекомендаціях Європейського товариства медичної онкології (European Society for Medical Oncology) зазначено, що як сальвадж-режим можна використовувати схеми R-DHAP (ритуксимаб + дексаметазон + цитарабін + цисплатин), R-ICE (ритуксимаб + іфосфамід + карбоплатин + етопозид) та R-GDP (ритуксимаб + гемцитабін + дексаметазон + цисплатин). У порівняльних дослідженнях з вивчення ефективності схем сальвадж-терапії не було встановлено певних переваг якоїсь із них, тому її вибір залежить від локальної практики центрів (C. Gisselbrecht et al., 2012).
Якщо пацієнти з р/рДВКЛ не є кандидатами на трансплантацію, 3- та 5-річна ЗВ цих хворих є низькою та складає 25 і 18% відповідно, а отже потрібне удосконалення наявних схем терапії (J. Rovira et al., 2015; M.J. Maurer et al., 2015).
У контексті зазначеної проблеми особливої уваги заслуговує полатузумабу ведотин – препарат, що належить до групи антитіло – лікарський засіб. Його механізм дії полягає у зв’язуванні моноклонального антитіла з рецептором CD79b на поверхні злоякісних B-клітин і подальшому проникненні утвореного комплексу всередину пухлинної клітини з утворенням лізосоми, з якої вивільняється цитотоксичний агент, що призводить до руйнування мікротрубочок і загибелі клітини.
У рандомізованому дослідженні GO29365 було встановлено, що медіана ЗВ у пацієнтів з р/рДВКЛ, які приймали полатузумабу ведотин + бендамустин + ритуксимаб (Pola-BR), складала 12,4 міс порівняно з 4,7 міс у групі BR (відносний ризик – ВР – 0,42; 95% ДІ 0,24-0,75; p=0,0023), тобто ЗВ збільшилася у 2 рази при використанні схеми Pola-BR. ВБП при призначенні Pola-BR за оцінкою незалежного комітету (INV) була у 3 рази вищою порівняно з такою при використанні BR та складала 7,6 проти 2,0 міс відповідно (ВР 0,34; 95% ДІ 0,20-0,57; p<0,0001). За даними ПЕТ-КТ повна відповідь при застосуванні Pola-BR складала 40,0%, а при прийомі BR – 17,5%, середня тривалість відповіді у групі Pola-BR становила 10,3 проти 4,0 міс у групі BR (L.H. Sehn et al., 2019).
Раніше використання Pola-BR рекомендувалося у 3-й лінії терапії ДВКЛ, однак у січні 2021 р. NCCN розширила показання до застосування цієї схеми, додавши її в 2-гу лінію терапії. Такі зміни пов’язані з тим, що у дослідженні L.H. Sehn (2018) було продемонстровано вищу частоту повної відповіді за даними ПЕТ-КТ при використанні Pola-BR у 2-й, ніж у 3-й лінії терапії р/рДВКЛ порівняно з BR. Так, повної відповіді у 2-й лінії терапії було досягнуто у 64% пацієнтів з р/р ДВКЛ, яких лікували за схемою Pola-BR, та 8% пацієнтів, котрі отримували BR, що удвічі перевищило результати 3-ї лінії терапії. Медіани ЗВ у 2-й лінії не було досягнуто при застосуванні Pola-BR, а у групі BR цей показник дорівнював 5,9 міс. Це дає надію пацієнтам і лікарям на досягнення безрецидивної виживаності при ДВКЛ (рис. 3).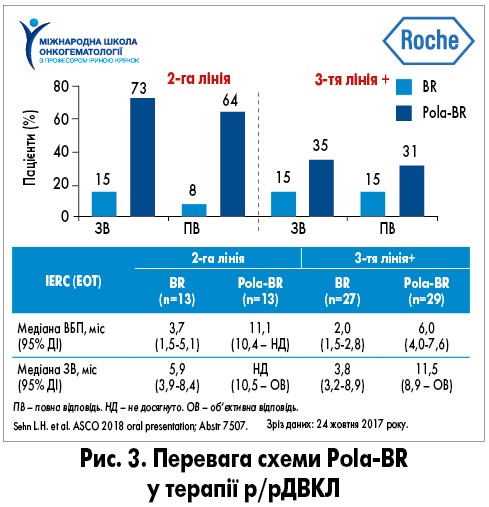
Крім того, ефективність Pola-BR була продемонстрована при всіх підтипах ДВКЛ, особливо високого ризику (ABС чи експресія MYC та BCL2 та/або BCL6 – double-expressor). При аналізі профілю токсичності комбінації Pola-BR було встановлено дещо вищу частоту нейтропенії, тромбоцитопенії та периферичної нейропатії, однак ці побічні реакції були контрольованими.
На основі результатів дослідження GO29365 полатузумабу ведотин при р/рДВКЛ отримав статуc «прорив у терапії» від Управління з контролю якості харчових продуктів і лікарських препаратів США та «препарат пріоритетної терапії» (Priority medicine, PRIME) від Європейського агентства з лікарських засобів.
З метою підвищення ефективності лікування пацієнтів з р/рДВКЛ сьогодні активно проводяться дослідження щодо вивчення комбінацій Pola+R-GemOx (гемцитабін + оксаліплатин + ритуксимаб) та Pola+R-ICE, біспецифічних моноклональних антитіл, нових моноклональних антитіл, CAR-T-клітинної терапії та малих молекул. Отже, численні дослідження у напрямі покращення терапії 1-ї лінії при р/рДВКЛ, можливо, з часом зумовлять зміну її стандартів та підвищення ефективності лікування таких хворих.
 Професор кафедри гематології та трансфузіології Національного університету охорони здоров’я України імені П.Л. Шупика (м. Київ), завідувачка відділення гематології Медичного центру імені Ю.П. Спіженка, доктор медичних наук Тетяна Петрівна Перехрестенко присвятила свою доповідь новим трендам ведення пацієнтів з ДВКЛ за даними 16-ї міжнародної конференції з питань злоякісної лімфоми (International Conference on Malignant Lymphoma, ICML).
Професор кафедри гематології та трансфузіології Національного університету охорони здоров’я України імені П.Л. Шупика (м. Київ), завідувачка відділення гематології Медичного центру імені Ю.П. Спіженка, доктор медичних наук Тетяна Петрівна Перехрестенко присвятила свою доповідь новим трендам ведення пацієнтів з ДВКЛ за даними 16-ї міжнародної конференції з питань злоякісної лімфоми (International Conference on Malignant Lymphoma, ICML).
– У рамках сателітного симпозіуму ICML (2021) активно обговорювалася тема персоналізованого підходу у лікуванні ДВКЛ, оскільки найближчими роками будуть доступні різні методи лікування таких пацієнтів.
Сьогодні шлях хворого на ДВКЛ починається від сімейного лікаря, який повинен вчасно направити його до спеціаліста онкогематологічного профілю. Хворому проводиться діагностична біопсія, імуногістохімічне дослідження (за можливості з визначенням групи ризику через виявлення реаранжування генів MYC, BCL2 та BCL6) із подальшим включенням до групи ризику за даними міжнародної прогностичної шкали, від чого залежатиме лікування. Золотим стандартом терапії є R-CHOP, інтенсифікацію дози проводять при виявленні реаранжування генів, а малоінтенсивні режими застосовують при наявності коморбідної патології. Крім того, можна розглядати участь пацієнтів у клінічних дослідженнях. Надалі відповідь на терапію оцінюють шляхом проведення ПЕТ-КТ. При рецидиві чи рефрактерності до терапії 1-ї лінії рекомендованою опцією у молодих пацієнтів є високодозова хіміотерапія з аутоТГСК. Якщо хворий не є кандидатом на аутоТГСК, визначена низка схем, однією з яких є Pola-BR, що сьогодні активно вивчається у багатьох клінічних дослідженнях. Попередні дані дослідженні GO29834 свідчать про помітну ефективність полатузумабу ведотину з ритуксимабом і леналідомідом у пацієнтів з р/рДВКЛ (особливо у хворих, які досягли повної відповіді на терапію у кінці індукції) при збереженні її доброї переносимості. Обнадійливі показники відповіді на терапію полатузумабу ведотином з обінутузумабом і венетоклаксом у пацієнтів з рецидивуючою/рефрактерною фолікулярною лімфомою були продемонстровані у попередніх результатах дослідження GO29833.
У серії клінічних досліджень також активно вивчаються біспецифічні моноклональні антитіла, які діють на антиген T-клітин (CD3) та B-клітин (CD-20), що індукує розпад пухлинної клітини. Попередні дані дослідження NP30179 із застосування глофітамабу у пацієнтів з р/рНХЛ свідчать про високу частоту повної відповіді у пацієнтів з тяжкою р/рНХЛ. Обнадійливі дані щодо комбінації мосунетузумабу з полатузумабу ведотином продемонстровані у первинних результатах дослідження GO40516, оскільки 100% пацієнтів з фолікулярною лімфомою та 47,4% хворих з агресивною НХЛ відповіли на терапію. У пацієнтів з р/рДВКЛ також активно вивчають використання епкоритамабу й тафаситамабу з леналідомідом. Крім того, сьогодні великі надії у лікуванні хворих на ДВКЛ науковці покладають на алогенну CAR-T-клітинну терапію.
Представлені у рамках майстер-класу попередні результати клінічних досліджень свідчать про те, що найближчим часом з’являться нові опції у лікуванні ДВКЛ, які можуть змінити сучасні стандарти терапії.
Підготувала Ірина Неміш
Матеріал підготовлено за підтримки ТОВ «Рош Україна».
Інформація для професійної діяльності медичних і фармацевтичних працівників. Для розміщення в спеціалізованих виданнях, призначених для медичних закладів або спеціалістів охорони здоров’я. Для демонстрації в рамках семінарів, конференцій, симпозіумів на медичну тематику.
Деякі схеми лікування можуть включати лікарські засоби, застосовані за межами їхніх показань та/або не зареєстровані в Україні.
Запит медичної інформації про продукти ТОВ «Рош Україна» ви можете надіслати на електронну адресу: ukraine.medinfo@roche.com.
ТОВ «Рош Україна», м. Київ, 03150, вул. Велика Васильківська, 139. Тел.: +380(44)354-30-40, факс: +380(44)354-30-41. www.roche.ua.
Повідомити про побічні явища під час лікування препаратом ТОВ «Рош Україна» або поскаржитись на якість препарату ви можете за контактними даними офісу або на електронну адресу: ukraine.safety@roche.com.
M-UA-00000485
Тематичний номер «Онкологія, Гематологія, Хіміотерапія» № 4 (71) 2021 р.