14 квітня, 2026
Фруквінтиніб – новий селективний інгібітор VEGFR у терапії метастатичного колоректального раку
Колоректальний рак (КРР) посідає третє місце серед найпоширеніших злоякісних новоутворень та друге – серед причин онкологічної смертності у світі. Терапевтичні можливості для пацієнтів із метастатичним КРР (мКРР), у яких захворювання прогресує після двох і більше ліній стандартної терапії, залишаються обмеженими. Фруквінтиніб – пероральний високоселективний інгібітор тирозинкіназ VEGFR‑1,-2 та -3 (IC50 33, 35 та 0,5 нмоль/л відповідно) з мінімальною активністю щодо інших кіназ. У двох рандомізованих подвійних сліпих плацебоконтрольованих дослідженнях III фази – FRESCO (n = 416, Китай) та FRESCO‑2 (n = 691, 14 країн) – фруквінтиніб продемонстрував статистично достовірне поліпшення загальної виживаності (ЗВ) – 9,3 проти 6,6 місяця та 7,4 проти 4,8 місяця відповідно – і виживаності без прогресування (ВБП) порівняно з плацебо за прийнятного та керованого профілю безпеки. Фруквінтиніб є важливим доповненням терапевтичного арсеналу для лікування рефрактерного мКРР у третій та подальших лініях терапії.
КРР залишається однією з найактуальніших проблем сучасної онкології, щорічно уражаючи близько 2 млн осіб у всьому світі [1]. Приблизно у половини пацієнтів із КРР розвиваються віддалені метастази, а загальна п’ятирічна виживаність за наявності метастатичного процесу становить лише 15% [2, 3]. Попри те що впровадження скринінгової колоноскопії та тестування калу на приховану кров дали змогу знизити показники смертності, терапевтичні підходи до лікування мКРР потребують подальшого вдосконалення.
На сьогодні основу лікування мКРР становить хімієтерапія із застосуванням фторпіримідинів, оксаліплатину та іринотекану [4]. Стандартом допомоги для мікросателітно стабільного мКРР є комбінація хімієтерапії з моноклональними антитілами, спрямованими проти рецептора епідермального фактора росту (EGFR) або судинного ендотеліального фактора росту (VEGF), залежно від молекулярного профілю пухлини та локалізації первинного вогнища [2, 5]. Проте значна частина пацієнтів із мКРР із часом стає нечутливою, резистентною або інтолерантною до зазначених препаратів, а арсенал лікувальних засобів для хворих, у яких захворювання прогресує після двох ліній терапії, залишається вкрай обмеженим [6].
У цьому контексті поява фруквінтинібу – нового перорального інгібітора рецепторів судинного ендотеліального фактора росту (VEGFR) – надає додаткові терапевтичні можливості для пацієнтів із мКРР, які вичерпали стандартні лінії лікування. Метою цього огляду є систематизація наявних даних щодо дизайну, розроблення, фармакологічних властивостей, результатів клінічних досліджень і потенційного місця фруквінтинібу в алгоритмах лікування мКРР у третій та подальших лініях терапії.
Ангіогенез і блокада VEGFR як терапевтична стратегія в онкології
Ангіогенез – процес утворення нових кровоносних судин із наявної судинної мережі – відіграє ключову роль і у фізіологічних процесах ембріонального розвитку, і в патогенезі злоякісних новоутворень [7, 8]. Неоангіогенез є одним із визначальних факторів проліферації пухлинних клітин, ремоделювання судинного русла та метастатичного поширення. Сигнальний шлях VEGF визнано центральним регулятором пухлинного ангіогенезу [9], а його пригнічення стало ефективною терапевтичною стратегією при різних типах злоякісних пухлин [10]. Антиангіогенні препарати реалізують свою дію двома основними способами – через блокаду ліганда (інгібітори VEGF) або його рецептора (інгібітори VEGFR).
VEGF сприяє пухлинному ангіогенезу через численні механізми. По-перше, він стимулює проліферацію, виживання, міграцію та інвазію ендотеліальних клітин. По-друге, підвищує проникність кровоносних судин із формуванням мережі для клітинної міграції. По-третє, посилює хемотаксис клітин-попередників кісткового мозку [11]. Окрім безпосереднього впливу на судинне русло, VEGF також реалізує несудинні ефекти включно з аутокринним впливом на функцію пухлинних клітин, що стосується їхнього виживання, міграції та інвазії; імуносупресією, а також хомінгом попередників кісткового мозку, що підвищує ризик метастатичного ураження органів-мішеней [11]. Ця багатовекторність дії VEGF підкреслює значущість інгібування VEGFR як протипухлинної стратегії через зниження інтенсивності пухлинного ангіогенезу – одного з ключових драйверів прогресування захворювання.
Бевацизумаб – гуманізоване моноклональне антитіло проти ліганда VEGF-A – став першим антиангіогенним препаратом, схваленим у комбінації з хімієтерапією для лікування мКРР [8]. Механізм його дії полягає у зв’язуванні з VEGF, що перешкоджає взаємодії останнього з рецептором і, відповідно, порушує сигнальний каскад, який забезпечує ангіогенез, проліферацію та міграцію пухлинних клітин [12]. Надалі в ключовому клінічному дослідженні було продемонстровано ефективність бевацизумабу в другій лінії терапії та у пацієнтів із прогресуванням захворювання [13].
Водночас блокада VEGF-A призводить до компенсаторного підвищення рівнів інших компонентів осі VEGF, зокрема VEGF-C, VEGF-D та тромбоцитарного фактора росту (PDGF), що зрештою зумовлює формування резистентності до бевацизумабу. Цей феномен підтвердив Hayashi Н. та співавтори під час оцінювання сироваткових концентрацій біомаркерів до та після лікування комбінацією бевацизумабу з режимом FOLFIRI (фолінова кислота, фторурацил, іринотекан). Дослідники виявили зниження рівнів VEGF-A, проте водночас більш високі VEGF-C і VEGF-D порівняно з первинними показниками – причому й у пацієнтів, які раніше отримували бевацизумаб, і в «наївних» хворих [14]. Ця обмежена селективність щодо мішені, яка може спричиняти позамішеневу токсичність, стала передумовою для розроблення препаратів, здатних одночасно блокувати кілька лігандів VEGF.
Додаткові обмеження клінічного застосування бевацизумабу включають внутрішньовенний шлях введення, ризик розвитку аутоімунних реакцій під час тривалого лікування, імуногенність і високу вартість терапії. Сукупність цих чинників обґрунтувала клінічну потребу в розробленні нового активного низькомолекулярного перорального інгібітора VEGFR, який можна було б комбінувати з хімієтерапією [15].
Фруквінтиніб: фармакодинаміка та механізм дії
Пригнічення ангіогенезу через сигнальний шлях VEGF може бути досягнуто інгібуванням ліганда або його рецептора. Рекомбінантні моноклональні антитіла проти VEGF, зокрема бевацизумаб, і низькомолекулярні інгібітори тирозинкіназ є основними фармакологічними засобами антиангіогенної терапії [16].
Фруквінтиніб (HMPL‑13) – це низькомолекулярний пероральний інгібітор тирозинкіназ (ІТК), який селективно блокує VEGFR‑1,-2 та -3 із високою афінністю [17]. Рецептори VEGFR належать до родини тирозинкіназних рецепторів, експресованих на поверхні ендотеліальних клітин, які активуються лігандом VEGF. Пухлинні клітини використовують цей сигнальний шлях у процесі так званого пухлинного ангіогенезу для забезпечення необхідного рівня кисню та нутрієнтів, що підтримує ріст пухлини і подальше метастатичне поширення [18].
Порівняно з інгібіторами тирозинкіназ першого покоління, такими як сорафеніб або сунітиніб, для яких досягнення максимально переносимої дози може бути обмежене внаслідок інгібування численних кіназ, фруквінтиніб є потужним і високоселективним інгібітором саме VEGFR‑1,-2 та -3 із показниками IC50 на рівні 33, 35 та 0,5 нмоль/л відповідно, що було підтверджено in vitro біохімічними кіназними аналізами з рекомбінантними ферментами VEGFR людини [19]. Водночас фруквінтиніб демонструє мінімальну активність щодо інших кіназ, зокрема RET (rearranged during transfection), рецептора фактора росту фібробластів 1 (FGFR‑1) та c-KIT [20].
Кожна з цих додаткових мішеней відіграє певну роль у канцерогенезі. Кіназа c-KIT стимулює проліферацію, рухливість та адгезію злоякісних клітин. RET інгібує клітинний апоптоз, сприяючи виживанню пухлинних клітин. FGFR‑1, зі свого боку, ініціює проліферацію пухлинних клітин і стимулює їхню дисемінацію на пізніх стадіях захворювання [20]. Важливо, що поєднання селективного інгібування VEGFR зі слабким пригніченням FGFR‑1 та RET може посилювати імунну активність інгібіторів контрольних точок імунітету та потенціювати їхню протипухлинну відповідь [21, 22]. Цей аспект є особливо значущим з огляду на активне вивчення комбінаторних стратегій із залученням імунотерапії.
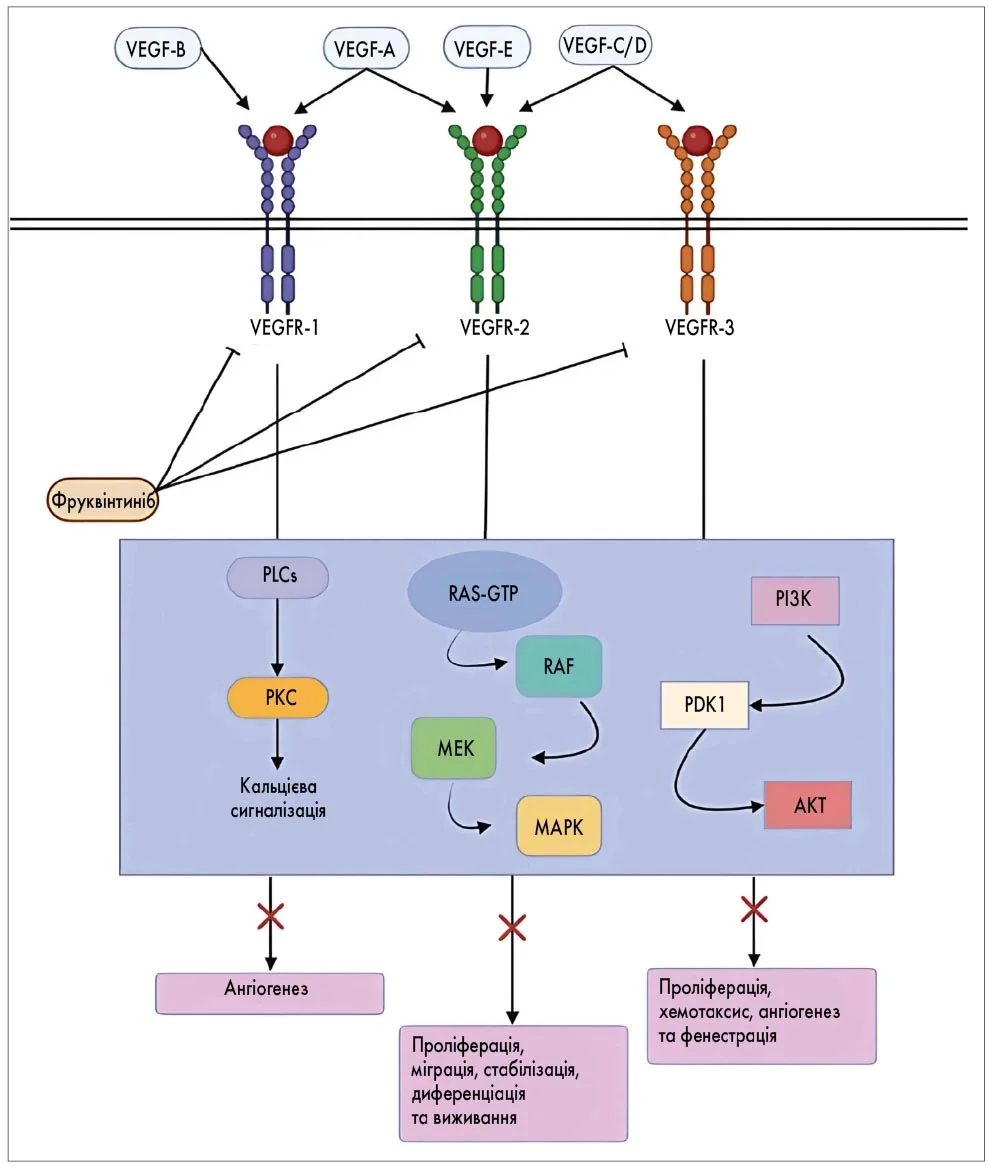
Під час зв’язування фруквінтинібу з VEGFR відбуваються конформаційні зміни і димеризація рецептора, що призводить до фосфорилювання внутрішньоклітинного кіназного домену та запуску низки сигнальних каскадів включно зі шляхами PI3K/AKT, PKC, RAF/RAS та ERK (рис.) [23-25]. Рецептор VEGFR‑2 відіграє критичну роль у проангіогенних процесах і є основною мішенню для пригнічення пухлинного неоангіогенезу. VEGFR‑3, зі свого боку, експресується виключно на лімфатичних судинах і бере участь у процесах лімфангіогенезу і метастазування в лімфатичні вузли. Значущість лімфангіогенезу в метастатичному поширенні злоякісних пухлин робить VEGFR‑3 привабливою терапевтичною мішенню. На сьогодні не розроблено інших препаратів, які специфічно інгібують VEGFR‑3, через що фруквінтиніб є унікальним представником свого класу з потенційними перевагами саме в контексті впливу на лімфогенне метастазування [19].
Рисунок. Блокада рецепторів VEGF фруквінтинібом та уражені сигнальні шляхи
PLC – фосфоліпаза C; PKC – протеїнкіназа C; RAS-GTP – білок саркоми щурів, зв'язаний із гуанозинтрифосфатом; RAF – швидко прискорена фібросаркома; MEK – мітоген-активована протеїнкіназа кіназа; MAPK – мітоген-активована протеїнкіназа; PI3K – фосфоінозитид‑3-кіназа; PDK1 – фосфоінозитид-залежна кіназа 1; AKT – протеїнкіназа B.
Доклінічні дослідження та протипухлинна активність
Доклінічні дослідження фруквінтинібу продемонстрували його значну протипухлинну ефективність in vivo. Зокрема, препарат виявив дозозалежне пригнічення росту пухлин у ксенографтних моделях злоякісних новоутворень людини включно з колоректальним раком (клітинні лінії HT‑29 та HCT‑116), раком легені (NCI-H460) та раком шлунка (BGC‑823) [19]. Окрім протипухлинної активності як монопрепарату, фруквінтиніб продемонстрував синергічні ефекти під час комбінування з хімієтерапевтичними засобами.
В умовах in vivo після одноразового введення фруквінтинібу в дозі 2,5 мг/кг було досягнуто 85% інгібування VEGFR‑2 у тканині легень протягом 8 годин і більше. Відповідна плазмова концентрація становила 176 нг/мл, що відповідало ефективній концентрації фруквінтинібу для досягнення 85% інгібування мішені (EC85). Показник EC85 є важливим фармакокінетичним параметром, який використовується для розрахунку тривалості інгібування мішені при рекомендованих дозах у клінічних дослідженнях [19].
В іншому дослідженні на мишачій пухлинній моделі було продемонстровано синергізм під час спільного застосування фруквінтинібу з таргетними препаратами – інгібіторами тирозинкіназ EGFR (гефітиніб і телатиніб) та інгібітором c-MET саволітинібом, а також з анти-PD-L1 інгібітором – порівняно з монотерапією фруквінтинібом [26]. Ці доклінічні дані свідчать про потенціал комбінаторних стратегій із залученням фруквінтинібу та обґрунтовують проведення відповідних клінічних досліджень.
Фармакокінетичний профіль
Фруквінтиніб характеризується сприятливими фармакокінетичними властивостями, зокрема швидкою абсорбцією, високою пероральною біодоступністю та помірно тривалим періодом напіввиведення. У доклінічних дослідженнях на мишах, щурах, собаках та мавпах препарат демонстрував лінійну фармакокінетику з мінімальним ризиком міжлікарських взаємодій [27].
Важливою характеристикою фармакокінетичного профілю фруквінтинібу є відсутність інгібування основних ізоформ CYP у мікросомах печінки, що мінімізує ризик клінічно значущих міжлікарських взаємодій – критичний фактор для пацієнтів із мКРР, які часто отримують багатокомпонентну терапію. Крім того, фруквінтиніб не зазнає впливу змін зв’язування з білками плазми, оскільки препарат переважно елімінується печінковим шляхом із низьким коефіцієнтом екстракції [27]. Сукупність цих фармакокінетичних характеристик забезпечує передбачуваний профіль експозиції та зручність клінічного застосування.
Клінічні дослідження: дизайн та результати
Ефективність і безпека фруквінтинібу були вивчені у двох ключових рандомізованих подвійних сліпих плацебоконтрольованих дослідженнях III фази – FRESCO і FRESCO‑2, результати яких стали основою для реєстрації препарату в різних юрисдикціях.
FRESCO – мультицентрове рандомізоване подвійне сліпе плацебоконтрольоване дослідження III фази, проведене в Китаї, до якого було залучено 416 пацієнтів із мКРР, у яких захворювання прогресувало під час або після попередньої хімієтерапії на основі фторпіримідинів, оксаліплатину та іринотекану [28]. Вони були довільно розподілені у співвідношенні 2:1 до групи фруквінтинібу (5 мг перорально один раз на добу з 1-го по 21-й день 28-денного циклу) або групи плацебо. Середній вік учасників становив 55 років, усі мали мКРР із прогресуванням після щонайменше двох ліній хімієтерапії, проте раніше не отримували терапії інгібіторами VEGF [28]. На підставі результатів цього дослідження фруквінтиніб було схвалено в Китаї у 2018 р. для третьої та подальших ліній терапії мКРР [18, 20].
FRESCO‑2 – мультицентрове рандомізоване подвійне сліпе дослідження III фази, яке було проведено у 124 центрах 14 країн світу [29]. У дослідженні взяв участь 691 пацієнт віком від 18 років із мКРР. Захворювання у них прогресувало після лікування хімієтерапією на основі фторпіримідинів, оксаліплатину та іринотекану, а також після таргетної терапії, спрямованої проти VEGF та EGFR (за відповідними показаннями). Група фруквінтинібу (5 мг перорально один раз на добу з 1-го по 21-й день 28-денного циклу) щодо групи плацебо формувалася за аналогічним принципом: у співвідношенні 2:1, рандомний розподіл пацієнтів. Медіана віку учасників дослідження становила 64 роки, водночас 73% пацієнтів отримали інтенсивне попереднє лікування – понад три лінії терапії [29]. Ця характеристика досліджуваної популяції принципово важлива, оскільки саме у пацієнтів із вичерпаними стандартними терапевтичними опціями потреба в нових ефективних препаратах є найгострішою.
Обидва дослідження досягли первинної кінцевої точки – ЗВ – та ключової вторинної кінцевої точки – ВБП (табл.) [16].
|
Таблиця. Результати клінічних досліджень |
||
|
Показник |
FRESCO28 |
FRESCO‑229 |
|
ЗВ |
|
|
|
Група фруквінтинібу |
9,3 міс. |
7,4 міс. |
|
Група плацебо |
6,6 міс. |
4,8 міс. |
|
ВР |
0,65 |
0,66 |
|
95% ДІ |
0,510,83 |
0,550,80 |
|
p |
< 0,001 |
< 0,0001 |
|
ВБП |
|
|
|
Група фруквінтинібу |
3,7 міс. |
3,7 міс. |
|
Група плацебо |
1,8 міс. |
1,8 міс. |
|
ВР |
0,26 |
0,32 |
|
95% ДІ |
0,210,34 |
0,270,39 |
|
p |
< 0,001 |
< 0,0001 |
|
ВР – відношення ризиків; ДІ – довірчий інтервал. |
||
У дослідженні FRESCO медіана ЗВ у групі фруквінтинібу становила 9,3 місяця порівняно з 6,6 місяця в групі плацебо (ВР 0,65; 95% ДІ 0,51-0,83; p < 0,001). Медіана ВБП становила 3,7 місяця в групі фруквінтинібу проти 1,8 місяця в групі плацебо (ВР 0,26; 95% ДІ 0,21-0,34; p < 0,001) [28].
Особливу увагу привертають результати дослідження FRESCO‑2, оскільки воно охоплювало більш інтенсивно попередньо ліковану популяцію пацієнтів, у такий спосіб розширюючи потенційне застосування фруквінтинібу на пацієнтів, що вичерпали інші стандартні варіанти терапії. Медіана ЗВ у групі фруквінтинібу становила 7,4 місяця порівняно з 4,8 місяця в групі плацебо (ВР 0,66; 95% ДІ 0,55-0,80; p < 0,0001), що відповідає збільшенню медіани ЗВ на 2,6 місяця та зниженню відносного ризику смерті на 34%. ВБП також достовірно покращилася: медіана ВБП становила 3,7 місяця в групі фруквінтинібу порівняно з 1,8 місяця в групі плацебо (ВР 0,32; 95% ДІ 0,27-0,39; p < 0,0001) [29].
Перевага виживаності у дослідженні FRESCO‑2 була стабільною в різних заздалегідь визначених підгрупах. Зокрема, позитивний ефект зберігався за стратифікаційними факторами рандомізації: у пацієнтів, які раніше отримували лікування трифлуридином/тіпірацилом або регорафенібом, незалежно від статусу мутації RAS та тривалості метастатичного захворювання [29, 30-32]. Також було продемонстровано перевагу ЗВ і ВБП незалежно від кількості попередніх ліній терапії, що має важливе практичне значення для клінічного ухвалення рішень. Детальні дані щодо ефективності фруквінтинібу в обох ключових клінічних дослідженнях підсумовано в таблиці.
Профіль безпеки
Оцінка безпеки фруквінтинібу базується на даних обох ключових клінічних досліджень, які продемонстрували загалом передбачуваний та керований профіль небажаних явищ (НЯ), що відповідає ефектам інгібіторів VEGFR.
У дослідженні FRESCO НЯ 3-4 ступеня тяжкості зареєстровано у 61% пацієнтів групи фруквінтинібу порівняно з 19% у групі плацебо [28]. До найчастіших НЯ 3-4 ступеня, асоційованих із фруквінтинібом, було зараховано артеріальну гіпертензію (21%), долонно-підошовну еритродизестезію (ДПЕ) (11%) та протеїнурію (3%) [28].
У дослідженні FRESCO‑2 НЯ 3-4 ступеня тяжкості зареєстровано у 63% пацієнтів групи фруквінтинібу та у 50% пацієнтів групи плацебо із зафіксованим одним летальним випадком, пов’язаним із лікуванням, у кожній групі [29]. Серед НЯ 3-4 ступеня, пов’язаних із фруквінтинібом, найчастіше реєструвалася артеріальна гіпертензія (14%), астенія (8%) та ДПЕ (6%) [29, 30-32]. Слід зауважити, що частота тяжкої артеріальної гіпертензії у FRESCO‑2 була нижчою порівняно з FRESCO (14% проти 21%), що може пояснюватися відмінностями в досліджуваних популяціях та стандартах супровідної терапії.
Загалом результати оцінювання безпеки в обох дослідженнях були узгодженими між собою та відповідали відомому профілю безпеки фруквінтинібу. Спектр НЯ характерний для класу інгібіторів VEGFR і загалом керований засобами стандартної супровідної терапії.
Місце фруквінтинібу в терапевтичному алгоритмі та подолання резистентності
Розроблення нового антиангіогенного інгібітора тирозинкіназ, яким є фруквінтиніб, вирішує суттєву клінічну проблему медикаментозної резистентності під час лікування мКРР. На відміну від бевацизумабу, який блокує лише один ліганд – VEGF-A, фруквінтиніб діє безпосередньо на рівні рецепторів VEGFR‑1,-2 та -3, що дає змогу ефективніше пригнічувати ангіогенез навіть за наявності компенсаторного підвищення рівнів альтернативних лігандів VEGF – механізму, відповідального за формування резистентності до бевацизумабу [14].
Водночас імунотерапевтичні модальності, зокрема інгібітори анти-PD‑1, рекомендовані Національною онкологічною мережею США (NCCN) та схвалені Управлінням з контролю якості харчових продуктів і лікарських засобів США (FDA) для лікування мКРР із мікросателітною нестабільністю (MSI). Застосування інгібіторів контрольних точок імунітету, таких як ніволумаб та пембролізумаб, продемонструвало суттєве поліпшення показників ВБП і частоти об’єктивної відповіді у пацієнтів із високим рівнем MSI [33]. Отже, перспективною стратегією лікування мКРР із високим рівнем MSI може бути комбінування фруквінтинібу з інгібітором PD‑1 [33]. Доклінічні дані вже продемонстрували синергізм фруквінтинібу з анти-PD-L1 інгібітором на мишачих моделях [26], що додатково обґрунтовує раціональність такої комбінаторної стратегії.
Перспективні напрямки досліджень
Одним із актуальних напрямків подальших досліджень є визначення оптимальної послідовності застосування доступних терапевтичних опцій. Мультицентрове спостережне дослідження в реальній клінічній практиці (NCT05993702) спрямоване на вивчення ефективності та безпеки комбінації трифлуридину/тіпірацилу з регорафенібом або фруквінтинібом для третьої та подальших ліній терапії мКРР. У контексті секвенування терапії також актуальною є ідентифікація ключових біомаркерів, які допоможуть визначити популяцію пацієнтів, що з найбільшою ймовірністю отримають користь від конкретних терапевтичних послідовностей [16].
Не менш перспективним є вивчення потенційних синергічних ефектів під час комбінування фруквінтинібу з іншими таргетними препаратами або імунотерапевтичними засобами. Зважаючи на доведену ефективність антиангіогенних інгібіторів при мКРР, їхнє комбінування з іншими терапевтичними модальностями може забезпечити кращі клінічні результати. На сьогодні зареєстровано понад 15 поточних клінічних досліджень II або I/II фази, в яких фруквінтиніб вивчається в різних комбінаціях (переважно з хімієтерапією) як терапія першої лінії (NCT04296019 [34], NCT05004441, NCT04866108), другої лінії (NCT05634590, NCT05555901) або підтримувальна терапія (NCT05451719 – як монотерапія, NCT05016869, NCT05451719, NCT04733963, NCT05659290) у пацієнтів із мКРР [34]. Результати цих досліджень можуть суттєво розширити спектр показань для застосування фруквінтинібу і визначити його роль не лише в пізніх, а й у ранніх лініях терапії.
Висновки
Фруквінтиніб є першим високоселективним пероральним інгібітором VEGFR‑1, -2 та -3, який продемонстрував статистично достовірне й клінічно значуще поліпшення ЗВ та ВБП у пацієнтів із мКРР, що прогресує після двох і більше ліній стандартної терапії. Результати двох ключових рандомізованих досліджень III фази – FRESCO та FRESCO‑2 – підтвердили ефективність препарату за прийнятного профілю безпеки (табл.).
Список літератури – у редакції
Підготувала Олена Речмедіна
Тематичний номер «Онкологія. Гематологія. Хімієтерапія» № 1 (101) 2026 р.