30 квітня, 2026
Клітини-попередники гліального ряду як первинне джерело IDH-мутантних гліом: нові докази та клінічне значення
IDH-мутантні гліоми є найпоширенішою злоякісною пухлиною головного мозку в осіб молодших 50 років, однак питання про клітину-попередника, що першою набуває ініціюючої мутації, досі не з’ясоване. У цій оглядовій статті викладено результати дослідження J.W. Park et al. (Science, 2026), в якому за допомогою ультрачутливих методів секвенування (цифрова крапельна ПЛР, глибоке панельне секвенування) проаналізовано 142 зразки від 70 пацієнтів, зокрема пухлини, перитуморальну кору, субвентрикулярні зони (СВЗ) та кров. Також дослідники створили мишачу модель із введенням драйверних мутацій (Idh1, Trp53, Atrx та Nf1). Принципова новизна цього дослідження полягає в тому, що ультрачутливе секвенування вперше надає прямі докази існування мутації IDH у «нормальній» на вигляд тканині мозку за декілька років до того, коли пухлину можна виявити методами нейровізуалізації; ця мутація є першою генетичною подією, що ініціює пухлинний процес. Встановлено, що в 37,9% пацієнтів з IDH-мутантними гліомами перитуморальна кора містить низькорівневу мутацію IDH1R132H як єдину онкогенну подію – без жодних додаткових драйверних мутацій. Отримані дані формують цілісну модель гліомогенезу, де обидва підтипи – астроцитома й олігодендрогліома – виникають із спільної клітини-попередника і дивергують залежно від набору наступних драйверних подій. Виявлення мутантних клонів у нормальній перитуморальній корі сприяє розробленню методів ультраранньої молекулярної діагностики, превентивному спостереженню за групами ризику та обґрунтовує доцільність раннього застосування IDH-інгібіторів після операції.
IDH-мутантні гліоми посідають особливе місце в нейроонкології: це найпоширеніша злоякісна пухлина головного мозку в осіб молодших 50 років, на частку якої припадає близько 12% усіх гліом [1]. Клінічно виокремлюють два гістологічних варіанти – олігодендрогліому з коделецією 1p/19q та астроцитому без цієї коделеції, які, попри відмінну молекулярну архітектуру, об’єднані спільною патогенетичною ознакою: мутацією гена ізоцитратдегідрогенази (IDH) [2, 3]. Більшість таких мутацій є гетерозиготними замінами R132H у гені IDH1, що призводить до накопичення онкометаболіту D‑2-гідроксиглутарату і запуску каскаду епігенетичних і метаболічних порушень [1, 4-6].
Попри значні успіхи у вивченні молекулярної біології IDH-мутантних гліом, на питання, яка саме клітина мозку першою набуває ініціюючої мутації, тривалий час не було відповіді. Визначення клітини-попередника пухлини – не лише фундаментальне завдання онкобіології, а й пряма передумова для розроблення методів ранньої діагностики і превентивного втручання. Попередні дослідження за допомогою одноклітинного РНК-секвенування виявили спільні гліальні лінії та ієрархії розвитку для обох підтипів IDH-мутантних гліом, що вказувало на існування спільного клітинного попередника [7, 8]. Нещодавня публікація J.W. Park et al. (2026) у журналі Science [9] суттєво наближає до відповіді на це питання, надаючи прямі докази, що джерелом IDH-мутантних гліом є гліальні клітини-попередники (ГКП), зокрема попередники олігодендроцитів (ПО), у перитуморальній корі головного мозку.
Методологія дослідження
Дослідницька група проаналізувала 142 зразки тканин від 70 осіб: 32 пацієнтів із IDH-мутантними гліомами та 38 IDH-негативних учасників контрольної групи. До аналізу залучали матеріал пухлини, перитуморальну кору, субвентрикулярну зону (СВЗ) і кров. Гістологічна й радіографічна верифікація підтверджувала відсутність пухлинної інвазії у зразках нормальної тканини.
Для виявлення надзвичайно низьких рівнів мутацій застосовували крапельну цифрову полімеразну ланцюгову реакцію (ddPCR) для детекції IDH1R132H, глибоке панельне секвенування 15 генів, асоційованих із розвитком гліом (середня глибина 757,5×) та ультраглибоке ампліконне секвенування (середня глибина 391 958×). Порогове значення варіантної алельної частоти (VAF) для справжньої детекції мутації IDH1 встановлювали статистично – на рівні 0,114% (3 стандартні відхилення від середнього шуму, p < 0,00135). Чотирьом пацієнтам проводили повногеномне секвенування (WGS) з ультраглибоким ампліконним аналізом 58 пухлиноспецифічних варіантів. Просторова транскриптоміка на платформі Xenium у поєднанні з імуногістохімічним фарбуванням дала змогу картувати IDH1-мутантні клітини у зрізах мозку пацієнта. Клітинноспецифічний аналіз мутацій здійснювали методом флуоресцентного сортування ядер (FANS) із маркерами NEUN та OLIG2.
Перитуморальна кора як місце первинної події глiомогенезу
Низькорівневу мутацію IDH1^R132H^ виявлено у перитуморальній корі в 37,9% (11 із 29) пацієнтів з IDH-мутантними гліомами. У СВЗ групи IDH1-shared не виявлено взагалі. На підставі мутаційного аналізу пацієнтів розподілили на три групи: non-shared (відсутність спільних мутацій), tumor-microinvaded (повний збіг мутаційного профілю з пухлиною) та IDH1-shared (спільна лише мутація IDH1 або IDH1 з одним раннім драйвером). Остання група відображає ключовий феномен: наявність клону з первинною мутацією IDH1 у гістологічно незміненій корі – до накопичення будь-яких додаткових онкогенних подій.
Ультраглибоке ампліконне секвенування групи non-shared (середня глибина 479,928×) не виявило жодної драйверної мутації, що виключає існування генетичних подій, які передують IDH-мутації. Відсутність коделеції 1p/19q в перитуморальній корі пацієнтів з олігодендрогліомою (підтверджено FISH-аналізом) та дані серійних біопсій, де мутація IDH1 жодного разу не виникала після мутації TP53 або втрати 1p/19q [10-12], підтверджують: IDH-мутація є найбільш ранньою генетичною подією в патогенезі гліоми, яка передує всім іншим онкогенним змінам. Транскриптомний аналіз 20 пухлин не виявив молекулярної сегрегації між групами, що виключає інтерпретацію IDH1-мутантних клітин перитуморальної кори як маркера особливого підтипу пухлини.
ГКП як клітина-джерело
Сортування ядер з наступним ddPCR виявило IDH-мутацію в олігодендроцитній фракції (NEUN–/OLIG2+) у чотирьох із п’яти пацієнтів групи IDH1-shared та у фракції «інших гліальних клітин» – у двох із п’яти. Нейрони не містили мутацій в усіх випадках. В одного пацієнта обидві гліальні фракції містили мутантний клон, що відповідає сценарію, за якого первинна мутація виникла в ГКП, здатній диференціюватись і в олігодендроцити, і в астроцити [13]. Просторова транскриптоміка підтвердила, що серед усіх ненеопластичних клітинних типів саме ПО були єдиними, де частка IDH1-мутантних клітин перевищувала порогове значення фонового сигналу (1,5%). Мутантні клітини коекспресували маркери ПО – PDGFRA, CSPG4 та MYT1.
Мишача модель: від ПО до IDH-мутантної гліоми
Постнатальна електропорація PiggyBac-векторів з Ng2-Cre у мишей лінії IDH1loxP(R132H)/+; LSL-Cas9-EGFPfl/+ забезпечила введення мутацій у Ng2-експресуючі клітини (переважно ПО та підмножину астроцитних попередників, але не нейрони). Ізольована мутація IDH1R132H посилювала проліферацію ПО без ініціації пухлини [14, 15]. Комбінація IDH1, TRP53, ATRX та Nf1 (модель OPC-ITAN) призводила до формування IDH-мутантних астроцитом у 62,1% мишей із вірогідним скороченням виживаності. Гістологічно пухлини відтворювали повний спектр людської IDH-мутантної гліоми – від низькозлоякісних форм до високозлоякісних з ядерним атипізмом та крововиливами. Введення тих самих мутацій у диференційовані клітини кори і нейрональну лінію не спричиняло утворення пухлини, що остаточно виключає ці клітини як кандидатів на роль клітини-джерела. Одноклітинне РНК-секвенування підтвердило транскриптомну відповідність мишачої моделі людській IDH-мутантній гліомі, а траєкторний аналіз окреслив два шляхи розвитку ПО – нормальний (у зрілі олігодендроцити) та злоякісний (у пухлинні клітини).
Клінічне значення та обговорення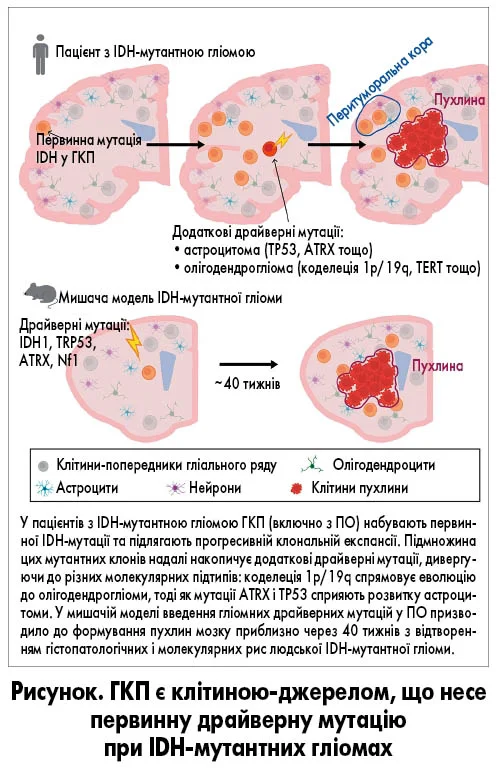
Отримані дані формують цілісну модель IDH-мутантного гліомогенезу: ГКП перитуморальної кори набувають мутації IDH1 як першої онкогенної події; частина цих мутантних клонів надалі дивергує до олігодендрогліоми (коделеція 1p/19q, TERT) або астроцитоми (ATRX, TP53) (рис.). Виявлення IDH1-мутантних клітин у гістологічно нормальній тканині в 37,9% пацієнтів свідчить про можливість детекції передракової фази до формування явної пухлини – перспектива, що відкриває шлях до рідкої біопсії та превентивного молекулярного скринінгу груп ризиків. Локалізаційна перевага цих гліом у лобовій частці може пояснюватися регіональною щільністю ПО та їхньою збереженою проліферативною активністю впродовж усього життя [16-19].
Висновок
Завдяки дослідженню J.W. Park et al. (2026) пряму та конвергентну доказову базу отримує концепція, що IDH-мутантні гліоми виникають із гліальних клітин-попередників – насамперед попередників олігодендроцитів – перитуморальної кори після набуття ініціюючої мутації IDH1 з наступним накопиченням додаткових драйверних подій. Ультрачутливе секвенування вперше прямо доводить, що ця мутація існує у «нормальній» на вигляд тканині мозку ще до появи пухлини, що виявляється під час нейровізуалізації, і це принципово змінює розуміння передпухлинного стану мозку. Мишача модель OPC-ITAN відтворює гістопатологічні та транскриптомні характеристики людської пухлини, підтверджуючи причинно-наслідковий зв’язок між ГКП-походженням і IDH-мутантним глiомогенезом.
Для нейроонкологів-практиків ці результати означають: 1) стратегічний напрямок розроблення методів ультраранньої молекулярної діагностики; 2) обґрунтування таргетної терапії після операції, оскільки навіть після тотальної резекції резидуальні IDH-мутантні клони залишаються в мозку і можуть ініціювати рецидив із генетично відмінного субклону; 3) наукову основу для вивчення ранніх режимів застосування IDH-інгібіторів як стратегії запобігання рецидиву.
Список літератури – у редакції.
Підготувала Олена Речмедіна
Тематичний номер «Онкологія. Гематологія. Хімієтерапія» № 1 (101) 2026 р.



