6 травня, 2026
Від локальної біостимуляції до системної імуномодуляції: нова комбінована стратегія лікування остеоартриту
Результати дослідження
Остеоартрит є однією з найпоширеніших патологій суглобів, що характеризується прогресуючою деградацією суглобового хряща, субхондральним склерозом, формуванням остеофітів і хронічним синовіальним запаленням. З огляду на хронічний перебіг і тенденцію до прогресування, лікування остеоартриту зумовлює потребу в пошуку терапевтичних стратегій, здатних впливати не лише на симптоми, а й на патогенетичні ланки розвитку захворювання. У статті представлено новий підхід до вдосконалення регенеративних методів лікування остеоартриту, а також висвітлено ефективні альтернативи інвазивним регенеративним методикам лікування.
Ключові слова: остеартрит, остеоартроз, гонартроз, лікування остеоартриту, біль у суглобах, неденатурований колаген, терапія збагаченою тромбоцитами плазмою, Меркана®.
Роль регенеративних технологій у лікуванні остеоартриту
Традиційні методи лікування остеоартриту, включаючи нестероїдні протизапальні препарати та внутрішньосуглобові кортикостероїди, забезпечують симптоматичний контроль болю й запалення, але не впливають на ключові патофізіологічні механізми захворювання. Їх тривале застосування пов’язане з ризиком побічних ефектів і не модифікує перебіг остеоартриту (Elmajee M. et al., 2025). У зв’язку з цим клінічна практика все більше орієнтується на патогенетично обґрунтовані підходи, спрямовані на зміну перебігу захворювання та стимуляцію репаративних процесів тканин суглоба.
Однією з найбільш досліджених і широко застосовуваних регенеративних технологій у травматології та ортопедії є терапія збагаченою тромбоцитами плазмою (platelet rich plasma – PRP). PRP – це аутологічний концентрат тромбоцитів, отриманий шляхом центрифугування цільної крові, який містить надфізіологічні концентрації факторів росту, цитокінів та інших активних молекул (Liang Y. et al., 2022). Терапевтична ефективність PRP при остеоартриті полягає у здатності змінювати біологічне мікросередовище суглоба з катаболічного на анаболічне, що сприяє активації процесів відновлення хрящової тканини. Ключову роль у реалізації хондроанаболічного потенціалу PRP відіграють фактори росту: зокрема, тромбоцитарний фактор росту (PDGF), трансформуючий фактор росту β (TGF-β), інсуліноподібний фактор росту (IGF), фактор росту фібробластів (FGF) і васкулярно-ендотеліальний фактор росту (VEGF). Сукупно вони стимулюють проліферацію мезенхімальних клітин, посилюють синтетичну активність хондроцитів і сприяють синтезу компонентів сполучної тканини. Особливе значення має TGF-β як найпотужніший регулятор, що індукує хондрогенез, пригнічує апоптоз хондроцитів і знижує активність прозапальних цитокінів (Kennedy M.I. et al., 2018; Louis M.L. et al., 2018). Крім стимуляції анаболічних процесів PRP демонструє протизапальні й імуномодулюючі властивості, здатність знижувати утворення матриксних металопротеїназ (ММП), які призводять до деградації колагену (Kennedy M.I. et al., 2018).
Незважаючи на переваги PRP, тривалість ефекту після введення концентрату становить у середньому 6-12 міс, що потребує повторення цих процедур. Ефективність PRP залишається варіабельною, що зумовлено відсутністю стандартизованих протоколів приготування розчину, гетерогенністю кінцевого продукту, а також впливом індивідуальних характеристик пацієнтів, наприклад зниження регенеративного потенціалу PRP в осіб старшого віку та при хронічному системному запаленні, що часто спостерігається в популяції хворих на остеоартрит (O’Donnell C. et al., 2019). Таким чином, сучасні доказові дані вказують на необхідність пошуку стратегій, здатних підвищити стабільність, тривалість і відтворюваність терапевтичного ефекту PRP у лікуванні остеоартриту.
Стратегічні напрями оптимізації PRP-терапії при остеоартриті
Ефективність локальних регенеративних втручань при остеоартриті значною мірою залежить від стану внутрішньосуглобового мікросередовища. Хронічне запалення та підвищена активність катаболічних ферментів і прозапальних цитокінів обмежують анаболічний потенціал факторів росту PRP, формуючи «вороже суглобове середовище», де біологічно активні молекули менш ефективні, і тому пацієнти потребують повторних курсів. У цьому контексті клінічно обґрунтованим є пошук підходів, здатних модулювати фонове запалення та підвищувати сприйнятливість суглобових тканин до локальної терапії.
Одним із перспективних напрямків є пероральне застосування неденатурованого колагену II типу (UC-II). На відміну від традиційних хондропротекторів, які розглядаються переважно як субстрати для синтезу хрящового матриксу, UC-II зберігає нативну тривимірну структуру та біологічно активні епітопи, що забезпечує реалізацію механізму оральної толерантності. Це передбачає взаємодію нативного колагену II типу з лімфоїдною тканиною кишечника (GALT), зокрема пеєровими бляшками, із подальшою індукцією специфічних регуляторних T-клітин (Tregs) (Pan P. et al., 2024). Потрапляючи у системний кровотік та суглобові тканини, Tregs, активовані у відповідь на фрагменти колагену II типу (UC II), запускають локальну протизапальну відповідь. Цей процес не супроводжується загальною імуносупресією, а забезпечує селективну імуномодуляцію зниження запальних реакцій у суглобі, що супроводжується секрецією протизапальних цитокінів (інтерлейкіни 10, 4, TGF-β) та зниженням активності ММП (Sahin E. et al., 2023; Gupta A. et al., 2025; Xu Jin et al., 2025).
Слід звернути увагу на синергію механізмів впливу щодо фактора росту TGF-β внаслідок уведення PRP та прийому UC-II: обидва підходи, використовуючи різні терапевтичні шляхи (локальний і системний), активують один із найбільш потужних регенеративних стимуляторів хрящової тканини. Тому з позицій патогенетичної терапії остеоартриту особливий інтерес становить концепція синергічної дії PRP та UC-II: PRP забезпечує локальну доставку факторів росту, зокрема TGF-β, що стимулює хондроцити та мезенхімальні клітини до синтезу позаклітинного матриксу, тоді як UC-II індукує тривалу ендогенну продукцію TGF-β через імунорегуляторні механізми. Крім того, системна імуномодуляція за допомогою UC-II може сприяти посиленню регенераторних ефектів PRP через зниження рівня фонового запалення та катаболічної активності металопротеїназ.
Клінічне дослідження комбінованої стратегії лікування остеоартриту
Метою дослідження, проведеного на базі ДУ «Національний інститут травматології та ортопедії НАМН України», було визначити клінічну ефективність, безпечність і переносимість трьох терапевтичних стратегій у пацієнтів із гонартрозом ІІ-ІІІ стадії за Келлгреном – Лоуренсом: комбінованого застосування PRP та UC-II, PRP-терапії та монотерапії UC-II. Оцінку клінічних результатів проводили за динамікою больового синдрому (ВАШ) і показниками функціонального стану колінного суглоба (KOOS) упродовж 12 міс спостереження, що дозволило визначити стійкість і практичну значущість отриманих ефектів. Запатентований неденатурований колаген II типу (UC-ІІ®) представлений на фармацевтичному ринку України засобом Меркана® (виробництво компанії «Лабораторіос Віренс С.Л.», Іспанія). Одна капсула Меркана® містить 40 мг неденатурованого колагену ІІ типу (UC-II®), який застосовується як джерело біологічно активного колагену для підтримки функціонального стану суглобів.
Меркана® тривалий час використовується в клінічній практиці як хондропротекторний засіб, що зумовлено вагомою доказовою базою та успішними результатами його застосування у пацієнтів із дегенеративними захворюваннями суглобів. Це сприяло її включенню у вивчення регенеративного потенціалу комбінованої схеми лікування остеоартриту. У дослідження було залучено 49 пацієнтів (90 суглобів) із вихідним рівнем болю за ВАШ ≥4 балів, які були розподілені на три групи. Дизайн передбачав трикратне внутрішньосуглобове введення PRP з інтервалом два тижні у відповідних групах, а також прийом хондропротектора Меркана® протягом 12 міс; у групі комбінованого лікування прийом Меркана® стартував разом із другою ін’єкцією PRP.
Динаміка больового синдрому
Аналіз динаміки больового синдрому за ВАШ продемонстрував клінічно значуще зниження болю в усіх групах у перші тижні спостереження (рис. 1). Вже на 4-му тижні в групі PRP + Меркана® відзначалося виражене зменшення інтенсивності болю з 6 до 4 балів (-33,3%), що відображає ранній клінічний ефект комбінованої терапії. На 8-му тижні статистично значуще зниження болю (p<0,001) спостерігалося в усіх групах. На 16-му тижні спостереження тенденція до зниження больового синдрому зберігалася у всіх пацієнтів, при цьому найбільш виражений ефект був зафіксований у групі PRP + Меркана®, де зменшення болю досягало 92% порівняно з початковим рівнем. У групі монотерапії Меркана® також відзначалося поступове, але менш виражене зниження больового синдрому. Важливо, що клінічно помітні зміни у цій групі ставали більш очевидними після 8-го тижня прийому, що узгоджується з імуномодулюючим і накопичувальним характером дії UC-II.
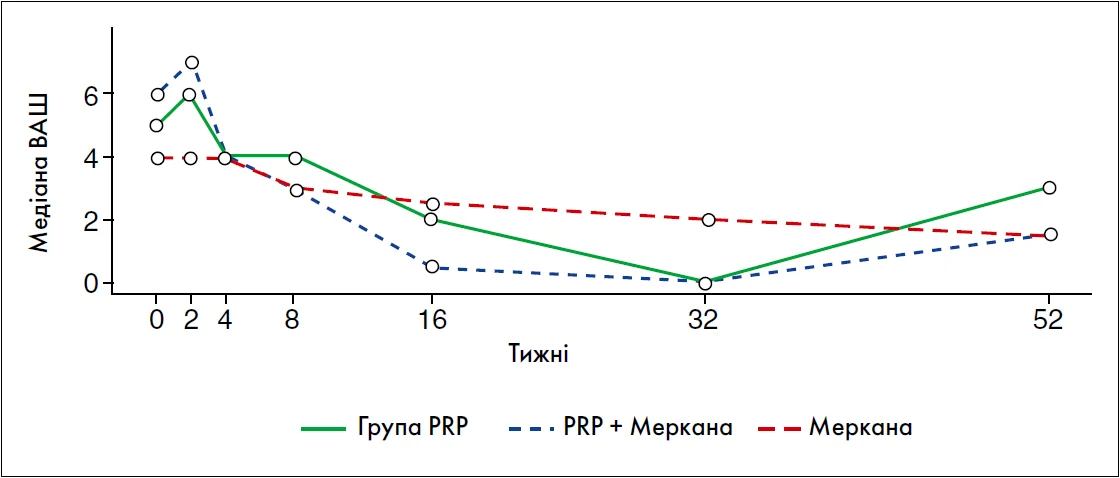 Рис. 1. Зміна больового синдрому в процесі спостереження за медіанними показниками ВАШ
Рис. 1. Зміна больового синдрому в процесі спостереження за медіанними показниками ВАШ
До 32-го тижня у групах із застосуванням PRP (як монотерапії, так і в комбінації з Меркана®) у більшості пацієнтів спостерігалася практично відсутність больового синдрому (≈0 за ВАШ). У групі прийому Меркана® протягом 16-32 тижнів також спостерігалося статистично значуще зниження болю за ВАШ (p<0,001). Важливо, що цей ефект мав поступовий і стабільний характер: інтенсивність болю зменшилася на 50% порівняно з початковим рівнем на 32-му тижні лікування без виражених коливань показників у динаміці. Така рівномірність відповіді свідчить про передбачуваність і контрольованість клінічного ефекту препарату.
Віддалені результати спостереження (52-й тиждень) продемонстрували принципово важливі відмінності між підходами. У групі PRP відзначалося певне збільшення інтенсивності болю порівняно з 32-м тижнем, причому рівень болю був статистично значуще вищим, ніж у групі Меркана® (p<0,01), що може свідчити про поступове зниження тривалості ефекту ін’єкційної терапії. Натомість у групі Меркана® зберігалося стабільне зменшення больового синдрому без клінічно значущих коливань між 32-м і 52-м тижнями. За рівнем болю наприкінці спостереження група Меркана® була зіставною з групою комбінованої терапії, що вказує на пролонгований ефект лікування UC-II.
У групі PRP після початкового періоду вираженого зниження болю відзначалися більш різкі коливання показників ВАШ із тенденцією до повернення симптомів у віддаленому періоді. Оптимальний клінічний профіль продемонструвала комбінована терапія PRP + Меркана®, яка забезпечувала статистично значуще й виражене зменшення болю на ранніх етапах лікування з подальшим підтриманням ефекту, що свідчить про потенційну синергію локального регенеративного та системного хондропротекторного впливу.
Динаміка функціонального стану колінного суглоба
Оцінка за опитувальником KOOS упродовж 52 тижнів продемонструвала чітку позитивну динаміку в усіх досліджуваних групах (рис. 2). На 4-му тижні спостереження всі групи статистично значуще відрізнялися між собою (p<0,001), причому в групі PRP + Меркана® зафіксовано найбільш стрімке зростання оцінки оцінки за KOOS (+113%) порівняно з результатами на 2-й тиждень. У групі PRP також відзначалося покращення функції суглоба (+76%), однак інтенсивність ефекту залишалася нижчою порівняно з комбінованою терапією, тоді як у групі Меркана® на цьому етапі зміни були незначними, але статистично значущими, що вказує на поступовий початок дії препарату.
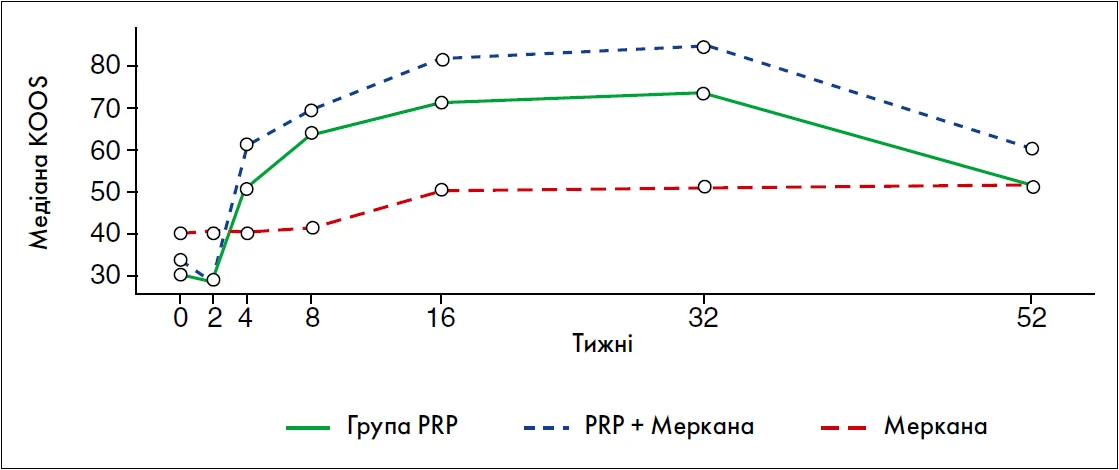 Рис. 2. Графік медіанної оцінки зміни показника KOOS
Рис. 2. Графік медіанної оцінки зміни показника KOOS
Подальше спостереження підтвердило наростання функціонального відновлення: на 8-му та 16-му тижнях у всіх групах реєструвалося достовірне підвищення показників KOOS. Найвищі значення функціонального покращення спостерігалися у групі PRP + Меркана®, що відображає більш швидке відновлення функції колінного суглоба при поєднанні регенеративної терапії з імунною. У групі PRP також відмічено покращення функціонального стану суглобів, однак із більшою варіабельністю результатів. Водночас у групі Меркана® клінічно помітні зміни з’являлися переважно після 8-16 тижнів терапії, що свідчить про кумулятивний механізм дії з часозалежним приростом показників KOOS. На 32-му тижні у всіх групах зберігалося статистично значуще покращення функціонального стану, хоча темп приросту KOOS закономірно сповільнювався, що відповідає фазі стабілізації клінічного ефекту. Найбільший приріст функціональних показників між 16-м і 32-м тижнями також було відзначено в групі PRP + Меркана®, тоді як у групі PRP зміни були менш вираженими. У групі Меркана® на цьому етапі фіксувався стабільно позитивний ефект.
Пролонговані результати (після 32-го тижня) у групі PRP + Меркана® залишалися кращими порівняно з монотерапією PRP (на 78% проти 69% від початкових показників), що вказує на синергічний ефект комбінованого підходу. У групі Меркана® на 52-му тижні лікування спостерігалося покращення функціональних показників за KOOS на 27% порівняно з початковим показником зі збереженням його стабільності без різкого регресу, що свідчить про тривале збереження досягнутого клінічного результату. Загалом, динаміка KOOS демонструє, що комбінована терапія PRP + Меркана® забезпечує найбільш швидке та виражене покращення функції колінного суглоба порівняно з лише PRP, тоді як монотерапія препаратом Меркана® характеризується повільнішим, але більш пролонгованим і стабільним функціональним результатом у довгостроковій перспективі.
Важливою перевагою дослідження є використання об’єктивного інструментального контролю за допомогою МРТ, що дозволило оцінити структурні зміни суглобів (рис. 3). Порівняльний аналіз МРТ у групі комбінованої терапії (PRP + Меркана®) до та після лікування показав позитивні зміни: збільшення товщини суглобового хряща, зменшення дефектів і набряку субхондральної кістки, а також редукцію зони субхондральної ерозії, що свідчить про регенеративний ефект комбінованого підходу.
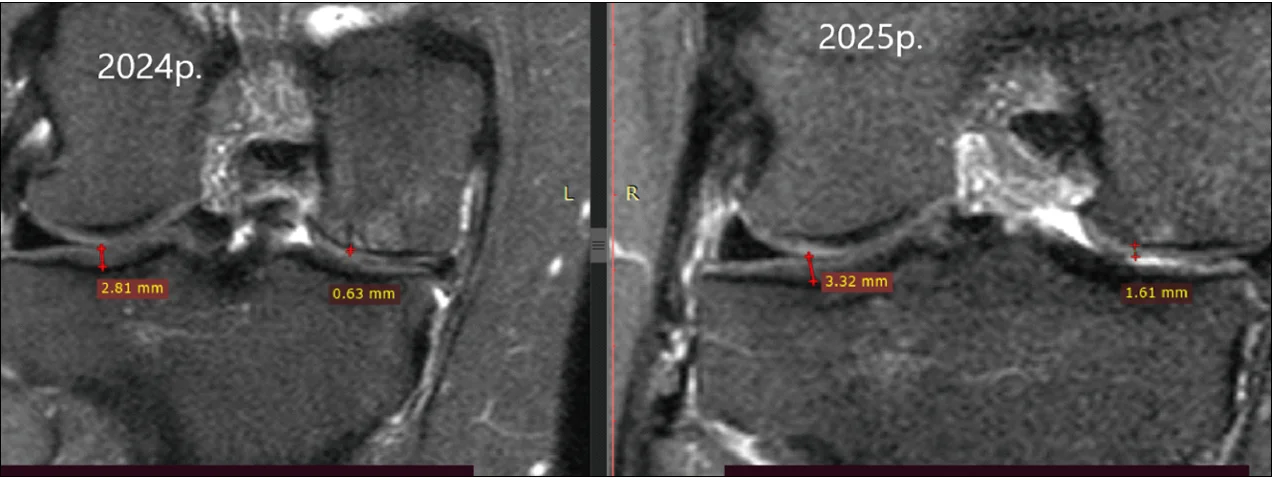 Рис. 3. Динаміка зміни товщини суглобового хряща латерального виростка великогомілкової кістки у групі PRP + Меркана®
Рис. 3. Динаміка зміни товщини суглобового хряща латерального виростка великогомілкової кістки у групі PRP + Меркана®
Практичні висновки та клінічні перспективи результатів дослідження
Отримані результати мають вагоме практичне значення для ведення пацієнтів із остеоартритом, особливо в контексті вибору між інвазивними та консервативними підходами лікування. Терапія PRP на сьогодні є перспективною регенеративною методикою, яка активно використовується в травматології та ортопедії, однак її клінічне застосування супроводжується низкою особливостей. У представленому дослідженні на 2-му тижні спостереження у групах із PRP відзначалося тимчасове підвищення больового синдрому та зниження функціонального стану за KOOS, що клінічно проявлялося помірним набряком, локальною болісністю й дискомфортом у суглобі. Це є типовою реакцією на внутрішньосуглобове введення аутологічних препаратів: стимуляція тканин запускає репаративні процеси, але може спричиняти транзиторне посилення запальної реакції синовії. Крім того, сама ін’єкційна процедура як інвазивна маніпуляція супроводжується мікротравматизацією тканин та індивідуальною реакцією пацієнта на біологічний матеріал.
Клінічні настанови залишаються неоднозначними щодо рутинного застосування PRP (Kolasinski S.L. et al., 2020), що зумовлено гетерогенністю препаратів, відмінностями протоколів приготування, кількістю ін’єкцій та характеристиками мікросередовища суглоба. Результати поточного дослідження підтверджують, що оптимізація ефекту плазмотерапії можлива за допомогою комбінованих підходів, спрямованих на модифікацію внутрішньосуглобового мікросередовища. Так, комбінована терапія PRP + Меркана® продемонструвала більш швидку, виражену та стійку позитивну динаміку як за показниками болю, так і за функціональною шкалою. З позиції патогенезу остеоартриту це може пояснюватися синергічністю механізмів дії, зокрема впливом на TGF-β, який відіграє ключову роль у регуляції метаболізму хрящової тканини. Результатами дослідження підтверджується ефект синергії, коли системний хондропротективний вплив неденатурованого колагену ІІ типу формує більш сприятливе середовище для реалізації регенеративного потенціалу PRP і пролонгації клінічного ефекту.
Не менш важливим є той факт, що монотерапія препаратом Меркана® продемонструвала достовірний і клінічно стійкий терапевтичний ефект. На відміну від PRP, де спостерігалися коливання показників у ранні терміни спостереження, у групі Меркана® відзначався накопичувальний характер дії з поступовою появою клінічно значущих змін. Слід зауважити, що на 52-му тижні саме у групі Меркана® зберігався більш стабільний терапевтичний ефект без вираженої втрати досягнутих результатів, що свідчить про пролонговану дію та потенційний хворобомодифікуючий вплив.
Із практичної точки зору плазмотерапія як інвазивна процедура потребує спеціалізованого обладнання, навичок внутрішньосуглобових ін’єкцій, дотримання стандартів роботи з біологічними матеріалами та має певні процедурні ризики, включаючи травматизацію внутрішньосуглобових структур. Це суттєво обмежує її широке застосування, особливо на рівні первинної медичної допомоги. Крім того, доступність PRP-терапії залишається нерівномірною, а її вартість та організаційні вимоги є складними для значної частини пацієнтів.
Важливо, що більшість пацієнтів із суглобовим болем вперше звертаються саме до лікарів первинної ланки, тоді як доступ до спеціалізованої ортопедичної допомоги часто є відтермінованим. За таких умов виникає клінічна потреба у призначенні ефективної, безпечної та довготривалої хворобомодифікуючої терапії вже на ранніх етапах лікування остеоартриту. Виключно симптоматичне лікування, спрямоване лише на купірування болю, асоціюється з ризиком розвитку побічних ефектів і не впливає на патогенез остеоартриту. З огляду на синергію механізмів впливу, зокрема вплив на фактор росту TGF-β, монотерапія препаратом Меркана® може розглядатися як раціональна альтернатива у випадках недоступності плазмотерапії, наявності протипоказань до інвазивних процедур або відмови пацієнта від внутрішньосуглобових
ін’єкцій.
Отримані результати демонструють, що за умови достатньої тривалості лікування (не менше 8-16 тижнів) можна досягти достовірного зниження болю та покращення функціонального стану суглоба з подальшим збереженням ефекту в довгостроковій перспективі. Інтеграція імунно-регенеративної терапії остеоартриту вже на первинному рівні медичної допомоги може сприяти ранньому впливу на перебіг захворювання, зменшенню потреби у знеболенні та підвищенню загальної ефективності терапевтичних підходів із відстроченням інвазивних процедур.
Підготувала Катерина Пашинська
Тематичний номер «Хірургія. Ортопедія. Травматологія. Інтенсивна терапія» № 1 (68), 2026 р.



